HPLC法测定鼻窦炎口服液中阿魏酸的含量
2014-03-08曹云飞
曹云飞,叶 飞,陈 娜
(1.镇江市药品检验所,江苏镇江212003;2.江苏大学附属医院细胞治疗中心,江苏镇江212001)
HPLC法测定鼻窦炎口服液中阿魏酸的含量
曹云飞1,叶 飞1,陈 娜2
(1.镇江市药品检验所,江苏镇江212003;2.江苏大学附属医院细胞治疗中心,江苏镇江212001)
目的高效液相色谱法测定鼻窦炎口服液中阿魏酸的含量。方法色谱柱:岛津C18柱(5020-39001);流动相:甲醇-1%醋酸溶液(30∶70);流速:1.0 mL·min-1;检测波长:321 nm;柱温:30℃;进样量:10μL。结果本法可用来测定鼻窦炎口服液中阿魏酸的含量。在10.22~102.20μg·mL-1浓度范围内呈线性关系,平均回收率为98.84%。结论该方法简便、准确,可作为鼻窦炎口服液质量控制的方法。
鼻窦炎口服液;高效液相色谱法;阿魏酸
鼻窦炎口服液主要由辛夷、荆芥、薄荷、桔梗、竹叶柴胡、仓耳子、白芷、川芎、黄芩等组方而成,具有补血益气功效。主要用于疏散风热,清热利湿,鼻窦炎见上述证候者。临床应用较为广泛。现行执行标准为《中国药典》2010年版(一部),由于本品中含有一定量的川芎,而川芎中主要含有阿魏酸成分,参照《中国药典》本文采用HPLC法同时对鼻窦炎口服液中阿魏酸的含量进行测定,该法简便,稳定性和重现性好[1,2]。
1 仪器与试药
1.1 仪器 Agilent 1100高效液相色谱仪、工作站(美国Agilent公司)。
1.2 试药 阿魏酸对照品(中国食品药品检定研究院,批号:110773-201012);甲醇(色谱纯,国药集团化学试剂有限公司);其余试剂为分析纯;鼻窦炎口服液(太极集团重庆桐君阁药厂有限公司,批号:11120114、11100087、10120102)。
2 方法与结果[3~8]
2.1 色谱条件 色谱柱:岛津C18柱(5020-39001);流动相:甲醇-1%醋酸溶液(30∶70);流速:1.0 mL·min-1;紫外检测波长:321 nm;柱温:30℃;进样量:10μL;在此条件下阿魏酸峰的理论塔板数为16 402。
2.2 标准曲线的制备 精密称取阿魏酸对照品适量,加70%甲醇适量溶解并定量稀释成含阿魏酸102.20μg·mL-1的贮备液。分别精密量取贮备液1、2、4、6、8 mL,用70%甲醇定量稀释至10 mL,制成对照品溶液,取对照品溶液及贮备液在上述色谱条件下进样分析,测定峰面积值(A),并以A对进样浓度(C)进行回归,绘制标准曲线。线性关系考察见表1,色谱图见图1。
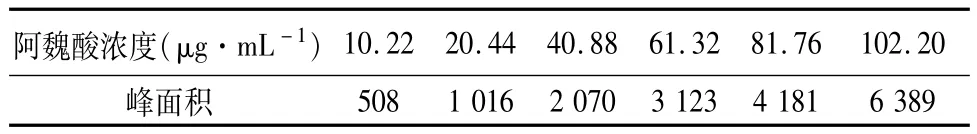
表1 阿魏酸线性关系考察
回归方程:A=62.901C-501.3,r=0.984 3,线性范围:10.22~102.20μg·mL-1。
2.3 供试品溶液的制备 取本品1 mL,精密加入70%甲醇至10 mL混匀即得;取供试品溶液,在上述色谱条件下测定。色谱图见图1。
2.4 稳定性试验 取对照品溶液,分别于0、4、8、12 h在上述色谱条件下测定,峰面积基本不变,RSD为0.33%。
2.5 精密度试验 取对照品溶液,在上述色谱条件下连续测定5次,RSD为0.2%,结果见表2。
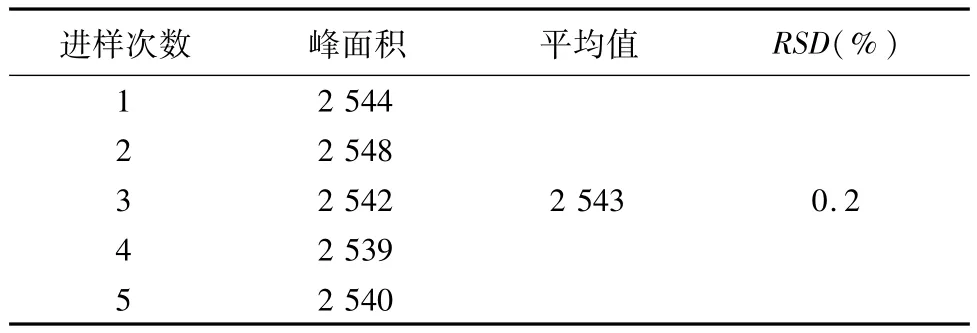
表2 对照品溶液精密度
2.6 重复性试验 按照拟订的含量测定方法,取同批号样品5份,分别制备供试品溶液,在上述色谱条件下测定,RSD为0.1%,结果见表3。
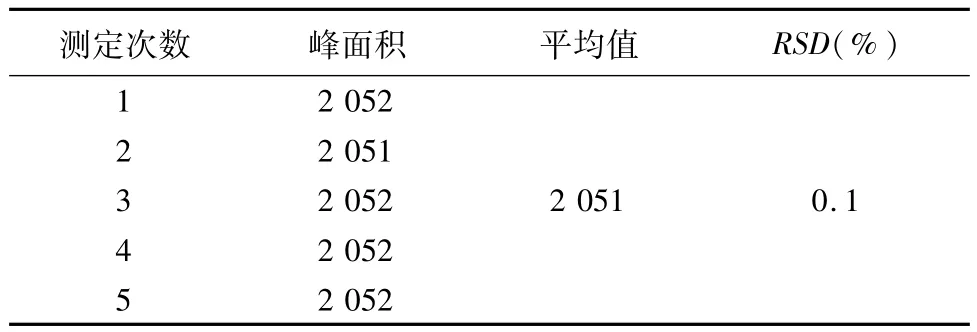
表3 重复性试验结果
2.7 回收率试验 取6份已知含量的样品,分别加入对照品贮备液1 mL,按“2.3”项下中所述方法操作,在上述色谱条件下测定,结果见表4。
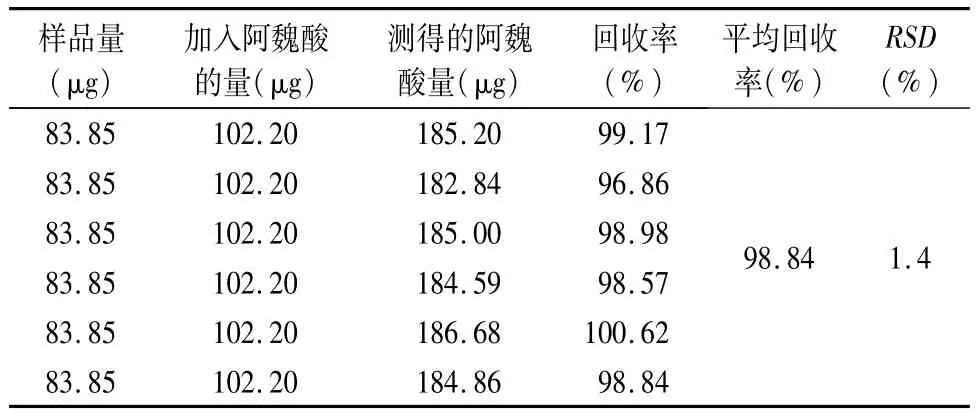
表4 回收率测定结果(n=6)
2.8 空白试验 按处方比例称取除了川芎以外的其他几味药,按制备工艺制成供试液,照样品测定法测定,在主成分出峰处无干扰。
2.9 样品测定 对同一厂家不同批号样品的含量测定结果见表5。

表5 样品的含量测定结果(n=3)
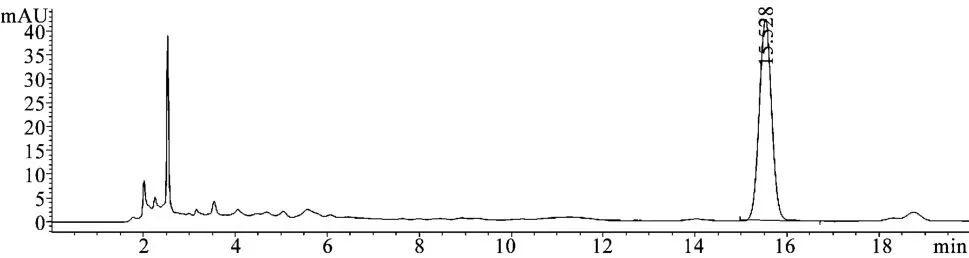
图1 阿魏酸样品的HPLC色谱图
3 讨论
3.1 在制备对照品溶液时,参考了《中国药典》2010年版(一部)中川芎的药材处理方法。
3.2 通常阿魏酸的检测波长为321 nm,该波长测定,其他组分及辅料无干扰。
3.3 实验过程中曾尝试乙腈-甲醇-0.1%磷酸(44∶46∶33)[3]、乙腈-水-冰醋酸(60∶40∶1)、乙腈-0.085%磷酸溶液(17∶83)为流动相,经比较得知,选用甲醇-1%醋酸溶液(30∶70)比例最佳,峰形及柱效较好。
3.4 采用HPLC法测定鼻窦炎口服液中阿魏酸含量,方法简便、准确、重现性好,可以作为鼻窦炎口服液质量控制的方法。
[1]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010.
[2]陈昌彪,罗明芳,陈少军.HPLC法测定当归补血颗粒中阿魏酸的含量[J].中国药师,2007,10(9):865-866.
[3]贺亚玲,车晓彦,姜卫东.高效液相色谱法测定当归配方颗粒中阿魏酸含量[J].中国药业,2006,15(3):39.
[4]黄华树,叶能胜,郝晓丽,等.用HPLC测定当归中阿魏酸含量方法的研究[J].现代仪器,2009,15(4):29-30.
[5]李喜凤,余云辉,郝哲,等.蒲公英中阿魏酸的含量测定[J].时珍国医国药,2010,21(5):1169-1170.
[6]任占军.速克感冒片质量标准控制及微波提取当归中阿魏酸的研究[D].北京:首都师范大学,2007.
[7]高逢喜,周用相.不同炮制方法对当归成分阿魏酸的影响[J].中国医院药学杂志,1989,9(8):363-364.
[8]黄宗玉,王晓明.反相高效液相色谱法测定当归调经露中阿魏酸[J].中成药,1991,13(8):11-12.
Determ ination of ferulic acid in Bidouyan Oral Solution by HPLC
CAO Yun-fei1,YE Fei1,CHEN Na2
(1.Zhenjiang Institute for Drug Control of Jiangsu Province,Zhenjiang 212003,China;2.Cell Therapy Centre,Affiliated Hospital of Jiangsu University,Zhenjiang 212001,China)
ObjectiveTo determine the content of ferulic acid by HPLC in Bidouyan Oral Solution.M ethodsThe determination was carried outwith Shimadzd C18column.Themobile phase wasmethanol-1%acetic acid solution(30∶70)and the flow rate was 1.0 mL·min-1.The column temperature was 30℃and the detective wavelength was 321 nm.ResultsThe content of ferulic acid can be determined by HPLC.The linear concentration range of these compound was 10.22~102.20μg·m L-1.The average recovery was 98.84%.ConclusionThe method was simple and accurate and can be used to control the quality of Bidouyan Oral Solution.
Bidouyan Oral Solution;HPLC;Ferulic acid
R927.2
A
2095-5375(2014)12-0691-002
曹云飞,男,研究方向:药物分析,E-mail:yunfei_cao@163.com
