非离子表面活性剂存在下纳米氢氧化镁的水热处理
2014-03-04唐卫平苏明阳
唐卫平,苏明阳
(河南工业职业技术学院,河南南阳473000)
非离子表面活性剂存在下纳米氢氧化镁的水热处理
唐卫平,苏明阳
(河南工业职业技术学院,河南南阳473000)
本文研究了在非离子表面活性剂PEG6000存在下纳米氢氧化镁的水热处理规律。产品采用X射线衍射、热重-差热分析、透射电子显微镜等进行了表征。结果表明:由于PEG6000的空间位阻作用以及与晶面的吸附作用,在PEG6000存在下进行氢氧化镁的水热处理,不仅可以改善氢氧化镁的结晶性和分散性,而且可有效地防止粒径的快速增长。当PEG6000的用量为氢氧化镁质量的4.4%,水热温度为180℃,水热时间为5h时,可制得结晶完整、分散性好、平均粒径61nm的六方片状纳米级氢氧化镁。
纳米氢氧化镁;水热处理
纳米Mg(OH)2是一种重要的无机材料,在阻燃、水处理、抗菌、文物保护、催化等方面具有广泛的应用前景[1-5]。但常压制备的纳米Mg(OH)2多为无定形晶体,结晶性能和过滤性能均不理想,并且有很强的凝聚性。这将对它的应用性能产生较大的影响。解决以上问题的有效方法之一是在特定的高温高压水溶液中,对常压合成的氢氧化镁进行水热处理[6-9]。如HongYan等通过加入阳离子表面活性剂CTAB,对Mg(OH)2进行水热处理。在水热温度150℃水热时间6h、pH值为11的条件下,制备出平均粒径400nm、厚度60nm的六角片状Mg(OH)2。Q.L.Wu等在CaCl2稀溶液中对形貌不规整的Mg(OH)2进行4h水热制备。研究发现,在CaCl2浓度1mol·L-1条件下,随着水热温度的升高,颗粒粒径由0.1~0.3μm增大到0.3~1.5μm,比表面积由28.5m2·g-1降低到10.5m2·g-1。分析认为,水热温度升高的条件下,CaCl2的存在促进了生长基元形成,结果造成颗粒粒径增大。向兰等以5mol·L-1NaOH溶液为介质,在200℃条件下对Mg(OH)2水热处理5h,Mg(OH)2颗粒的形状从不规则片状转变为规则的六角片状晶体,粒径增长至870nm,比表面积从35m2·g-1减小至6.3m2·g-1,但以NaOH或KOH等碱性溶液为水热介质,水热处理成本高,对设备的防腐要求较高。从以上这些报道的结果来看,水热处理效果较好,Mg(OH)2颗粒的分散性得到显著改善,但在水热处理中氢氧化镁晶体粒径一般快速生长至微米级,难以制得结晶良好的纳米级Mg(OH)2。由于分散剂可吸附在粒子表面产生空间位阻效应,有效抑制晶粒的生长和防止粒子团聚[10,11],故本实验选择非离子表面活性剂PEG6000作为分散剂,重点研究非离子表面活性剂存在下纳米氢氧化镁水热处理的规律。
1 实验方法
1.1试剂与仪器
NaOH、六水氯化镁均为分析纯试剂,由国药集团化学试剂有限公司生产。PEG6000(聚乙二醇6000)(A.R.天津市标准科技有限公司)。
JEM-2000EX型透射电子显微镜(日本电子光学公司);Rigaku D/max-2500型X射线衍射仪(日本理学公司)。
1.2实验方法
先将相当于Mg(OH)2理论产量3%的6mL PEG6000溶液(2.5(wt)%)和16mL去离子水加入恒速搅拌的三口烧瓶中。待温度升高到80℃时,同时滴加30.1mL 6mol·L-1NaOH溶液和28.7mL 3mol· L-1MgCl2溶液,约15min滴完。随后继续反应3h。再将得到的悬浮液转移到聚四氟乙烯衬底的容积为200mL的高压釜中,同时补加一定量的分散剂。高压釜密闭后置于油浴中,开启搅拌及加热装置,于一定温度下水热处理一段时间。水热处理结束后,自然冷却至室温,过滤,滤饼用50mL×4去离子水洗涤4次,50mL乙醇洗涤一次,之后于120℃下干燥3h得产品。
1.3分析与表征
通过透射电镜观察颗粒形貌、一次粒径及分散情况。用X射线衍射仪分析样品的晶体结构,采用Cu靶K系辐射,波长为0.15406nm,电压40kV。用STA449C热重分析仪对样品进行热重-差热分析,升温速率为10℃·min-1。
2 结果与讨论
2.1PEG6000用量对水热处理的影响
不同PEG6000用量下水热处理产物的形貌见图1。

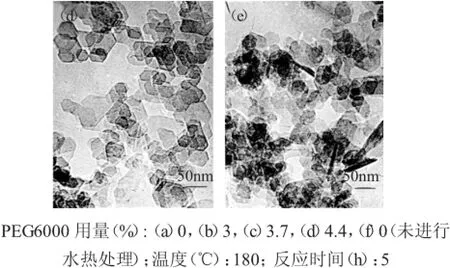
图1 PEG6000用量对水热产物形貌的影响Fig.1Influence of the amount of PEG6000 on the morphology of hydrothermal products.
由图1可以看出,水热处理能显著改善Mg(OH)2的结晶形态和分散性,水热处理后的Mg(OH)2晶体多为分散性好的边界清晰的六方片状。随着分散剂用量的增加,产品晶形发育逐渐完全,六方片状结构趋于规则,颗粒粒径分布均匀,分散性更好,但对Mg(OH)2粒度的影响不大,当PEG6000用量分别为0、3、3.7、4.4%时,产物的平均粒径分别约为60,69、71、61nm。PEG是一种有空间位阻稳定作用的高分子化合物。在水热处理中,PEG高分子长链的一端可以与溶液中Mg(OH)2的生长基元相联结,紧密地吸附于颗粒的表面;另一端分子长链伸向四周,将Mg(OH)2粒子表面包围,形成一层较强的大分子亲水膜,产生并强化位阻效应,从而实现稳定分散的效果。
图2是样品的XRD谱图,对应的特征峰强及半峰宽值见表1。

图2 PEG6000用量对水热产物XRD谱图的影响Fig.2Influence of the amount of PEG6000 on the XRD spectras of hydrothermal products
由图2可以看出,水热处理对Mg(OH)2晶体的衍射峰位置没有影响,说明Mg(OH)2的晶格结构保持不变。随着在水热处理过程中加入分散剂,图2中Mg(OH)2特征衍射峰峰型变尖,表1中半峰宽值降低,表明产品的结晶愈完整且产物的粒径增大,这与图1所得到的结果相吻合。此外表1中特征衍射峰的相对强度发生明显变化。当分散剂用量从0%增加到4.4%时,I(001)/I(101)由0.614增加到0.694,I(001)/I(110)由1.554增加到2.103。这表明水热处理过程中晶体的生长方向发生变化。原因在于PEG分子中O具有孤电子对,Mg2+具有空轨道,通过电荷匹配作用,PEG可与Mg2+配位聚合物。而在Mg(OH)2晶体中,(001)面是富镁离子面,因此PEG容易吸附在(001)面,降低晶面的表面能,促进晶面的生长速度。同时由于由于(001)面极性较小,(101)面(110)面极性较大,晶体生长优先选择极性较小的面,也使得颗粒的表面极性降低,团聚倾向变小。这也是水热处理后产品分散性有所改善的原因。此外PEG6000与Mg2+络合作用,强化了Mg(OH)2溶解,加速了Mg2+的传质输运,使得在结晶完整的同时,产品粒径并未有较大的增长。

表1 PEG6000用量对Mg(OH)2粒子特性参数的影响Tab.1Influence of the amount of PEG6000 on the characteristics of Mg(OH)2particles
2.2温度对水热处理的影响(图3)

图3 温度对水热产物形貌的影响Fig.3Influence of hydrothermal temperature on the morphology of hydrothermal products
图3表明,水热温度对Mg(OH)2的水热处理有较大的影响。140℃下的水热产物出现大量针状团聚体,随着温度的升高,水热处理效果越趋明显,出现的六角片状产物越来越多,粒径基本在65nm左右,分散性有较大改善;但200℃下水热产物粒径增大到78nm,出现粘连现象,并且出现了大量小颗粒。可能原因在于温度高,已经长大的晶粒在高温下溶解,导致粘连现象的出现。最终确定水热处理的较佳反应温度为180℃。
2.3反应时间对水热处理的影响(图4)

图4 反应时间对水热产物形貌的影响Fig.4Influence of hydrothermal reaction time on the morphology of hydrothermal products
由电镜照片图4可以看出,水热时间较短时,大部分是无定性颗粒。延长反应时间,有利于破坏吸附在晶面上的液体层,减少吸附层对晶体长大的阻力,Mg(OH)2的晶型逐渐发育完全,六方片状更趋规则,此时颗粒的分散性也较好。但考虑到一直延长反应时间,不仅增加水热处理的成本,而且粒径有增大的趋势,因此确定水热处理的反应时间为5h。
3 结论
由于PEG6000的空间位阻作用以及与晶面的吸附作用,在PEG6000存在下进行Mg(OH)2的水热处理,不仅可以改善Mg(OH)2的结晶性和分散性,而且可有效地防止Mg(OH)2粒径的快速增长。当PEG6000的用量为Mg(OH)2质量的4.4%,水热温度为180℃,水热时间为5h时,可制得结晶完整、分散性好、平均粒径61nm的六方片状纳米级Mg(OH)2。
[1]F.Laoutid,L.Bonnaud,M.Alexandre,et al.New prospects in flame retardant polymer materials:From fudamentals to nanocomposites[J].Materials Science and EngineeringR,2009,63:100-125.
[2]Kai Lu,Xiaojun Cao,Qiushi Liang,et al.Formation of a compactprotective layer by magnesium hydroxide incorporated with a small amount of intumescent flame retardant:new route to high performance nonhalogen flame retardant TPV[J].Industrial&EngineeringChemistryResearch,2014,53:8784-8792.
[3]Hui Ma,Zhixiang Chen,Zhiping Mao.Controlled growth of magnesium hydroxide crystals and its effect on the high-temperature properties of cotton/magnesium hydroxide composites[J].Vacuum, 2013,95:1-5.
[4]XiaohongPan,YonghaoWang,Zhi Chen,et al.Investigation of antibacterial activity and related mechanism of a series of nano-Mg(OH)2[J].Applied Materials&Interfaces,2013,(5):1137-1142.
[5]David Chelazzi,Giovanna Poggi,Yareli Jaidar,et al.Hydroxide nanoparticles for cultural heritage:consolidation and protection of wallpaintingsandcarbonatematerials[J].JournalofColloidand Interface Science,2013,392:42-49.
[6]L.Xiang,Y.C.Jin,Y.Jin,Hydrothermal modification of Mg(OH)2particles in NaOH solution[J].the Chinese Journal ofProcess Engineering,2003,(3):116-120.
[7]H.Yan,X.H.Zhang,J.M.Wu,et al.The use of CTAB to improve the crystallinity and dispersibility of ultrafine magnesium hydroxide byhydrothermal route[J].Powder Technology,2008,188:128-132.
[8]Q.L.Wu,L.Xiang,Y.Jin.InfluenceofCaCl2onthehydrothermalmodificationofMg(OH)2,[J].PowderTechnology,2006,165:100-104.
[9]A.Sierra-Fernandez,L.S.Gomez-Villalba,O.Milosevic,et al.Synthesis and morpho-structural characterization of nanostructured magnesium hydroxide obtained by a Hydrothermal method[J].Ceramics International,2014,40:12285-12292.
[10]Yun-Feng Yang,Xiang-Feg Wu,Guo-Sheng Hu,et al.Effects of stearic acid on synthesis of magnesium hydroxide via direct precipitation[J].Journal ofCrystal Growth,2008,310,3557-3580.
[11]Agnieszka Pilarska,Marcin Wysokowski,Ewa Markiewicz,et al. Synthesis of magnesiumhydroxide and its calcinates by a precipitation method with the use of magnesium sulfate and poly(ethylene glycols)[J].Powder Technology,2013,235:148-157.
Hydrothermal treatment of magnesium hydroxide nanoparticles in the presence of nonionic surfactant
TANG Wei-ping,Su Ming-yang
(Henan Polytechnic Institute,Nanyang 473000,China)
The rule of hydrothermal treatment on Mg(OH)2nanoparticles in the presence of nonionic PEG6000 was investigated in this paper.The resultant product was characterized by X-ray powder diffraction,hermogravimetric-differential thermal analysis and transmission electron microscopy.The experimental results indicated that the hydrothermal treatment in the presence of PEG may effectively control the fast growth of particle and improve the crystallinity and dispersibility of product due to the sterically hindered effect and absorption of PEG6000.The method led to the dispersive Mg(OH)2hexagonal flakes with perfect crystallintiy and mean size 61nm at 180℃for 5h in the presence of 4.4%PEG6000.
magnesium hydroxide nanoparticle;hydrothermal treatment
O614.22
A
1002-1124(2014)11-0068-04
2014-07-28
唐卫平(1967-),男,江苏姜堰人,副教授,主要从事高分子材料及其添加剂的应用研究。
苏明阳(1984-),男,助教,2010年毕业于青岛科技大学化学工艺专业,研究生,研究方向:精细化学品和精细化工技术的研究。
