毛细管电泳法分离检测饮料中的防腐剂
2014-03-04王钰杨思文代语林邓宁王燕何建波朱燕舞
王钰,杨思文,代语林,邓宁,王燕,何建波,朱燕舞
(合肥工业大学化学工程学院,安徽合肥230009)
毛细管电泳法分离检测饮料中的防腐剂
王钰,杨思文,代语林,邓宁*,王燕,何建波,朱燕舞
(合肥工业大学化学工程学院,安徽合肥230009)
采用高效毛细管电泳法,同时在线分离检测对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂。考察了运行缓冲液的浓度、pH值、分离电压、进样时间等因素对电泳分离的影响。在检测波长为230nm时,获得了3种防腐剂分离检测的最优化实验条件为:20mmol/L pH 9.2的硼砂缓冲溶液,分离电压为22kV,进样时间15s。在最优化实验条件下,3种防腐剂检测的线性相关系数均大于0.98,检出限为1.0×10-2g/kg。利用此方法检测了市售3种饮料中所含防腐剂的种类和含量,各种防腐剂的回收率在88%~102%之间。
毛细管电泳;防腐剂;分离;检测
食品是人类生存的基本物质保障,现代化的食品生产要求食品能够方便贮存和运输,防腐剂既能使食品保存期延长,也能防止食品腐败变质,因此被广泛应用于食品生产中。但是食品防腐剂的过量使用会对人体健康造成较大的危害,伤害人体正常机能,降低人体免疫力。我国明确规定了防腐剂使用标准,但仍然有一些商家没有按照标准合理使用防腐剂。2007年国家质检总局对北京等13个省、直辖市96家企业生产的117种产品进行抽查,抽查中发现部分碳酸饮料中防腐剂的含量超标[1]。近年来,食品安全的监督与管理已经是国务院食品安全工作的重要任务。因此,建立一种高效快速检测食品中多种食品防腐剂的方法非常重要。
目前,食品防腐剂的分离检测方法通常采用气相色谱法(gas chromatography,GC)[2-4]、高效液相色谱法(high per formance liquid chromatography,HPLC)[5-7]和毛细管电泳法(capillary electrophoresis,CE)[8-10]。其中CE由于具有分离效率高、试剂消耗量小、实验成本低、易与其他技术联用和环境友好等优点[2,11-13],引起研究者的关注并成为一项具有较强竞争力和良好选择性的新技术。运用CE能同时分离和检测多种食品防腐剂,如龙巍然等[14]运用CE分离检测苯甲酸、山梨酸、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、对羟基苯甲酸丁酯等6种防腐剂。YOSHIKAWA K等[11]运用CE分离检测苯甲酸、山梨酸、丙酸等食品中防腐剂。但是根据文献调研结果,截至目前,采用毛细管电泳-紫外检测法(capillary electrophoresis-ultraviolet,CE-UV)同时分离检测对羟基苯甲酸甲酯、山梨酸钾和苯甲酸这3种常用食品防腐剂的相关文献还未报道。本研究采用CE-UV同时分离检测对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂,考察了分离电压、进样时间、运行缓冲液的浓度及其pH值等电泳参数对分离效率的影响,确定了3种防腐剂分析检测的最优化实验条件,在最佳实验条件下测定了市售饮料中防腐剂的种类和含量,并通过回收率实验验证了方法的可靠性。
1 材料与方法
1.1 材料与试剂
对羟基苯甲酸甲酯、山梨酸钾、苯甲酸、硼砂和氢氧化钠均为分析纯:国药集团化学试剂有限公司;七喜柠檬味汽水:上海百事可乐饮料公司;美年达葡萄味汽水:上海百事可乐饮料公司;苹果醋:烟台绿杰苹果醋饮料股份有限公司;实验用水为二次蒸馏水。
1.2 仪器与设备
CL1020高效毛细管电泳仪(配置高压电源、CL1020紫外检测器,HW-2000色谱工作站):北京彩陆科学仪器公司;PHS-3C型精密pH计:上海雷磁仪器厂;HS2060A型超声波清洗器:昆山超声仪器有限公司。未涂层熔融石英毛细管柱(60cm×52cm×50μm):河北永年光导纤维厂。
1.3 实验方法
准确称取对羟基苯甲酸甲酯、山梨酸钾、苯甲酸各0.1g分别置于小烧杯中,用适量的无水乙醇溶解并定容至100mL容量瓶中,配制成1.0g/L标准样品溶液。称取一定量的硼砂置于烧杯中,用二次蒸馏水溶解,全部转移并定容于250mL容量瓶中,配制成20mmol/L的硼砂溶液。实验前,溶液均用孔径为0.45μm的超滤膜过滤。3种防腐剂的分子结构式如表1所示。为便于标记,在后文图中,对羟基苯甲酸甲酯、山梨酸钾和苯甲酸分别用M、P和B来表示。
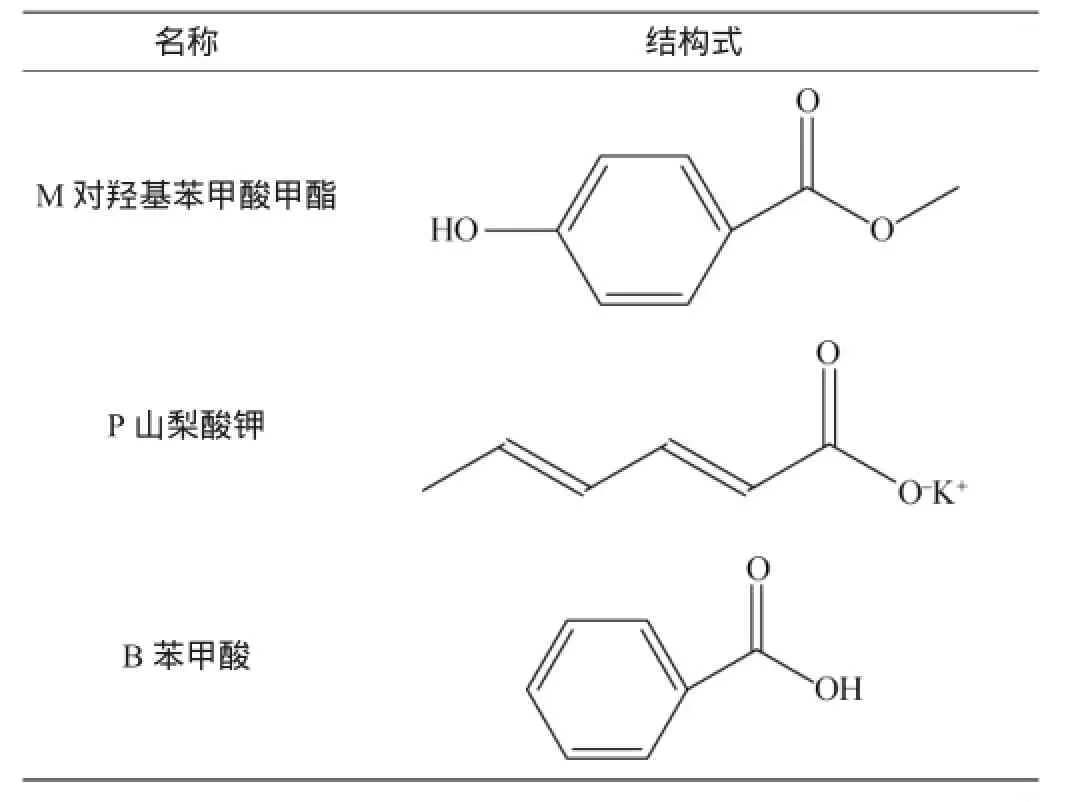
表1 分析物的结构式Table 1 Structure of the analyte
每次开机前,毛细管依次用1mol/L的HCl冲洗5min,水冲洗5min,1mol/L NaOH冲洗10min,水冲洗5min,缓冲溶液冲洗10min。每两次进样之间毛细管都要用缓冲溶液冲洗2~3min。
2 结果与讨论
2.1 电泳条件的选择
2.1.1 缓冲溶液浓度的确定
缓冲溶液的浓度会从缓冲容量、毛细管内扩散层的厚度、以及电泳介质导电性等方面对分离产生影响[15],因此,缓冲溶液的浓度是毛细管电泳分离物质的重要参数之一。在分离电压为18kV、检测波长为230nm、进样时间为15s、缓冲液pH为9.2的条件下,调节硼砂缓冲溶液的浓度分别为10mmol/L、20mmol/L、30mmol/L、40mmol/L、50mmol/L。图1(A)反映的是缓冲溶液浓度对分离度的影响,从图1(A)可以看出,在实验的5个缓冲液浓度条件下,对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂均能够实现基线分离,随着硼砂缓冲溶液浓度的增大,对羟基苯甲酸甲酯、山梨酸钾和苯甲酸之间的分离度逐渐增大。图1(B)是3种防腐剂柱效随缓冲溶液浓度的变化图,由图1(B)可以看出,当缓冲溶液浓度从10mmol/L增大为30mmol/L时,柱效逐渐升高;但是,当缓冲溶液浓度从30mmol/L进一步升高到50mmol/L时,由于高浓度的缓冲液导致分析电流增大,毛细管中的热效应急剧增加,柱效开始下降,因此当缓冲液浓度为30mmol/L时3种防腐剂的分析柱效最高。但是,实验工作中发现,当缓冲液浓度为30mmol/L时,由于热效应的影响,防腐剂的色谱峰开始出现拖尾现象,因此,选择3种防腐剂分析的最佳缓冲溶液浓度为20mmol/L。
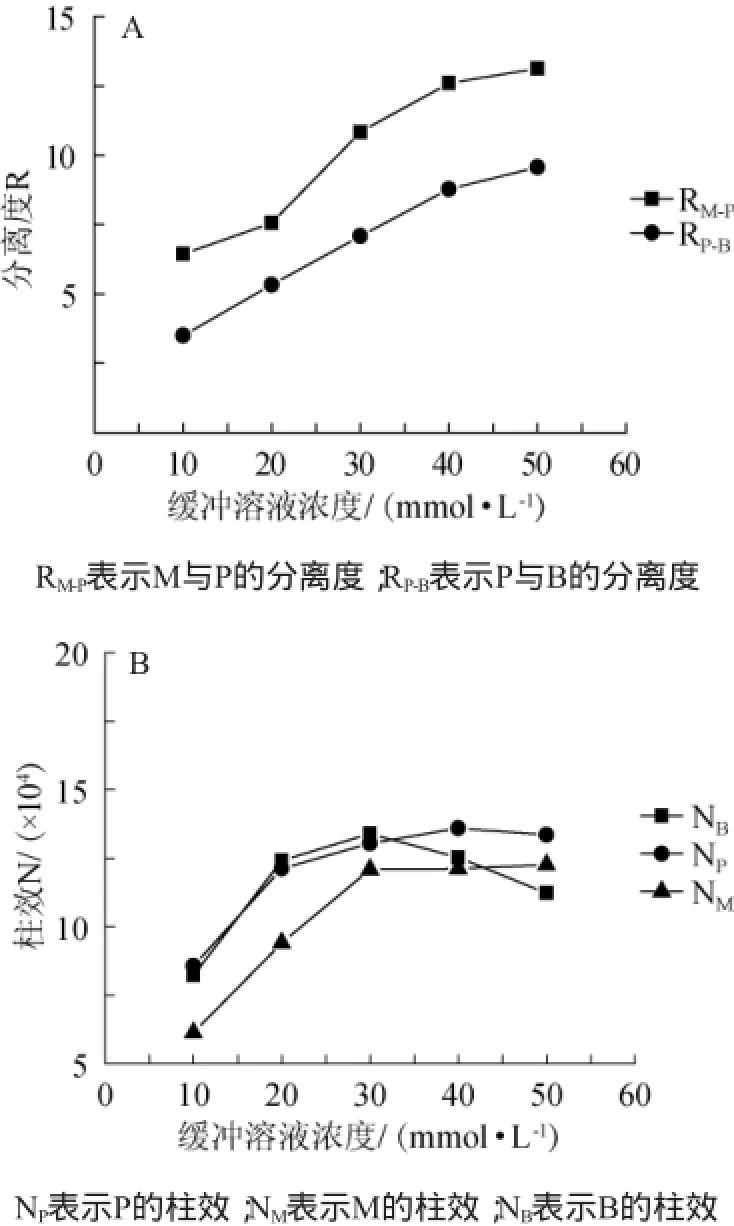
图1 缓冲溶液的浓度对分离度(A)及柱效(B)的影响Fig.1 Effect of buffer concentration on resolution and column efficiency
2.1.2 缓冲溶液的pH值的确定
在毛细管电泳中,缓冲溶液的pH值是影响电渗流的大小和分析物荷电状态的主要因素,因此pH值也是影响毛细管分析的重要参数之一[15]。在20mmol/L硼砂缓冲溶液,分离电压为18kV、检测波长为230nm、高差10cm、进样时间为15s的条件下,考察了缓冲液pH值从9.2升至10.0时3种防腐剂的分离情况。图2(A)是3种防腐剂的分离度随缓冲溶液pH值变化情况图,从图2(A)可以看出,随着缓冲溶液pH值的增加,对羟基苯甲酸甲酯、山梨酸钾和苯甲酸之间的分离度逐渐减小。图2(B)是3种防腐剂柱效随缓冲溶液pH值的变化图,从图2(B)可以看出,当缓冲溶液pH值为9.2时,3种防腐剂柱效较高。因此,选择最佳pH值为9.2。

图2 缓冲溶液pH值对分离度(A)及柱效(B)的影响Fig.2 Effect of buffer pH on resolution and column efficiency
2.1.3 分离电压的确定
为了考察分离电压对对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂分离度及柱效的影响,在20mmol/LpH9.2的硼砂缓冲溶液、检测波长为230nm、高差10cm进样时间为5s的条件下,在18~24kV范围内调节分离电压。图3(A)反映的是分离电压对3种防腐剂迁移时间的影响情况,从图3(A)中可以得出,随着分离电压的增大,3种防腐剂的迁移时间逐渐缩短,这主要是电渗流随着电压的升高而增大的结果。图3(B)是3种防腐剂柱效随分离电压的变化图,由图3(B)可以看出,3种防腐剂的分离柱效在电压为22kV的时候最大。当分离电压从18kV增大到22kV时,柱效逐渐升高;当分离电压从22kV进一步升高到24kV时,柱效开始降低。这是因为焦耳热与毛细管中的电流值平方成正比,当分离电压过高时,急剧增大的焦耳热难以有效驱散,从而导致柱效降低,运行不稳定[16]。因此,为了节约分析时间并获得较高的分离柱效,选择最佳分离电压为22kV。
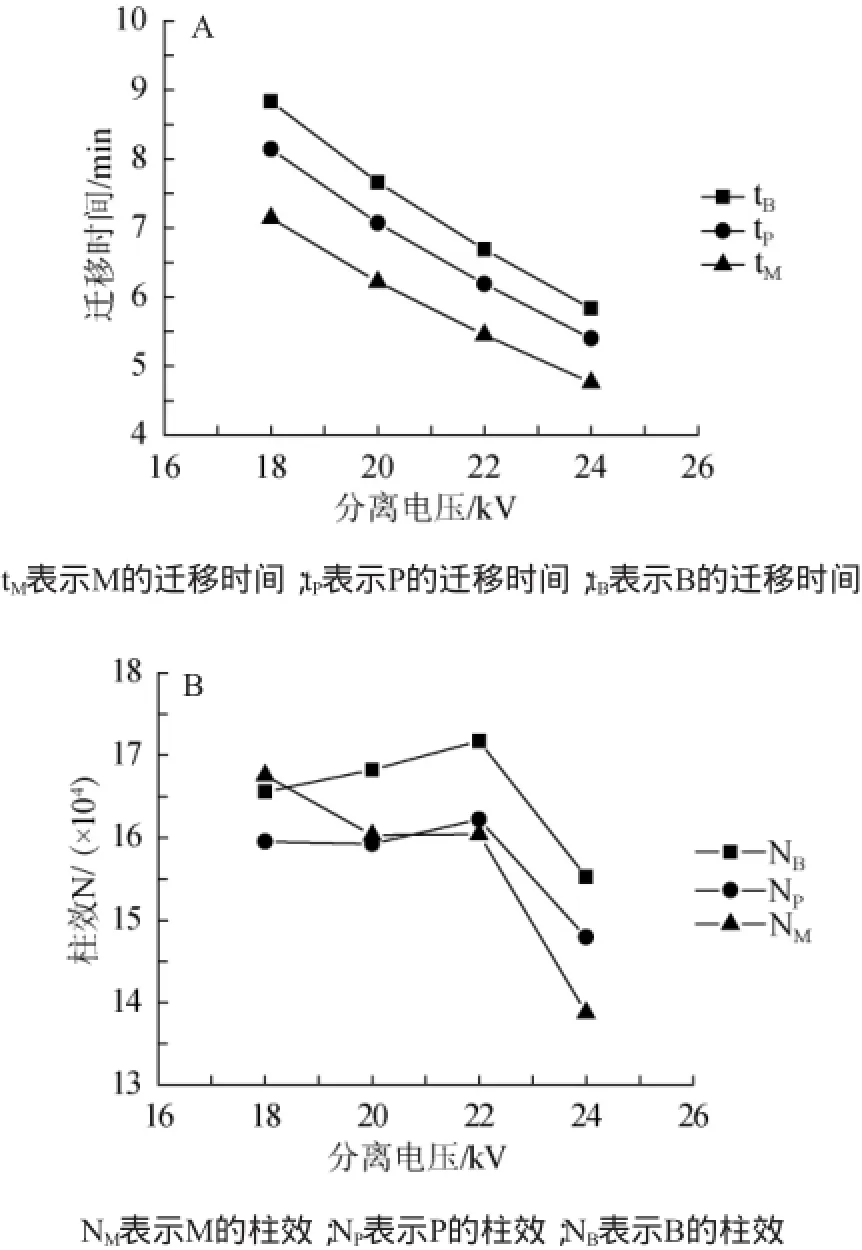
图3 分离电压对分析时间(A)及柱效(B)的影响Fig.3 Effect of separation voltage on analysis time and column efficiency
2.1.4 进样时间的确定
在20mmol/LpH9.2的硼砂缓冲溶液、检测波长为230nm、分离电压为22kV的条件下,采用高差10cm进样,在5~25s范围内调节进样时间。随着进样时间的延长,3个色谱峰峰高均增大,检测灵敏度均提高;但是,当进样时间大于15s时,色谱峰有所展宽,柱效开始降低。同时考虑检测灵敏度和柱效,选择最佳的进样时间为15s。
2.1.5 最优化条件的确定
综上所述,在检测波长为230nm的条件下,对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂实现基线分离的最佳毛细管电泳条件为20mmol/L pH 9.2的硼砂缓冲溶液,分离电压22kV,高差10cm进样,进样时间15s。图4是3种防腐剂在最佳实验条件下的电泳分离谱图,在此条件下对羟基苯甲酸甲酯、山梨酸钾和苯甲酸在7min之内实现了基线分离,相邻色谱峰的分离度分别为7.78和5.29。

图4 最优化条件下防腐剂的毛细管电泳图谱Fig.4 Capillary electrophoresis of preservative under the optimal condition
2.2 检测线性范围、重现性和检出限分析
配制一系列不同浓度的对羟基苯甲酸甲酯、山梨酸钾和苯甲酸混合标准溶液,在最优化条件下进行毛细管电泳实验,建立了同时分离测定3种防腐剂的方法。对羟基苯甲酸甲酯、山梨酸钾和苯甲酸毛细管电泳测定的线性范围、回归方程、相关系数和检出限(S/N=3)等结果见表2。3种防腐剂分析的线性范围为0.05~1.00mmol/L,线性相关系数均大于0.98,检出限为1×10-2g/kg。

表2 不同浓度混合标样的测定结果Table 2 Determination results of different concentrations of mixed standard sample
2.3 实际样品检测
2.3.1 样品的预处理
对美年达葡萄味汽水、苹果醋进行适当的稀释,并且对美年达葡萄味汽水、苹果醋和七喜柠檬味汽水等实际样品分别进行超声脱气。
2.3.2 检测结果
实际样品经预处理后,按上述确定的最优化实验条件进行毛细管电泳分离测定,根据线性回归方程,计算出各种样品中各防腐剂的含量[17],测定结果如表3所示。其中柠檬味汽水中测出含有苯甲酸钠1种防腐剂,含量为0.91g/kg,相对标准偏差(relativestandarddeviation,RSD)为5.6%;葡萄味汽水中测出含有山梨酸钾和苯甲酸2种防腐剂,含量分别为0.56g/kg和0.58g/kg,RSD分别为4.3%和2.1%;苹果醋中检测出含有山梨酸钾1种防腐剂,含量为1.69g/kg,RSD为2.7%。

表3 样品中添加剂的含量Table 3 Content of additives in samples
根据GB2760—1996《食品添加剂使用卫生标准》[18]中规定饮料中苯甲酸钠的含量以苯甲酸计不得超过2g/kg(相当于苯甲酸钠含量2.36g/kg),山梨酸钾的含量以山梨酸计不得超过2g/kg(相当于山梨酸钾含量2.68g/kg),苯甲酸不得超过2g/kg。因此所检测的3种实际样品中所含防腐剂的量都符合国家卫生标准。
2.4 回收率实验
在七喜柠檬味汽水中加入一定量的苯甲酸,美年达葡萄味汽水中加入一定量的山梨酸钾和苯甲酸,苹果醋中加入一定量的山梨酸钾,进行加标回收实验,根据测定的结果计算回收率,结果如表4所示。从表4可以看出,3种防腐剂的测定回收率在88%~102%之间,说明实验建立的毛细管电泳法同时分析测定对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种常用防腐剂,方法可靠,可适用于实际产品的检测。

表4 样品加标回收率实验Table 4 Experiment recovery of standard addition
3 结论
建立了毛细管电泳同时分离检测对羟基苯甲酸甲酯、山梨酸钾和苯甲酸3种防腐剂的新方法。在检测波长为230nm条件下,考察了缓冲溶液浓度、缓冲液pH值、分离电压和进样时间等因素对分析结果的影响,确定了3种防腐剂分析测定的最佳电泳条件为20mmol/L pH 9.2的硼砂缓冲溶液,分离电压22kV,进样时间15s。在最佳实验条件下,检测了3种市售饮料中添加防腐剂的种类和含量,结果表明,其防腐剂含量均符合国标GB2760—1996《食品添加剂使用卫生标准》。回收率实验结果表明3种防腐剂的回收率均在100%左右,证明了实验建立的分析方法可靠性高。该方法步骤简便、检测快速、试剂用量少、成本低、环境友好等优点而利于推广使用,因此该技术具有广泛的应用前景。
参考文献:
[1]吕冰.国家质检总局:碳酸饮料二成多质量不合格[N].市场报,2007-08-27(06).
[2]KOKYAT A,FARHADIK,KALHORIAA.Optimized dispersive liquidliquid microextraction and determination of sorbic acid and benzoic acid in beverage samples by gas chromatography[J].Food Anal Methods, 2012,5(3):351-358.
[3]DONG G X,YANG C Y,WAN Q Q.Simultaneously Determination of six kinds of preservatives in food by gas chromatography with AC10 bore capillary column[J].Prev Med Trib,2008,14(8):738-743.
[4]李春娟,鞠福龙,李东刚.GC-MS法同时检测葡萄酒中10种防腐剂和抗氧化剂[J].中国酿造,2009,28(6):149-152.
[5]PYLYPIW H M,GRETHER M T.Rapid high-performance liquid chromatography method for the analysis of sodium benzoate and potassium sorbate in foods[J].J Chromatogr A,2000,883(1-2):299-304.
[6]SAAD B,BARI M F,SALEH M I,et al.Simultaneous determination of preservatives(benzoic acid,sorbic acid,methylparaben and propylparaben)in foodstuffs using high-performance liquid chromatography[J]. J Chromatogr A,2005,1073(1):393-397.
[7]夏静,张敬轩,李挥.高效液相色谱法同时检测酱油中7种防腐剂[J].食品科学,2011,32(14):219-222.
[8]CHENG Y C,WANG C C,CHEN Y L,et al.Large volume sample stacking with EOF and sweeping in CE for determination of common preservatives in cosmetic products by chemometric experimental design [J].Electrophoresis,2012,33(9-10):1443-1448.
[9]郭东山,陈冠华,童明珠,等.毛细管电泳-量子点间接激光诱导荧光检测5种食品防腐剂[J].分析化学,2012,40(9):1379-1384.
[10]高文惠,裴红,杨桂君.毛细管电泳在食品添加剂检测中的应用[J].食品与生物技术学报,2010,29(3):326-330.
[11]YOSHIKAWA K,SAITO S,SAKURAGAWA A.Simultaneous analysis of acidulants and preservatives in food samples by using capillary zone electrophoresis with indirect UV detection[J].Food Chem,2011, 127(3):1385-1390.
[12]CHEN Q,HUANG J R,LING Y,et al.Fast qualitative analysis of 32 preservatives and antioxidants in food sample by comprehensive two dimensional gas chromatographycoupled time of flight mass spectrometry [J].Chinese J Anal Chem,2011,39(5):723-727.
[13]ZHANG X F,XU S X,SUN Y H,et al.Simultaneous determination of benzoic acid and sorbic acid in food products by ce after on-line preconcentration by dynamic pH junction[J].Chromatographia,2011,73 (11-12):1217-1221.
[14]龙巍然,岑怡红,王兴益,等.毛细管区带电泳法同时测定饮料中16种食品添加剂[J].色谱,2012,30(7):747-751.
[15]姚晔,邓宁,余沐洋,等.胶束电动毛细管电泳法分离检测5种β-内酰胺类抗生素[J].食品科学,2011,32(16):253-256.
[16]陈志涛.基于离子液体相互作用毛细管电泳新方法[D].重庆:重庆大学博士论文,2011.
[17]余炳生,梁广华,刘子阳,等.饮料及果品中糖精,苯甲酸,山梨酸和咖啡因的反相HPLC同时快速测定[J].食品科学,2001,22(2):67-70.
[18]高鹤娟,陈瑶君,郑鹏然.GB2760—1996食品添加剂使用卫生标准[S].北京:中国标准出版社,1997.
Separation and detection of preservatives in beverage by capillary electrophoresis
WANG Yu,YANG Siwen,DAI Yulin,DENG Ning*,WANG Yan,HE Jianbo,ZHU Yanwu
(School of Chemical Engineering,Hefei University of Technology,Hefei 230009,China)
A high performance capillary electrophoresis method was developed for the simultaneous determination of three kinds of preservatives, such as methylparaben,potassium sorbate and benzoic acid.The effect of running buffer concentration,pH,separation voltage,sampling time on electrophoretic separation was investigated.At the detection wavelength of 230 nm,the optimal separation and detection of three preservatives conditions were optimized as follows:20 mmol/L sodium borate buffer at pH 9.2,running voltage 22 kV and sampling time 15 s.Under the optimized condition,the linearly dependent coefficients of three preservatives were all greater than 0.98,and the detection limits was 1×10-2g/kg.The method has been successfully used for determination of preservatives in three kinds of beverages,and the recoveries of the preservatives were between 88%-102%.
capillary electrophoresis;preservatives;separation;detection
O657.8
A
0254-5071(2014)04-0124-05
10.3969/j.issn.0254-5071.2014.04.030
2014-03-05
国家自然科学基金资助项目(21102030)
王钰(1988-),女,硕士研究生,研究方向为工业及仪器分析。
*通讯作者:邓宁(1976-),女,副研究员,博士,研究方向为毛细管电泳、毛细管电色谱。
