含羧基官能团杂多酸盐的制备及其性能测试
2014-03-03张冷思吉海玲
张冷思,柴 文,吉海玲, 李 静
(1.常州大学石油化工学院,江苏 常州 213164;2.常熟理工学院化学与材料工程学院,江苏 常熟 215500)
含羧基官能团杂多酸盐的制备及其性能测试
张冷思1,柴 文2,吉海玲2, 李 静2
(1.常州大学石油化工学院,江苏 常州 213164;2.常熟理工学院化学与材料工程学院,江苏 常熟 215500)
设计合成氯化1-(2-丙酸基)吡啶离子液体([2-CA-PY]Cl),并通过离子交换法合成一组新型的含有羧基官能团的杂多酸盐,使用1H-NMR、IR以及XRD对合成的离子液体和杂多酸盐结构进行表征;同时,测定此类杂多酸盐的酸度及其热稳定性。结果表明:在250℃左右,合成的杂多酸盐具有较好的热稳定性;当物质量浓度为5×10-5mol/L时,此类杂多酸盐都具有较强的酸度,其中1-(2-丙酸基)吡啶磷钨酸盐的酸度最高;可以作为此类杂多酸盐酸催化性能的理论依据。
离子液体;氯化1-(2-丙酸基)吡啶;杂多酸盐;酸度;酸催化
0 引 言
离子液体是一种具有离域电荷的有机阳离子和无机阴离子组成的有机盐[1-2]。由于其优异的性能,被用作绿色化学的反应介质;同时,研究发现其作为催化剂具有可设计性强、反应速率快、反应转化率高、反应选择性好、催化体系可重复使用等优点[3],越来越多地受到人们的关注。
目前,在酸催化反应研究中发现,具有Keggin结构的杂多酸及其衍生物是一类既具有强酸性又具有强氧化性的化合物,可通过设计不同阳离子,对其酸性和氧化还原性进行调节[4]。它不但易溶于水和有机溶剂,且固态时还具有“假液相”的性质,因此可以作为理想的酸催化剂[5]。
Wang等[6]报道了含羧基官能团离子液体合成方法的研究,但合成方法复杂,产物结构表征不明确,无法对合成条件改变后的结果做出合理解释。本文期望通过改进方法和原料,合成含羧基官能团的离子液体并与杂多酸进行阴离子交换[7],得到新型的含有羧基官能团的杂多酸盐,对其结构及热稳定性进行测定分析,并使用紫外光谱法对其作为酸催化剂[7]的酸度性质进行测定。
1 实验部分
1.1 试剂和仪器
吡啶、2-氯丙酸、乙腈、磷钨酸、磷钼酸、硅钨酸,以上试剂均为分析纯。
傅里叶变换红外光谱仪(Nicolet380,Thermo公司),热重分析系统(Sta449C,Netzsch公司),核磁共振光谱仪(AVANCE300,瑞士BRUKER公司),紫外分光光度仪(UV-3600,岛津制作所),X射线衍射仪(D/max-2200PC,Rigaku公司)。
1.2 氯化1-(2-丙酸基)吡啶离子液体的合成
将2.82mL吡啶(0.035 mol)、2.58mL 2-氯丙酸(0.03 mol)和10 mL乙腈依次加入到三颈圆底烧瓶中,并连接冷凝管,油浴加热至70℃,磁力搅拌24 h后,旋转蒸发并烘干,得到有季铵结构的氯化1-(2-丙酸基)吡啶离子液体([2-CA-PY]Cl)。
1.3 1-(2-丙酸基)吡啶杂多酸盐的合成
将制得的1.77 g(0.009 1 mol)[2-CA-PY]Cl和8.66 g(0.003 0 mol)磷钨酸分别用蒸馏水溶解,不断搅拌的条件下将氯化1-(2-丙酸基)吡啶水溶液缓慢滴加到装有磷钨酸水溶液的烧瓶中,生成不溶于水的白色沉淀。滴加完成后于室温搅拌20h,反应完全后抽滤,用蒸馏水洗涤,烘干得到产物1-(2-丙酸基)吡啶磷钨酸盐([2-CA-PY]3PW12O40)。1-(2-丙酸基)吡啶的磷钼酸盐和硅钨酸盐的合成方法与之相同。本文合成的离子液体与杂多酸盐的名称及其缩写见表1。
1.4 杂多酸盐酸度测定方法
将20 μL对甲基偶氮苯指示剂加入2 mL比色皿中,再加入一定浓度的1-(2-丙酸基)吡啶杂多酸盐的乙腈溶液,静置5min,充分反应。以乙腈做参比,记录其在210~560 nm范围内紫外可见光吸收光谱[8],用以计算不同浓度1-(2-丙酸基)吡啶杂多酸盐的酸度。

表1 离子液体及其杂多酸盐的名称及缩写
2 结果与讨论
2.1 离子液体合成条件的优化及其杂多酸盐的制备
为研究离子液体[2-CA-PY]Cl合成反应的最优化条件,本文采用控制变量法,分别测定反应温度、反应时间、反应物摩尔比对产率的影响。结果如图1所示:当反应时间为24 h、反应温度为70℃、n(吡啶):n(2-氯丙酸)为1.1∶1时,[2-CA-PY]Cl的产率最高,可达到83.9%。
用制得的[2-CA-PY]Cl分别与磷钨酸、磷钼酸、硅钨酸反应,得到相应的杂多酸盐产物[2-CA-PY]3PW12O40、[2-CA-PY]3PMo12O40、[2-CA-PY]4SiW12O40,产率分别为79.7%、66.1%、68.4%。相对于磷钼酸、硅钨酸盐,1-(2-丙酸基)吡啶磷钨酸盐的产率最高。
2.2 离子液体[2-CA-PY]Cl及其杂多酸盐结构的表征
为表征离子液体[2-CA-PY]Cl的结构,分别测得其红外图谱和1H-NMR图谱。
1)[2-CA-PY]Cl红外图谱分析。从[2-CA-PY]Cl的红外图谱(如图2所示)可以看出:3 437 cm-1处为羧基上-OH的伸缩振动峰;3 131 cm-1为C-H的伸缩振动峰;1 400 cm-1为-CH3弯曲振动吸收峰;1 616 cm-1为吡啶环C=C伸缩振动峰;1 537 cm-1也为吡啶环伸缩振动峰;证明合成的离子液体中含有羧基官能团和吡啶环。图中没有C-Cl键的特征吸收峰,这表明原料2-氯丙酸上的C-Cl键发生了断裂。

图1 离子液体[2-CA-PY]Cl的优化合成条件

图2 [2-CA-PY]Cl的红外图谱图
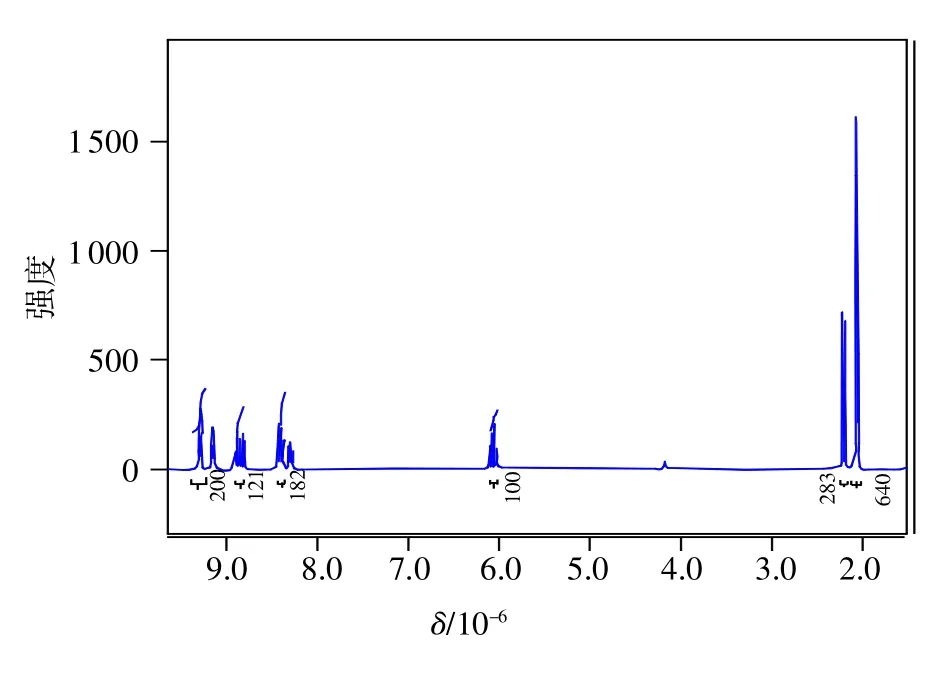
图3 [2-CA-PY]Cl的核磁图谱
2)[2-CA-PY]Cl的1H-NMR图谱分析。以氘代丙酮为溶剂,测得1H-NMR图谱如图3所示。其中δH:9.15×10-6,8.84×10-6,8.39×10-6(t,5H)为吡啶环上5个氢的化学位移;6.06×10-6(t,1H)为侧链叔碳上氢的化学位移;2.16×10-6(t,3H)为侧链上-CH3的氢化学位移;这符合吡啶与2-氯丙酸发生取代,生成吡啶氮原子与丙酸上2位碳原子结合的季铵盐的结构化学位移特征。通过1H-NMR图谱表明合成的离子液体结构符合设计的[2-CA-PY]Cl结构特点。
3)1-(2-丙酸基)吡啶杂多酸盐的结构表征
①1-(2-丙酸基)吡啶杂多酸盐的红外图谱分析。由于阴离子部分要比有机阳离子大很多,因此在杂多酸盐的红外图谱中阳离子的吸收峰不是特别明显。以[2-CA-PY]3PW12O40为例(图4),1079,981,894,808cm-1为keggin结构的PW12O403-的特征峰,对应的PMo12O403-的特征峰为1062,960,877,795cm-1,SiW12O404-的特征峰为973,918,795cm-1。这与keggin型磷钼酸和硅钨酸盐的红外特征峰的文献值[11]一致。
②1-(2-丙酸基)吡啶杂多酸盐1H-NMR图谱分析,如图5所示。由于1-(2-丙酸基)吡啶杂多酸盐的阳离子部分和[2-CA-PY]Cl的相同,以1-(2-丙酸基)吡啶磷钨酸盐为例,使用相同氘代试剂测得的1H-NMR图谱与[2-CA-PY]Cl的基本一致,表明该类杂多酸盐中1-(2-丙酸基)吡啶阳离子结构没有变化。

图4 [2-CA-PY]3PW12O40的红外图谱
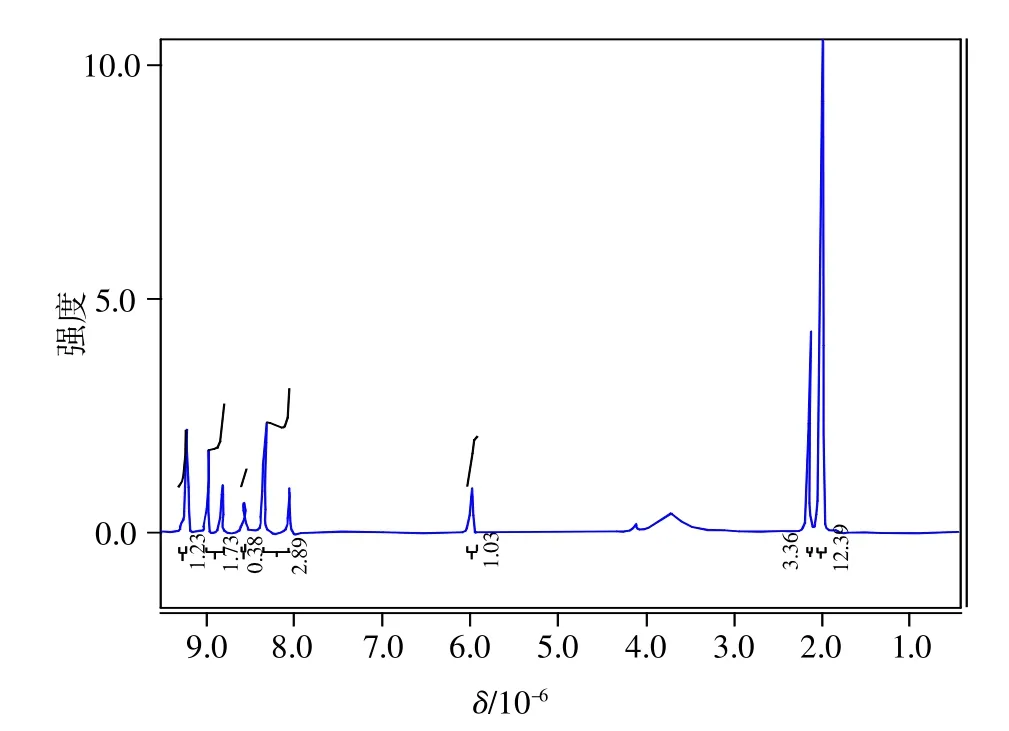
图5 [2-CA-PY]3PW12O40的1H-NMR图谱
③吡啶杂多酸盐XRD图谱分析。傅相锴课题组研究表明[9]:Keggin结构有机磷钨酸、磷钼酸、硅钨酸等杂多酸阴离子具有4大特征衍射峰,这4个峰的范围分别为7°~10°,16°~22°,25°~30°,33°~38°。通过测定制备得到的1-(2-丙酸基)吡啶杂多酸盐XRD图谱(如图6所示,以[2-CA-PY]3PW12O40的XRD图谱为例),其XRD图谱上在7°~10°,16°~22°,25°~30°,33°~38°都具有Keggin结构有机杂多酸阴离子的四大特征衍射峰,说明其阴离子部分确实保留了原来的Keggin结构。

图6 [2-CA-PY]3PW12O40的XRD图谱

图7 杂多酸盐的热失重分析
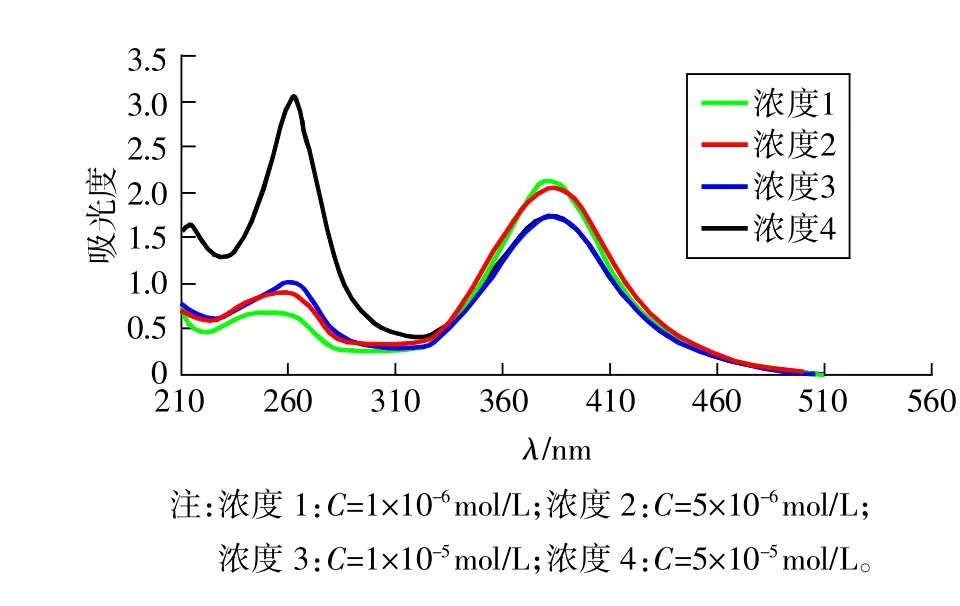
图8 4种不同浓度条件下磷钨酸盐的紫外光谱

图9 杂多酸盐浓度与H0的关系
胡小玲等[10]的研究也表明,由于杂多酸盐阴离子上存在大量的氧原子,因此在形成季铵类杂多酸盐时,除了离子键作用以外,季铵和杂多酸盐阴阳离子之间还通过氢键结合,使它们的相互结合更加紧密,同时也保证了杂多酸阴离子的Keggin结构不会被破坏,这与本文对1-(2-丙酸基)吡啶杂多酸盐的结构表征结果相符。
综上所述,1-(2-丙酸基)吡啶杂多酸盐的1H-NMR图谱表明其结构中存在1-(2-丙酸基)吡啶阳离子结构,其IR、XRD图谱表明该类杂多酸盐保留了原来Keggin结构的杂多酸阴离子,该类杂多酸盐的结构符合设计的预期。
2.3 1-(2-丙酸基)吡啶杂多酸盐性能测试研究
2.3.1 热失重分析
热稳定性是酸催化剂的一个重要性能,可通过热失重分析来表征。由图7可知,[2-CA-PY]3PW12O40的热失重分解主要有两个阶段,第1阶段为250~300℃,第2阶段为350~500℃。[2-CA-PY]3PMo12O40的热分解可以观察到两个失重区间,300~550℃是阳离子发生了分解,其显著失重出现在500℃以上区域。[2-CA-PY]4SiW12O40的热分解也分为两个阶段,第1阶段为300~350℃,第2阶段从350~600℃。
由此可知,这3种吡啶类杂多酸盐在0~250℃都保持了很好的热稳定性,因此,作为催化剂时不会因为温度过高而分解,不会导致催化性能的下降。
2.3.2 酸度分析
酸度是衡量酸催化剂性能的一个重要参数,由于pH计在非水溶液中测试的局限性,使用紫外光谱法测定合成杂多酸盐在乙腈溶剂中的酸度值。在杂多酸盐溶液中加入一定量的Hammett指示剂溶液,利用它与酸性杂多酸盐反应得到平衡关系:BH+⇌B+ H+,定义出酸函数为:H0=pKa+log[B]/[BH+]。其中pKa值为指示剂的pKa值,测定出指示剂碱性活度B与其共轭酸的活度的比值即可得到杂多酸盐的酸函数。在紫外光谱上,酸性物种、碱性物种吸光度的比值即为[B]/[BH+],由此得到杂多酸盐酸函数H0。以1-(2-丙酸基)吡啶磷钨酸盐的紫外图谱为例(图8),在210~310nm处其峰强度最大处的吸光度对应着碱性物种的值,310~460nm处其峰强度最大处的吸光度对应着酸性物种的值,通过两者之比可计算出1-(2-丙酸基)杂多酸盐的H0。
由图9、表2可知:这3种杂多酸盐的酸度都是随着浓度的增大而逐渐变强。由于Keggin结构的杂多酸盐可以让氢离子自由流动,且杂多酸-离子液体中阴阳离子还通过氢键作用使得相互间的连接更加紧密[10];与固载类杂多酸相比,所合成的该类杂多酸盐在乙腈溶液中均有着较高的酸度值[12],当其物质量浓度达到5×10-5mol/L时,[2-CA-PY]3PW12O40的酸度最强,符合酸催化剂使用的浓度要求。

表2 不同浓度下杂多酸盐的H0值
3 结束语
本文改进了含羧基离子液体的合成方法,设计合成了一组新型的含有羧基官能团的杂多酸盐。通过1H-NMR、IR、XRD图谱对合成产物进行结构表征,确定了卤代酸C-Cl键断裂后与吡啶上N原子形成季铵盐结构,并生成了相应的1-(2-丙酸基)吡啶杂多酸盐。通过紫外光谱法测定1-(2-丙酸基)吡啶杂多酸盐的H0值,获得其在溶液中的酸度信息,对杂多酸盐性质的研究有重要的理论意义和学术价值。同时,通过性能测试研究发现此类杂多酸盐具有良好的热稳定性和较强的酸度,可作为酸催化剂使用,具有较好的应用前景。
[1]Rogers R D,Seddon K R.Ionic liquids-solvents of the future[J].Science,2003,302:792-793.
[2]Wasserscheid P, Keim W.Ionic liquids-new“Solutions”for transition metal catalysis[J].Angew Chem Int Ed,2000,39(21):3772-3789.
[3]张锁江,徐春明,吕兴梅,等.离子液体与绿色化学[M].北京:北京科学出版社,2009:3-8.
[4]张烨红.Keggin型杂多酸相转移催化剂的合成、表征及催化性能研究[D].兰州:兰州理工大学,2009.
[5]亢世杰.磷钨酸盐催化剂的制备表征及应用研究[D].哈尔滨:哈尔滨工程大学,2007.
[6]Zhou H Y,Gu T L,Yang D G,et al.Synthesis and characterization of novel ester functionalized chiral ionic liquids[J].Advanced Materials Research,2011(197-198):471-477.
[7]Leng Y,Wang J,Zhu D R,et al.Polyoxometalatebased amino-functionalized ionic solid catalysts lead to highly efficientheterogeneous epoxidation ofalkenes with H2O2[J].Green Chem,2011,12(7):1636-1639.
[8]谢文华,叶兴凯,杨向光,等.紫外光谱法测定杂多酸的酸强度[J].化学世界,1996(9):490-491.
[9]陈静蓉.Keggin型有机膦酸-钨杂多酸的合成、表征及性质研究[D].广西:西南师范大学,2001.
[10]赵亚梅,胡小玲,管萍.离子液体1-仲丁基-3-甲基咪唑六氟磷酸盐的微波辅助合成[J].高等学校化学学报,2009,9(30):1814-1818.
[11]柴文,周虞峰,陈吕莉,等.4-甲基吡啶杂多酸盐的合成及其酯化催化性能的研究[J].常熟理工学院院报,2012,26(4):10-15.
[12]赵景联,赵靓,苏慈,等.SiW12/NaY固体杂多酸催化剂的微波合成及LAS降解性能研究[J].化学世界,2006(6):321-324.
Preparation of heteropolyacid salts containing carboxyl functional groups and its properties
ZHANG Leng-si1,CHAI Wen2,JI Hai-ling2,LI Jing2
(1.School of Petrochemical Engineering,Changzhou University,Changzhou 213164,China;2.School of Chemistry&Materials Engineering,Changshu Institute of Technology,Changshu 215500,China)
This paper designed and synthesized the ionic liquid of chlorinated 1-(2-propionyloxy)pyridine([2-CA-PY]Cl),then exchanged the anion of the ionic liquid with heterop-olyacids to design a new kind of heteropolyacid salts containing carboxylic groups.The structures of the ionic liquid and the heteropolyacid salts were characterized by 1H-NMR,IR or XRD spectra,and the kind of heteropolyacid salts’properties including acid strength and thermostability were tested.The study shows that all of the heteropolyacid salts had good thermostability under 250℃. 1-(2-propionyloxy) pyridine phosphotungstate performed strongest acid strength when its concentration is 5×10-5mol/L.In conclusion,all of the three heteropolyacid salts can be used as catalysts,the results can be used as theoretical foundation for these heteropolyacid salts in catalytic reactions.
ionic liquid;chlorinated 1-(2-Propionyloxy) pyridine;heteropolyacid salt;acid strength;acidic catalysis
O621.2;O623.25;O657.33;TB99
:A
:1674-5124(2014)05-0047-05
10.11857/j.issn.1674-5124.2014.05.012
2013-12-11;
:2014-01-24
张冷思(1988-),男,江苏盐城市人,硕士研究生,专业方向为环境友好型有机合成。
