退变性腰椎滑脱症伴发滑脱椎体骨折的手术治疗
2014-02-13王辉马雷丁文元申勇张迪杨大龙
王辉 马雷 丁文元 申勇 张迪 杨大龙
退变性腰椎滑脱症伴发滑脱椎体骨折的手术治疗
王辉 马雷 丁文元 申勇 张迪 杨大龙
目的 探讨骨水泥强化下腰后路减压植骨融合内固定术治疗退变性腰椎滑脱症伴滑脱椎体骨折的有效性。方法 回顾性分析 2007 年 7 月至 2011 年 3 月,于我院行手术治疗的 17 例退变性腰椎滑脱症合并滑脱椎体压缩骨折患者的临床及影像学资料,所有患者均表现为腰痛伴或不伴有下肢神经根刺激症状,MRI 证实滑脱椎体 T2加权像及 STIR 序列高信号。记录患者的手术时间、出血量、并发症及骨水泥的注入量。采用 Taillard 指数评估椎体滑脱程度及术后复位情况,采用疼痛视觉模拟评分评估手术前后腰痛的程度。结果 所有患者均获得 1 年以上随访,骨水泥的注入量平均 ( 4.2±0.7 ) ml,手术时间平均为 ( 167±28 ) min,术中出血量平均为 ( 708±45 ) ml,腰痛 VAS 评分术后 1 年随访时改善为 ( 4.6±0.2 ) 分,术前 Taillard 指数平均为 ( 17.6±1.8 ) %,术后为 ( 8.2±1.3 ) %,滑脱复位率为 53.4%;所有病例均未发生严重骨水泥渗漏及神经血管并发症,末次随访时植骨均已融合,未发现椎间融合器移位及螺钉松动、断裂、脱出等内固定物相关并发症。结论 骨水泥强化下腰后路减压植骨融合内固定术,是治疗退变性腰椎滑脱症伴滑脱椎体骨折的有效方法,骨水泥的应用增加了椎弓根螺钉把持力,彻底的减压及植骨融合改善了神经刺激症状,疗效确切。
骨水泥成形术;减压术,外科;骨折固定术,内; 脊柱融合术;脊椎滑脱;脊柱骨折;腰椎
退变性腰椎滑脱症常见于老年人,当出现明显的椎管狭窄症状如间歇性跛行等和 ( 或 ) 出现下肢的神经刺激症状,经严格保守治疗无效时,常需手术治疗[1-5]。我们在临床实践中发现,少数退变性腰椎滑脱的椎体核磁共振 T1WI 呈低信号,T2WI 和( 或 ) STIR 序列上呈高信号,提示椎体发生了骨折。此类患者往往有外伤史,临床表现为腰痛症状和下肢神经刺激症状并存,由于老年人对疼痛的敏感度较低,骨折引起的腰痛可能被滑脱导致的神经刺激症状所掩盖,既往文献中对于此类患者的治疗原则及疗效分析未见报道。
为同时解决腰椎滑脱引起的神经刺激症状和椎体骨折引起的腰痛症状,我们采用骨水泥强化下腰后路减压植骨融合内固定术 ( posterior lumbar interbody fusion,PLIF )。一方面通过向骨折椎体内注入骨水泥,在增加椎弓根螺钉把持力的同时改善骨折引起的腰痛症状;另一方面 PLIF 手术通过彻底的减压改善神经刺激症状,提高手术的综合疗效。本研究采用此方法治疗退变性腰椎滑脱症合并椎体骨折患者 17 例,目的在于评估骨水泥强化下 PLIF 手术治疗退变性腰椎滑脱症伴滑脱椎体骨折的有效性,并总结骨水泥强化下 PLIF 手术的操作要点。
资料与方法
一、一般资料
回顾性分析 2007 年 7 月至 2011 年 3 月,于我院行手术治疗的 17 例退变性腰椎滑脱症合并滑脱椎体压缩骨折患者的临床及影像学资料,男 5 例,女12 例,年龄 56~73 岁,平均 ( 63.2±4.3 ) 岁,所有患者均表现为腰痛及下肢神经根刺激 ( 麻木、憋胀、疼痛等 ) 症状。其中,左侧 5 例,右侧 7 例,双侧 5 例。有明确外伤史者 15 例,受伤至手术的时间为 3~67 天。所有患者均为经 3 个月严格保守治疗 ( 卧床、口服止痛药物、理疗等 ),且无效者。术前 X 线片证实均为 L4椎体的退变性滑脱,MRI 证实存在椎管狭窄及滑脱椎体的压缩骨折 ( T2加权像及STIR 序列表现为高信号 )。所有患者均于全麻下接受骨水泥强化腰后路减压植骨融合内固定术。
二、手术方法
所有手术均由同一组手术医师完成,患者全麻后取俯卧位,常规消毒铺巾,约平髂棘连线为中心行腰后路正中纵切口,长约 15 cm,棘突及椎板骨膜下剥离椎旁肌,清晰显露至 L4及 L5双侧关节突外缘。以“人字脊”法定位并植入双侧 L5椎弓根螺钉,同法于 L4椎体双侧的“人字脊”处以皮质骨开口器破开皮质骨,将椎弓根扩椎经开口的皮质骨裂口处进入并通过椎弓根扩入椎体内,术中 C 型臂透视并调整椎弓根扩椎的方向及角度,拔出扩椎后,以注射器将“拉丝状”骨水泥经扩椎通道注入 L4椎体内,待骨水泥凝固前迅速经扩椎通道拧入椎弓根螺钉,C 型臂监视骨水泥的渗漏情况。咬除 L4棘突、椎板及部分下关节突充分减压后,探查是否发生骨水泥椎管内渗漏,必要时行唤醒实验。完整取出 L4~5髓核行椎间松解,采用钉棒适当提拉复位,刮除软骨终板,于椎间隙植骨并放入合适大小的椎间融合器 1 枚,连接钉棒后锁紧,冲洗后查无活动性出血,留置引流并逐层缝合,术后 24 h 内常规应用抗生素,24~48 h 视伤口引流情况拔除引流管,术后 1 周带腰围下地活动,腰围佩戴 2 个月。
三、评价指标
记录患者的手术时间、出血量以及并发症的情况,记录骨水泥的注入量。采用 Taillard 指数[6]评估椎体滑脱程度及术后复位情况,Taillard 指数=滑移距离 ( AB ) 与下位椎体上缘矢状径 ( AC ) 的比值。滑脱复位率=( 术前 Taillard 指数-术后 Taillard 指数 ) / 术前 Taillard 指数 (图1 )。采用疼痛视觉模拟评分 ( visual analog scale,VAS ) 评估手术前后腰痛的改善。0 分表示无痛,10 分表示难以忍受的剧痛。术后第 3、6、12 个月于门诊复查,评估腰痛 VAS评分、行腰椎正侧位 X 线片检查,测量椎体滑脱复位程度。

图1 腰椎滑脱程度 ( Taillard 指数 ):滑移距离 ( AB ) 与下位椎体上缘矢状径 ( AC ) 的比值Fig.1 The degree of lumbar spondylolisthesis ( the Taillard index ): the slide distance ( AB ) and the ratio of the sagittal diameter on the superior border of the lower vertebral body ( AC )
四、统计学分析
结 果
所有患者均获 14~17 个月随访,骨水泥的注入量为 3~6 ml,平均 ( 4.2±0.7 ) ml。手术时间 125~210 min,平均为 ( 167±28 ) min,术中出血量 550~860 ml,平均为 ( 708±45 ) ml,腰痛 VAS 评分术前 4~8 分,平均为 ( 6.4±0.4 ) 分,术后 1 年随访时 1~3 分,平均为 ( 1.8±0.2 ) 分,疼痛改善为( 4.6±0.2 ) 分;术前 Taillard 指数 13%~23%,平均为 ( 17.6±1.8 ) %,术后 1 年随访时平均为 ( 8.2± 1.3 ) %,滑脱复位率为 53.4%;所有病例均未发生严重骨水泥渗漏及神经血管并发症,末次随访时植骨均已融合,未发现椎间融合器移位及螺钉松动、断裂、脱出等内固定物相关并发症。1 例患者发生伤口愈合不良及高热,引流液培养未发现细菌生长,经换药对症处理后痊愈出院 (图2 )。
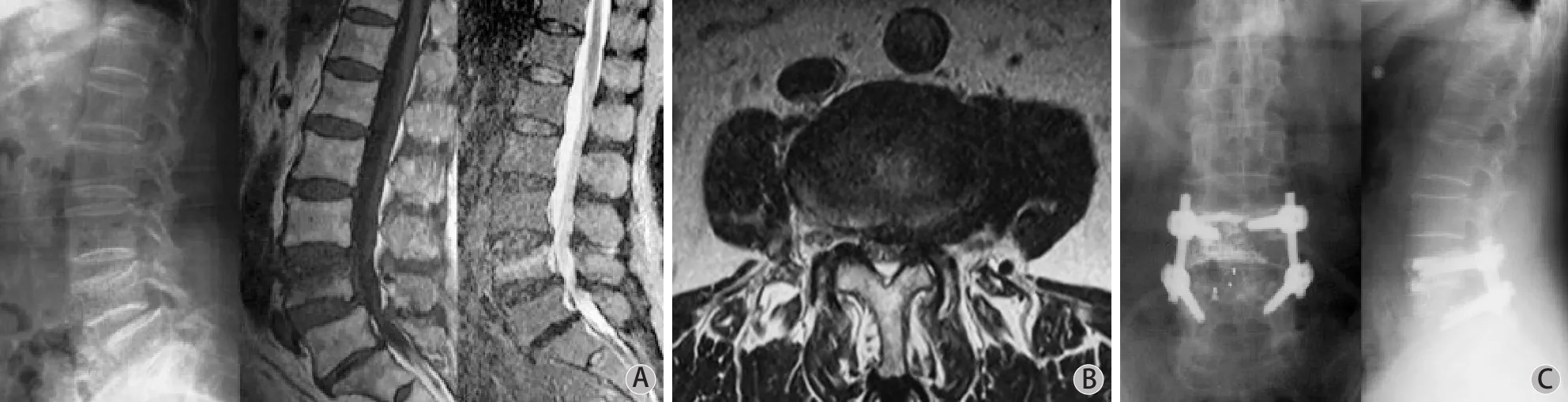

图2 患者,女,65 岁,腰痛伴左下肢疼痛 3 年入院A:术前 X 线片示 L4 椎体滑脱伴轻度楔形变,Taillard指数为 17%;B:矢状位 MRI 显示 L4 椎体 T1 加权像低信号和 STIR 序列高信号,水平位 MRI 显示 L4~5 左侧椎间孔狭窄,神经根受压明显;C~D:术后 X 线片及CT 证实椎弓根钉棒及骨水泥位置良好,Taillard 指数为8%,无骨水泥渗漏发生;E:术后 12 个月 X 线片未见钉棒松动脱出等并发症,椎间植骨融合良好Fig.2 A 65-year-old female patient with low back pain combined with pain in the left lower limb for 3 years before admission A: The preoperative X-ray showed L4 spondylolisthesis combined with slight wedging, and the Taillard index was 17%; B: The sagittal MRI showed low signal of L4 vertebral body on T1-weighted images and high signal of the STIR sequence. The horizonal MRI showed foraminal stenosis in the left side of L4-5 and obvious nerve root compression; C-D: The postoperative X-ray and CT showed good position of pedicle screws and PMMA. The Taillard index was 8%, and no leakage of bone cement occurred postoperatively; E: The X-ray at the 12th month after the operation showed no loose or slipping out of screws and rods, with good interbody fusion
讨 论
退变性腰椎滑脱症同时发生滑脱椎体骨折在临床中并非少见,典型的临床特征为神经刺激症状与腰痛症状并存。在滑脱和骨折发生的先后顺序上,由于退变性腰椎滑脱是一个慢性的病理过程,影像学显示滑脱节段椎管或神经根管狭窄明显,下肢神经刺激症状往往长期存在,部分患者有近期明确的外伤史,MRI 显示滑脱椎体 T2加权像及 STIR 序列表现为高信号,因此,我们认为退变性腰椎滑脱先于椎体骨折而发生。椎体滑脱和骨折均可引起腰痛,腰椎滑脱所导致的腰痛往往是由于椎间不稳或椎间盘源性疼痛,而椎体骨折所导致的腰痛则主要是由于椎体内微小骨折的异常错动。由于此类患者多数年龄较大,对疼痛的敏感性较低,所表现出的腰痛症状常常不明显或被下肢神经刺激症状所掩盖,对于疼痛源的判定和治疗方案的选择造成了困难。
腰后路减压椎间植骨融合内固定术是治疗腰椎管狭窄症的经典术式,通过减压可有效地改善神经刺激症状,椎间植骨融合确保了脊柱的长期稳定性,内固定的使用实现了滑脱复位及脊柱生理曲度的重建和维持[7-11]。但是当退变性腰椎滑脱合并发生滑脱椎体骨折时,骨折椎体对椎弓根螺钉的把持力大大降低,术后发生钉棒松动及脱出等内固定物失败的风险更高。此外,如果忽视骨折而单纯采取手术减压和复位治疗,术后往往因为神经症状的改善而导致腰痛症状的突显,影响了手术的综合疗效。
对于骨质疏松性椎体压缩骨折的治疗,经皮椎体成形术 ( percutaneous vertebroplasty,PVP ) 和经皮椎体后凸成形术 ( percutaneous kyphoplasty,PKP ) 通过经皮穿刺向骨折椎体内注入“拉丝状”骨水泥,恢复椎体高度的同时固定了椎体内的微小骨折,使其活动时不再挤压和刺激神经末梢从而缓解疼痛[12-17],骨水泥在聚合反应时释放的热效应以及骨水泥单体所具有的细胞毒性,破坏了椎体内的神经末梢也可起到止痛作用[18-21]。当退变性腰椎滑脱与椎体骨折同时存在时,单纯应用微创技术将骨水泥注入椎体内,虽然可以缓解骨折引起的腰痛,但是骨水泥的注入会显著增加骨折椎体的弹性模量,与邻近骨质疏松椎体之间形成明显的刚度差异,应力的集中可能会加重局部的不稳。
本研究采用骨水泥强化下 PLIF 手术治疗退变性腰椎滑脱症合并椎体骨折,术中首先采用 PLIF 手术入路,行脊柱后方结构的显露,按照腰椎椎弓根螺钉的置钉方法,以皮质骨开口器破开骨折椎体“人字脊”处的皮质骨,采用椎弓根扩椎经开口的皮质骨裂口处进入并通过椎弓根扩入椎体内,形成骨水泥注入和椎弓根螺钉拧入的共同通道,直视下将“拉丝状”骨水泥注入骨折椎体内。相比于 PVP 或PKP 手术时需要在术中透视下应用穿刺导针和管芯建立骨水泥注入的工作通道,本方法术中直视下注入骨水泥,节约了微创操作器械的使用,降低了微创手术穿刺风险和费用,同时也减少了术中透视的次数。由于在椎弓根螺钉拧入过程中骨水泥发生了凝固,螺钉的方向和位置不宜调整,术前通过分析骨折椎体的压缩程度以制定进针的位置,术中 X 线透视调整进针角度,避免在骨水泥注入过程中发生渗漏等并发症。骨水泥的应用,一方面在于通过其热效应和细胞毒性实现止痛作用,另一方面增加了骨折椎体对于椎弓根螺钉的把持力,避免了术后螺钉松动及脱出等并发症的出现。
文献 [22-23] 报道骨水泥的注入量与疼痛缓解程度并不呈正相关,而与骨水泥的渗漏呈正相关。每个椎体注入骨水泥的量只需达到椎体体积的15%,其强度即可恢复到损伤前的水平[24]。本组资料骨水泥的注入量平均 4.2 ml,术中及术后透视均未发生明显的骨水泥渗漏。退变性腰椎滑脱的病史较长,在其形成和长期的发展过程中,周围的组织结构会逐渐发生适应性改变,具有对抗牵拉复位、维持滑脱的固有应力,如强行复位会破坏已适应的解剖关系,导致术后神经根紧张及神经牵拉损伤等并发症[25]。虽然骨水泥的使用增加了椎弓根螺钉的把持力,但术中我们并没有强求滑脱椎体的完全复位,而是通过对狭窄部位的彻底减压来实现神经症状的改善,术后随访期间均未出现原有神经症状的加重,疗效满意。
本研究采用回顾性分析方法,尽管术前 X 线检查可见多数患者椎体存在骨质疏松现象,但由于术前只是部分患者接受了骨密度检查,因此,骨质疏松在退变性腰椎滑脱症合并椎体骨折发病中的作用及对术后疗效的影响有待于进一步前瞻性的病例观察。
[1] Grados F, Depriester C, Cayrolle G, et a1. Long-term observations of vertebral osteoporotic fractures treated by percutaneous vertebroplasty. Rheumatology, 2000, 39(12):1410-1414.
[2] Majid K, Fischgrund JS. Degenerative lumbar spondylolisthesis: trends in management. J Am Acad Orthop Surg, 2008, 16(4):208-215.
[3] Iguchi T, Wakami T, Kurihara A, et al. Lumbar multilevel degenerative spondylolisthesis: radiological evaluation and factors related to anterolisthesis and retrolisthesis. J Spinal Disord Tech, 2002, 15(2):93-99.
[4] Sengupta DK, Herkowitz HN. Degenerative spondylolisthesis: review of current trends and controversies. Spine, 2005, 30(6 Suppl):S71-81.
[5] Lee JH, Kim KT, Suk KS, et al. Analysis of spinopelvic parameters in lumbar degenerative kyphosis: correlation with spinal stenosis and spondylolisthesis. Spine, 2010, 35(24): 1386-1391.
[6] Taillard WF. Etiology of spondylolisthesis. Clin Orthop Relat Res, 1976, 117:30-39.
[7] Huang KY, Lin RM, Lee YL, et al. Factors affecting disability and physical function in degenerative lumbar spondylolisthesis of L4-5: evaluation with axially loaded MRI. Eur Spine J, 2009, 18(12):1851-1857.
[8] Klocker C, Weber U. Correction of lunbosacral kyphosis in high grade spondyblisthesis and spondybptosis. Orthopade, 2001, 30(12):983-987.
[9] Madan SS, Harlry JM, Boeree NR. Circumferential and posterolateral fusion for lumbar disc disease. Clin Orthop Relat Res, 2003, 209:114-123.
[10] Wang JC, Mummaneni PV, Haid RW. Current treatment strategies for the painful lumbar motion segment: posterolateralfusion versus interbody fusion. Spine (Phila Pa 1976), 2005, 30(16 Suppl):S33-43.
[11] Yu CH, Wang CT, Chen PQ. Instrumented posterior lumbar interbody fusion in adult spondylolisthesis. Clin Orthop Relat Res, 2008, 466(12):3034-3043.
[12] Belkof SM, Mathis JM, Erbe EM, et a1. Biomechanical evaluation of a new bone cement for use in vertebroplasty. Spine, 2000, 25(9):1061-1064.
[13] Coumans JV, Reinhardt MK, Lieberman IH. Kyphoplasty for vertebral compression fractures: 1-year clinical outcomes from a prospective study. J Neurosurg, 2003, 99(1):44-50.
[14] Hierholzer J, Fuchs H, Westphalen K, et a1. Incidence of symptomatic vertebral fractures in patients after percutaneous vertebroplasty. Cardiovasc Intervent Radiol, 2008, 31(6): 1178-1183.
[15] Lindsay R, Silverman SL, Cooper C, et a1. Risk of new vertebral fracture in the year following a fracture. JAMA, 2001, 285(3):320-323.
[16] Pflugmacher R, Schroeder RJ, Klostermann CK. Incidence of adjacent vertebral fractures in patients treated with balloon kyphoplasty: two years prospective follow-up. Acta Radial, 2006, 47(8):830-840.
[17] Pitton MB, Herber S, Bletz C, et a1. CT-guided vertebroplasty in osteoporotic vertebral fractures: incidence of secondary fractures and impact of intradiscal cement leakages during follow-up. Eur Radial, 2008, 18(1):43-50.
[18] Komemushi A, Tanigawa N, Kariya S. Percutaneous Vertebroplasty for osteoporotic compression fracture: multivariate study of predictors of new vertebral body fracture. Cardiovase lntervent Radiol, 2006, 29(4):580-585.
[19] Lin EP, Ekholm S, Hiwatashi A, et a1. Vertebroplasty: Cement leakage into the disc increases the risk of new fracture of adjacent vertebral body. Am J Neuroradiol, 2004, 25(2): 175-180.
[20] Berlemann U, Ferguson SJ, Nolte LP, et al. Adjacent vertebral failure after vertebroplasty: a biomechanical investigation. J Bone Joint Surg , 2002, 84(5):748-752.
[21] Villarraga ML, Bellezza AJ, Harrigan TP, et al. The biomechanical effects of kyphoplasty on treated and adjacent nontreated vertebral bodies. J Spinal Disord Tech, 2005, 18(1):84-91.
[22] Cotten A, Dewatre F, Cortet B, et a1. Percutaneous vertebroplasty for osteolytic metastases and myeloma: effects of the percentage of lesion filling and the leakage of methylmethacrylate at clinical follow-up. Radiology, 1996, 200(2):525-530.
[23] Kaufmann TJ, Trout AT, Kallmes DF, et al. The effects of cement volume on clinical outcomes of percutaneous vertebroplasty. AJNR Am J Neuroradiol, 2006, 27(9):1933-1937.
[24] Lieberman H, Dudeney S, Reinhardt M, et a1. Initial outcome and efficacy of kyphoplasty in the treatment of painful osteoporotic vertebral compression fracture. Spine, 2001, 26(14):1631-1638.
[25] Csecsei GI, Klekner AP, Dobai J, et al. Posterior interbody fusion using laminectomy bone and transpedicular screw fixation in the treatment of lumbar spondylolisthesis. Surg Neurol, 2000, 53(1):2-6.
( 本文编辑:马超 )
本刊正式被美国化学文摘数据库收录公告
本刊现为中国科技论文统计源期刊。2013 年 1 月,本刊经美国化学文摘数据库审理委员会审核通过,并从2013 年第 1 期开始,正式被美国化学文摘数据库收录。
特此公告!
《中国骨与关节杂志》编辑委员会
Surgical treatment of degenerative lumbar spondylolisthesis combined with vertebral fractures
WANG Hui, MA Lei, DING Wen-yuan, SHEN Yong, ZHAGN Di, YANG Da-long. Department of Spinal Surgery, the third Hospital of Hebei Medical University, Shijiazhuang, Hebei, 050051, PRC
ObjectiveTo explore the effects of posterior lumbar interbody fusion ( PLIF ) and polymethylmethacrylate ( PMMA ) for degenerative lumbar spondylolisthesis combined with vertebral fractures.Methods17 patients with degenerative lumbar spondylolisthesis combined with vertebral compression fractures underwent the surgical treatment of PLIF and PMMA in our hospital from July 2007 to March 2011, whose clinical and imaging data were retrospectively analyzed. All the patients complained of low back pain with or without nerve root irritation of lower limbs. The Magnetic Resonance Imaging ( MRI ) showed high signal on T2-weighted images and of the Software for Tomographic Image Reconstruction ( STIR ) sequence. The surgery time, blood loss, complications, cement amount of the patients were recorded. The Taillard index was used to evaluate the spondylolisthesis degree and the postoperative reduction, and the Visual Analogue Scale ( VAS ) to assess the degree of low back pain before and after the operation.ResultsAll the patients were followed up for more than 1 year. The mean cement amount was ( 4.2±0.7 ) ml, the mean operation time was ( 167±28 ) min, and the mean intraoperative blood loss was ( 708± 45 ) ml. The VAS score of low back pain was improved to ( 4.6±0.2 ) points at the 1st year after the operation, and the mean Taillard index was ( 17.6±1.8 ) % and ( 8.2±1.3 ) % preoperatively and postoperatively. The reduction rare of spondylolisthesis was 53.4%. No severe leakage of bone cement or neurovascular complications occurred in all the patients. Bony fusion was achieved, and no complications such as the displacement of the cage or the loose, breakage or slipping out of screws were found in the latest follow-up.ConclusionsIt is an effective method of PLIF and PMMA in the treatment of degenerative lumbar spondylolisthesis combined with vertebral fractures, with good curative effects. The holding force of pedicle screws is increased after the usage of PMMA, and the nerve root irritation is improved by the complete decompression and interbody fusion.
Cementoplasty; Decompression, surgical; Fracture fixation, internal; Spinal Fusion; Spondylolysis; Spinal Fractures; Lumbar vertebrae
10.3969/j.issn.2095-252X.2014.01.001
R681, R683.2
050051 石家庄,河北医科大学第三医院脊柱外科,河北省骨科生物力学重点实验室
丁文元,Email: dingwenyuan2012@126.com
2013-07-10 )
