两台国产生化仪器在常规试验室的精密度性能评价
2014-02-06成景松朱小莉陕西省安康市白河县人民医院检验科725800
成景松,朱小莉(陕西省安康市白河县人民医院检验科 725800)
生化仪器厂家在出厂时提供了检测系统的分析性能的资料,数据和结论说明检测系统的分析性能符合临床要求,才允许出厂。但是,投入到具体的常规实验室,由于检测条件的改变,比如温度、电压波动、试剂的改变,必须在实验室的具体条件下,用实验去证实检测系统的基本分析性能[1-2]。基于此目的,现将投入运行的两台国产生化仪器在常规条件下对其方法性能进行评价,从而评判这些常规项目的服务质量。
1 材料与方法
1.1 检测仪器 梅州康立AFT-500E电解质分析仪(以下简称仪器1)和深圳迈瑞BS-800全自动生化分析仪(以下简称仪器2)。
1.1.1 AFT-500E分析项目及使用试剂 分析钾(K)、钠(Na)、氯(Cl)、钙(Ca)4个项目,校准液和质控液为康立公司原装配套,方法为直接离子选择性电极法。
1.1.2 BS-800分析项目及使用试剂 检测总胆红素(TBIL,采用重氮法)、总蛋白(TP,采用双缩脲法)、清蛋白(ALB,采用溴甲酚绿法)、丙氨酸氨基转移酶(ALT,采用连续监测法)、天门冬氨酸氨基转移酶(AST,采用连续监测法)、碱性磷酸酶(ALP,采用连续监测法)、γ-谷氨酰基转移酶(γ-GT,采用γ-谷氨酰4硝基苯胺连续监测法)、尿素(Ure,采用脲酶紫外速率法)、肌酐(Cr,采用苦味酸法)、尿酸(UA,采用尿酸酶紫外法)、糖(GLU,采用氧化酶法)、总胆固醇(TC,采用氧化酶法)、三酰甘油(TG,采用GPO-PAP酶法)、高密度脂蛋白胆固醇(HDLC,直接一步法)、淀粉酶(AMY,采用麦芽七糖苷底物酶法)、肌酸激酶(CK,采用N-乙酰半胱氨酸连续监测法)、乳酸脱氢酶(LDH,采用LDH-L连续监测法)、磷(P,采用磷钼酸紫外法)18个项目。除AMY、CK试剂分别为浙江伊利康生物技术有限公司和上海科华生物工程股份有限公司提供外,剩下16个项目试剂均为迈瑞公司配套试剂。18个项目用迈瑞复合校准品进行校准。质控品为英国RANDOX人基质定值质控血清。
1.2 方法 所有分析项目按照仪器和试剂原厂家配套说明书设置和操作,用Westgard多规则控制方法进行常规室内质控[3],并且根据室内质控规则进行重新定值[4]。根据美国临床和实验室标准协会(CLSI)发布的EP5-A2(临床化学设备操作精密度评价标准指南)文件进行实验操作,每天对稳定的试验样品(冻干人血清)测定2次(2次测定时间间隔大于2h),每次测定2遍,共测定20d,取得80个数据,结果剔除离群值[5],计算批内、批间不精密度标准差(s)。以实验获得的批内不精密度分别与厂家声明的批内不精密度和1/4CLIA′88(美国临床实验室改进修正法规室间评估指标)指标比较,以实验获得的批间不精密度分别与厂家声明的批间不精密度和1/3CLIA′88指标比较,并且作χ2检验,判断可接受性。
2 结 果
22个常规生化项目中,(1)批内精密度:P不能接受厂家声明的批内精密度性能和CLIA′88固定限指标的1/4,5个项目即Na、TC、GLU、Ure、ALB不能接受CLIA′88固定限指标的1/4。(2)批间精密度:ALT不能接受厂家声明的批间精密度性能,3个项目即Cl、Na、Ure不能接受CLIA′88固定限指标的1/3。结果见表1。
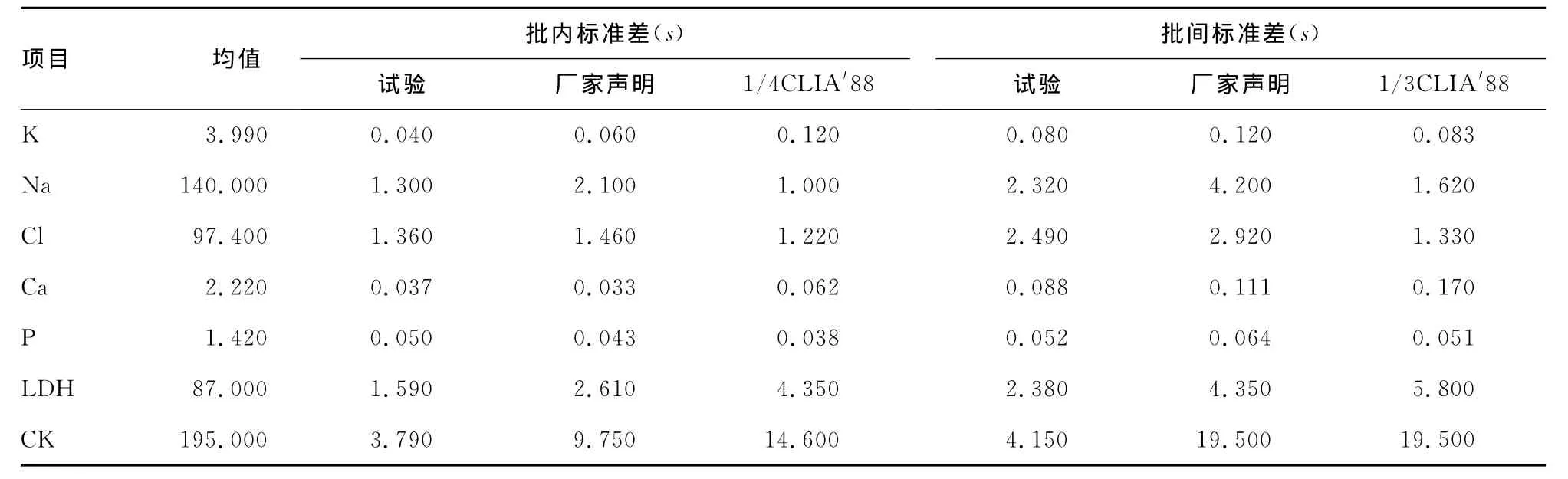
表1 不精密度试验结果及厂家声明不精密度和CLIA′88指标

续表1 不精密度试验结果及厂家声明不精密度和CLIA′88指标
3 讨 论
3.1 按照CLSI出版的EP5-A2文件评价实验室现用方法的精密度,可准确、客观的得出各项目批内、批间、天间和总不精密度,为了简单起见,按文献介绍,可按EP5-A2文件进行实验,然后直接对所有数据作均值和标准差的统计,求出批间的变异(即总不精密度)[6]。著名的Westgard和Ceroblewski等提出高效检验对精密度要求的观点,从中引出批内不精密度CV应是CLIA指标的1/4,批间不精密度CV应是CLIA指标的1/3,做法简单、明确。所以从20世纪90年代起,国际上推荐使用总不精密度,并且为了更好地检出不稳定的误差,已明确提出检测系统的批内标准差s应为美国的临床实验室室间质量评估允许误差(TE,允许总误差)即CLIA′88的1/4,批间标准差s应为该允许误差的1/3。1/4允许误差范围为批内不精密度判断限,1/3允许误差范围为批间不精密度判断限,小于或等于判断限的,检测系统的不精密度属可接受;大于判断限的表示不精密度不符合要求。达到这样要求的检测系统,可认为它的随机误差属于可接受的低水平[7-8]。
3.2 与厂家声明的精密度性能指标比较,在常规条件下,只有P不能接受厂家声明的批内精密度性能,ALT不能接受厂家声明的批间精密度性能,说明仪器1和仪器2声明的精密度性能大部分是符合常规条件下的,P和ALT不能接受可能厂家是在最佳条件下做出的性能指标或者厂家当时标本的决定性水平和本实验室不同。
根据相关要求,在实际工作中,给定的分析方法的允许总误差必须小于分析物CLIA固定界限,批内不精密度应是CLIA固定限的1/4,并且将批间不精密度降低到1/3的CLIA固定限目标[6-7]。根据以上实验结果,其中仪器1的Na项目批内、批间不精密度都超过了CLIA′88固定限的相应指标,Cl项目的批间不精密度超过了CLIA′88固定限的1/3;仪器2的Ure项目批内、批间不精密度都超过了CLIA′88固定限的相应指标,另外有4个项目(P、TC、GLU、ALB)批内不精密度超过了CLIA′88固定限的1/4。
3.3 厂家声明的精密度性能与CLIA固定限的相应指标相比,除P和ALT以外,其余项目全部能接受,说明部分国产仪器和试剂虽然声明的精密度性能指标比较真实,但个别指标不够严格,除厂家要严格按六西格马质量管理和要求生产[9],进一步改善仪器性能外,也建议主管部门制定出更严格的标准审批企业的生产。在临床实验室常规条件下,除严格按厂家说明书维护好仪器外,对于仪器1类型的仪器,因为电气性能要求高,要改善室内条件,严格稳定室内电压,定期更换电极。而对于仪器2类型的仪器,每天要对试剂针、样品针、搅拌系统、清洗系统进行擦拭,并且设置好项目测试顺序,防止携带污染和交叉污染。另外要制订更高的质量目标,严格控制全过程质量,最好优选方法,找到性能更佳的替代方法,如更换试剂厂家等。改进后,要重新评价其方法性能,提高方法可接受性,以保证常规检验工作中的质量。
3.4 国家最新发布了行业标准WS-T403-2012(临床生物化学检验常规项目分析质量指标)文件,从2013年8月1日实施。该文件对总误差、不精密度和偏倚作出了具体规定,明确指出总误差、不精密度和偏倚指标分别主要用于室间质量评价、室内质量控制管理和正确度验证。这些指标的制订是根据检验项目的个体内生物学变异和个体间生物学变异同时考虑目前可实现的分析质量水平,所以本次国家发布的质量指标是很科学的。但单纯从指标上与CLIA比较,WS-T 403-2012标准更严格,例如ALT的WS-T 403-2012总误差为16%,不精密度CV为6%,而CLIA总误差为20%,1/3CLIA为6.7%;TP的WS-T 403-2012总误差为5%,不精密度CV为2%,而CLIA总误差为10%,1/3CLIA为3.3%。作者从2013年5月起按照WS-T 403-2012标准设定质量目标,进行改进,重新评估这22项常规指标后,所有项目批内、批间精密度已能达到厂家声明标准和批间不精密度低于CLIA1/3指标,只有个别项目如Ure、Na、Cl批内不精密度尚未低于CLIA1/4指标,只有在以后的工作中更换进口试剂和(或)更换进口仪器后再重新评估。
[1]Centers for Disease Control and Prevention(CDC),Centers for Medicare &Medicaid Services(CMS),HHS.Medicare,Medicaid,and CLIA programs;laboratory requirements relating to quality systems and certain personnel qualifications.Final rule[J].Fed Regist,2003,68(16):3639-3714.
[2]Medicare,Medicaid and CLIA program:Regulations implementing the clinical laboratory improvement amendments of 1988(CLIA).Final Rule[J].Fed Regist,1992,57(40):7002-7186.
[3]Westgard JO,Groth T,Aronsson T,et al.Performance characteristics of rules for internal quality control:probabilities for false rejection and error detection[J].Clin Chem,1977,23(10):1857-1867.
[4]冯仁丰.临床检验质量管理技术基础[M].2版.上海:上海科学技术文献出版社,2007:81-98.
[5]CLSI.Evaluation of precision performance of quantitative measurement methods;approved guideline second edition Document EP-5A2[S].Wayne,PA:CLSI,2004.
[6]王治国.临床检验质量控制技术[M].2版.北京:人民卫生出版社,2008:93-114.
[7]叶应妩,王毓三,申子瑜.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:66-67.
[8]冼江,孙朝晖,方旭成,等.方法学验证-常见生化项目参考区间的确认[J].现代检验医学杂志,2011,26(2):38.
[9]Westgard JO.Six Sigma quality design &control[M].Medison WI:Westgard Quality Corporation,2001.
