茶碱、烟酰胺与异丙醇三元系统在298.15和308.15 K的相图研究
2014-02-06郭晶晶党乐平卫宏远
郭晶晶,党乐平,卫宏远
(天津大学化工学院,天津300072)
共晶是一类已为人所知但研究甚少的复合物,室温下为固体的各组分热力学、动力学、分子识别的平衡的结果[1]。当活性药物成分(API)与其他生理可接受的酸、碱、非离子化合物,以氢键等非共价键形式结合在同一晶格中,形成药物共晶,其组分中至少有1个是分子或者离子型API,同时任意组分在室温下为固体[2]即为药物共晶。在共晶体系中,其间的相互作用力一般是氢键、π-π键和分子间作用力,氢键键能远大于其他的几种作用力,所以氢键是共晶形成的最重要的作用力[3]。制药共结晶物可以在不损害活性药物成分(API)结构的情况下,改善药物的溶解度和溶解速率并且增加药物的稳定性[4-5]。
共晶形成的体系可以由活性药物成分(API)、配体(coformer)和溶剂(solvent)组成的三元相图描述,是用固相和液相的总体组成表示的三角相图[6-7],简称TPD。目前药物共晶的研究主要集中在共晶体的溶解度[8]、共晶体筛选[9-10]、形成机制、形成动力学和稳定性[11],只有少数的相图被研究并报道[12]。共晶三元相图的绘制有助于帮助人们了解共晶是如何从溶液中形成的,对药物活性成分共晶的制备提供了理论指导。
茶碱(theophylline,TP)是存在于茶叶、咖啡等植物中的一种生物碱,有较强的松弛支气管平滑肌、兴奋心脏和利尿作用[13]。茶碱在临床上的应用很普遍,主要用于治疗支气管哮喘、心原性哮喘和心原性水肿等[14]。虽然这种药物已经使用了30多年,但是由于它在水中的溶解度较小,生物利用率受药物溶出速率的影响,要达到治疗的效果必须要通过大量的用药。烟酰胺(nicotinamide,NCT)是一种水溶性维生素类药,是制药工业中常用的材料,它作为配体可以与茶碱形成共结晶。因此考虑通过制备茶碱-烟酰胺共晶来改变药物活性成分的一些理化性质。由于在异丙醇中茶碱-烟酰胺共晶的溶解度比较小,且茶碱和烟酰胺在异丙醇中的溶解度相差较大,可以形成非对称三元相图,对于此类体系通过溶剂蒸发不能获得纯共晶,绘制三元相图对于纯共晶的制备更有意义。目前关于茶碱、烟酰胺和异丙醇三元体系相图的研究还未有相关的报道,因此本研究以茶碱-烟酰胺-异丙醇三元体系为研究对象,通过测定不同温度下该体系的三元相图帮助了解相图随温度的变化,为药物共晶生产过程中的目标产物的控制提供理论基础。
1 实验部分
1.1 材料
烟酰胺,分析纯,天津市光复经济化工研究所;茶碱,分析纯,阿拉丁试剂(中国)有限公司;异丙醇,分析纯,天津市科威公司;实验用水为市售去离子水。
1.2 仪器
电子分析天平,JHS-2190型,上海上平仪器公司;水浴恒温振荡器,WE-1型,天津市欧诺仪器仪表有限公司;真空干燥箱,DZF-6020501,上海一恒科学仪器有限公司;循环水式多用真空泵,SHB-Ⅲ,郑州长城科工贸有限公司;差示扫描量热仪(DSC),Mettler DSC204 型;高效液相色谱(HPLC),Lab A lliance液相色谱仪,Ultimate AQ-C18色谱柱(5μm,4.6mm×250mm),柱温:303.15 K,流速:1 mL/min,进样量:10μL,检测波长为 271nm。流动相:16.56 mmol/L的乙酸缓冲溶液,用冰乙酸调节 pH值为4.05,然后加入体积分数为7%的乙腈;X-射线粉末衍射(XRD),日本理学(Rigaku)D/max-2500 型单色X-射线衍射仪。
1.3 茶碱-烟酰胺共晶的三元相图绘制
称取不同比例的茶碱、烟酰胺、异丙醇,混合后,加入密封的50 mL锥形瓶中,并加入小玻璃珠。然后将锥形瓶放入水浴恒温振荡器中,设定一定温度,振荡24 h,使其充分混合以达到固液平衡状态。水浴恒温振荡器的温度波动小于0.1 K。静置一段时间后,用0.45μm PTFE过滤头进行固液分离,并用高效液相色谱对液体样品进行含量分析,用X射线粉末衍射法对干燥后的固体进行分析。重复前面的步骤,绘制茶碱-烟酰胺共晶在不同温度的条件下的三元相图。
2 实验结果与讨论
2.1 茶碱-烟酰胺共晶的溶度积理论
由共晶的定义可知,药物共晶的组分在常温下均为固体,可以将溶度积理论引入到共晶中来,建立数学模型,从而解释共晶的形成机理、共晶的相图等等。以1∶1共晶为例,用A表示活性药物成分,B表示共晶配体,AB表示1∶1的共晶。当共晶 AB溶解于溶液中时,存在的化学平衡如式(1)和(2):
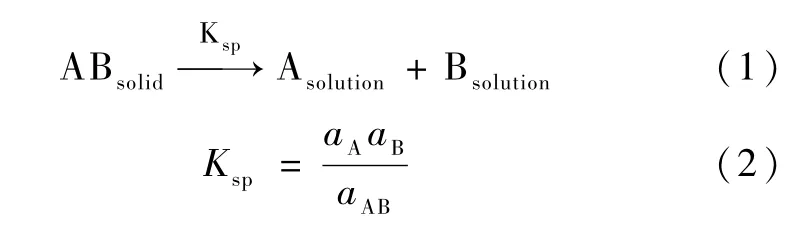
因为纯固体的活度aAB为1,难溶强电解质的溶解度很小,溶液的浓度很稀,可以用浓度代替活度来进行计算,由式(2)可以得到共晶溶度积的表达式。

若共晶在溶液中不形成溶液络合物,那么[A]T=[A],[B]T=[B],上式整理可得:
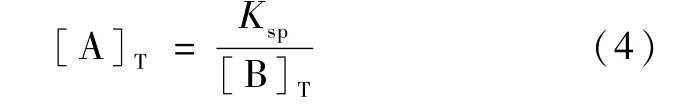
式(4)中,下标“T”代表溶液中的总浓度。
若溶液中存在1∶1的溶液络合,其化学平衡式如式(5):
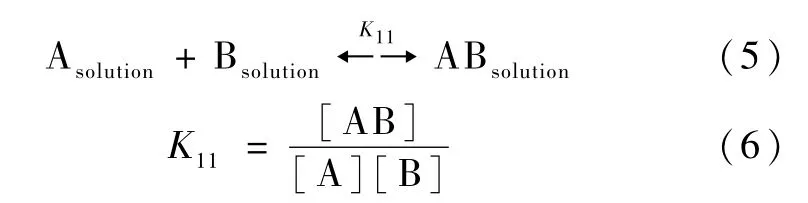
利用质量守恒与上式结合可得K11和Ksp的表达式:
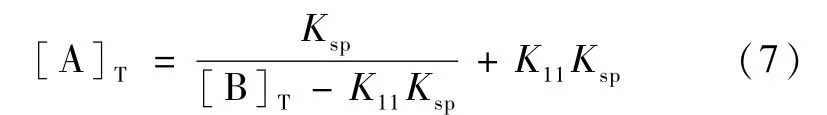
式(7)中,K11表示络合常数[15]。
为了考察茶碱-烟酰胺共晶在溶液中是否形成络合及络合的形式,以异丙醇为溶剂,分别测定298.15 K及308.15 K时茶碱-烟酰胺共晶在溶剂中的溶解度数据如表1所示,利用式(4)和式(7)分别对实验数据进行非线性拟合。
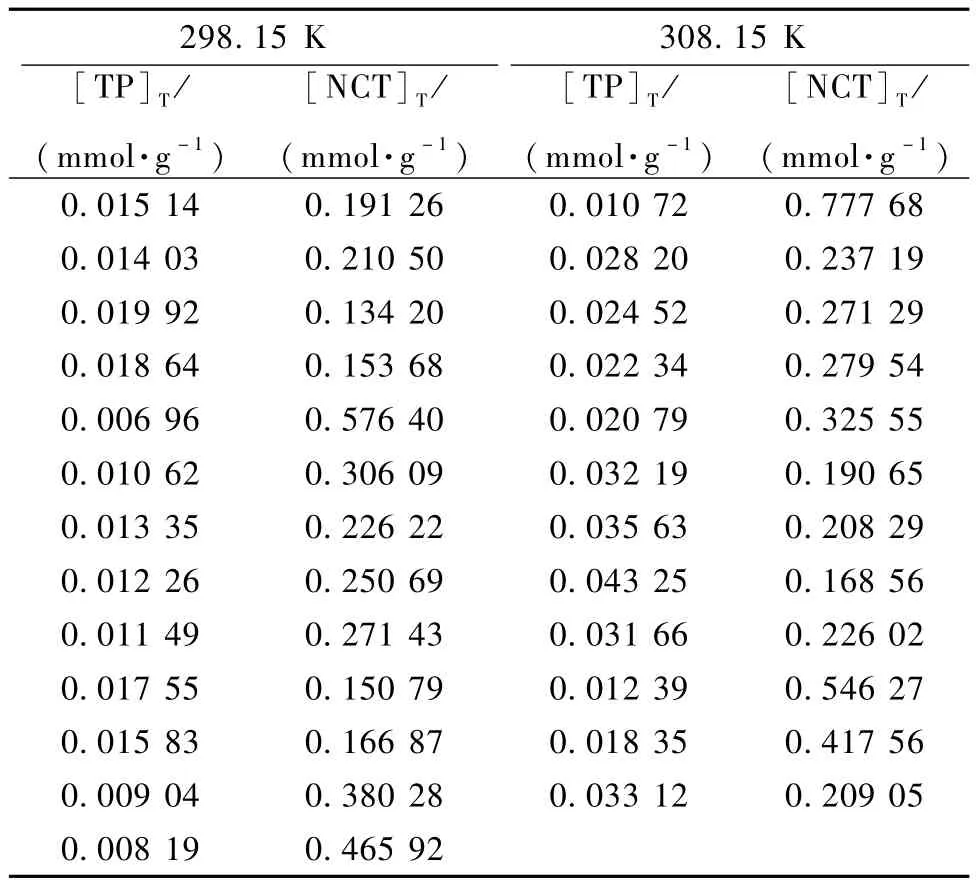
表1 298.15 K和308.15 K茶碱-烟酰胺共晶的溶解度数据Table 1 Solubility data for 1:1 TP-NCT cocrystal at 298.15 K and 308.15 K
将表1中298.15 K茶碱-烟酰胺共晶的溶解度数据按式(4)进行非线性拟合,根据拟合结果可得到Ksp,实验数据非线性拟合结果度如图1所示。
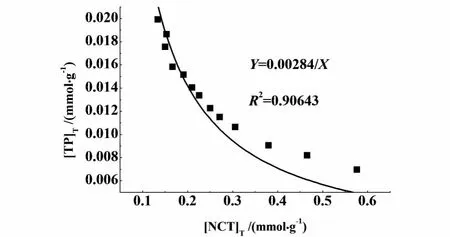
图1 298.15 K异丙醇中的溶解度实验数据按式(4)非线性拟合结果Fig.1 Non-Linear relation curve according to equation(4)for solubility data of 1:1 TP-NCT cocrystal at 298.15 K
将上述数据按式(7)进行非线性拟合,根据拟合结果可得到Ksp和K11,实验数据非线性拟合结果度如图2所示。
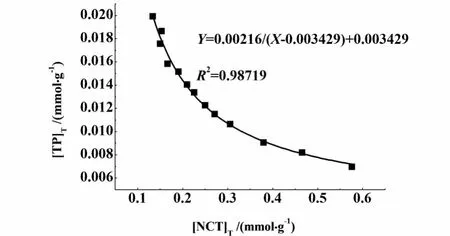
图2 298.15 K异丙醇中的溶解度实验数据按式(7)非线性拟合结果Fig.2 Non-Linear relation curve according to equation(7)for solubility data of 1:1 TP-NCT cocrystal at 298.15 K
同理将表1中茶碱-烟酰胺共晶在308.15 K的溶解度数据按式(4)进行非线性拟合,根据拟合结果可得到 Ksp,实验数据非线性拟合结果度如图3所示。
同理将表1所示的308.15 K茶碱-烟酰胺的溶解度数据按络合模型式(7)进行非线性拟合,根据拟合结果可得到 Ksp,K11实验数据非线性拟合结果度如下图4所示。
从上述图2和图4中可以看出R2极高,用络合模型拟合得到的结果与实验数据相差不大,而若使用无络合模型,可以看出298.15 K时拟合得到的结果与实验结果偏差较大,所以茶碱-烟酰胺共晶溶解于异丙醇中时,共晶组元茶碱与烟酰胺浓度之间的关系可以用1∶1络合形式的络合模型进行描述。
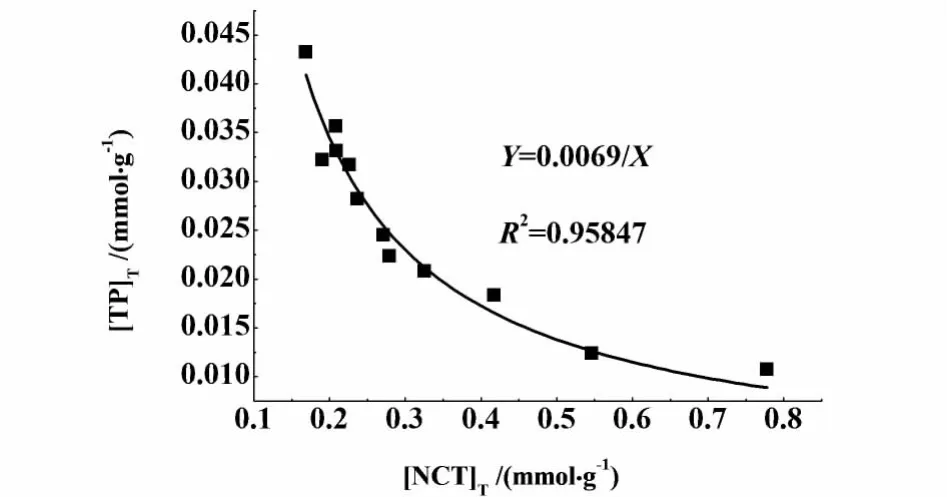
图3 308.15 K异丙醇中的溶解度实验数据按式(4)非线性拟合结果Fig.3 Non-Linear relation curve according to equation(4)for solubility data of 1:1 TP-NCT cocrystal at 308.15 K
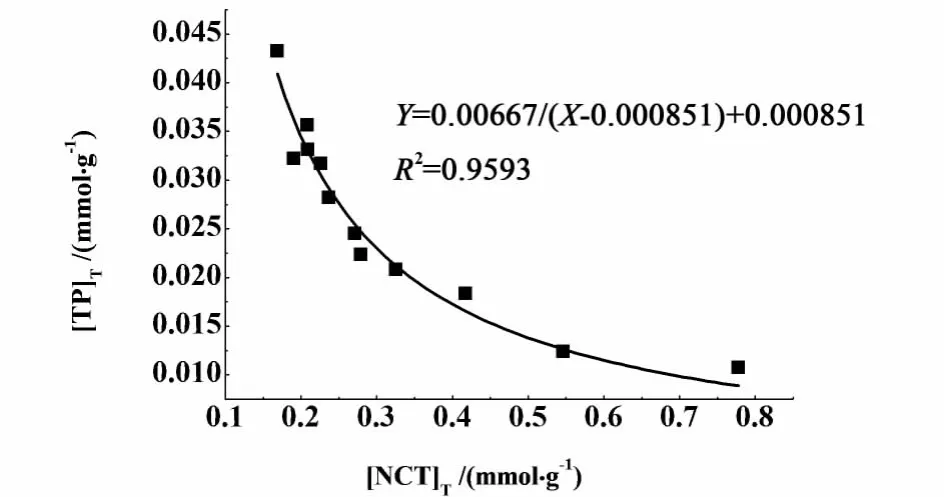
图4 308.15 K异丙醇中的溶解度实验数据按照式(7)非线性拟合结果Fig.4 Non-linear relation curve according to equation(7)for solubility data of 1:1 TP-NCT cocrystal at 308.15 K
将表1中的茶碱-烟酰胺的溶解度数据按式(7)进行非线性拟合,根据拟合结果可得到Ksp及K11,实验数据非线性拟合结果见表2。

表2 TP-NCT共晶在异丙醇中的溶度积K sp,络合常数K11Table 2 Complexation and solubility product constant for 1:1 TP-NCT cocrystal
由表2可看出在298.15 K时茶碱-烟酰胺共晶的溶度积为 0.002 16,308.15 K时的溶度积为0.006 67。溶度积随温度的升高而增大,表明茶碱、烟酰胺与异丙醇之间的作用力增强。298.15 K时K11为 1.587 46,308.15 K时 K11为 0.127 59,随着温度的升高,溶液络合常数K11减小,与溶度积的变化趋势相反,这是因为相对于茶碱与烟酰胺之间的作用力而言,茶碱、烟酰胺与异丙醇分子间的作用力增强,所以茶碱与烟酰胺分子之间形成络合的可能性减小,故络合常数减小。随着溶液体系温度的升高,共晶组元茶碱、烟酰胺与异丙醇的分子间的氢键作用增强,而共晶组元间的氢键作用相对减弱,所以茶碱-烟酰胺共晶的溶解度升高,溶度积增大。
2.2 茶碱-烟酰胺共晶的三元相图
三元相图的测定及绘制是件工作量庞大的工作,共晶三元相图中,共晶的溶解度曲线即是共晶的溶度积曲线,因此可以利用上述共晶溶度积曲线的测定方法,获得共晶三元相图中的溶解度曲线。通过实验测得的茶碱-烟酰胺共晶三元相图的相关数据后,绘制三元相图。因为相对于溶剂质量而言,茶碱和烟酰胺的溶解度很小,很接近顶部,按照实际质量分数绘制出的相图,因此图5和图6为共晶的三元相图顶部的局部放大图,表3为三元相图相对应的数据。
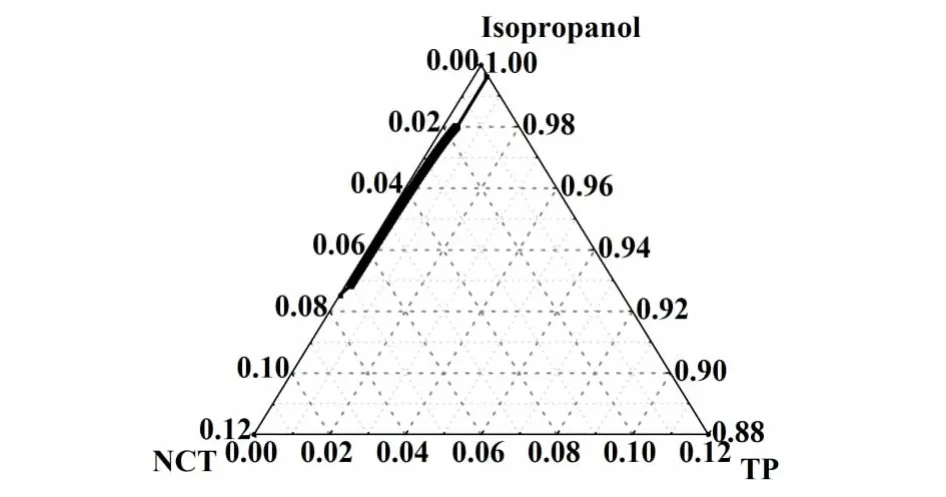
图5 298.15 K TP-NCT共晶三元相图的局部放大图Fig.5 Section of ternary phase diagram of TP-NCT-isopropanol at 298.15 K
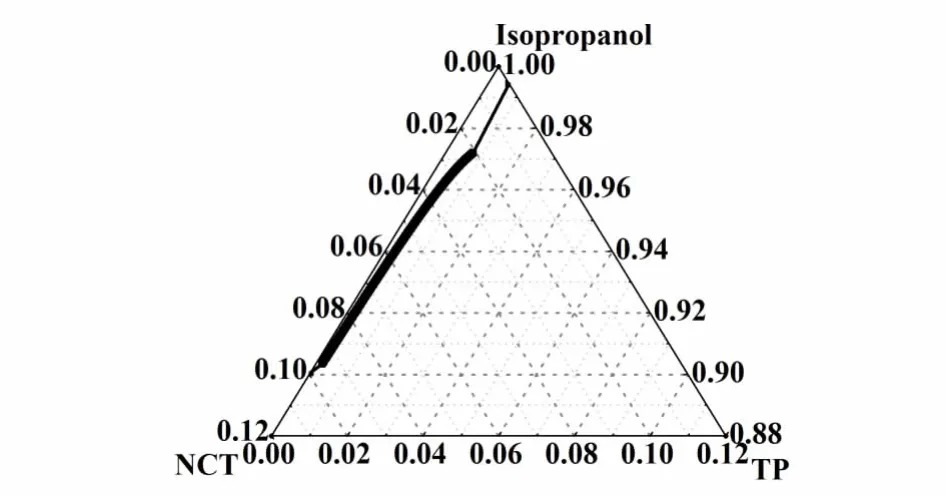
图6 308.15 K TP-NCT共晶三元相图的局部放大图Fig.6 Section of ternary phase diagram of TP-NCT-isop ropanol at 308.15 K
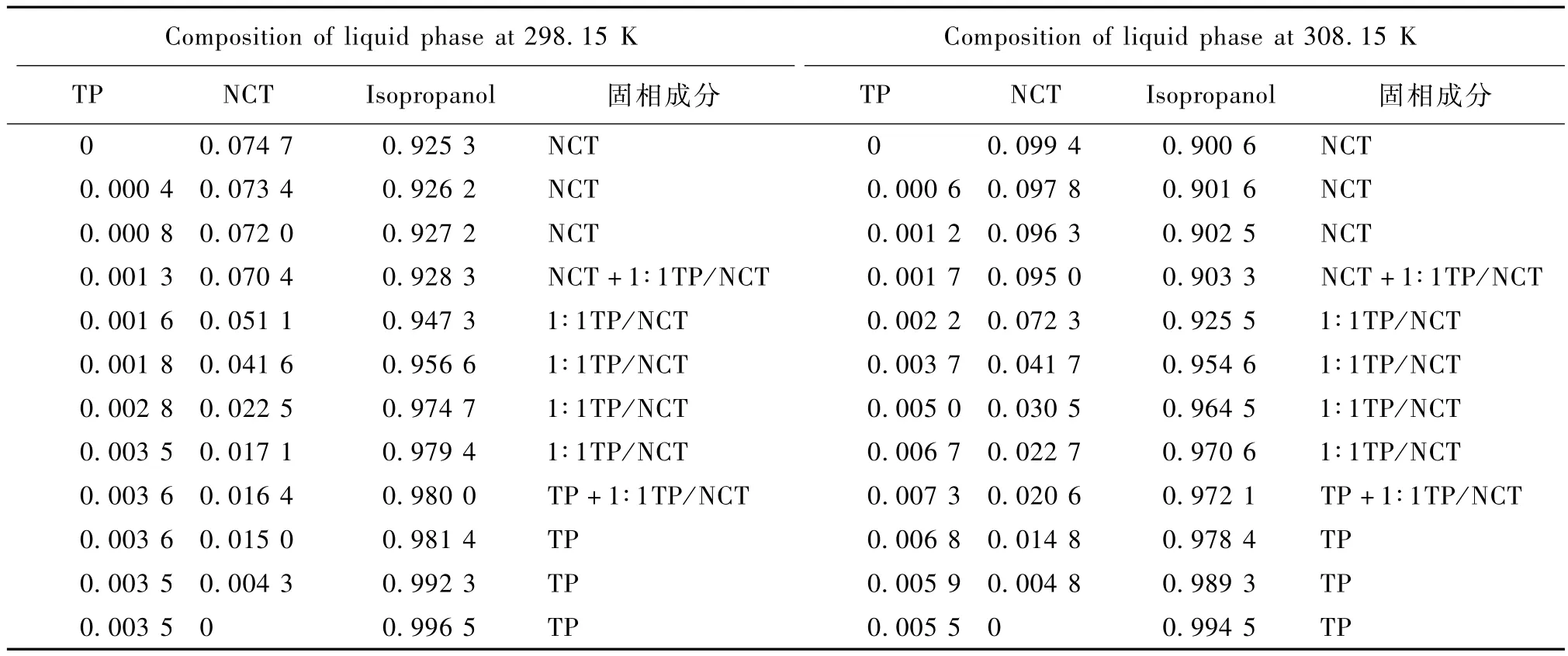
表3 298.15和308.15 K茶碱、烟酰胺和异丙醇三元体系的溶解度数据Table 3 Solubility data of TP,NCT and Isopropanol system at 298.15 and 308.15 K
从图5和图6中三元相图的局部放大图可以看出温度对三元相图的影响。当温度从298.15 K上升到308.15 K时,共晶的溶解度随着温度的升高而升高,不饱和液相区的面积变大,但是溶解度曲线的变化趋势保持一致。通过实验中对相图的一系列研究发现,对共晶的溶度积的研究可以帮助我们绘制三元相图,并能根据已知相图对未知相图进行合理、有效的预测,为以后的工艺放大提供有效的数据基础和理论依据。
3 结论
1)考察了茶碱-烟酰胺共晶在异丙醇溶剂中是否形成络合以及温度对溶度积的影响。随着溶液中烟酰胺总浓度的增加,茶碱的总浓度呈现出减小的趋势,两者之间为非线性变化关系。通过对实验所得数据进行拟合可以得出茶碱-烟酰胺共晶溶解于异丙醇中时,共晶组元茶碱与烟酰胺浓度之间的关系可以用1∶1络合形式的络合模型进行描述。随着温度的升高,茶碱-烟酰胺共晶的溶解度升高,溶度积增大,络合常数则与溶度积的变化趋势相反,随着温度的升高减小。
2)绘制了不同温度下茶碱-烟酰胺共晶在异丙醇中的三元相图。在同种溶剂中,共晶溶解度随着温度的升高而增大,溶解度曲线的变化趋势保持一致,但不饱和液相区的面积变大。通过测定不同温度下的三元相图帮助了解了相图随温度的变化,为药物共晶生产过程中的目标产物的控制提供理论基础。
[1]Schultheiss N,Newman A.Pharmaceutical co-crystals and their physicochemical properties[J].Cryst Growth Des,2009,9:2950-2967
[2]闻聪,金方.药物共晶在药学中的应用[J].中国新药杂志,2007,16(15):1167-1171 Wen Cong,Jin Fang.The application of pharmaceutical co-crystals in pharmacy[J].Chinese Journal of New Drugs,2007,16(15):1167-1171(in Chinese)
[3]Kim SD,Ryoo I J,Kim C J.Taxonomy,fermentation,isolation and characterization of a herbicida compound[J].JMicrobiolo Biotechnol,1993,3(1):57-60
[4]Hickey M B,Peterson M L,Scoppettuolo L A,et al.Performance comparison of a co-crystal of carbamazepine with marketed product[J].Eur J Pharm Biopharm,2007,67(1):112-119
[5]Schultheiss N,Newman A.Pharmaceutical cocrystals and their physicochemical properties[J].Cryst Growth Des 2009,9(6):2950-2967
[6]Renato A,Chiarella,Roger J,et al.Making co-crystals the utility of ternary phase diagrams[J].Crystal Growth and Design,2007,7(7):1223-1226
[7]Ainouz A,Authelin JR,Billot P,et al.Modeling and prediction ofcocrystal phase diagrams[J].International Journal of Pharmaceutics,2009,374:82-89
[8]Good D J,Rodríguez-Hornedo N R.Solubility advantage of pharmaceutical cocrystals[J].Cryst Growth Des,2009,9(5):2252-2264
[9]Lu E,Rodríguez-Hornedo N,Suryanarayanan R.A rapid thermal method for cocrystal screening[J].Cryst Eng Comm,2008,10(6):665-665
[10]Ter Horst JH,Deij M A,Cains PW.Discovering new co-crystals[J].Cryst Growth Des,2009,9(3):1531-1537
[11]Chieng N,Hubert M,Saville D,et al.Formation kinetics and stability of Carbamazepine-nicotinamide cocrystals prepared by mechanical activation[J].Cryst Growth Des,2009,9(5):2377-2386
[12]Gagnière E,Mangin D,Puel F,et al.Formation of cocrystals:Kinetic and thermodynamic aspects[J].Cryst Growth,2009,311(9):2689-2695
[13]马康,赵敏,王海峰,等.茶碱标准物质的研制与定值[J].分析测试学报,2011,30(4):418-424 Ma Kang,Zhao Min,Wang Haifeng,et al.Development and certification of theophylline certified reference material[J].Journal of Instrumental Analysis,2011,30(4):418-424(in Chinese)
[14]Schreiber D E,Bruguerolle B.Simultaneous high-perfor mance liquid chromatographic determination of caffeine and theophylline for routine drug monitoring in human plasma[J].JChromatogr:B,1996,677(2):305-312
[15]Sarah J N,Rodríguez-Spong B.Phase solubility diagrams of cocrystals are explained by solubility product and solution complexation[J].Crystal Growth and Design,2006,6(2):592-600
