不同溶质型桃果实成熟衰老过程中线粒体内细胞色素氧化酶的变化
2014-01-18陆燕飞金昌海
阚 娟,陆燕飞,刘 俊,金昌海
(扬州大学食品科学与工程学院,江苏 扬州 225127)
不同溶质型桃果实成熟衰老过程中线粒体内细胞色素氧化酶的变化
阚 娟,陆燕飞,刘 俊,金昌海*
(扬州大学食品科学与工程学院,江苏 扬州 225127)
以软溶质型桃‘雨花3号’和硬溶质型桃‘加纳岩’果实为试材,研究不同溶质型桃成熟衰老过程中细胞色素氧化酶(cytochrome c oxidase,COX)活性以及线粒体编码的COX 3 种亚基(COXⅠ、COXⅡ、COXⅢ)基因表达量的变化。结果表明:桃果实成熟前期,COX活性不断增加,成熟后期,COX活性开始下降。‘加纳岩’COX 3 种亚基基因的表达量高于‘雨花3号’,且COX 3 种亚基在桃果实成熟前期表达量较高。说明线粒体DNA编码的COX 3 种亚基主要作用于桃果实成熟前期,为果实生长代谢提供所需能量,到了后期表达量降低,活性受影响,导致果实线粒体内的活性氧积累,机体代谢失衡,呼吸速率增加,线粒体编码的COX 3 种亚基与桃果实成熟衰老之间存在一定的内在联系。
桃;线粒体;呼吸速率;细胞色素氧化酶
近年来,研究线粒体功能障碍已成为国际上衰老机制研究的一个热点。一系列实验表明,细胞衰老时线粒体功能会发生退行性改变[1]。细胞色素氧化酶(cytochrome oxidase,COX)是线粒体呼吸链末端氧化反应过程中的关键酶,是线粒体特有的酶,也是细胞有氧呼吸的限速酶[2]。COX的损伤又可直接影响线粒体的功能,导致三磷酸腺苷(adenosine triphosphate, ATP)合成减少,促使线粒体呼吸链产生大量的活性氧簇(reactive oxygen species,ROS),造成机体不断衰老[3]。COX有13 个亚基,为一多亚基、多形式、多基因组来源的酶蛋白复合体,其中最大的3 个亚基(COXⅠ、COXⅡ、COXⅢ)由线粒体DNA(mtDNA)编码,是酶活性不可缺少的部分。目前有研究人员从活性氧代谢的角度,通过蛋白质组学、蛋白免疫杂交以及其他生理生化分析,证明了线粒体蛋白氧化损伤与果实成熟衰老的关系[4]。有研究表明[5-6]以生命能量逐步丧失为特征的衰老的部分原因可能是由于“细胞色素氧化酶”作用效率下降的结果。在有关动植物的报道中指出,COX的表达量大小会关系到COX活性的大小[7]。在对玉米[8]、水稻[9]等植物以及动物体[10-11]的研究中发现,不同状态的机体中线粒体COX的活性存在着很大差异,机体代谢失衡后会表现出相应区域COX活性下降和COX基因表达的改变。前期研究中亦发现桃果实在成熟软化过程中COX活性总体有下降趋势,且伴随着活性氧含量的增加[12]。果实的成熟软化与其呼吸代谢关系密切,而线粒体是果实进行呼吸作用的细胞器,COX的变化可直接影响线粒体功能。目前对果实成熟软化中线粒体呼吸代谢作用研究较少,对线粒体DNA编码的COX与果实成熟衰老之间关系的研究尚未见报道。以软溶质型‘雨花3号’和硬溶质型‘加纳岩’桃果实为材料,研究桃果实成熟衰老过程中线粒体内COX活性的变化,分析线粒体编码的COX 3种亚基的基因表达量,探明COX基因及其表达的改变以及蛋白质酶活性变化与桃果实成熟衰老之间的关系,为有关桃果实成熟软化衰老过程中线粒体功能损伤及线粒体能量代谢障碍的分子机理提供实验依据,进一步从分子水平完善桃果实成熟软化机理。
1 材料与方法
1.1 材料及处理
供试品种为软溶质型‘雨花3号’水蜜桃果实和硬溶质型‘加纳岩’桃果实。按果实的不同成熟度进行分批采样,采收后立刻运至实验室,剔除病果、伤果,果实成熟度划分如下:
‘雨花3号’:成熟度Ⅰ:盛花后55 d,果皮颜色青绿,基部很硬;成熟度Ⅱ:盛花后65 d,果皮颜色青绿,基部较硬;成熟度Ⅲ:盛花后70 d,果皮颜色青绿微黄,基部微软;成熟度Ⅳ:盛花后75 d,果皮颜色微青带黄,基部较软;成熟度Ⅴ:盛花后80 d,果皮颜色黄带微白,基部很软。
‘加纳岩’:成熟度Ⅰ:盛花后85 d,顶部红色,整果很硬;成熟度Ⅱ:盛花后90 d,顶部红色面积增大,整果很硬;成熟度Ⅲ:盛花后95 d,基本全红,顶部暗红,果实较硬;成熟度Ⅳ:盛花后100 d,顶部暗红,果实较硬;成熟度Ⅴ:盛花后105 d,顶部暗红面积达1/2,果实微软。
在采收当天去掉果皮和果核,将果肉部分切成小块,用液氮处理后装在聚乙烯薄膜塑料袋中,并立即保存于-80 ℃超低温冰箱中用于实验分析。
1.2 试剂与仪器
焦碳酸二乙酯、十六烷基三甲基溴化铵、聚乙烯吡咯烷酮、乙二胺四乙酸二钠、十二烷基硫酸钠、β-巯基乙醇、LiCl、Tris、亚精胺、3-[(3-胆酰胺基丙基)-二甲基铵基]-1-丙磺酸盐、二硫苏糖醇、苯甲基磺酰氟生工生物工程(上海)股份有限公司;PrimeScriptTM1st Strand cDNA Synthesis Kit反转录试剂盒、TaKaRa TaqTMDNA聚合酶、DL 2000TMDNA Marker 宝生物工程(大连)有限公司;NaCl、HCl、氯仿、异戊醇、蔗糖、氯化镁均为分析纯。
GY-1型果实硬度计 牡丹江市机械研究所;高速冷冻离心机(5804R)、梯度PCR仪(5341) 德国Eppendorf公司;荧光定量仪(7300) 美国ABI公司。
1.3 方法
1.3.1 果实硬度的测定
采用GY-1型果实硬度计(调头直径3.5 mm),测定鲜果去除果皮后果肉的硬度。每个果实胴部不同部位对称均匀选取6 个点,每次测量6 个果实,均匀取平均值。
1.3.2 呼吸速率的测定
采用静置法[13]。
1.3.3 线粒体的提取
参照Bonner[14]、Liang[15]等方法。
1.3.4 COX活性的测定
取上述提取的线粒体制备液1 mL,COX活性的测定参照Errede等[16]的方法。
1.3.5 桃果实总RNA提取
参照Meisel等[17]方法提取。
1.3.6 COXⅠ、COXⅡ、COXⅢ基因的实时聚合酶链式反应(real-time polymerase chain reaction,RT-PCR)和荧光定量PCR
根据N C B I上C O XⅠ、Ⅱ、Ⅲ基因序列信息(GenBank登录号分别为M16884.1,Z11980.1,X15131.1),用Primer premier5.0 软件设计引物,RT-PCR特异性引物COXⅠ(5’-ATT GGT CTG TTC CGA TTC-3’)和(5’-CCG CTA CCC ACT TCT ACT-3’),COXⅡ(5’-AAG ACG CAG CAA CAC CTA-3’)和(5’-CTA ACC ACC TCA ACT CCC-3’),COXⅢ(5’-TTC CTT TAG CCT TTC GTG-3’)和(5’-CCT CAA TCC ACT GTT TCG-3’),用于扩增目的基因。Actin(5’-GAT TCT GGT GAT GGT GTG AGT CA-3’)和(5’-GAG AGA TGG CTG GAA GAG GAC TT-3’)用于内参基因。荧光定量PCR引物COXⅠ(5’- GACACCCGAGCCTACTTTAC-3’)和(5’-GCTATGATGGCGAATACTGC-3’),COXⅡ(5’-GCTTACAAGACGCCACATCACC-3’)和(5’-CGTAGGGAGGGAAGGGCAAT-3’),COXⅢ(5’-CAGCCTAGTTCCTACCCACGAC-3’)和(5’-CCCGTTGCTATGAAGAATGTTG-3’)用于扩增目的基因。Actin(5’-CCTCTATGCCAACACAGTGC-3’)和(5’-GTACTCCTGCTTGCTGATCC-3’)用于内参基因。
1.4 数据差异性分析
所有数据用SPSS软件进行统计分析。
2 结果与分析
2.1 不同溶质型桃果实成熟软化过程中果实硬度的变化
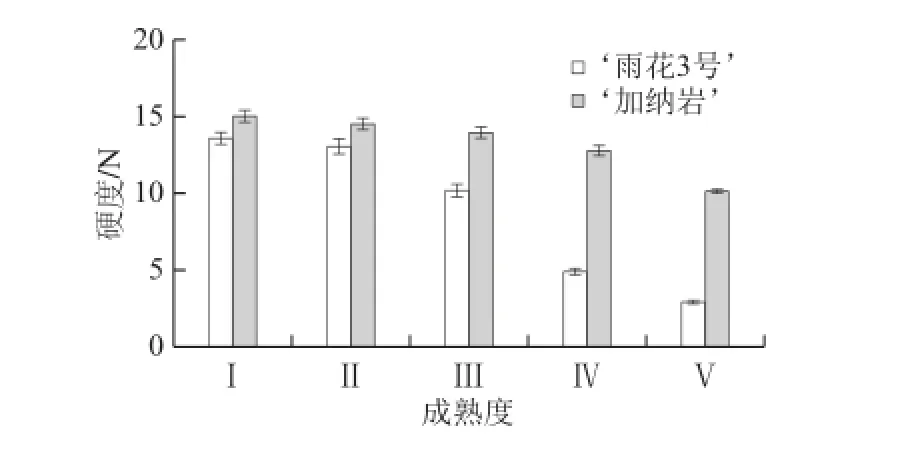
图1 桃果实成熟过程中硬度的变化Fig.1 Change in firmness during peach fruit maturation
果实硬度是反映果实质地和耐贮藏性的一个重要指标,也是反映果实成熟软化的重要指标之一。如图1所示,不同溶质型桃果实成熟过程中果实硬度均发生一定程度的下降。‘雨花3号’桃果实在成熟的第Ⅰ~Ⅲ成熟度时硬度变化较小,第Ⅲ~Ⅴ成熟度时果实硬度迅速下降。‘加纳岩’桃果实在成熟过程中果实硬度变化缓慢,仅在成熟末期有明显下降,但在成熟过程中整体保持较高的硬度。
2.2 不同溶质型桃果实成熟软化过程中呼吸速率的变化
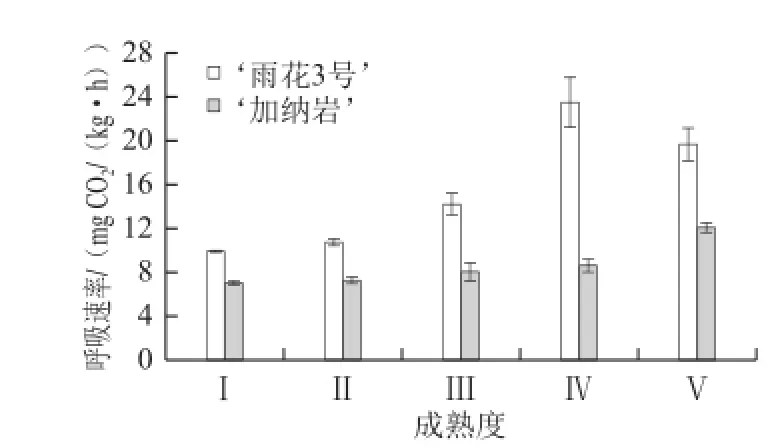
图2 桃果实成熟过程中呼吸速率的变化Fig.2 Change in respiration rate during peach fruit maturation
由图2可知,随着果实的成熟,‘雨花3号’桃果实的呼吸速率呈现显著上升的趋势,至成熟度Ⅳ时达到峰值,然后缓慢下降。而‘加纳岩’桃果实成熟过程中其呼吸速率虽也呈现上升的趋势,但上升的幅度显著低于‘雨花3号’桃果实的呼吸速率。
2.3 不同溶质型桃果实成熟软化过程中COX活性的变化
COX是呼吸链中特有的酶类,它能直接反应生物的有氧呼吸代谢水平,由图3可知,不同类型桃果实在成熟前期(Ⅰ~Ⅲ),COX活性不断增加,在成熟度Ⅲ时达最大值。且COX活性在不同类型桃果实中存在显著性差异(P<0.05)。随着果实的不断成熟软化,在桃果实成熟后期(Ⅳ~Ⅴ),COX活性不断下降,尤其是‘雨花3号’桃果实下降幅度较大,表明此时桃果实体内有氧呼吸代谢下降,可能致使线粒体内呼吸链上有大量电子漏产生,从而导致了果实内活性氧的增加,加速了果实衰老。
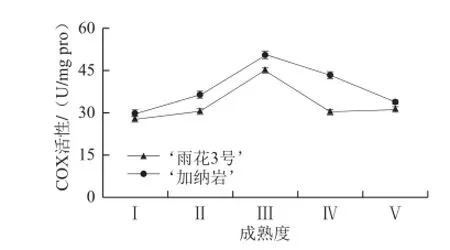
图3 桃果实成熟过程中COX活性的变化Fig.3 Change in COX activity during peach fruit maturation
2.4 不同溶质型桃果实成熟软化过程中COXⅠ、COXⅡ、COXⅢ基因表达水平的比较
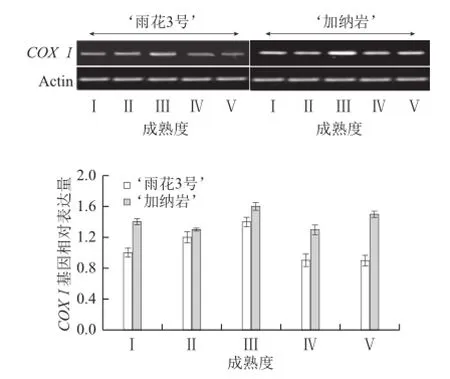
图4 桃果实成熟过程中COX Ⅰ的变化Fig.4 Change in COX Ⅰ gene expression during peach fruit maturation
由图4可知,不同溶质型桃果实在成熟软化过程中COXⅠ均有表达。软质型桃果实‘雨花3号’COXⅠ的表达量在成熟度Ⅲ达到较大值,与COX活性有一定相关性,到了成熟后期,表达水平略有下降。硬溶质型桃果实‘加纳岩’也是在成熟度Ⅲ表达量达最大值。
由图5可以看出,软溶质型桃果实‘雨花3号’COXⅡ基因表达量整体都较低,在果实成熟前期(Ⅰ~Ⅲ)的表达量略高于成熟后期(Ⅳ~Ⅴ),表明‘雨花3号’COXⅡ基因可能在成熟前期发挥作用。硬溶质型桃果实‘加纳岩’同样在成熟前期(Ⅰ~Ⅲ)的表达量高于成熟后期(Ⅳ~Ⅴ),在成熟度Ⅲ时表达量达最大值。
由图6可以观察到,软溶质型桃果实‘雨花3号’COXⅢ的基因表达量在前期随着果实的不断成熟而增加,硬溶质型桃果实‘加纳岩’COXⅢ也是在果实成熟前期表达量较高。比较不同类型桃果实COXⅢ基因表达量的大小,‘加纳岩’的表达量整体都高于‘雨花3号’。
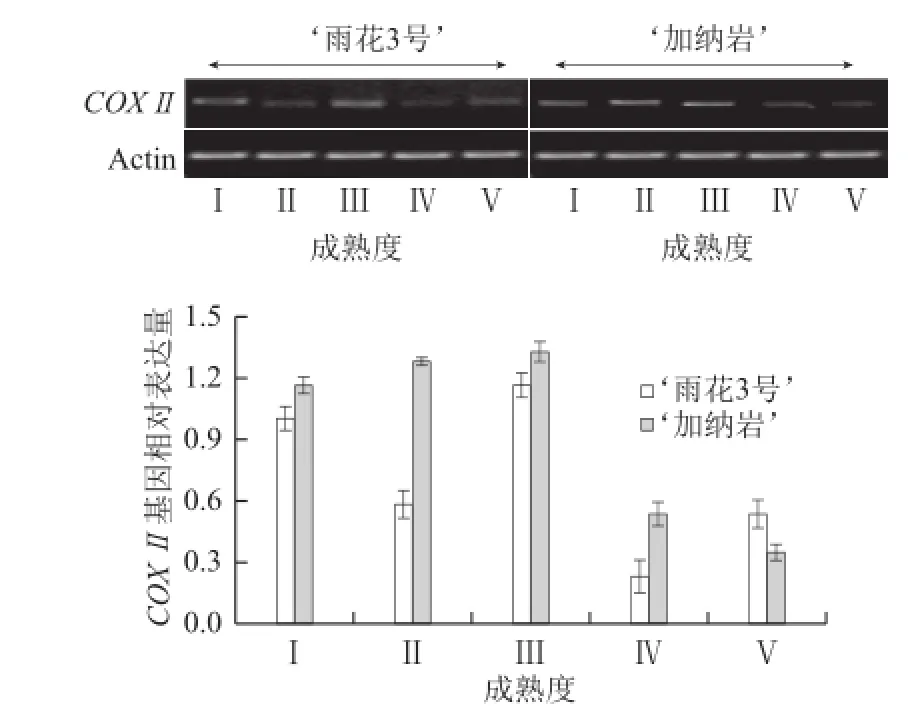
图5 桃果实成熟过程中COXⅡ的变化Fig.5 Change in COXⅡ gene expression during peach fruit maturation
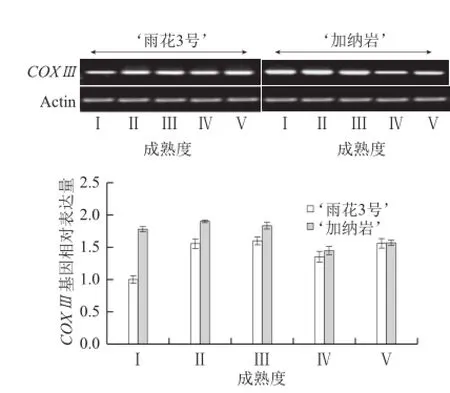
图6 桃果实成熟过程中COXⅢ的变化Fig.6 Change in COXⅢ gene expression during peach fruit maturation
3 讨 论
不同溶质型的桃果实其呼吸速率有显著差别(P<0.05),硬度的显著性差异变化与呼吸速率的显著性差异变化相一致。说明了呼吸速率对果实软化的作用,而线粒体是呼吸作用的场所,这也证实了线粒体中所进行的呼吸作用与果实成熟软化之间的重要关系。Brennan等[18]指出果实的成熟和衰老与活性氧有着密切的关系,线粒体呼吸链产生的O2-·和H2O2构成生物体内最大数量ROS的恒定来源,线粒体是产生ROS的主要部位[19],因此线粒体代谢、线粒体活性氧的产生等都是果实成熟衰老的重要影响因素。而Qin等[4]也证实了,由线粒体内的活性氧所引起的植物线粒体的氧化损伤与果实的衰老之间有着密切的关系。
COX位于线粒体呼吸链的末端,是线粒体呼吸酶系的关键酶[2]。在不同的生物种类甚至在同一生物种类、同一器官的不同部位,COX表达皆存在着一定的差异[20]。COXⅠ、COXⅡ及COXⅢ 3 个亚基作为构成COX的核心结构,与其他亚基共同影响着COX的活性,COX在线粒体呼吸链电子传递中发挥着极其重要的作用[21-23]。COX活性直接影响到线粒体功能状态,一旦线粒体功能受损,就会促使呼吸链产生大量的活性氧,导致机体受损,从而出现果实硬度下降,产生呼吸高峰以及诱导乙烯生成等一系列生理变化,加速果实的成熟衰老。
本实验中,在桃果实成熟前期,COX活性逐渐增大,到成熟度Ⅲ时达最大值(图3)。可以得出,COX活性的增加,促使线粒体功能稳定,进行细胞能量代谢,为果实成熟提供充足的代谢能量。到了桃果实成熟后期,COX活性不断下降,直接影响了线粒体功能,导致细胞内能量合成减少,膜电位丧失,呼吸链末端的电子流被阻断,电子漏出增多,从而使O2-·和H2O2产生的可能性大大增大,活化凋亡信号通路,细胞开始出现死亡现象,机体进入衰老状态[3]。在桃果实成熟后期,软溶质型桃果实‘雨花3号’在成熟度Ⅳ时COX活性下降幅度较大,导致线粒体呼吸代谢中细胞色素氧化酶途径受阻,诱导了抗氰呼吸作用的加强,而乙烯的产生与抗氰呼吸上升有平行的关系,乙烯刺激抗氰呼吸,从而诱发呼吸跃变的产生[24],因此‘雨花3号’在成熟度Ⅳ时出现呼吸高峰。呼吸高峰的出现标志着果实进入衰老状态,初步证明了COX与果实成熟衰老的关系。而硬溶质型桃果实‘加纳岩’在成熟后期COX活性下降幅度较‘雨花3号’小,变化较平缓,因此可能使细胞色素氧化酶途径受到影响较小,抗氰呼吸作用并没有‘雨花3号’明显,从而未诱导呼吸高峰的出现。但在成熟后期,随着果实不断成熟软化,‘加纳岩’线粒体内积累了大量的活性氧,使呼吸代谢受影响,抑制了COX活性,从而加速了果实的软化衰老。由此可见,COX活性与呼吸速率、活性氧及果实衰老之间存在着密切联系。
COX的蛋白表达受mtDNA和COX亚基基因的影响[25],COX最大的3个亚基(COXⅠ、COXⅡ及COXⅢ)是酶活性不可缺少的部分,因此研究COX基因表达可以为从分子水平上探明COX对果实成熟软化的作用提供理论依据。有研究证明,COX的表达量大小会关系到COX活性的大小[7],而COX活性一旦受到影响,就会直接影响线粒体功能状态,从而影响果实线粒体的呼吸代谢作用,导致活性氧的积累、果实的衰老等。本研究中COXⅠ在‘雨花3号’和‘加纳岩’中的基因表达量相近。COXⅡ基因在成熟前期‘加纳岩’中整体表达量高于‘雨花3号’,可见COXⅡ基因主要在成熟前期发挥作用。在‘加纳岩’中COXⅡ表达量相对‘雨花3号’的较高,而‘加纳岩’中COX活性略高于‘雨花3号’,表明COX活性可能受到COXⅡ基因的影响较大,COX蛋白可能更多的会受到COXⅡ基因的调控。同时,‘加纳岩’呼吸速率远低于‘雨花3号’,果实硬度变化较小,衰老程度缓慢。初步表明,COXⅡ基因表达量及COX活性与果实成熟衰老有较大的相关性。COXⅢ基因在桃果实中的表达量都较高,同样在‘加纳岩’中的表达量要略高于‘雨花3号’。在不同类型桃果实的成熟前期(Ⅰ~Ⅲ),线粒体编码的COX基因表达量相对高于成熟后期(Ⅳ~Ⅴ)的表达量,而COX活性在成熟前期(Ⅰ~Ⅲ)不断增加,线粒体功能稳定,为机体提供所需能量,促进果实正常生长代谢。到了成熟后期,基因表达量大幅降低,使COX活性受到了影响,诱导了抗氰呼吸作用的加强,从而诱发呼吸跃变的产生,促进果实衰老。同时COX活性变化也影响了线粒体功能的稳定性,使呼吸代谢失衡,ATP合成减少,导致呼吸链产生了大量的活性氧,加速机体损伤,促使果实不断软化衰老。
4 结 论
本研究首次比较研究了不同溶质型桃果实不同发育期线粒体DNA编码的细胞色素氧化酶的活性及基因的表达。研究表明,COX作为线粒体呼吸代谢中的关键酶,同一成熟度不同桃品种的COX活性都呈显著性差异(P<0.05),在桃果实成熟前期,COX基因表达量较高,COX活性相对较高,为桃果实成熟提供了所需能量,促进果实正常生长,线粒体内活性氧代谢平衡。到了桃果实成熟后期,COX表达量降低,COX活性受影响下降,使线粒体内正常呼吸代谢受影响,导致活性氧代谢紊乱,机体内形成活性氧的积累,加速果实受损,导致桃果实呼吸速率出现相应变化,并且使果实硬度出现显著降低。
[1] KATAOKA M, FUKURA Y, SHINOHARA Y, et al. Analysis of mitochondrial membrane potential in the cells by microchip flow cytometry[J]. Electrophoresis, 2005, 26(15): 3025-3031.
[2] COOPER C E, MASON M G, NICHOLLS P. A dynamic model of nitric oxide inhibition of mitochondrial cytochrome C oxidase[J]. Biochimica et Biophysica Acta, 2008, 1777: 867-876.
[3] PARTRIDGE R S, MONROE S M, PARKS T J, et al. Spin trapping of azidyl and hydroxyl radical in azide-inhibited rat brain submitochondrial particals[J]. Archives of Biochemistry and Biophysics, 1994, 310(1): 210-217.
[4] QIN G Z, MENG X H, WANG Q, et al. Oxidative damage of mitochondrial proteins contributes to fruit senescence: a redox proteomics analysis[J]. Journal of Proteome Research, 2009, 8(5): 2449-2462.
[5] COLLMAN J P, DEVARAJ N K, DECREAU R A, et al. Cytochrome C oxidase model catalyzes oxygen to water reduction under ratelimiting electron flux[J]. Science, 2007, 315: 1565-1568.
[6] FAXÉN K, GILDERSON G, ÄDELROTH P, et al. Mechanistic principle for proton pumping by cytochrome C oxidase[J]. Nature, 2005, 437(7): 286-289.
[7] POYTON R O, BELLUS G, MCKEE E E, et al. In organello mitochondrial protein and RNA synthesis systems from Saccharomyces cereuisiae[J]. Methods of Enzymology, 1996, 264: 36-42.
[8] DEWEY R E, TIMOTHY D H, LEVINGS C S. Chimeric mitochondrial genes expressed in the C made-sterile cytoplasm of maize[J]. Current Genetics, 1991, 20(6): 475-482.
[9] LEVING C S, BROWN G G. Molecular biology of plant mitochondria[J]. Cell, 1989, 56: 171-179.
[10] 顾卫东, 陈群, 曾因明. 低温对脑缺血/再灌注期间沙土鼠海马CA1区延迟性神经元死亡及ATP水平和细胞色素氧化酶活性的影响[J].徐州医学院学报, 2009, 29(1): 4-7.
[11] 陈飞雄, 申林娜, 蒲军, 等. 线粒体DNA编码蛋白质亚基的研究[J].中国医药指南, 2011, 9(1): 6-9.
[12] KAN Juan, WANG Hongmei, JIN Changhai, et al. Changes of reactive oxygen species and related enzymes in mitochondria respiratory metabolism during the ripening of peach fruit[J]. Agricultural Sciences in China, 2010, 9(1): 101-105.
[13] 李正国, 曾凯芳, 黄琼珍, 等. 农产品贮藏运销学实验教程[M]. 重庆:西南农业大学, 1997.
[14] BONNER W D. A general method for the preparation of plant mitochondria[J]. New York: Academic Press, 1967, 10: 126-133.
[15] LIANG W S, PAN J, LIANG H G. Activation of cyanideresistant respiration by pyruvate in mitochondria of aged potato tuber slices[J]. Plant Physiology and Plant Molecular Biology, 2003, 29: 317-321.
[16] ERREDE B, KAMEN M D, HATEFI Y. Preparation and properties of complex Ⅳ (ferrocytochrome c: oxygen oxidoreductase EC 1.9.3.1) [J]. Methods in Enzymology, 1978, 53: 40-47.
[17] MEISEL L, FONSECA B, GONZÁLEZ S, et al. A rapid and efficient method for purifying high quality total RNA from peachs (Prunus persica) for Functional genomics analyses[J]. Biological Research, 2005, 38: 83-88.
[18] BRENNAN T, FRENKEL C. Involvement of hydrogen peroxide in the regulation of senescence in pear[J]. Plant Physiology, 1977, 59: 411-416.
[19] NAVROT N, ROUHIER N, GELHAYE E, et al. Reactive oxygen species generation and antioxidant systems in plant mitochondria[J]. Physiology Plant, 2007, 129(1): 185-195.
[20] DUA R, SUNKARIA A, KUMAR V. Impaired mitochondrial energy metabolism and kinetic properties of cytochrome oxidase following acute aluminium phosphide exposure in rat liver[J]. Food and Chemical Toxicology, 2010, 48: 53-60.
[21] FRANCISCA D. Cytochrome C oxidase deficiency: patients and animal models[J]. Biochimica et Biophysica Acta, 2010, 1802: 100-110.
[22] CHEN Q, VAZQUEZ E J, MOGHADDS S, et al. Production of reactive oxygen species by mitochondria: central role of complexⅢ [J]. Journal of Biological Chemistry, 2003, 278: 36027-36031.
[23] DUA R, SUNKARIA A, KUMAR V. Impaired mitochondrial energy metabolism and kinetic properties of cytochrome oxidase following acute aluminium phosphide exposure in rat liver[J]. Food and Chemical Toxicology, 2010, 48: 53-60.
[24] SOLOMOS T, LATIES G G. Effects of ethylene and cyanide on the respiration of cyanid sensitive and cyanide-resistant plant tissues[J]. Plant Physiology, 1976, 58: 47-50.
[25] SAULEDA J, GARCI´A-PALMER F J, WIESNER R. Cytochrome oxidase activity and mitochondrial gene expression in skeletal muscle of patients with chronic obstructive pulmonary disease[J]. American Journal of Respiratory and Critical Care Medicine, 1998, 157: 1413-1417.
Changes in Mitochondrial Cytochrome c Oxidase in Two Peach Cultivars during Maturation and Senescence
KAN Juan, LU Yan-fei, LIU Jun, JIN Chang-hai*
(College of Food Science and Engineering, Yangzhou University, Yangzhou 225127, China)
The activity of cytochrome c oxidase (COX) and the expression levels of mitochondrial DNA (mtDNA)-encoded COX subunits in two peach (Prumus persica) cultivars ‘Yuhuasanhao’ and ‘Jianayan’ were determined for analyzing their relationship with peach fruit ripening and senescence. The results showed that COX activities in the two peach cultivars increased in the early stages of maturity (Ⅰ-Ⅲ), followed by a decrease. COX activities were higher in ‘Jianayan’ peach fruit than in ‘Yuhua 3’ peach fruit. The expression levels of mtDNA- encoded COX subunits were higher in the early stage than in the later stage of maturity. MtDNA-encoded COX subunits played a major role in the early maturity stage of peach fruit and provided the energy needed for peach growth and metabolism. In the later maturity stage, the decreases in the abundance of catalytic subunits of mtDNA-encoded COX could underlie the senescence-associated loss of enzyme activity, which could change a component of the mitochondrial electron transport chain and underlie the senescence-related decrease in mitochondrial respiratory activity and reactive oxygen species accumulation.
peach; mitochondria; respiration rate; cytochrome c oxidase
TS255.1
A
1002-6630(2014)20-0276-05
10.7506/spkx1002-6630-201420054
2013-09-13
国家自然科学基金青年科学基金项目(31101586);江苏省科技计划项目(BC2013401);江苏省自然科学基金项目(BK2010310)
阚娟(1980—),女,副教授,博士,研究方向为农产品贮藏与加工。E-mail:kanjuan@yzu.edu.cn
*通信作者:金昌海(1963—),男,教授,博士,研究方向为农产品贮藏与加工。E-mail:chjin@yzu.edu.cn
