阿魏酸改性胶原蛋白-壳聚糖复合膜工艺优化
2014-01-18陈达佳袁美兰
陈达佳,赵 利,袁美兰,苏 伟,刘 华
(江西科技师范大学生命科学学院,国家淡水鱼加工技术研发分中心,江西 南昌 330013)
阿魏酸改性胶原蛋白-壳聚糖复合膜工艺优化
陈达佳,赵 利*,袁美兰,苏 伟,刘 华
(江西科技师范大学生命科学学院,国家淡水鱼加工技术研发分中心,江西 南昌 330013)
以鮰鱼皮胶原蛋白与壳聚糖为原料制备可食用复合膜,用阿魏酸进行改性。通过正交试验考察阿魏酸添加量、热处理温度和热处理时间对复合膜性能的影响,以期降低复合膜的水蒸气透过率和增强复合膜的机械性能。结果表明:阿魏酸添加量、热处理温度、热处理时间对复合膜的性能影响显著。最佳改性条件为:阿魏酸添加量2%、热处理温度70 ℃、热处理时间30 min。在此条件下,得到复合膜拉伸强度(24.72±0.86) MPa、断裂伸长率(102.99±1.58)%、水蒸气透过率(0.25±0.01) (g·mm)/(h·m2·kPa)、溶解度(27.96±0.76)%、透光率(84.1±0.9)%。
阿魏酸;胶原蛋白;壳聚糖;改性;复合膜
在过去10 a中,可再生、可降解的天然聚合物在食品包装膜上的应用引起了人们的广泛关注。然而用这些天然聚合物做成的包装膜并不能完全取代合成塑料[1],原因是可食用膜与合成聚合膜(如低密度聚乙烯膜、高密度聚乙烯膜)相比,其拉伸强度低、水蒸气透过率高[2]。针对可食用膜的这些缺点,一些可食用膜改良剂逐渐被研究出来,使得可食用膜在一些应用上仍然有潜力代替合成聚合膜。
常见可食用膜的基质主要有蛋白质、多糖、脂质及它们之间的混合物[3-4]。可食用膜可以被微生物所降解或与被包装食品一起食用,也可以作为添加剂的载体,例如抗菌剂、抗氧化剂、维生素、芳香物质及色素等[5-8]。此外可以用来制作可食用膜的天然聚合物(如胶原蛋白、壳聚糖)都可以从工业下脚料中获得。
蛋白质和多糖具有亲水性,由这些高分子做成的可食用膜能有效的阻隔氧气、二氧化碳、香味物质和油脂等,但与合成聚合物相比,它们的一些性能(如高水蒸气透过率、低机械性能)限制了其应用[9]。因此,可食用膜常常需要改性,常用改性的方法有化学改性、物理改性和酶法改性。化学改性、物理改性和酶法改性分别是通过使用交联剂戊二醛、γ射线和转谷氨酰胺酶交联聚合物链改变聚合物网络结构,从而提高生物膜的性能。但戊二醛有细胞毒性,超声波、γ射线和转谷氨酰胺酶成本太高[10]。
阿魏酸是广泛存在于植物界的一种酚酸,可以交联蛋白质[11]、多糖[12]、蛋白质与多糖[13]、多糖与多糖[14],安全无毒、价格低廉[15]。阿魏酸能增加蛋白质或者多糖的交联主要通过以下一些机制:一是通过以醌为媒介反应进行交联[16-17];二是通过与蛋白质或者多糖的羟基进行酯化来交联;三是以自由基为媒介进行交联[18]。
本研究旨在利用阿魏酸交联胶原蛋白与壳聚糖复合成膜,以期在维持良好的机械性质、溶解度、透光率性质的基础上降低水蒸气透过率性质。
1 材料与方法
1.1 材料与试剂
胶原蛋白由农业部淡水鱼加工技术研发分中心(南昌)提供[8];壳聚糖 北京索莱宝科技有限公司;阿魏酸、甘油、冰乙酸等均为分析纯。
1.2 仪器与设备
CT3质构仪 美国BrookField公司;N-1100旋转蒸发仪 东京理化器械公司;79HW-1恒温磁力搅拌器江苏省金坛市荣华仪器制造有限公司;烘箱 上海一恒科学仪器有限公司;UV-1100紫外分光光度计 上海美谱达仪器有限公司。
1.3 方法
1.3.1 复合膜的制备
将壳聚糖溶于2%的乙酸溶液中,加热搅拌后得到质量分数为2%的壳聚糖溶液。用0.5 mol/L的乙酸提取鮰鱼皮中的胶原蛋白3 d,取一定量旋转蒸发浓缩至质量分数为6.67%。
将上述胶原蛋白溶液与壳聚糖溶液按质量比6∶4混合,加入占总溶质质量分数20%的甘油,然后加入一定量的阿魏酸,在一定温度条件下加热搅拌一段时间,去除气泡,流延于聚乙烯盘内,在50 ℃条件下干燥24 h,移出后揭膜,将膜置于盛有饱和Mg(NO3)2·6H2O溶液的干燥器中,25 ℃条件下,保持相对湿度(50±3)%,48 h后测定膜的各项性能指标。
1.3.2 机械性能的测定
按照Arvanitoyannis等[19]的方法,采用质构仪TAXT2i测定各膜的抗拉伸强度(tensile strength,TS)和断裂拉伸率(elongation at break,EAB)。每种膜测定5 个平行样,每个样品大小为1.5 cm×8 cm。
TS指膜在轴向拉伸力作用下,破裂前所承受的最大应力,按式(1)计算:
式中:TS为膜的抗拉伸强度/MPa;F为轴向拉伸力/ N;L为膜的宽度/mm;X为膜的厚度/mm。
EAB是评价膜在拉伸测试中破裂时延伸能力的指标,按式(2)计算:
式中:EAB为断裂伸长率/%;E为膜样品在断裂时所达到的长度/mm;E0为膜的初始长度/mm。
1.3.3 水蒸气透过率(water vapor permeability,WVP)的测定
采用修正的ASTM[20]方法测定。干燥器底部加入蒸馏水,25 ℃条件下,蒸馏水使干燥器内的相对湿度保持在100%。透湿杯内装无水氯化钙,透湿杯上覆盖待测膜,置于相对湿度为50%的干燥器内,每隔1 h称量透湿杯的质量。水蒸气透过率按式(3)计算:
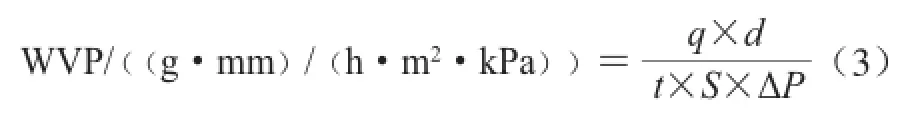
式中:WVP为水蒸气透过率/((g·mm)/(h·m2·kPa));q/t为单位时间内透湿杯增加质量的算术平均值/(g/h);d为样品膜厚度/mm;S为样品膜实验面积/m2;ΔP为试样两侧的蒸汽压/kPa,由于膜两侧的相对湿度梯度为50%、测定温度为25℃,故Δ P为1.58 kPa。
1.3.4 溶解度的测定
按照Gontard等[21]的方法,将膜样(2 cm×2 cm)在100 ℃条件下干燥至质量恒定,称质量M1,然后将样品直接放入盛有50 mL蒸馏水的离心管中,在室温25 ℃条件下浸泡24 h,隔一段时间搅动离心管。将没有溶解的膜取出来,用滤纸吸干表面的水分,在100 ℃条件下干燥至质量恒定,称质量M2。溶解度(S)按式(4)计算:

式中:S为膜的溶解度/%;M1为膜溶解前干燥后的质量/g;M2为未溶物干燥后的质量/g。
1.3.5 透光率的测定
将待测样品裁剪成10 mm×50 mm矩形,贴于比色皿内侧,采用修正过的ASTM[22]方法在800 nm波长处测定透光率,以空比色皿作为对照,用透光率(T)大小间接表示膜的透明度。
1.3.6 单因素试验
1.3.6.1 阿魏酸添加量对复合膜性质的影响
分别添加占总溶质质量1%、2%、3%、4%、5%的阿魏酸,在70 ℃条件下加热搅拌30 min,按照1.3.1节所述制备复合膜后测定各项指标。
1.3.6.2 热处理温度对复合膜性质的影响
了空法师轻轻地叹了口气,看来这孩子尘缘未了,暂时不给他受戒看来是对的。佛门修身更修心,若只受戒而不持戒,又有何用?说来这寺院也气象庄严,进了这佛门净地,遁入了空门,应当四大皆空,六根清净的,可人心偏偏既不清也不静,消除不了世俗欲念,连一个小和尚也不例外。了空法师又沉沉地叹息了一声,离开佛殿,穿过天井,进自己的禅房去了。
加入占总溶质质量2%的阿魏酸,分别在50、60、70、80、90 ℃条件下加热搅拌30 min,按照1.3.1节所述制备复合膜后测定各项指标。
1.3.6.3 热处理时间对复合膜性质的影响
加入占总溶质质量2%的阿魏酸,分别在70 ℃条件下加热搅拌10、30、50、70、90 min,按照1.3.1节所述制备复合膜后测定各项指标。
1.3.7 正交试验
综合考虑阿魏酸添加量、热处理温度、热处理时间对复合模制备的影响,按照L9(34)进行正交试验设计,以拉伸强度、断裂伸长率、水蒸气透过率为表观特征评分指标,表观评分标准公式:评分=A+B+2C(A代表TS表观特征得分,B代表EAB表观特征得分,C代表WVP表观特征评分)。相应正交试验的因素和水平、复合膜表观特征评分标准分列在表1、2。
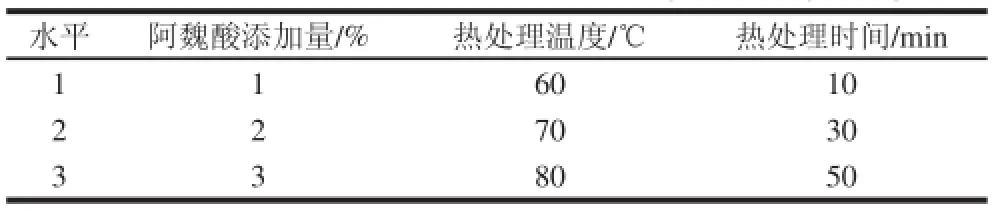
表1 正交试验因素水平Table1 Factors and levels used in orthogonal array design
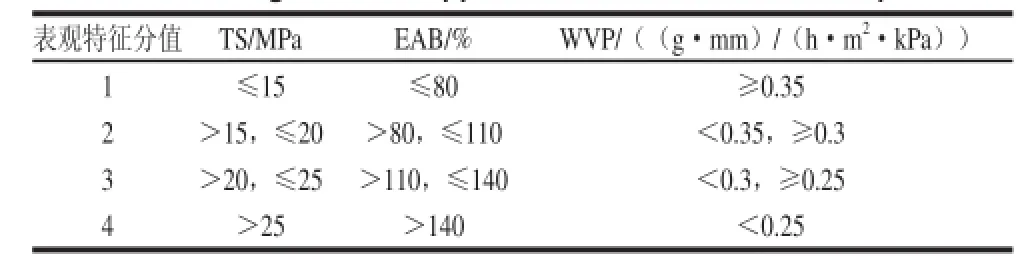
表2 复合膜表观特征评分标准Table2 Grading criteria for apparent characteristics of the composite film
2 结果与分析
2.1 单因素试验
2.1.1 阿魏酸添加量对复合膜性质的影响
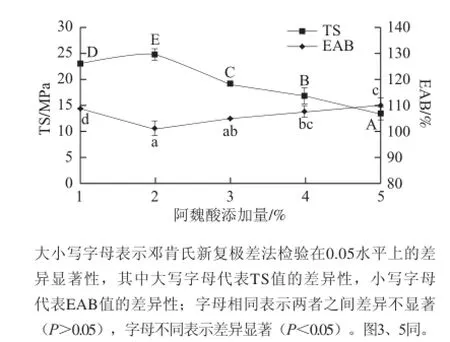
图1 阿魏酸添加量对复合膜机械性质的影响Fig.1 Effect of ferulic acid concentration on mechanical properties of the composite film
由图1可知,复合膜的TS随着阿魏酸添加量的增加先增加后减小。当阿魏酸添加量开始增加,复合膜的抗拉伸强度增加,阿魏酸的含量为2%时,TS值达到最大(24.69±1.04) MPa,这可能是由于阿魏酸的交联作用使CO—CH形成稳定化网络结构,使得膜更加致密,从而使得复合膜TS值增加[13]。但随着阿魏酸添加量的进一步增加,多余的阿魏酸不能与CO—CH反应而游离于复合膜中,形成相分离,从而降低了复合膜的TS,这与Ou Shiyi等[11]的研究结果相似。复合膜的EAB值随着阿魏酸添加量的增加先减小后增加。当阿魏酸添加量开始增加时,EAB值减小,阿魏酸添加量为2%时,EAB达到最小值(101.03±2. 51)%,这可能是由于阿魏酸增加了CO—CH分子间的交联,减小了其分子间的距离,使得EAB值降低。但当阿魏酸含量进一步增加时,EAB值开始增加,这可能是由于多余的阿魏酸减弱了CO—CH分子之间的相互作用,使得成膜分子间的距离增加。
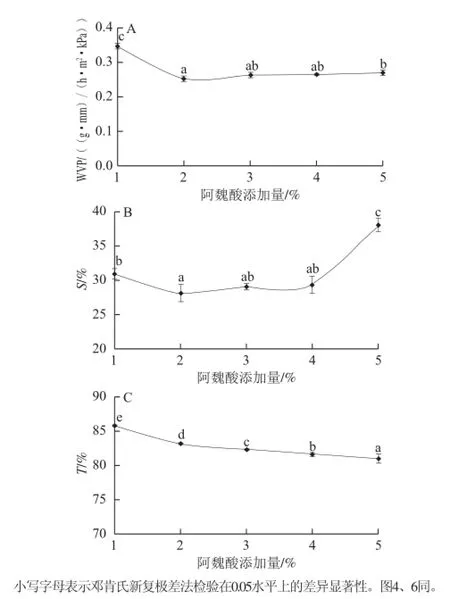
图2 阿魏酸添加量对复合膜水蒸气透过率(A)、溶解度(B)、透光率(C)的影响Fig.2 Effect of ferulic acid concentration on WVP (A), S (B), and T (C) properties of the composite film
综上可知,当添加阿魏酸添加量为2%时,复合膜的TS值达到最大,WVP值最低,故选择阿魏酸添加量2%为最佳单因素。
2.1.2 热处理温度对复合膜性质的影响
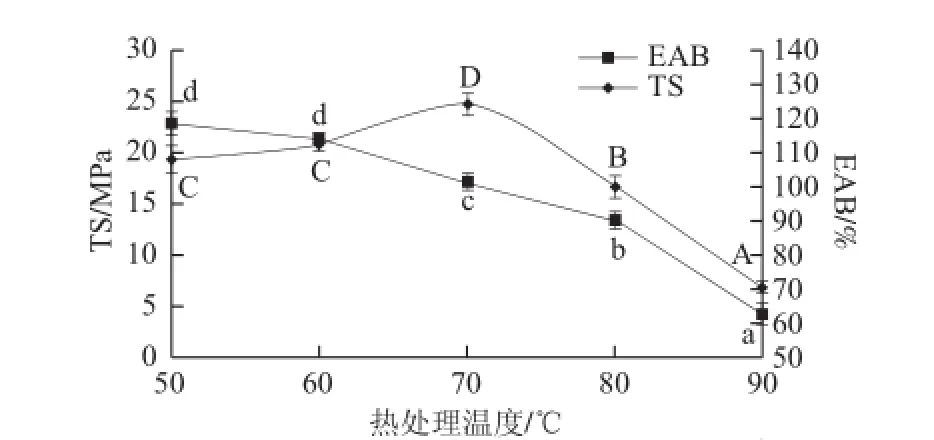
图3 热处理温度对复合膜机械性质的影响Fig.3 Effect of heat treatment temperature on mechanical properties of the composite film
由图3可知,复合膜的TS值随着热处理温度的升高先增加后减小。热处理温度为70 ℃时TS值达到最大为(24.69±1.04)MPa,这可能是由于较高的热处理温度有助于胶原蛋白与壳聚糖分子的运动速度,提高阿魏酸交联两者的机率,增加了两种分子相互作用的机会,使得相互作用力逐渐增强,形成膜的结构也趋于致密。当热处理温度达到80、90 ℃,TS值显著降低到(16.53±1.20)、(6.86±0.61)MPa,这可能是由于此加热温度导致胶原蛋白与壳聚糖形成的交联物质热变性,使得膜的TS值下降。复合膜的EAB值随着热处理温度的增加而先显著减小,在热处理温度为50~70 ℃时,复合膜EAB值减小,这可能是由于较高的热处理温度有助于提高胶原蛋白与壳聚糖分子的运动速度,增大阿魏酸交联两者的机率,增强了两种分子之间相互作用的机会,使相互作用力逐渐增强,膜结构趋于致密。当热处理温度为80、90 ℃,复合膜EAB值从(101.03±2.51)%降低到(90.06±2.42)%、(62.38±3.42)%,这可能是由于此时加热温度导致胶原蛋白与壳聚糖形成的交联物质热变性,使得EAB值降低。
由图4A、B可知,复合膜WVP值和S值随着热处理温度升高先减小后增加。在70 ℃时,两者均达到最低(0.25±0.01)(g·mm)/(h·m2·kPa)、(28.19±1.27)%。这可能是由于较高的热处理温度有助于提高胶原蛋白与壳聚糖分子的运动速率,提高了阿魏酸交联两者的机率,增加两种分子相互作用的机会,使得相互作用力逐渐增强,形成的膜结构也趋于致密,从而降低水蒸气透过率,并使膜不易破裂和溶解。当温度达到80、90 ℃,WVP值和S值显著增加,S值分别显著增加到(44.66±1.98)%、(56.42±1.58)%,这可能是由于此加热温度导致胶原蛋白与壳聚糖形成的交联物质热变性。由图4C可知,热处理温度对复合膜在800 nm波长处的透光率有显著影响,复合膜T值随着热处理温度的升高而逐渐增加。
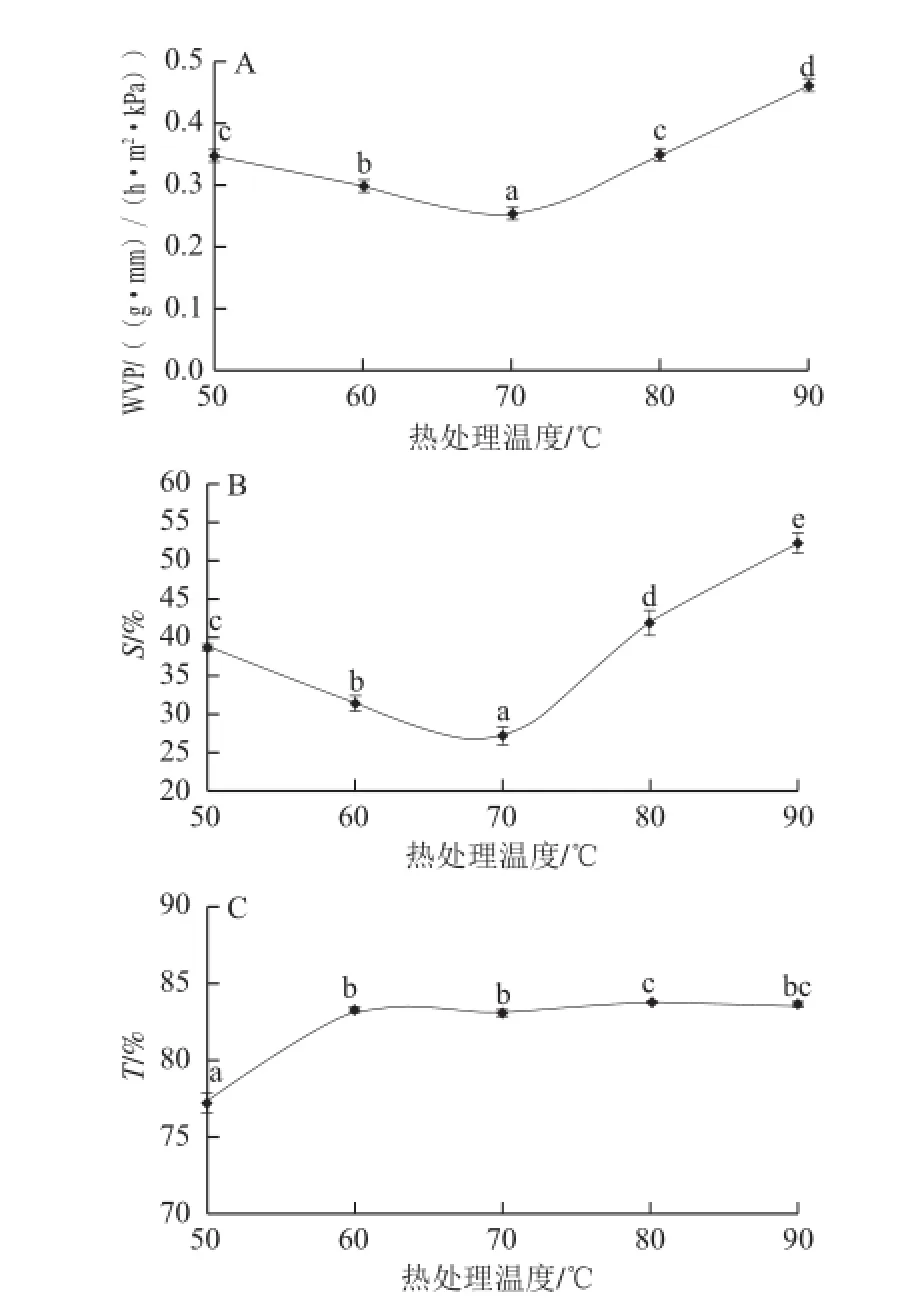
图4 热处理温度对复合膜水蒸气透过率(A)、溶解度(B)、透光率(C)的影响Fig.4 Effect of heat treatment temperature on WVP (A), S (B) and T (C) properties of the composite film
综上可知,当热处理温度为70 ℃时,复合膜的TS值达到最大,WVP值最低,故选择热处理温度70 ℃为最佳单因素。
2.1.3 热处理时间对复合膜性质的影响
由图5可知,复合膜TS值随着热处理时间的延长先显著增加后显著减小。当热处理时间开始增加时,复合膜TS值增加,热处理时间为30 min时,TS值达到最大(24.69±1.04)MPa,这可能是由于热处理时间较短时,胶原蛋白与壳聚糖在较短时间的磁力搅拌作用下分子间相互作用位点增多,有利于阿魏酸交联,使得分子间作用力增强,TS值增加。但在时间进一步延长时,搅拌容易打断部分已形成的胶原蛋白-壳聚糖交联结构,从而使得TS值降低。复合膜的EAB值随着热处理时间的延长先增加后显著减小。当热处理时间开始延长时,复合膜EAB值增加,这可能是由于在热处理时间为10 min时,胶原蛋白-壳聚糖混合的不均匀,不利于阿魏酸的交联,且阿魏酸可能与胶原蛋白-壳聚糖溶液相分离,有较低EAB值。当热处理时间达到30 min时,胶原蛋白-壳聚糖混合均匀,开始有利于阿魏酸的交联,EAB值增加到(101.03±2.51)%。但当热处理时间进一步延长,搅拌容易打断部分已形成的胶原蛋白-壳聚糖交联结构,使得EAB值降低。
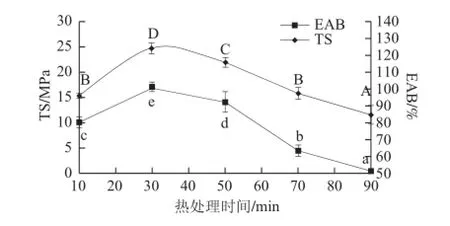
图5 热处理时间对复合膜机械性质的影响Fig.5 Effect of heat treatment time on mechanical properties of the composite film
由图6A、B可知,复合膜WVP值和S值随着热处理时间的延长而先减小后缓慢增加。当热处理时间更长时,二者减小,当热处理时间为30 min时,WVP值达到最小(0.25±0.01)(g·mm)/(h·m2·kPa),S值达到最小(28.19±1.27)%。这可能是由于胶原蛋白与壳聚糖在较短时间的磁力搅拌作用下分子间相互作用位点增多,有利于阿魏酸交联,使得分子间作用力增强,膜结构更加致密,有利于阻隔水分的迁移,使得膜不易破裂和溶解。当热处理时间进一步增加时WVP值没有显著的改变,而复合膜的S值的显著增加可能是由于搅拌容易打断部分已形成的胶原蛋白-壳聚糖交联结构。由图6C可知,热处理温度对复合膜在800 nm波长处的透光率有显著影响,复合膜T值随着热处理温度的增加而逐渐增加。
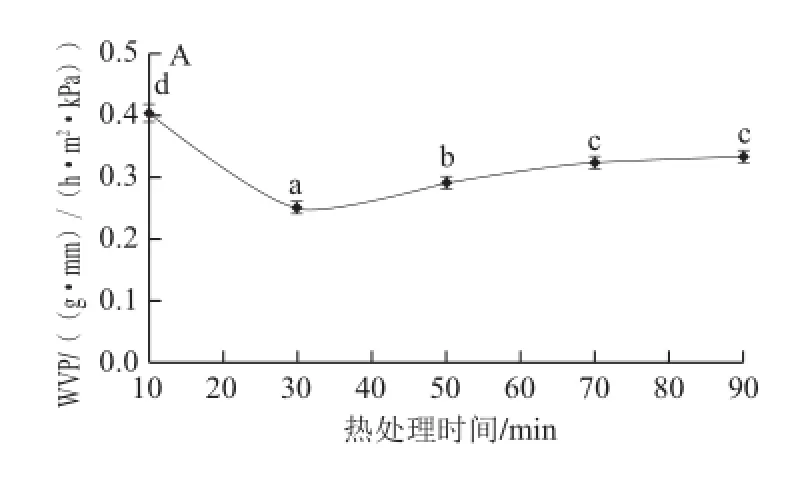
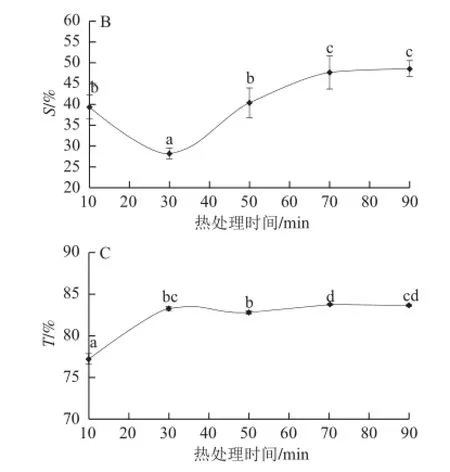
图6 热处理时间对复合膜水蒸气透过率(A)、溶解度(B)、透光率(C)的影响Fig.6 Effect of heat treatment time on WVP (A), S (B) and T (C) properties of the composite film
综上可知,当热处理时间为30 min时,复合膜的TS值达到最大,WVP值最低,故选择热处理时间30 min为最佳单因素。
2.2 改性复合膜制备工艺优化
2.2.1 正交试验
通过单因素试验表明,阿魏酸添加量、热处理温度、热处理时间对复合膜的机械性能和水蒸气透过率性能有不同程度的影响。正交试验结果见表3、4。
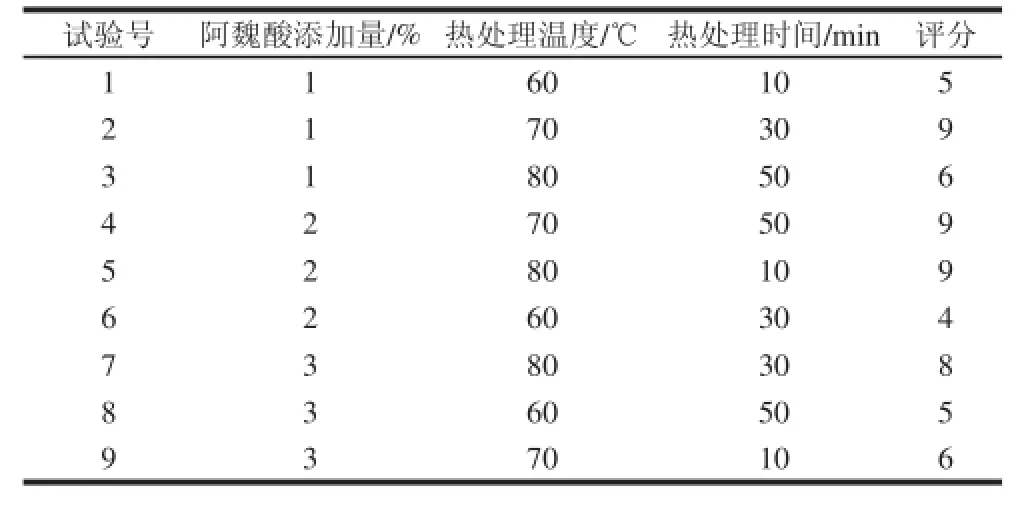
表3 正交试验设计及结果Table3 Orthogonal array design and results
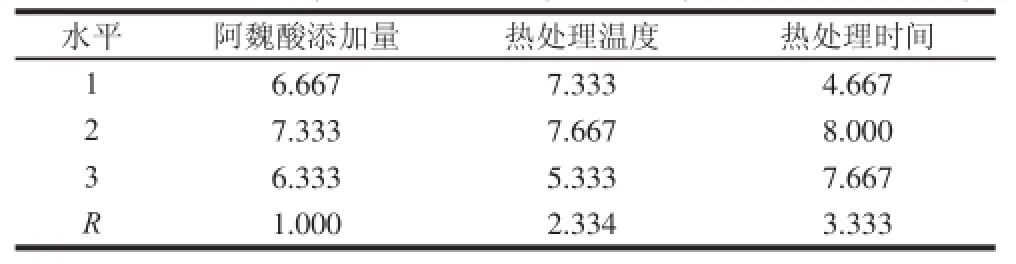
表4 正交试验方差分析结果Table4 Visual analysis of the orthogonal array experimental design
由表4可以看出,水平2得分最高,所以最优工艺条件为阿魏酸添加量2%、热处理温度70 ℃、热处理时间30 min。
2.2.2 验证实验
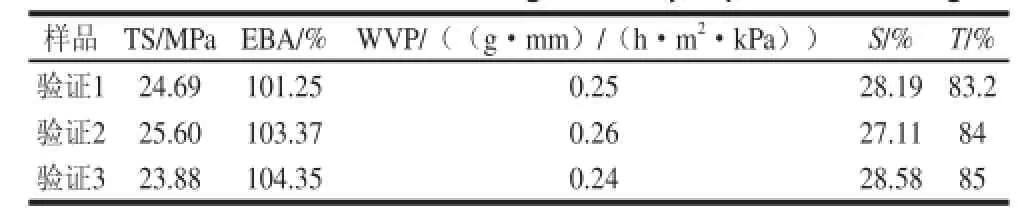
表5 正交试验验证结果Table5 Validation of the orthogonal array experimental design
按照正交试验筛选出的工艺条件阿魏酸添加量2%、热处理温度70 ℃、热处理时间30 min进行3 次验证实验。由表5可以看出,3 次验证实验的结果没有显著性差异。得到结果为伸强度(24.72±0.86)MPa、断裂伸长率(102.99±1.58)%、水蒸气透过率(0.25±0.01)(g·mm)/(h·m2·kPa)、溶解度(27.96±0.76)%、透光率(84.1±0.9)%。说明所筛选出来的工艺合理可行,稳定可靠,具有可重复性。
3 结 论
通过阿魏酸改性胶原蛋白-壳聚糖复合膜实验表明:阿魏酸添加量、热处理温度、热处理时间对复合膜的性能影响显著。最佳改性条件为阿魏酸添加量2%、热处理温度70 ℃、热处理时间30 min,此时得到复合膜拉伸强度(24.72±0.86)MPa、断裂伸长率(102.99±1.58)%、水蒸气透过率(0.25±0.01)(g·mm)/(h·m2·kPa)、溶解度(27.96±0.76)%、透光率(84.1±0.9)%。这些性能的改变说明阿魏酸能够增加胶原蛋白-壳聚糖复合膜分子间的交联,改善复合膜的特性。机械性能的增加能够增强可食用膜的物理包装性能,水蒸气透过率的降低能够减少食品与外部环境的水分转移速率,不仅能减少食品水分的损失,而且能够减少食品受到外界环境的污染,在此基础上可望开发出一种具有广发应用前景的新型可食用膜材料。
[1] KROCHTA J M, MULDER-JOHNSTON C D. Edible and biodegradable polymer films: challenges and opportunities[J]. Food Technology, 1997, 51(2): 61-74.
[2] CUNNINGHAM P, OGALE A A, DAWSON P L. Tensile properties of soy protein isolate lms produced by a thermal compaction technique[J]. Journal of Food Science, 2000, 65(4): 668-671.
[3] CAO Na, FU Yuhua, HE Junhui. Preparation and physical properties of soy protein isolate and gelatin composite films[J]. Food Hydrocolloids, 2007, 21(7): 1153-1162.
[4] CUQ B, GONTRAD N, CUQ J L, et al. Selected functional properties of fish myofibrillar protein-based films as affected by hydrophilic plasticizers[J]. Journal of Agricultural and Food Chemistry, 1997, 45(3): 622-626.
[5] CAMPOS C, GERSCHENSON L, FLORES S. Development of edible films and coatings with antimicrobial activity[J]. Food Bioprocess Technology, 2011, 4(6): 849-875.
[6] BASTARRACHEA L, DHAWAN S, SABLANI S. Engineering properties of polymeric-based antimicrobial films for food packaging[J]. Food Engineering Reviews, 2011, 3(2): 79-93.
[7] SILVA M A, BIERHALZ A C K, KIECKBUSCH T G. Alginate and pectin composite films crosslinked with Ca2+ions: effect of the plasticizer concentration[J]. Carbohydrate Polymers, 2009, 77(4): 736-742.
[8] AIDER M. Chitosan application for active bio-based films production and potential in the food industry: revie w[J]. LWT-Food Science Technology, 2010, 43(6): 837-842.
[9] NOBREGA M, OLIVATO J, VICTORIA M, et al. Effects of the incorporation of saturated fatty acids on the mechanical and b arrier properties of biodegradable films[J]. Journal of Applied Polymer Science, 2012, 124(5): 3695-3703.
[10] SINDHU M T, EMILIA A. Characterisation of ferulic acid incorporated starch-chitosan blend film[J]. Food Hydrocolloids, 2008, 22(5): 826-835.
[11] OU Shiyi, WANG Yong, TANG Shuze, et al. Role of ferulic acid in preparing edible films from soy protein isolate[J]. Journal of Food Engineering, 2005, 70(2): 205-210.
[12] MATHEW S, ABRAHAM T E. Characterisation of ferulic acid incorporated starch-chitosan blend film[J]. Food Hydrocolloids, 2008, 22(5): 826-835.
[13] OUDGENOEG G, HILHORST R, PIERSMA S R, et al. Peroxidasemediated cross-linking of a tyrosine-containing peptide with ferulic acid[J]. Journal of Agricultural and Food Chemistry, 2001, 49(5): 2503-2510.
[14] HATFIELD R D, RALPH J, GRABBER J H. Cell wall cross linking by ferulates and diferulates in grasses[J]. Journal of the Science of Food and Agriculture, 1999, 79(3): 403-407.
[15] PAN G X, SPENCER L, LEARY G J. Reactivity of ferulic acid and its derivatives towards hydrogen peroxide and peracetic acid[J]. Journal of Agricultural and Food Chemistry, 1999, 47(8): 3325-3331.
[16] HURRELL R F, FINOT P A. Nutritional consequences of the reactions between proteins and oxidized polyphenolic acids[J]. Advances in Experimental Medicine and Biology, 1984, 177: 421-435.
[17] O’CONNELL J E, FOX P F. Proposed mechanism for the effect of polyphenols on the heat stability of milk[J]. International Dairy Journal, 1999, 9(8): 523-536.
[18] FIGUEROA-ESPINOZA M C, MOREL M H, SURGET A, et al. Attempt to crosslink feruloylated arabinoxylans and proteins with a fungal laccase[J]. Food Hydrocolloids, 1999, 13(1): 65-71.
[19] ARVANITOYANNIS I, BILIADERIS C G. Physical properties of polyol-plasticized edible films made from sodium caseinate and soluble starch blends[J]. Food Chemistry, 1998, 62(3): 333-342.
[20] ASTM. Standard test method for water vapor transmission of materials (E 96-93)[S]. Philadelphia: American Society for Testing and Materials, 1993.
[21] GONTARD N, GUILBERT S, CUQ J L. Edible wheat gluten films: influence of the main process variables on film properties using response surface methodology[J]. Journal of Food Science, 1992, 57(1): 190-195.
[22] ASTM. Standard test method for haze and luminous transmittance of transparent plastics (D 1003-07)[S]. Philadelphia: American Society for Testing and Materials, 2007.
Effect of Modification with Ferulic Acid on Properties of Collagen-Chitosan Edible Films
CHEN Da-jia, ZHAO Li*, YUAN Mei-lan, SU Wei, LIU Hua
(National R&D Branch Center for Conventional Freshwater Fish Processing, School of Life Science, Jiangxi Science and Technology Normal University, Nanchang 330013, China)
The aim of this work was to develop composite edible film based on Amiurus nebulosus skin collagen and chitosan using ferulic acid to modify functional properties of the composite film. The effects of ferulic acid concentration, temperature and heating time on the water vapor permeability and mechanical properties of the edible film were investigated by using an orthogonal array design. The results showed that all the investigated variables could affect significantly the properties of the films. The tensile strength, elongation at break, water vapor permeability, solubility, and light transmittance of the composite film prepared by adding 2% ferulic acid and heating at 70 ℃ for 30 min were (24.72 ± 0.86) MPa, (102.99 ± 1.58)%, (0.25 ± 0.01) (g mm)/(h m2kPa), (2 7.96 ± 0.76)%, and (84.1 ± 0.9)%, respectively.
ferulic acid; collagen; chitosan; modification; composite film
TS254.4
A
1002-6630(2014)20-0073-06
10.7506/spkx1002-6630-201420015
2014-01-11
江西省高等学校科技落地计划项目(KJLD12009)
陈达佳(1986—),男,硕士研究生,研究方向为食品化学。E-mail:kjchendajia@163.com
*通信作者:赵利(1967—),女,教授,博士,研究方向为食品化学。E-mail:lizhao618@hotmail.com
