老年冠心病患者下肢动脉硬化危险因素分析
2014-01-18张小波于俊民王慧冬李大鹤陈洪叶
张小波 于俊民 王慧冬 姜 文 李大鹤 胡 爽 陈洪叶
哈尔滨医科大学附属第四医院老年病一病房,黑龙江哈尔滨 150001
伴随着人口老龄化的加速,冠心病的发病率随增龄而逐年增高。动脉粥样硬化是一系统性进展的病理过程,常可累及冠状动脉、颈动脉及下肢动脉,其具有相同的发病机制及一致的病理衍变过程[1]。 下肢动脉硬化闭塞症 (lower extremity atherosclerosis disease,LEASD)是由于下肢动脉发生粥样硬化进而累及下肢动脉狭窄甚至闭塞,出现不同程度的缺血性疾病[2],主要累及下肢大中动脉,引起下肢缺血症状,缺血性溃疡,甚至干性坏疽,导致行走困难,重者截肢[3]。LEASD病变广泛,呈渐进性发展,是多种因素共同作用的结果。 LEASD 患者的早期发现并积极干预防治,对于改善患者生存质量显得尤为重要。 本研究通过对70 岁以上老年冠心病LEASD 患者伴发疾病等因素进行分析, 旨在探讨影响LEASD 发生、 发展的相关危险因素,为有效预防老年冠心病下肢动脉硬化性病变提供新的思路。
1 资料与方法
1.1 一般资料
选择2014 年1~3 月哈尔滨医科大学附属第四医院住院冠心病稳定型心绞痛患者114 例为研究对象,其中男87 例,女27 例,平均年龄(81.22±5.94)岁,其中LEASD 患者74 例,诊断标准参照老年人四肢动脉粥样硬化性疾病诊治中国专家建议(2012)临床诊断标准[4]。入选患者排除恶性肿瘤、代谢综合征、脑卒中、肺感染及其他炎症患者。根据彩色多普勒超声将下肢动脉硬化者依血管狭窄程度分为狭窄率≥70%组(n=21)和狭窄率<70%组(n=53)。
1.2 观察指标
观察各组患者年龄及相关伴发因素,包括高血压、糖尿病、腔隙性脑梗死、高密度脂蛋白-胆固醇(HDL-C)降低(<1.2 mmol/L)、载脂蛋白A(apoA)降低(<1 g/L)、高同型半胱氨酸血症(HHCY)[同型半胱氨酸(HCY)>15 μmol/L]、超敏C 反应蛋白(hs-CRP)增高(>3 mg/L),并对狭窄率≥70%下肢动脉硬化患者上述伴发因素进行分析。
1.3 统计学方法
采用SPSS 17.0 统计学软件进行数据分析, 计量资料数据用均数±标准差(±s)表示,两组间比较采用t 检验;计数资料用率表示,组间比较采用χ2检验;相关因素分析采用二元Logistic 回归分析, 以P < 0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较
实验入选老年冠心病患者114 例,检出下肢动脉硬化者74 例,均伴发腔隙性脑梗死,占64.9%;下肢动脉硬化者平均年龄为(82.24±5.43)岁、非下肢动脉硬化者为(79.33±6.43)岁,二者年龄差异有统计学意义(P <0.05);下肢动脉硬化狭窄率≥70%组患者21例,狭窄率<70%组53 例,分别占18.4%、46.5%。
2.2 年龄与下肢动脉硬化血管狭窄程度相关性
狭窄率≥70%组≥90 岁的患者所占比例明显高于狭窄率<70%组,差异有高度统计学意义(P <0.01)。见表1。

表1 两组不同年龄患者下肢动脉硬化病变发生情况[n(%)]
2.3 各组患者伴发疾病因素分析
下肢动脉硬化狭窄率≥70%组患者伴发高血压、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高者多于狭窄率<70%组,差异有统计学意义(P <0.05),而两组患者伴发apoA 降低情况比较,差异无统计学意义(P >0.05)。 见表2。
2.4 狭窄率≥70%相关因素分析
以狭窄率≥70%事件为因变量,高血压、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高及年龄为自变量,行二元Logistic 回归分析,结果发现高龄(>90 岁)、高血压、糖尿病、HDL-C 降低、HHCY、hs-CRP 增高是预测老年下肢动脉硬化患者狭窄率≥70%的独立危险因素。 见表3。

表2 各组患者伴发疾病及因素[n(%)]
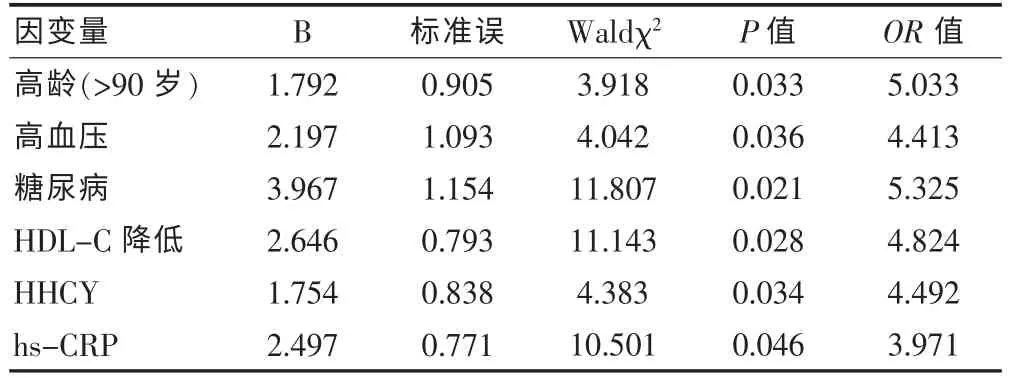
表3 下肢动脉硬化狭窄率≥70%危险因素分析
3 讨论
动脉粥样硬化是中老年人的常见疾病,近年来该病在我国逐年增多[5],病变多发于大、中型动脉,动脉增厚、变硬,伴有粥样斑块及钙化斑,可继发血栓形成。 LEASD 是常见的肢体动脉闭塞性疾病,以动脉粥样硬化和微血管病变为主要机制的病理学改变,临床上表现为以组织缺血为特征的一种慢性病症[6],近年来其发病率、致残率和致死率日趋增高,严重影响老年人群的身心健康[7]。 LEASD 下肢缺血症状仅为全身动脉硬化的外周血管表现,患者往往合并心脑血管疾病。 有文献报道40 岁以后,LEASD 每10 年的发病率增高2~3 倍[8],70 岁以上人群中LEASD 的发病率高达20%[9]。 本研究入选老年冠心病患者114 例,64.9%发生不同程度下肢动脉硬化,所有下肢动脉硬化患者同时患有腔隙性脑梗死,18.4%下肢动脉硬化狭窄率≥70%,下肢动脉硬化者平均年龄为(82.24±5.43)岁,随着年龄的增长,LEASD 的发生呈明显增长趋势,与上述报道相符。
目前,LEASD 流行病学资料研究较少,仍缺乏大样本研究[10],既往发现其危险因素比较复杂,例如:吸烟、高血脂、糖尿病等,但这些因素尚不能完全解释LEASD 的发生和发展, 临床资料亦显示并不是所有患者都存在这些危险因素。 已证实氧化应激、慢性炎症和内皮损伤是LEASD 的核心环节[11]。 近年来国内外多项实验证实体内HCY 对血管内皮细胞有毒性作用,造成血管内皮细胞骨架结构发生变化,易于促进血管内壁增厚,刺激血管平滑肌细胞增殖,增加血液中血小板的黏附性,甚至形成闭塞[12]。 HCY 是蛋氨酸代谢产生的中间产物, 生理情况下HCY 的代谢处于动态平衡状态,维持体内含硫氨基酸的平衡。 血HCY水平升高可损伤动脉内皮,导致动脉管腔狭窄甚至闭塞[13],而氧化应激贯穿高HCY 引起动脉粥样硬化发生和发展的全过程。动脉粥样硬化同时是一种慢性炎症性疾病,研究表明hs-CRP 是独立的动脉粥样硬化发展预测指标[14]。CRP 作为一种全身炎症的血清标志物,反映炎症的范围和活动力,其改变早于临床症状,同时反映粥样斑块的活动度,它的升高可能在动脉硬化发生发展中起促进作用。 在多重因素作用下,下肢动脉粥样硬化病变进展、加重,促使易损斑块破裂、出血,甚至引发血栓、栓塞。
本次研究入选冠心病LEASD 患者中发现下肢动脉硬化狭窄率≥70%组伴发高血压、 糖尿病、HDL-C降低、HHCY、hs-CRP 增高者明显多于狭窄率<70%组,并且通过二元Logistic 回归分析,结果表明高龄(>90 岁)、高血压、糖尿病、HDL-C 降低、HHCY、hs-CRP增高是预测老年下肢动脉硬化患者狭窄率≥70%的独立危险因素, 由此可见上述各伴发因素在LEASD的发生、发展过程中发挥重要作用。因此在LEASD 患者的治疗过程中, 不仅应注重下肢血管的病变情况,更要进行全身性伴发因素的干预,使患者血压、血糖、血脂达到目标值,同时血HCY、hs-CRP 增高者,积极补充叶酸、维生素B12,有效控制hs-CRP 水平,可能是一个潜在的预防或延缓LEASD 发生、 发展的治疗策略。 HDL 在动脉粥样硬化中的有益作用与其主要结构性蛋白apoA1 密切相关,apoA1 是HDL 的主要成分,含有243 个氨基酸序列,由规则重复的双性螺旋组成[15]。 研究证apoA1 模拟肽在动物模型和人体内具有抗炎抗氧化、抗血小板聚集、抗排斥反应等特性,进而在抗动脉粥样硬化、抗心脏移植排斥反应以及肥胖的相关治疗领域发挥积极的作用[16-17]。 有学者证实apoA1 降低为2 型糖尿病合并LEASD 的相关危险因素[18],但在本研究入选114 例患者中,下肢动脉硬化者apoA 降低与LEASD 无明显相关性,分析原因可能与apoA 含AⅠ、AⅡ、AⅣ等成分,且与apoAⅡ、apoAⅣ在LEASD 发生、发展中是否存在相互作用有关。因此针对apoA 及其各相关亚型在LEASD 进展中的作用尚有待进一步探讨。
LEASD 的治疗已从最初的内膜剥脱术、人工血管或自体大隐静脉旁路开放式手术,转化为血管腔内修复。目前,国内LEASD 的腔内治疗正处于探索实践阶段,尚未得出可靠的循证医学结论[19]。 因此,早期识别积极地控制血压、血糖,调脂,降低血HCY、hs-CRP水平,改善生活方式,可减少或延缓老年冠状动脉及下肢动脉粥样硬化的发生、发展,对降低老年冠心病下肢动脉硬化患者的发病率、致残率及致死率具有极为重要的意义。
[1] 寇璐,冯津萍,秦勤.老年人下肢动脉硬化与冠心病关系的研究[J].中国慢性病预防与控制,2010,18(4):423-424.
[2] 洪泓,关丽卿,陈慕洁.下肢动脉硬化闭塞症治疗趋势与思考[J].中国医学创新,2013,10(24):162-164.
[3] 叶弘,臧晓鹭.中药熏洗辅助治疗以静息痛为主诉的老年下肢动脉硬化闭塞症30 例[J].中国老年学杂志,2013,33(16):4041-4042.
[4] 老年人四肢动脉粥样硬化性疾病诊治中国专家建议写作组.老年人四肢动脉粥样硬化性疾病诊治中国专家建议(2012)[J].中华老年医学杂志,2013,32(2):121-131.
[5] 崔明勇,王珊,黄荣,等.颈动脉彩色多普勒超声在中老年脑梗死患者检查中的临床价值[J].中国医药导报,2013,10(3):100-102.
[6] 史均宝,孙庆华,聂建东,等.糖尿病腹膜透析患者下肢动脉硬化闭塞症的临床状况分析[J].北京大学学报:医学版,2013,45(1):109-113.
[7] 刘永升,魏梅,刘会英,等.西洛他唑对老年下肢动脉硬化闭塞症患者超敏C 反应蛋白、血脂及基质金属蛋白酶-9 的影响[J].实用老年医学,2012,26(4):285-287.
[8] Hiatt WR. Pharm acologic therapy for peripheral arterial disease and clandication[J].J Vasc Surg,2002,36(6):1283-1291.
[9] 赵晓宁.下肢动脉硬化闭塞症的诊断方法[J].现代生物医学进展,2007,7(4):629-631.
[10] 王利会,边忠平,高海涛,等.老年患者下肢动脉硬化闭塞症综合治疗体会[J].中华老年心脑血管病杂志,2012,14(1):86.
[11] 范利,朱冰坡,曹剑.普罗布考对老年下肢动脉硬化症患者血管内皮活性因子及炎性因子的影响[J].微循环血杂志,2006,16(3):55-57.
[12] 尤忠孝,时东彦,张静,等.血清同型半胱氨酸和载脂蛋白a 水平与脑梗死相关性研究[J].脑与神经疾病杂志,2013,21(4):211-212.
[13] 张小波,于俊民,王慧冬,等.阿托伐他汀联合福辛普利对老年稳定型心绞痛血同型半胱氨酸的影响[J].齐齐哈尔医学院学报,2010,31(5):688-689.
[14] Juhan-Vague I,Pyke DM,Alessi MC,et al. Fibrinolytic factors and the risk of myocardial infarction or sudden death in patients with angina pectoris[J].Circulation,1996,94(9):2057-2063.
[15] 郭玉松,曹剑,范利.载脂蛋白A1 模拟肽研究进展[J].中华老年医学杂志,2013,32(12):1368-1371.
[16] 杜林,张振刚.载脂蛋白A-1 模拟肽[J].国际心血管病杂志,2012,39(1):25-27.
[17] 叶颖剑,胡乃中.肝硬化并发肾上腺皮质功能不全患者的临床特点分析[J].临床肝胆病杂志,2012,28(5):364-367.
[18] 殷禄昌,隋萍,林松娟.2 型糖尿病合并下肢动脉硬化闭塞症的危险因素探讨[J].潍坊医学院学报,2011,33(6):474-476.
[19] 吴庆华,杨培.下肢动脉硬化闭塞症治疗现状与努力方向[J].心肺血管病杂志,2013,32(1):1-2.
