月见草油微乳体系的微观结构研究
2014-01-14吴红艳孙长豹刘宁许英一刘然
吴红艳,孙长豹,刘宁,许英一,刘然
(1.东北农业大学食品学院,乳品科学教育部重点实验室,哈尔滨 150030;2.齐齐哈尔大学食品与生物工程学院,黑龙江齐齐哈尔 161006)
月见草油微乳体系的微观结构研究
吴红艳1,2,孙长豹2,刘宁1*,许英一2,刘然2
(1.东北农业大学食品学院,乳品科学教育部重点实验室,哈尔滨 150030;2.齐齐哈尔大学食品与生物工程学院,黑龙江齐齐哈尔 161006)
采用差示扫描量热法鉴定微乳的类型及微乳中水存在状态;通过对不同组分中苏丹Ⅱ熔点测定,推断体系中苏丹Ⅱ存在位置;通过透射电镜观察微乳形态;采用电导法划分微乳液类型。结果表明,微乳液为均匀球状液滴。通过电导法可将微乳分为W/O微乳区、O/W微乳区、LC液晶区和B.C.双连续区。不同类型的微乳热分析曲线不同,10∶1微乳液随水分含量的增高体系由W/O型微乳液转变为O/W型微乳;体系中水存在状态由束缚水过渡到自由水。7∶3微乳含水量小于30%时热分析曲线无明显改变。苏丹Ⅱ在水包油型微乳中被包封在月见草油中。
微乳;月见草油;微观结构;差示扫描量热法;电导法
月见草油是由月见草种子经低温压榨精制而成。月见草油中主要含有不饱和脂肪酸,如亚油酸、α-亚麻酸、γ-亚麻酸等营养成分[1],具有降低血脂、血糖、抗氧化和抗炎作用[2-3]。微乳液是两种互不相溶的物质在界面膜的作用下形成热力学稳定的、低黏度的、各向同性的、透明或半透明的均相分散体系。以月见草油为油相制备食品级微乳,其营养成分更易于被吸收利用,也可作为食品功能因子载体,提高机体利用率[4-5]。目前导电性、黏度、显微成像、热分析、红外光谱等分析技术已被应用在纳米级系统相行为和微观结构研究中[6-7]。Yaghmur等采用差式扫描量热法(Differential scanning calorimetry,DSC)研究低温下含有丙二醇、非离子型表面活性剂微乳体系多组分行为[8]。Thanasukarn等将DSC法用于检测结晶区熔融相变,并分析固体脂肪比例或乳液中冰晶比例[9]。Bauduin等研究反相SDS微乳的组成和结构对电导率影响[10]。Destrée等使用透射电子显微镜观察粒子形态及大小[11]。秦娟等通过透射电镜观察辅助研究微乳液的油水分离机理[12]。
本文研究以月见草油为油相,Tween80和月桂酸为表面活性剂的微乳液微观结构。分别使用电导法、负染色透射电镜法及差示扫描量热法研究微乳液的结构及性能。为考查月见草油微乳液对药物包封情况,试验中以包封油溶性色素苏丹Ⅱ为例,分析微乳载体性质、探究苏丹Ⅱ存在位置。
1 材料与方法
1.1 试剂与仪器
Tween80、月桂酸、苏丹Ⅱ、磷钨酸(国药集团化学试剂有限公司);月见草油(长白山保护开发区长白工坊生态产品有限公司);试验用水为超纯水。
H-7650透射电子显微镜(日本HITACHI公司);BS124S型电子天平(北京赛多利斯仪器系统有限公司);Q-20DSC差示扫描量热仪(美国TA公司);C-MAG HS 4数显型磁力搅拌器(德国IKA);DL-360E型智能超声波清洗器(江苏省昆山市超声仪器有限公司);Heal Force PW系列超纯水器(力新仪器上海有限公司);DDSJ-308A型电导率仪(郑州博科仪器设备有限公司)。
1.2 试验方法
1.2.1月见草油微乳制备
以Tween80与月桂酸质量比为10∶1配制混合表面活性剂,将二者在恒温磁力搅拌器上充分混匀。分别以混合表面活性剂与月见草油按质量比为10∶1,8∶1,6∶1,4∶1,7∶3混合并在恒温磁力搅拌器上进行搅拌(以下分别称作10∶1,8∶1,6∶1,4∶1,7∶3微乳),控制温度为25℃,边搅拌边向其中缓慢滴加水,同时观察烧杯中液体的变化。当体系变得澄清透明,且使用激光笔平行光入射后激光成束,光感强烈、不分散,即形成微乳液。
将过量的苏丹Ⅱ溶解于月见草油中,离心取上层清液。以含有苏丹Ⅱ的月见草油为油相按上述方法制备含苏丹Ⅱ的微乳液。
1.2.2 热分析
1.2.2.1微乳液的DSC分析
分别取10 mg不同配方的微乳放入液体铝盒中称重然后加盖密封。升温速率为10℃·min-1,温度范围为-40~40℃,样品皿为标准液体铝制坩埚,用液固通用压盖机(美国Perkin—Elmer公司)压制。在参比侧放置与样品皿相同的空皿作为对照参比。
1.2.2.2包封苏丹Ⅱ微乳的热分析
精密称取约10 mg的月见草油和苏丹Ⅱ混合物、水和苏丹Ⅱ混合物、以含有苏丹Ⅱ的月见草油为油相制备的微乳、以月见草油为油相,用含有苏丹Ⅱ的水滴加制备的微乳,分别装入液体铝制坩埚压盖,在氮气保护下进行测试。同时精密称取2 mg苏丹Ⅱ粉末于固体坩埚中在相同条件下进行测量,空白铝皿为参比。热分析条件为气氛:高纯氮气;升温速率:10℃·min-1;温度范围:20~200℃。
1.2.3 电导率测量
将一定量的月见草油和混合表面活性剂混合,在25℃下,固定磁力搅拌器转速,将DDSJ-308A型电导率仪的电极放入微乳液中,边搅拌边滴加纯水,同时测定体系电导率。待数据稳定后记录其数值,同时记录此时的滴加水量。电导率测量范围为0~1.999×105μS·cm-1,精确度为±0.5%。
1.2.4 微乳电镜观察
采用透射电镜观察微乳形态。将相应的微乳稀释100倍,滴加约2 μL在铜网上,自然晾干,用2%磷钨酸进行负染,15 min后吸取多余液体上电镜观察其形态。
1.2.5 数据分析
每个试验均进行3次平行试验,采用Origin8.5,Excel等软件对每个样品进行统计分析,所有试验数据取3次平行试验的平均值。
2 结果与分析
2.1 Tween80/月桂酸/月见草油/水微乳体系微观结构的DSC研究
按照油(O)与水(W)的比例不同,微乳液分为油包水型(W/O)微乳液、水包油型(O/W)微乳液和双连续型(B.C.)微乳液三种基本结构。对于W/O型微乳液,油作为连续相,微乳液中水与其他组分相互作用较强;而O/W型微乳液,水作为连续相,所占比例较大,体系中油与表面活性剂紧密结合。
微乳体系中各组成成分即单质水、月见草油、混合表面活性剂(月桂酸和Tween80)的DSC图谱见图1。可知,在-40~40℃温度范围内月见草油、混合表面活性剂的DSC曲线平滑,未出现较大热峰值,而单质水在0℃时有明显吸热峰,对应是自由水在升温过程中吸收热量导致热焓值变化。因此图2中出现吸热峰均可归于样品加热过程中固体水融化时吸收热量。对于10∶1、8∶1、6∶1、4∶1等O/W型微乳,DSC曲线呈现出大而尖锐的吸热峰,与单质水的DSC曲线相似,其对应的温度也与自由态水的融化温度相近,但二者并不重合,随微乳中含油量增高(从10∶1到4∶1)DSC曲线在0℃附近变化趋势越平缓,说明微乳体系中表面活性剂与水和油存在相互作用,影响水溶解和结晶。而7∶3为W/O型微乳,水被包裹在界面膜内,DSC曲线平滑,在0℃附近未见峰值出现。因此在0℃附近存在吸收峰是DCS法区分微乳类型的关键。
2.1.2 DSC法考查微乳液中水存在状态
当水分子接近乳化液界面膜时,其物理化学性质就会发生变化,这一部分水称为界面水或附着水(包括结合水)。这部分水分子所占比例很小,与界面水相比自由水在热力学(如熔点、热焓值、热容量等)、流变学和动力学方面都会发生变化,因此采用热分析法分析检测出微乳液中不同状态水含量变化。
10∶1的O/W型微乳含水质量分数分别在5%~80%时微乳液的DSC图谱见图3。当含水质量分数在5%~30%时,样品DSC曲线无明显吸热峰,此时体系中的水为结合水和和少量束缚水,以表面活性剂亲水基相连的结合水和界面水形式存在,水与表面活性剂相互作用较强,看不见单独的水的融化峰,此时微乳介于油包水和液晶相之间,油作为连续相而水被包裹在内相。随着水含量增加,分散相水滴增大,自由水越多。含水量50%时-5℃出现吸热峰,说明在30%~50%,体系中束缚水含量越多,形成游离的自由水,峰值温度趋向于自由水熔点0℃。当含水量大于50%时,明显的吸热峰出现在0~10℃附近,这是微乳中自由水融化温度,随水含量增加,峰开始温度向右偏移,放热峰面积逐渐增大,说明微乳液中自由水含量逐渐增加,此时体系随着水量的增加逐渐转变成水包油型微乳液。
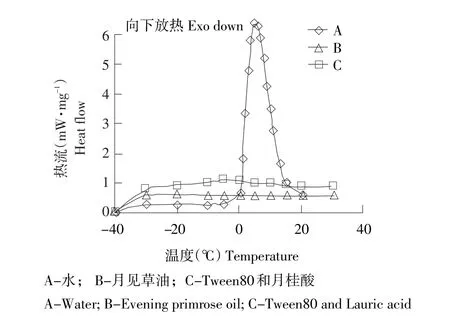
图1 微乳中不同组分的DSC图谱Fig.1 DSC themorgrams of various components of microemulsion
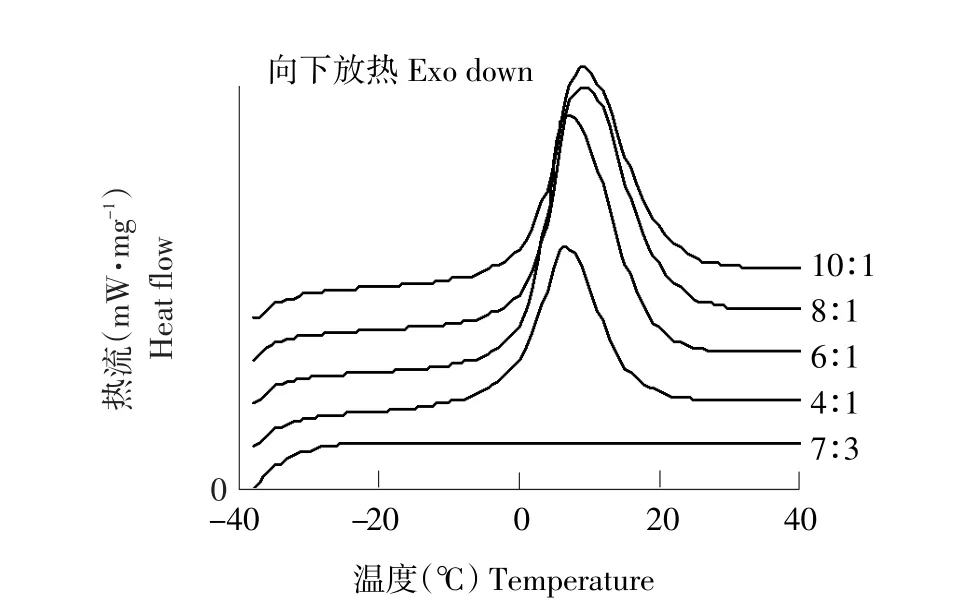
图2 不同配方的微乳液DSC图谱Fig.2 DSC themorgrams of different formulations of microemulsion
而在相对应的图4中7∶3微乳的DSC图谱中可以看出,当体系含水量在小于30%时,DSC谱图没有呈现明显的吸热峰,这也是W/O微乳的特征图谱。当含水量达到30%时,DSC图谱开始呈现较小的吸热峰,即体系束缚水含量增多,随着水量的逐渐增加微乳中水的存在状态也由束缚水向自由水转化。由于7∶3微乳不是U型微乳,不能无限稀释,因此随着水分的增大微乳液出现浑浊,黏度加大,体系已经失去微乳特征,由W/O型微乳过渡到乳浊液。体系中的表面活性剂的量明显不足,水以游离的状态分散在油中,所以DSC曲线上可以看到自由水的吸热峰,而且随着水量的增加峰面积也逐渐增大。因此采用差示扫描量热法(DSC)可以测定出水在微乳液中的存在状态[13-15],也可判断出微乳液的类型和结构,但是不能用此方法判断此液体是否为微乳液。
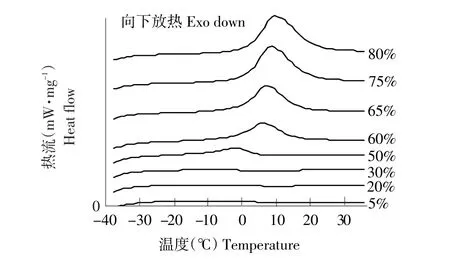
图3 不同含水量的水包油型微乳(10∶1)的DSC图谱Fig.3 DSC themorgrams of various content of water in microemulsion(10∶1)

图4 不同含水量的油包水型微乳(7∶3)的DSC图谱Fig.4 DSC themorgrams of various content of water in microemulsion(7∶3)
2.1.3 水包油型月见草油微乳热分析表征
对逆变器与DC/DC的级联系统建立MATLAB/Simulink仿真模型,其中电感值设置为4 mH,电容值设置为8 000 μF,内阻0.044 Ω,电池侧直流电压为1 100 V,直流环节侧的期望电压设置为1 500 V。
DSC可以测定多种热力学和动力学参数,例如比热容、转变热等,也可用来表征微乳液形成过程中混合物各组分的相互作用,进而分析微乳液的结构。试验中以包封油溶性色素苏丹Ⅱ为例,对微乳液的微观结构进行分析。

图5 不同组分中苏丹Ⅱ的DSC图谱Fig.5 DSC thermograms of different components
图6中显示单质苏丹Ⅱ的熔点为166.35℃。将苏丹Ⅱ分别溶于月见草油中和水中时,苏丹Ⅱ的熔点分别是166.18℃和164.78℃,与单质苏丹Ⅱ的熔点相比分别下降0.17℃和1.57℃。说明油和水对苏丹Ⅱ熔点确有影响,而且不同物质影响程度不同。按1.2.1的方法制备包封苏丹Ⅱ的6∶1微乳,将含有苏丹Ⅱ的微乳进行热分析。结果显示微乳液中苏丹Ⅱ的熔点为166.67℃,与单质苏丹Ⅱ的熔点相差0.32℃,与油中的苏丹Ⅱ熔点比较接近,相差0.49℃,而与水中的苏丹Ⅱ熔点相差较大为1.89℃。由此可以分析月见草油微乳液中苏丹Ⅱ的存在位置应在微乳的油相中。
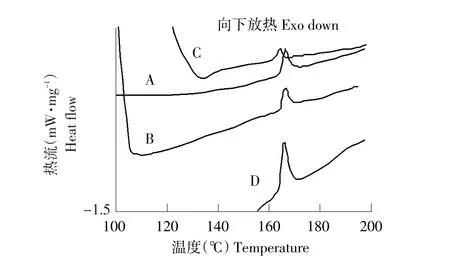
图6 不同组分的DSC图谱的局部放大图Fig.6 DSC thermograms and its local enlarge graphs near the endothermic peak of different components
2.2 Tween80/月桂酸/月见草油/水微乳体系微观结构的电导研究
2.2.1 含水量对微乳电导率的影响
研究表明电导行为是微乳的重要性质之一,可以根据电导率变化考查微乳的相转变[16-17]。试验中以月见草油为油相,Tween80和月桂酸为表面活性剂,以滴加水的方式制备微乳。随着体系中水分含量的增大,微乳液由澄清变成浑浊,继续滴加水,体系配方不同现象也不同:如澄清→浑浊,澄清→粘稠→浑浊,澄清→浑浊→粘稠→澄清。试验中可以通过现象来判断相转变点,同时也可通过电导率划分微乳结构。
图7为表面活性剂与月见草油的比分别为4∶1、8∶1、10∶1、7∶3时测得的微乳液电导率随水分含量变化的曲线。对应微乳的结构可以把曲线分为Ⅰ、Ⅱ、Ⅲ、Ⅳ四个区如图7(a)。由图可知随着体系中水分含量的增加,四条曲线的变化趋势基本相同。对于水包油型的微乳图7中的(a~c),曲线开始阶段都显示出一段平缓上升区(Ⅰ区),达到最高点后电导率突然变小,通过试验中可见,当含水量小于15%时体系为透明溶液,之后随着滴加水量的增加体系开始变得浑浊,而含水量为20%时体系黏度最大,因此结合现象划分出Ⅰ区即W/O区。含水量大于20%之后随着水量的增加黏度逐渐减小,电导率呈线性上升,且随着含油量的增高,斜率越来越小,双连续相区也越来越窄。含水量达到60%~65%时,电导率达到最大值,此时体系又变得澄清透明转变为O/W型微乳。而对于7:3的微乳来说含水量大于18%后体系则由粘稠逐渐变为乳白色不透明的乳浊液。有研究认为Ⅰ和Ⅱ区为W/O型微乳液,但由于试验中以长链脂肪酸为油相,体系在进入Ⅱ区时明显表现出液晶状的特点,因此将此区定为液晶相(LC)区。
2.2.2 制备温度对微乳电导率的影响
前期研究表面温度升高可提高微乳的形成速度,也可使难溶物质的溶解度提高。但试验中所用表面活性剂Tween80属于非离子表面活性剂,溶解度随温度的升高而降低。温度升高到一定程度时会产生“起昙现象”,主要是由于Tween80与水分子之间形成的氢键作用强度减弱或发生断裂,亲水作用下降;温度太低非离子表面活性剂也会自身聚集而产生混浊。因此试验通过电导率探讨制备温度对Tween80/月桂酸/水/月见草油四组分组成的体系微乳形成能力的影响。
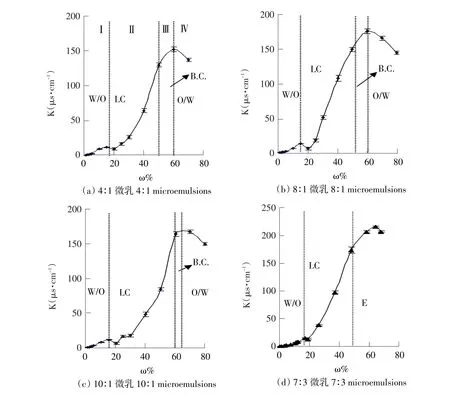
图7 含水量对微乳电导率的影响Fig.7 Effect of the water content on electrical conductivity of microemulsions
当表面活性剂与月见草油的比为8∶1时,在25、45及65℃下制备可无限稀释的微乳中水分含量随电导率变化见图8。由图8可知,25℃电导率曲线呈现典型的渗滤电导特性。当体系中水分含量较低时(小于15%),水滴彼此相距较远不能相连,微乳液的导电性由液滴(也就是油)的导电性决定,因此导电率低。当含水量增到20%(25℃)时电导率曲线出现拐点,此后开始呈突然上升趋势,这是由于体系中的液滴浓度增大,在油连续相中形成狭窄的水管或通道,开始相连形成导电链,体系的电导率随含水量的增加而快速上升,因此水分含量在0~15%形成的是W/O型微乳液。继续增加水量液滴间距离减小由水滴到水分子簇,相互连接,电导率增加开始变缓慢直至增至最高点(60%),此后的微乳液应为O/W型状态,包含连续相为水、月见草油为核、混合表面活性剂为界面膜。当含水量在55%~60%,此时随着含水量的增加电导率变化较小,Lada等认为此时形成的是双连续相,溶液处于油和水皆为局部连续的一种过渡态中间结构为B.C.型(双连续型)[18]。但在不同制备温度下电导率曲线中有一段反常,随着温度升高曲线的拐点向后推迟,25、45、65℃所对应的含水量分别为20%、30%和45%,随着温度升高体系的最黏稠点推后,即W/O型微乳的区域加大。这是因为温度升高会使界面上的表面活性剂分子间距离增大,分子间的相互作用减弱,柔性增加,使黏度逐渐降低,有助于油包水微乳的形成。图中还可看出在三种制备温度下微乳电导率最大值均出现在水分含量60%处,这也与用相图研究的结论一致,即制备温度不会改变水包油微乳区的面积,可使微乳形成的速度明显加快。
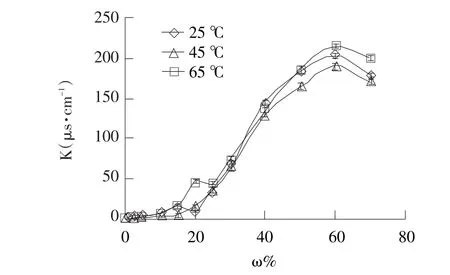
图8 制备温度对8∶1微乳电导率的影响Fig.8 Effect of operating temperature on electrical conductivity of microemulsions
2.3 Tween80/月桂酸/月见草油/水微乳体系微观结构的微观形态观察
成像技术成为表征微乳重要手段。Bouchemal等使用透射电子显微镜研究纳米乳液的形态和结构;增加分辨率和衍射模式的组合揭示乳液形式和大小[19]。由于7∶3的微乳加水稀释后失去微乳特性,体系呈乳白色,变得不透明为乳浊液。而不稀释的7∶3微乳粒子浓度大,体系黏度较大,无法进行负染,因此试验只对可稀释的4∶1和8∶1微乳进行透射电镜观察。分别取不同配方的微乳液用纯水稀释100倍,经磷钨酸负染后,进行对比观察见图9。
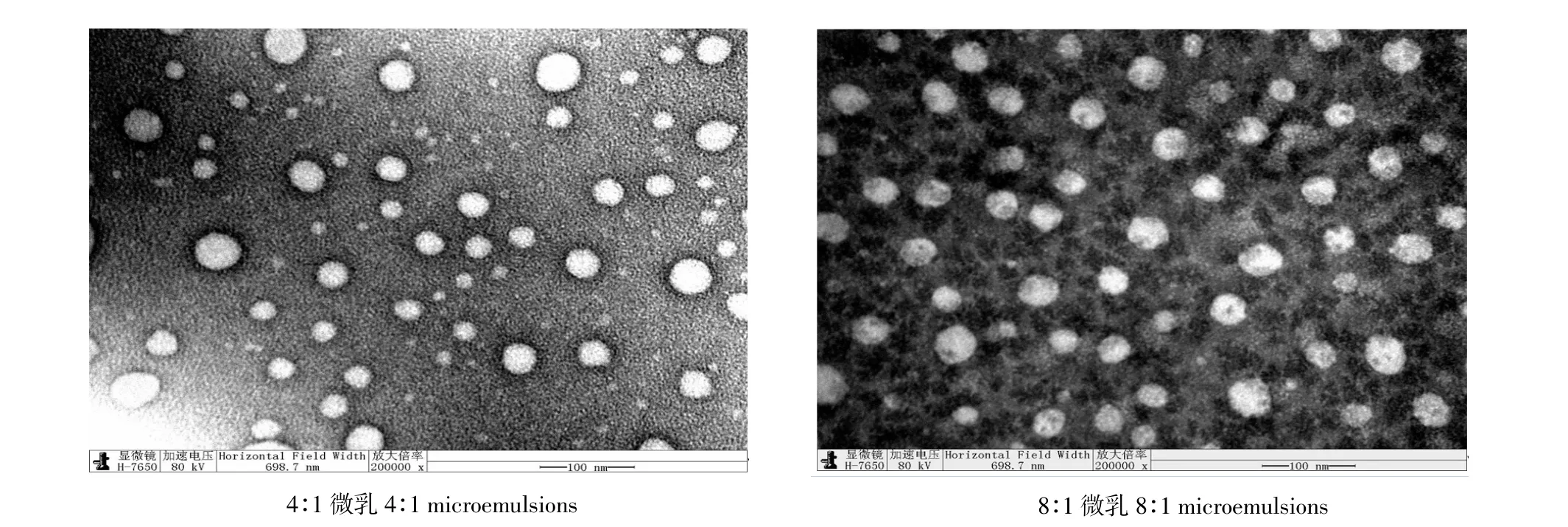
图9 微乳的透射电镜图谱(放大倍率200000×)Fig.9 Electro-microscopic images of microemulsion
如图9可见,通过透射电镜扫描可观察到微乳粒子形态大多呈现圆形,外层为水相,被磷钨酸染成黑色,光线透不过去,内部为油相,不会被磷钨酸染色,光可以透过形成一个亮点,符合O/W型微乳的结构特点。随着微乳中月见草油含量的降低,粒径分布更为均一。
3 讨论
用差示扫描量热法(DSC)得到曲线可测定水在微乳液中存在状态,判断微乳液的类型和结构。通过测定微乳液过冷凝结过程或升温熔解过程中温度和热焓值变化,比较微乳液中各种状态水含量。此外该方法可优化体系中各组分最佳配比,表征乳化液稳定性等。对于月见草油微乳是由Tween80/月桂酸/月见草油/水四组分组成体系,体系中油、表面活性剂在-40~40℃之间热焓值没有明显变化,而对于纯水(自由水)的熔点为0℃,束缚水熔点为-10℃。即在升温到0℃时固化自由水(冰)会吸收热量转变为液态水,在DSC曲线上表现出明显吸热峰,束缚水在-10℃附近热焓值会有明显变化。因此根据DSC曲线形态可以判断体系中水存在形式,判断出微乳类型。试验中以月见草油微乳为载体包封苏丹Ⅱ,此时微乳为五组分的复杂体系,各种物质间相互作用组成稳定均一的微乳体系。物质间相互作用对苏丹Ⅱ熔点会有一定影响,通过差式扫描量热法对微乳进行热分析可证明微乳中不同的组分会改变苏丹Ⅱ熔点,在水包油型微乳中苏丹Ⅱ被包封在油相中。
电导是研究微乳液的重要方法之一,能够反映微乳结构和性质。因此可以采用电导率法研究微乳液的相行为及结构变化。在O/W型微乳中由于水是连续相因而具有较高的电导率,油的导电性差使W/O型的微乳具有低电导率。介于这两种结构之间的双连续相在电导性质上表现出明显突变。由于月见草油微乳中作为油相的月见草油属于长链脂肪酸,因此在微乳形成过程中出现液晶相(LC),由于黏度大、流动性差,在电导率曲线上表现出低电导率。对于水包油型微乳从电导率随增溶水量变化曲线可知随微乳制备过程中水量增加,月见草油微乳结构经历油包水型微乳液、液晶相、油水双连续相和水包油型微乳转变。对于油包水型7∶3微乳由于含油量增加则不能转变成水包油型微乳,以多相的乳浊液形式存在。形貌规整和尺寸均一的纳米粒子对其物理化学性质具有重要影响,成像显微技术可用来观察纳米乳液的大小、形状和聚合纳米乳液状态。采用负染法通过透射显微镜可清晰观测到微乳微观结构,但对于油包水型的微乳由于其黏度大,用水稀释后会改变微乳状态,因而不宜用此方法。
4 结论
通过微乳液的DSC曲线确定不同类型的微乳液及水存在状态。对于10∶1微乳液当水分含量小于20%时体系中的水主要为束缚水,形成W/O型微乳液,随水含量增大体系中水存在状态也由束缚水转化为自由水。而对于7∶3微乳,水分含量小于30%体系中水主要为束缚水,当水分含量大于30%时体系变得粘稠浑浊,已失去微乳液特征。对微乳热分析表明微乳中不同组分会改变苏丹Ⅱ熔点,在水包油型微乳中苏丹Ⅱ是被包封在内相月见草油中。通过对微乳体系的电导研究可知,对于10∶1~4∶1微乳液当水分含量小于15%时形成W/ O型微乳液,随着水含量的增大,体系逐渐过渡到为双连续型微乳,水分含量大于65%时即转变为O/W型微乳液。而对于7∶3微乳,水分含量小于18%体系透明、稳定为油包水型微乳,当水分含量大于50%时体系转变为乳浊液。随制备温度升高,微乳速度明显加快,油包水区域增大但不会改变水包油微乳区的面积。通过透射电镜扫描可观察到微乳粒子形态大多呈现圆形,分布较为均一。
[1]赵雅霞,张军辉,刘玉平.月见草油中各成分分析[J].农产品加工·学刊,2010(8):106-107.
[2]Kakutani S,Kawashima H,Tanaka T,et al.Uptake of dihomoγ-linolenic acid by murine macrophages increases series-1 prostaglandin release following lipopolysaccharide treatment[J]. Prostaglandins,Leukotrienes and Essential Fatty Acids,2010,83 (1):23-29.
[3]周同永,任飞,邓黎,等.γ-亚麻酸及其生理生化功能研究进展[J].贵州农业科学,2011,39(3):53-58.
[4]Liu D,Kobayashi T,Russo S,et al.In vitro and in vivo evaluation of a water-in-oil microemulsion system for enhanced peptide intestinal delivery[J].The AAPS Journal,2013,15(1):288-298.
[5]王晶,刘宁.食品级番茄红素微乳的质量评价[J].东北农业大学学报,2012,5:11-16.
[6]Venturini C G,Jäger E,Oliveira C P,et al.Formulation of lipidcore nanocapsules[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2011,375(1):200-208.
[7]Budai M,Szabó Z,Zimmer A,et al.Studies on molecular interactions between nalidixic acid and liposomes[J].International Journal of Pharmaceutics,2004,279(1):67-79.
[8]Yaghmur A,Aserin A,Tiunova I,Garti N.Sub-zero temperature behaviour of non-ionic microemulsions in the presence of propylene glycol by DSC[J].Journal of Thermal Analysis and Calorimetry,2002,69(1):163-177.
[9]Thanasukarn P,Pongsawatmanit R,McClements D.Influence of emulsifier type on freeze-thaw stability of hydrogenated palm oil-in-water emulsions[J].Food Hydrocolloids,2004,18(6):1033-1043.
[10]Bauduin P,Touraud D,Kunz W,et al.The influence of structure and composition of a reverse SDS microemulsion on enzymatic activities and electrical conductivities[J].Journal of Colloid and Interface Science,2005,292(1):244-254.
[11]Destrée C,George S,Champagne B,et al.J-complexes of retinol formed within the nanoparticles prepared from microemulsions[J]. Colloid and Polymer Science,2008,286(1):15-30.
[12]秦娟,辛寅昌,马德华.微乳液的油水分离和机理探讨及应用[J].化工学报,2013,64(5):1797-1802.
[13]Koetz J,Bahnemann J,Kosmella S.Influence of a cationic polyelectrolyte on the inverse micellar region of the ternary system sulfobetaine/water/alcohol[J].Journal of Polymer Science Part A: Polymer Chemistry,2004,42(3):742-751.
[14]Raemy A,Nouzille C A,Frossard P,et al.Thermal behaviour of emulsifier-water systems studied by micro-DSC[J].Journal of thermal analysis and calorimetry,2005,80(2):439-443.
[15]Spernath A,Aserin A,Garti N.Phase transition induced by water dilution in phospholipid U-type food-grade microemulsions studied by DSC[J].Journal of Thermal Analysis and Calorimetry, 2006,83(2):297-308.
[16]Bauduin P,Touraud D,Kunz W,et al.The influence of structure and composition of a reverse SDS microemulsion on enzymatic activities and electrical conductivities[J].Journal of Colloid and Interface Science,2005,292(1):244-254.
[17]Mo C,Zhong M,Zhong Q.Investigation of structure and structural transition in microemulsion systems of sodium dodecyl sulfonate+ n-heptane+n-butanol+water by cyclic voltammetric and electrical conductivity measurements[J].Journal of Electroanalytical Chemistry,2000,493(1):100-107.
[18]Lada A,Lang L,Zana R.Relation between electric percolation and rate constant for exchange of material between droplets in water in oil microemulsions[J].J Phys Chem,1989,93:10.
[19]Bouchemal K,Briançon S,Perrier E,et al.Nano-emulsion formulation using spontaneous emulsification:solvent,oil and surfactant optimisation[J].International Journal of Pharmaceutics. 2004,280(1):241-251.
Study on the microcosmic structure of evening primrose oil microe-mulsion
WU Hongyan1,2,SUN Changbao2,LIU Ning1,XU Yingyi2,LIU Ran2(1.School of Food Science,Key Lab of Dairy Science,Ministry of Education,Northeast Agricultural University,Harbin 150030,China;2.School of Food and Biological Engineering,Qiqihar University,Qiqihar Heilongjiang 161006,China)
The structure and the structural transformation of the microemulsions were investigated by DSC method.The existing position of SudanⅡwas determined by melting point of the different component.The shape of microemulsions droplets was measured by transmission electron microscope(TEM).The microstructures of microemulsions were determined through conductance.These results indicated that the microemulsions were partitioned as W/O,O/W,LC and B.C.microemulsion domains. Differential scanning calorimeter(DSC)curves were significantly different because of different type microemulsions.Along with the increase of water content,the systems inverted from water-in-oil to oil-in-water in 10∶1 microemulsion.As the water content is less than 30%,DSC curve did not change significantly in 7∶3 microemulsion.SudanⅡparticles were exsited in the oil phase of oil-in-water microemulsions.
microemulsions;evening primrose oil;microstructure;differential scanning calorimeter; conductometry
TS201.2
A
1005-9369(2014)05-0044-08
2013-12-03
黑龙江省自然科学基金项目(C201333);黑龙江省普通高等学校农产品加工重点实验室开放项目
吴红艳(1969-),女,教授,博士研究生,研究方向为食品化学与食品添加剂。E-mail:wuhonggang@sohu.com
*通讯作者:刘宁,教授,博士生导师,研究方向为营养与黏膜免疫。E-mail:ningliu66@163.com
时间2014-5-19 11:26:25[URL]http://www.cnki.net/kcms/detail/23.1391.S.20140519.1126.011.html
吴红艳,孙长豹,刘宁,等.月见草油微乳体系的微观结构研究[J].东北农业大学学报,2014,45(5):44-51.
Wu Hongyan,Sun Changbao,Liu Ning,et al.Study on the microcosmic structure of evening primrose oil microemulsion[J]. Journal of Northeast Agricultural University,2014,45(5):44-51.(in Chinese with English abstract)
