响应面法优化及制备丹参酮ⅡA 白蛋白纳米粒
2014-01-13刘丽薇
刘丽薇, 承 伟
(辽宁医学院药学院,辽宁 锦州121000)
丹参酮是从唇形科植物丹参Salvia miltiorrhiza Bge 根中提取的具有抑菌作用的脂溶性菲醌化合物,其中丹参酮ⅡA是丹参中脂溶性成分的代表[1]。丹参酮ⅡA具有保护大脑、治疗心血管方面疾病、抑制肝细胞损伤、抗感染和抑制成纤维化神经元细胞增殖等多方面的药理作用。尤其近些年研究者越来越关注其在抗肿瘤方面的作用,并在临床上用于治疗肝肿瘤、胃肿瘤、白血病等疾病,显示出较好疗效[2-5]。研究表明通过联合使用丹参酮ⅡA,可使细胞停止生长,阻滞于G0/G1期,阻止细胞进入s 期、DNA 合成期,从而有效控制了癌细胞的生长繁殖[6]。丹参酮ⅡA作用于ERK 通路上抑制其活化程度,从而延缓卵巢癌细胞增殖,并使大量细胞被诱导凋亡,其主要作用机理是使降低bcl-2 表达,使Bax 表达上调[7]。由于丹参酮ⅡA为脂溶性小分子药物,口服生物利用度较低,在体内代谢和排泄较快[8],故临床上多采用丹参酮ⅡA 磺酸钠注射液,但该制剂在临床应用时稳定性较差,刺激性较强,病人耐受性差[9]。本实验主要针对丹参酮ⅡA的化学性质,拟应用纳米生物给药系统,以提高丹参酮ⅡA的生物利用度以及延长其在体内的滞留时间,提高其抗肿瘤效果。作者采用牛血清白蛋白作为载体材料,白蛋白分子中的氨基酸通过肽键相互接接,形成大量的网状孔隙,并且互相扭曲形成团状,药物可镶嵌在其中,便于携带。同时具有可生物降解和低免疫原性的特点。采用去溶剂化交联法制备丹参酮ⅡA白蛋白纳米粒,响应面法优化纳米粒处方工艺,并对其体外释放特性进行研究。
1 仪器与试药
1.1 仪器 UV-2450 紫外可见分光光度计(日本岛津公司);RC-6 溶出度测试仪(天津市新天光仪器分析技术有限公司);JEM-1200EX 透射电子显微镜(日本电子公司);KQ-300E 型超声波清洗器(上海生析超声仪器有限公司);透析袋(MV:1000-3000,美国spectrum 公司);Nano ZS90纳米粒度和Zeta 电位及分子量分析仪(英国Malvern 公司);
1.2 试药 牛血清白蛋白(BSA) (FractionV SIGMA 公司);丹参酮ⅡA对照品(中国食品药品检定研究院,编号110766-200918,纯度>98%);丹参酮ⅡA(批号20090723,陕西昂盛生物医药科技有限公司,质量分数>95%);其余试剂(分析纯,市售)。
2 方法与结果
2.1 丹参酮ⅡABSA 纳米粒的制备[10]通过去溶剂化交联法,取适量BSA 溶解于去离子水中,震荡、涡旋至全部溶解,取适量乙醇加入丹参酮ⅡA使之充分溶解。在一定转速搅拌下缓缓滴加含有药物的无水乙醇,注意控制滴速,至出现乳光后,滴加0.2%戊二醛,继续涡旋至混匀,旋转蒸发至除去乙醇,得到出现明显乳光的溶液体系,即得丹参酮ⅡABSA 纳米粒,继续搅拌一定时间,即得。最后经过冷冻干燥得到纳米粒。
2.2 检测波长的确立及绘制标准曲线
2.2.1 检测波长的选择 精密称取丹参酮ⅡA对照品适量,加乙醇定容至50 mL,配成对照品溶液。分别将对照品和辅料水溶液稀释至一定浓度后,以乙醇为空白对照,在波长260 ~600 nm 扫描,丹参酮ⅡA在270 nm 处有最大吸收,而除丹参酮ⅡA外的其他辅料在此波长下则不吸收。故选定270 nm 作为测定波长。
2.2.2 标准曲线的绘制 精密吸取对照品贮备液0.5、1.0、1.5、2.0、2.5、3.5、5.0 mL 加乙醇定容至50 mL。以270 nm 吸光度(A)对丹参酮ⅡA的质量浓度(C)作标准曲线,进行标准曲线绘制,得到的标准回归方程A =0.012 6C+0.169 (n=6),r =0.999 9,表明丹参酮ⅡA在3.06 ~30.6 μg/mL 范围内线性关系良好。
2.3 测定纳米粒包封率 精密称取适量丹参酮ⅡABSA 纳米粒分散于10 mL 乙醇溶液中,在20 000 r/min 下冷冻离心30 min,根据回归方程计算上清液中的丹参酮ⅡA的量。即得到未被纳米粒包封的游离药物含有量,根据以下公式计算纳米粒包封率:

2.4 响应面分析方案及试验结果
2.4.1 模型建立与方差分析 在前期大量预试验的基础上,最终选定药物量与BSA 比例 (A)、乙醇与水比例(B)、乙醇滴速(C)3 因素作为考察对象,利用Design-Expert 软件,以药物包封率(EE%)为响应指标进行实验考察。根据Box-Benhnken 试验设计原理设计实验[11-12],响应面分析方案见表1。回归方程各项的方差分析见表2。由Box-Benhnken 设计拟合,得响应值(Y)对编码自变量的二次多项回归方程为Y = +81.12 -3.96A -4.41B +2.43C -1.75AB+2.52AC+2.53BC- 8.14A2+1.01B2-4.21C2。对上述回归模型进行方差分析,回归模型的F 值为58.01,概率P <0.000 1,表明模型极显著。失拟项为0.65,没有显著性差异;其r2值为0.963 5,表明96.35% 响应值变化可以用此模型解释,这表明该模型相关性良好。从回归模型方差分析结果上看,该模型的拟合度较好。各因素的一次项存在极显著性,二次项A2、C2也表现出极显著性。
2.4.2 模型优化与预测 由回归方程经处理得到的药物量与BSA 比例、乙醇与水比例、乙醇滴速的交互作用对药物包封率影响的响应面。回归模型预测的最佳处方工艺为药物量与BSA 比例为0.09 (g/g),乙醇与水比例为0.53(g/g)、乙醇滴速为1.27 mL/min,模型预测包封率为84.35%。
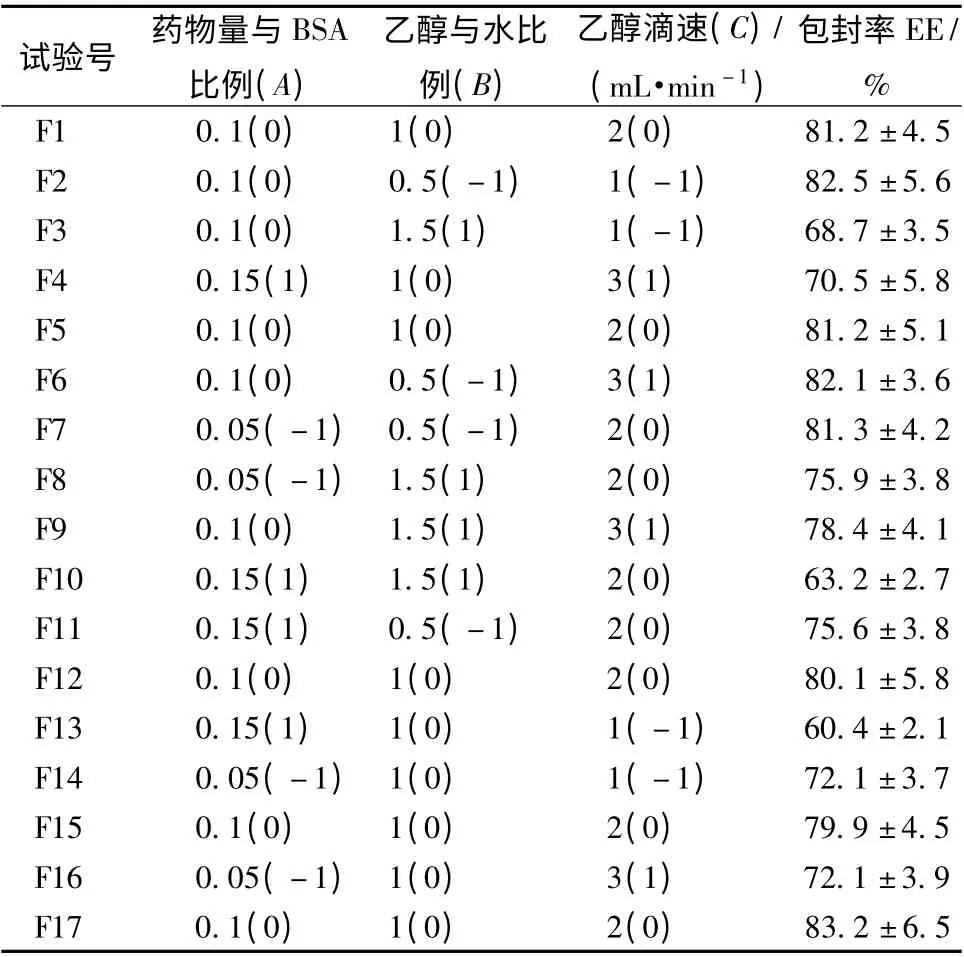
表1 响应面设计和包封率

表2 响应面法方差分析
2.4.3 验证试验 为验证响应面法的可靠性,采用上述最优条件进行丹参酮ⅡABSA 纳米粒制备,测定药物包封率重复3 次,结果见表3。获得的包封率分别为85.79%、87.43%、84.12%,平均包封率为85.78%,结果与预测值84.35%比较接近,所以,工艺条件采用响应面法进行筛选,数据准确可靠,具有一定的实际应用价值。模型预测值和实验观察值都比较接近,模型具有良好的预测性。
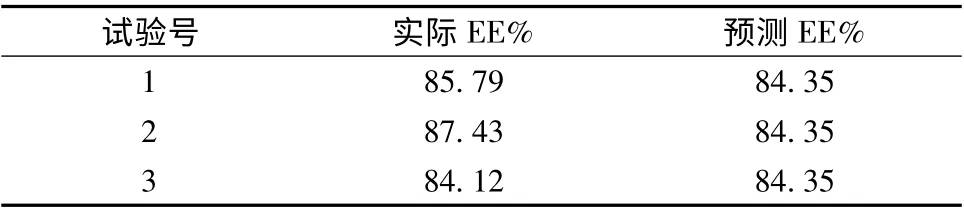
表3 响应面法验证试验结果
2.5 丹参酮ⅡABSA 纳米粒的形态学及粒径分析 通过透射电子显微镜观察纳米粒的形态和大小,在覆有支持膜的铜网上滴加丹参酮ⅡABSA 纳米粒溶液2 ~3 滴,干燥10 min,观察。见图1。从图1 可以看出,丹参酮ⅡABSA 纳米粒为球形或类球形,分散度和球形度良好,大小相对均一。
2.6 释放率测定 分别精密称取冷冻丹参酮ⅡABSA 纳米粒和丹参酮ⅡA原料药适量,置于透析袋中,扎紧袋口,悬浮于加有50 mL 磷酸盐缓冲液(pH 7.4)的具塞锥形瓶中,以100 r/min 的振荡频率于37 ℃下水浴振摇,在不同时间点(0.5、1、2、4、6、9、12、18、24 h)取透析液5 mL,照“2.3”项下进行含量分析,计算出各时间点的药物浓度和累积释放率,同时补加介质5 mL。取3 份样品平行实验,所得结果绘制累积释放率-时间曲线,比较丹参酮ⅡABSA 纳米粒与原料药体外释放行为。由图2 可以看出,纳米粒比原料药具有明显的缓释作用;原料药在4 h 内累计释放率为95.1%,基本释放完全。纳米粒的体外释放体现出两相释放形式,前4 h 药物累积释放率为(46.5 ±3.7)%,属于快速释放。4 h 后释药由药物扩散导致,24 h 累积释放率为(97.3 ±6.6)%,为缓慢低速释放。对最佳工艺条件制备的丹参酮ⅡABSA 纳米粒按不同释药模型拟合,由表4可看出,通过相关系数判断拟合程度,丹参酮ⅡABSA 纳米粒体外释放特征用一级方程拟合最佳。表明药物释放主要通过Fick 扩散完成。
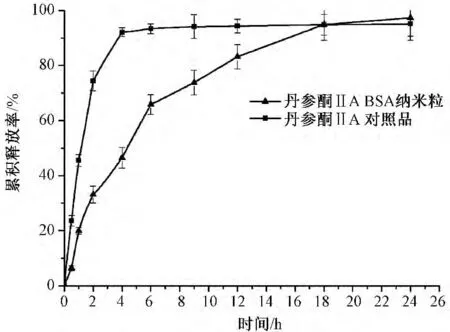
图2 丹参酮ⅡA BSA 纳米粒和丹参酮ⅡA 原料药的体外释放曲线(n=3)

表4 丹参酮ⅡA BSA 纳米粒体外释药模型拟合
3 讨论
其他文献报道制备丹参酮ⅡA纳米粒所用的制备方法如乳化交联法、乳化溶剂挥发法,反应剧烈,并且需要采用大量有机溶剂[13-14],药物包封率低[15]。本实验通过使用去溶剂化交联法制备丹参酮ⅡABSA 纳米粒,采用乙醇破坏BSA 周围形成的水化膜而使其沉淀出来,形成纳米粒。得到的纳米粒粒径均一,分散度好,药物的包封率高,纳米粒具有明显的缓释效应。本法制备工艺简单易行,反应温和,不需要使用有毒的有机溶剂,不存在溶剂残留问题。得到的分散体系通过加入戊二醛进行交联,提高纳米粒的分散度和稳定性。选用牛血清白蛋白(BSA)作为载体材料,生物相容性好,无免疫原性,BSA 已成为一种非常成熟的药物传递系统载体材料,常被作为药物及反义寡核苷酸的载体。
根据文献报道和已完成初步试验结果,笔者将其他条件固定,主要考察了药物量与BSA 比例、乙醇与水比例、乙醇滴速这3 个因素对纳米粒包封率的影响,以纳米粒的制剂学有关参数为指标,运用响应面法筛选出了丹参酮ⅡABSA 纳米粒合理的工艺条件,验证试验表明,处方工艺合理,稳定可行。
纳米粒体外释放呈现出一级释放特征,说明药物从纳米粒释放主要受Fick 扩散影响。初始阶段,吸附在纳米粒表面的药物与溶出液接触,进入溶出介质,造成药物快速释放。随着外液逐步扩散到其内部,再携带着丹参酮ⅡA从内部向外扩散;从整个释放过程可以看出,BSA 纳米粒能够使药物长时间维持在稳态浓度,能够起到控制药物缓慢释放作用,使其更好地发挥治疗效率。
[1] 蔡丽萍,习志刚,杨 红. 丹参酮的药理作用和临床研究进展[J]. 广东药学院学报,2008,24(3):321-324.
[2] 张民庆,龚惠明. 抗肿瘤中药的临床应用[M]. 北京:人民卫生出版社,1998:256-258.
[3] 王 旭,颉玉欣,单保恩. TanⅡA 对人胃肿瘤BGC-823 细胞增殖及凋亡的影响[J]. 肿瘤防治,2008,20(1):56-59.
[4] 冯玉光,邢国辉,宗绪山,等. TanⅡA 联合5-Fu 对人胃癌SGC7901 细胞增殖和凋亡与突变型p53 蛋白表达的研究[J]. 中华肿瘤防治杂志,2010,17(11):831-834.
[5] 邢国辉,冯玉光,宗绪山,等. TanⅡA 联合5-Fu 对低氧下人胃癌SGC7901 细胞增殖、凋亡的影响及与HIF-1α 和突变型P53 表达的关系[J]. 世界华人消化杂志,2010,18(3):222-228.
[6] 王修杰,袁淑兰,黄韧敏,等. Brdu 和PCNA 标记观察丹参酮对癌细胞增殖的影响[J]. 华西医科大学学报,1996,27(4):390.
[7] 刘 伟,陈 吴. 丹参酮ⅡA对人卵巢癌细胞株CAOV-3增殖与凋亡的影响[J]. 医药导报,2007,26 (12):1398-1400.
[8] 陈新谦,金有豫. 新编临床药物学[M]北京:人民卫生出版社,1998:101-105.
[9] 钱名堃,杨保津,顾文华,等. 丹参有效成分的研究-I.TanⅡA 磺酸钠和次甲丹参醌的化学结构[J]. 化学学报,1978,36(3):199-206.
[10] 张良珂,侯世祥,宋相容,等. 一种白蛋白纳米粒的制备与评价[J]. 中国药学杂志2007,42(5):365-367.
[11] 李春英,李晓娟,杨 磊,等. 响应面分析法优化甘草酸和甘草黄酮联合提取工艺[J]. 黑龙江大学自然科学学报,2009,26(3):390-395.
[12] 孙丽君,林长春,赵翔宇,等. 响应面设计优化超临界CO2抗溶剂法制备负载β-胡萝卜素的玉米蛋白纳米粒[J]. 食品科学,2011,32(8):19-23.
[13] 甘良春,侯世祥,毕岳琦,等. 星点设计-效应面法优化丹参酮ⅡA纳米粒的制备工艺[J]. 中国药学杂志,2007,42(10):758-761.
[14] 李 琦,王 炎,范忠泽,等. 丹参酮ⅡA及其纳米粒诱导肝癌细胞凋亡及对p38MAPK,TGFβ1 信号蛋白表达的影响[J]. 肿瘤,2008,28(1):8-12.
[15] 安 芸,苗 方,尹祥敏,等. 丹参酮ⅡA固体脂质纳米粒的制备[J]. 医学理论与实践,2009,22(7):869-870.
