中华剑角蝗共生真菌Penicillium oxalicum中抗肿瘤次级代谢产物研究
2014-01-10喻梦岚陈剑锋
喻梦岚,徐 帮,程 凡,邹 坤,陈剑锋
三峡大学生物与制药学院 天然产物研究与利用湖北省重点实验室,宜昌 443002
昆虫与微生物的共生是自然界的一种普遍的现象,缘于昆虫庞大的种群和复杂的生活环境,其共生菌有着异常丰富的多样性,故有可能产生结构新颖,类型丰富的活性次级代谢产物,因而昆虫共生真菌已成为寻找新生物活性物质的新的重要来源[1]。本课题组从中华剑角蝗的肠道中分离得到一株草酸青霉(Penicillium oxalicum)菌株,采用细胞毒活性追踪法对其发酵产物进行了化学分离,从中分离得到1个具有较好抗肿瘤活性的化合物,通过波谱数据分析及理化性质鉴定结构。同时对其进行了体外抗肿瘤活性研究并利用流式细胞仪技术初步探究了该活性活性产物的抗肿瘤机制,为进一步的开发利用奠定基础。
1 材料与方法
1.1 仪器与试剂
Bruker AV 400 核磁共振波谱仪,瑞士布鲁克公司;AmozonSL+1200 液相色谱-双重漏斗传输离子阱质谱仪,德国布鲁克·道尔顿公司;Dionex Ultimate 3000 型高效液相色谱仪,美国戴安公司;Cosmosil MS-II RP-C18色谱柱(5 μm,250 ×10 mm 半制备型;5 μm,250 ×4.6 mm 分析型);EPICS XL-4 型流式细胞仪,美国Beckman Coulte 公司;Stat Fax-2100 型酶标仪,美国Awareness 公司;倒置显微镜,日本Olympus CKX41 公司;四甲基偶氮唑盐(MTT)购自Sigma 公司;Annexin V-FITC 细胞凋亡检测试剂盒、JC-1 细胞线粒体膜电位检测试剂盒购自南京凯基生物。
1.2 菌株和细胞株
实验菌株分离自中华剑角蝗肠道,昆虫样品于2011 年7 月采集于湖北省神农架大九湖国家湿地公园,菌株由三峡大学涂璇博士鉴定为草酸青霉(Penicillium oxalicum),保存于三峡大学天然产物研究与利用湖北省重点实验室;人永生化表皮细胞HaCAT、犬肾细胞MDCK、人肝癌细胞HepG2、人肺癌细胞A549、人宫颈癌细胞Ca Ski、鼻咽癌细胞CNE2 和人乳腺癌细胞(MDA-MB-231)购自武汉大学中国典型培养物保藏中心,由三峡大学天然产物研究与利用湖北省重点实验室传代保藏。
1.3 培养基
培养基:SDA 培养基(葡萄糖40 g,蛋白胨10 g,琼脂20 g,水1000 mL,pH 值自然);SD 培养基(葡萄糖40 g,蛋白胨10 g,水1000 mL,pH 值自然),1.25 ×105Pa 灭菌20 min。
1.4 菌株Penicillium oxalicum 的发酵
菌株经SDA 培养基斜面活化后,接种于SD 种子培养基中,于28 ℃、125 rpm 振荡培养3 d;将培养好的种子以5%的接种量接种于SD 发酵培养基中,于28 ℃、125 rpm 振荡培养16 d,共发酵40 L。
1.5 活性追踪法分离提取Penicillium oxalicum 的发酵次级代谢产物
发酵液40 L 过滤,用乙酸乙脂萃取滤液,减压浓缩得12.2 g 粗提物;菌丝体经37 ℃烘干处理后,用氯仿-甲醇(1∶1)浸提烘干的菌丝体,过滤,上清液减压浓缩得10.6 g 粗提物。将上述粗提物合并,经正相硅胶柱色谱(800 g 正相硅胶,200~300 目)分离,氯仿-甲醇(100∶0~50∶50%,v/v)梯度洗脱,得5个洗脱部分(1~5)。对合并的粗提物和5个洗脱部分进行体外抗肿瘤活性研究(MTT 法[2])。根据各段活性进行下一步分离,其中1 部分在低温下析出一黄色晶体化合物(36.6 mg),通过波谱分析与查阅文献对纯化合物进行结构鉴定,并测定其体外抗肿瘤活性。
1.6 单体化合物抗肿瘤活性机制初步探究
鉴于1 部分及其分离到的单体化合物对HepG2细胞抑制活性相对较好,故以HepG2 细胞为检测模型,应用倒置显微镜观察细胞凋亡形态学变化、流式细胞仪检测细胞凋亡和线粒体膜电位的变化。细胞凋亡用AnnexinV-PI 双染法检测,线粒体膜电位用JC-1 探针法检测,试剂盒均购自南京凯基生物,按照说明书提供的方法操作。
2 结果与分析
2.1 菌液粗提物及5个分离部分的活性筛选结果
菌液粗提物及经正相硅胶柱色谱分离后的1~5,5个洗脱部分,用DMSO 溶解配制成100 mg/mL的储存浓度,然后用细胞培养基稀释成100、50、25至1.56 μg/mL,分别通过MTT 法进行体外抗肿瘤活性试验,以丝裂霉素为阳性药物对照,根据SPSS软件计算IC50值。其结果如表1 所示。
表1 粗提物及各洗脱部分对不同肿瘤细胞的IC50(μg/mL)(n=3,)Table 1 IC50(μg/mL)of total extract and its eluted fractions against tumor cells (n=3,)

表1 粗提物及各洗脱部分对不同肿瘤细胞的IC50(μg/mL)(n=3,)Table 1 IC50(μg/mL)of total extract and its eluted fractions against tumor cells (n=3,)
从表1 可以看出,菌株发酵产物的粗提物具有一定的抗肿瘤活性,而且对HepG2 细胞的细胞毒性要比A549 细胞强。过正相硅胶柱,用不同比例的氯仿-甲醇梯度洗脱后,抗肿瘤活性化合物主要集中于100∶0 (v/v)的氯仿-甲醇洗脱部位(1 部分),IC50值达到9.34 μg/mL,相对其他部分而言活性最好,故综合考虑首先分离1 部分。将1 部分放置于4 ℃冰箱过夜,结果析出大量黄色晶体化合物。
2.2 单体化合物的结构鉴定
化合物1 的理化性质和波谱数据如下:黄色针晶,mp.244~248 ℃;ESI-MS m/z:639[M+1]+;1H NMR(400 MHz,CDCl3)δ:13.78(2H,s,8,8'-OH),11.74(2H,s,1,1'-OH),7.45(2H,d,J=8.5Hz,H-3,3'),6.63(2H,d,J=8.5 Hz,H-4,4'),3.93(2H,d,J=11 Hz,H-5,5'),3.72(6H,s,13,13'-OCH3),2.73(2H,dd,J=6.0,19.1 Hz,H-7a,7a'),2.41(2H,m,H-6,6'),2.31(2H,dd,J=10.5,19.2 Hz,H-7b,7b'),1.17(6H,d,J=6.6 Hz,H-11,11');13C NMR(100 MHz,CDCl3)δ:187.2(C-9,9'),177.5(C-8,8'),170.3(C-12,12'),159.4(C-1,1'),158.3(C-4a,4a'),140.2(C-3,3'),117.3(C-2,2'),107.5(C-4,4'),106.3(C-9a,9a'),101.7(C-8a,8a'),84.7(C-10a,10a'),77.0(C-5,5'),53.2(13,13'-OCH3),
36.3 (C-7,7'),29.3(C-6,6'),18.0(C-11,11')。结合文献报道[3-5]的波谱数据,化合物1 可能是secalonic acid A(SAA)或secalonic acid D(SAD),两者不同之处在于5、6、10a 和5'、6'、10a' 位羟基构型不同。通过测定比旋光度与文献值相比较,化合物1的比旋光度[α]20D-73.3°(c=0.10,氯仿),文献中,SAD 的比旋光度[α]20D+88°(c=0.10,氯仿)[3,5],SAA 的比旋光度[α]20D-75°(c=0.10,氯仿)[4]。最终鉴定化合物1 为secalonic acid A,结构式如图1 所示。
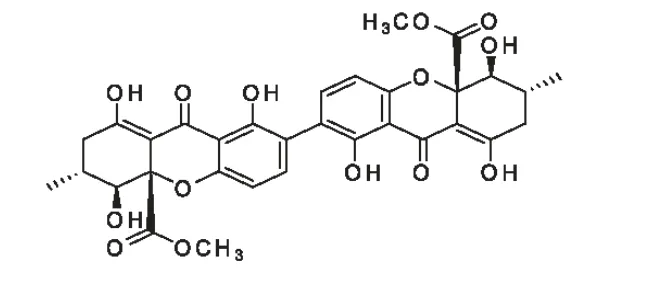
图1 secalonic acid A 的化学结构Fig.1 The structure of secalonic acid A
2.3 secalonic acid A 的体外抗肿瘤活性
为了评价secalonic acid A (SAA)的体外抗肿瘤活性,我们扩大了肿瘤细胞谱,并增加了2 种正常细胞株,结果如表2 所示,secalonic acid A 对多种肿瘤细胞株均具有较好的细胞毒活性,其中对肝癌HepG2 细胞的毒性最强,IC50值为1.12 μM,而且对2 种正常细胞的毒性均较小,IC50值在100 μM 以上,两者相差100 倍左右,可见secalonic acid A 具有一定的细胞毒选择性。
表2 secalonic acid A 对不同肿瘤细胞的IC50(μM)(n=3,)Table 2 IC50(μM)of secalonic acid A against tumor cells (n=3,)

表2 secalonic acid A 对不同肿瘤细胞的IC50(μM)(n=3,)Table 2 IC50(μM)of secalonic acid A against tumor cells (n=3,)
2.4 secalonic acid A 对HepG2 细胞形态的影响
用不同浓度(5.0、2.5、1.25 μM)的secalonic acid A 作用HepG2 细胞48 小时,在光学显微镜下观察细胞形态的变化(放大倍数10 ×10),如图2 所示,与未加药的对照组细胞相比,1.25 μM Secalonic acid A 作用后,可见细胞收缩变圆,细胞贴壁能力减弱,随着药物作用浓度的增加,细胞的生长逐渐受到抑制,细胞表面逐渐突起形成小膜泡不断脱落悬浮于细胞培养液中。5.0 μM Secalonic acid A 作用于HepG2 细胞48 h 后,细胞出现大量的细胞碎片,细胞坏死。而对照组细胞生长良好。
2.5 secalonic acid A 对HepG2 细胞凋亡的影响

图2 A :正常HepG2 细胞;Fig.2 A:normal HepG2 cell;
HepG2 细胞经不同浓度的Secalonic acid A(5.0、2.5、1.25 μM)作用24 h 后,用流式细胞仪检测细胞凋亡的变化,FITC+/PI-为早期凋亡细胞,FITC+/PI+为晚期凋亡细胞,结果如图3 所示,Secalonic acid A 诱导HepG2 细胞发生了显著的凋亡,且具有浓度依赖性。0、1.25、2.5 和5.0 μM 的Secalonic acid A 诱导的早期凋亡率分别为2.6%、27.8%、32.5%、40.6%,晚期凋亡率分别为1.8%、17.2%、23.6%和23.2%。

图3 A :正常HepG2 细胞Fig.3 A:normal HepG2 cell
2.6 secalonic acid A 对HepG2 细胞线粒体膜电位的影响
HepG2 细胞经不同浓度的Secalonic acid A(5.0、2.5、1.25 μM)作用24 h 后,用流式细胞仪检测细胞凋亡的变化(JC-1 探针法),结果如图4 所示,Secalonic acid A 显著破坏了HepG2 细胞的线粒体膜电位,相对破坏率由15.3%(0 μM SAA)上升到97.3%(5.0 μM SAA)。
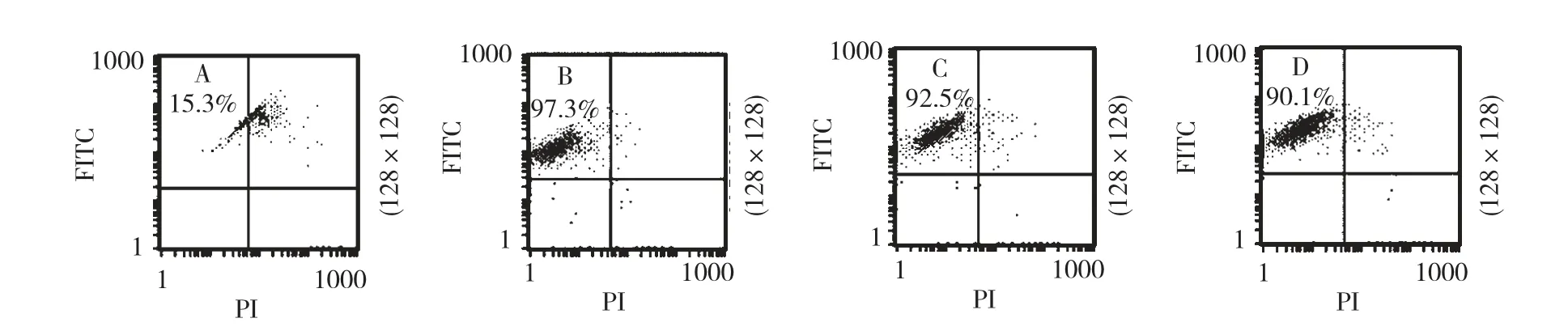
图4 A :正常HepG2 细胞Fig.4 A:normal HepG2 cell
3 讨论
本研究将1 株昆虫来源的草酸青霉(Penicillium oxalicum)菌株的发酵液和菌丝体的粗提物经正相硅胶柱色谱分离,氯仿-甲醇(100∶0~50∶50%,v/v)梯度洗脱,得5个洗脱部分(1~5),通过细胞毒性MTT 法进行活性追踪分离,从1 洗脱部分获得了1个较好活性的单体化合物Secalonic acid A,该化合物为首次从该属菌种中分离得到。Secalonic acid A对多种肿瘤细胞株均具有较好的细胞毒性,尤其对人肝癌细胞Hep G2,IC50值达到1.12 μM,而且对正常细胞株的毒性较小,显示了一定的选择性细胞毒力。初步的机制研究结果表明,Secalonic acid A 主要通过线粒体途径诱导肿瘤细胞凋亡从而发挥抗肿瘤作用。另外,该化合物得率高,分离方法简单(低温结晶析出),容易获得较大产量,所以下一步我们将进行动物试验和深入的机制研究,以综合评估Secalonic acid A 的应用价值。
微生物次级代谢产物之间往往存在着各种拮抗或协同作用,因此粗提物的活性与分离到的单体化合物活性之间没有绝对的联系,各种活性次级代谢产物在微生物体内的代谢产生与分布平衡可能取决于微生物的体内生长代谢机制和所处外部环境等[6]。所以有必要对其余部分的化合物进行分离。本课题组从余下的2~5 洗脱部分分离到5个化合物[7],分别为asperpyrones A、asperpyrones B、asperpyrones C、asperpyrones D 和aurasperone A,均为苯并吡喃酮二聚体类化合物。但MTT 结果显示,上述5个化合物对人肝癌细胞Hep G2 和人肺癌细胞A549 均无细胞毒活性,IC50值均大于100 μM,这也和洗脱部位的活性结果相符,说明Penicillium oxalicum 菌株次级代谢产物的抗肿瘤活性主要由Secalonic acid A 体现。苯并吡喃酮类化合物的单体及二聚体类广泛分布于黑曲霉和镰刀属真菌的次级代谢产物中[8-11]。根据文献报道,这类化合物对大鼠和小鼠的中枢神经系统表现出急性毒性作用[12],并且对Taq DNA 聚合酶具有抑制作用。所以其其它活性更是有待于进一步研究。
1 Zhang YL(张应烙).Microbes associated with Insect– an extensive Source of new drug molecules.2011Chinese Medicinal Chemistry Symposium(2011 年全国药物化学学术会议).
2 Tan WD(谭卫东),Jin H(金红),Luo DX(罗弟祥),et al.Comparison Of MTT With SRB assays in vitro anticancer drug screening.Nat Prod Res Dev (天然产物研究与开发),1999,11(3):17-22.
3 Steyn PS.The isolation,structure and configuration of secalonic acid D,the toxic metabolite of Penicillium Oxalicum.Tetrahedon,1970,26:51-57.
4 Steffens JC,Robeson DJ.Secalonic acid A,a vivotoxin in pink root-infected onion.Phytochem,1987,26:1599-1602.
5 Chen L(陈立),Gu QQ(顾谦群).Study on the antitumor metabolites of a sponge-derived fungus,Aspergillus repens.Periodi Ocean Univer China (中国海洋大学学报),2010,40(5):69-71.
6 Li HY(李海燕),Liu L(刘丽).Recent advances on bioactive compounds producing endophytes.Nat Prod Res Dev (天然产物研究与开发),2004,16:482-485.
7 Xu B(徐帮),Zou Kun(邹坤),Guo LZ(郭玲芝),et al.Dimeric naphthopyrones from Penicillium oxalicum,a fungus residing in Acrida cinerea.Nat Prod Res Dev(天然产物研究与开发),2013(accepted).
8 Tanaka H,Wang PL,Yamada O.Yellow pigments of Aspergillus niger and Asp.awamori.I.Isolation of aurasperone A and related pigments.Agric Biol Chem,1966,30:107-113.
9 Wang PL,Tanaka H.Yellow pigments of Aspergillus niger and Aspergillus awamori.II.Chemical structure of aurasperone A.Agric Biol Chem,1966,30:683-687.
10 Tanaka H,Wang PL,Namiki M.Structure of Aurasperone C.Agric Biol Chem,1972,36:2511-2517.
11 Priestap HA.New naphthopyrones from Aspergillus fonsecaeus.Tetrahedron,1984,40:3617-3624.
12 Ghosal S,Biswas K,Chakrabarti DK.Toxic naphtho-gammapyrones from Aspergillus niger.J Agric Food Chem,1979,27:1347-1351.
