中国南海隋氏蒂壳海绵Theonellaswinhoei 的化学成分研究
2014-01-09甘建红于豪冰
甘建红,席 达,于豪冰,闵 倩,芶 了,谢 晶*
1上海海洋大学食品学院,上海水产品加工及贮藏工程技术研究中心,上海 201306;2 第二军医大学附属长征医院海洋药物研究室,上海 200433;3 第二军医大学附属东方肝胆医院 微创外科2 室,上海 200438
海绵属动物界多孔动物门(Porifera),是最原始的低等多细胞动物,可分为钙质海绵纲(Calcarea)、六放海绵纲(Hexactinellida)和寻常海绵纲(Demospongiae)三个纲。Theonella 属海绵属寻常纲(Demospongiae)、石海绵目(Lithistida)、蒂壳海绵科(Theonellidae)海绵。目前,已从该属海绵中获得了环肽、大环内酯、甾体、聚酮、生物碱、糖脂等成分。其中的甾体类化台物多为独特的4-亚甲基结构[1,2];从中分离得到的环肽类化合物富含非常见氨基酸残基,具有良好的抗肿瘤活性[3,4]。我们对采自西沙永兴岛和七连屿附近的隋氏蒂壳海绵T.swinhoei 的化学成分进行了研究,从其正丁醇萃取部位首次分离鉴定了6 个化合物(1~6)(图1),包括5 个嘧啶类化合物以及1 个咯嗪类化合物。
1 实验部分
1.1 样品
隋氏蒂壳海绵(Theonellaswinhoei Gray,1868)样品于2007 年5~6 月采自中国南海西沙永兴岛(Woody Island)和七连屿(Seven connected islets)。种属名称由青岛海洋研究所李锦和研究员鉴定。标本(No.DS-TS01)存放于第二军医大学长征医院海洋药物实验室。
1.2 仪器与试剂
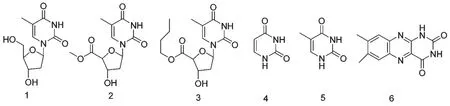
图1 化合物1~6 的结构Fig.1 Structures of compounds 1-6
MS 谱用Q-Tof micro YA019 型液质联用仪测定;NMR 由Bruker AV-600 型核磁共振仪测定;HPLC 在Agilent 1200 高效液相色谱仪上完成;Sephadex-LH20 为Pharmacia 公司产品;层析硅胶(200~300、300~400 目)为烟台江友硅胶开发有限公司产品;常用有机溶剂均为国产分析纯。
1.3 提取与分离
将冷冻的隋氏蒂壳海绵(T.swinhoei,干重1.2 kg)切碎成小块,用95%乙醇(8 ×15 L)室温渗滤,合并提取液,减压浓缩得到总浸膏。将总浸膏混悬分散于水中,用乙酸乙酯萃取4 次,浓缩萃取液得到脂溶性浸膏。将脂溶性浸膏混悬于90%的甲醇水溶液中,用石油醚萃取3 次,浓缩萃取液得到石油醚部位浸膏56 g;加水将混悬液的甲醇浓度调整至60%,用二氯甲烷萃取3 次,浓缩萃取液得二氯甲烷部位浸膏5 g;余下的60%甲醇部分浓缩至干得浸膏1 g。将最初的水相用正丁醇萃取3 次,浓缩得正丁醇部位浸膏36 g。将正丁醇部位浸膏36 g 进行减压柱色谱,以二氯甲烷-甲醇(50∶1,20∶1,15∶1,10∶1,5∶1,2∶1)梯度洗脱成50 个流份,根据HPTLC 显色合并相似流份得到8 个组分。对第五组分进行反相硅胶柱色谱、凝胶柱色谱以及高效液相制备得到化合物1~6。
2 结果与讨论
2.1 结构鉴定
从海绵正丁醇萃取部位分离鉴定了6 个化合物(1~6)(图1),包括5 个嘧啶类化合物以及1 个咯嗪类化合物。
化合物1 白色粉末,易溶于甲醇;mp.184~185 ℃;[α]+30.6°(c 1.029,H2O);。ESI-MS 显示有[M+Na]+峰m/z 265.15 及[2M +Na]+峰m/z 507.22,确定其分子量为242;IR(KBr)νmax3312,1700,1659 cm–1;结合13C NMR 谱,确定其分子式为C10H14N2O5。1H NMR(600 MHz,DMSO-d6):δ 11.24(1H,brs,NH-3),7.68(1H,d,J=1.2 Hz,H-6),6.16(1H,dd,J=7.6,6.2 Hz,HO-5'),5.21(1H,brd,J=3.2 Hz,HO-3'),5.00(1H,t,J=5.6 Hz,H-1'),4.23(1H,m,H-3'),3.76(1H,m,H-4'),3.56(2H,m,H-5'),2.07(2H,m,H-2'),1.77(3H,d,J=1.1 Hz,CH3)。13C NMR (150 MHz,DMSO-d6):δ163.7(C-4),150.5(C-2),136.1(C-6),109.4(C-5),87.3(C-l'),83.8(C-4'),70.4(C-3'),61.3(C-5'),39.3(C-2'),12.2(5-CH3)。以上数据与文献[6]报道一致,鉴定化合物1 为thymidine。
化合物2 白色粉末,mp.244~246 ℃,易溶于甲醇。ESI-MS 显示有[M +Na]+峰m/z 293.10 及[2M+Na]+峰m/z 563.20,确定其分子量为312;结合13C NMR 谱,确定其分子式为C11Hl4N2O6。1H NMR(600 MHz,C5D5N):δ13.19(1H,brs,NH-3),8.33(1H,brs,H-6),7.18(ov,H-1'),4.95(m,H-3'),4.94(brs,H-4'),2.63(1H,dd,J=13.4,5.4 Hz,Ha-2'),2.28(1H,m,Hb-2'),2.01(3H,brs,HCH3),3.68(3H,d,J=1.2 Hz,H-1″)。13C NMR(150 MHz,C5D5N):δ172.3(C-5'),164.6(C-4),151.7(C-2),136.2(C-6),110.7(C-5),86.7(C-l'),85.6(C-4'),74.7(C-3'),52.0(C-1″),39.3(C-2'),12.7(5-CH3)。以上数据与文献[7]报道一致,鉴定化合物2 为thymidine-5'-carboxylic acidmethylester。
化合物3 白色粉末,易溶于甲醇,mp.208~214 ℃。ESI-MS 显示有[M+Na]+峰m/z 355.14及[2M+Na]+峰m/z 647.26,确定其分子量为312;结合13C NMR 谱,确定其分子式为C14H20N2O6。1H NMR(600 MHz,C5D5N):δ13.20(1H,brs,NH-3),8.38(1H,brs,H-6),7.20(dd,J=13.4,5.4 Hz,Hl'),4.98(m,H-3'),4.97(brs,H-4'),4.17(2H,t,J=6.6 Hz,H-1″),2.66(1H,dd,J=9.2,5.4 Hz,Ha-2'),2.31(1H,m,Hb-2'),2.03(3H,brs,H-CH3),1.49(2H,m,H-2″),1.21(2H,m,H-3″),0.76(3H,t,J=7.4 Hz,H-14″)。13C NMR(150 MHz,C5D5N):δ172.0(C-5'),164.6(C-4),151.7(C-2),136.2(C-6),110.7(C-5),86.8(C-1'),85.9(C-4'),74.8(C-3'),65.2(C-l″),39.3(C-2'),30.5(C-2″),19.0(C-3″),13.4(C-4″),12.7(5-CH3)。以上数据与文献[6]比对,鉴定化合物3 为thymidine-5’-carboxylic acid butyl ester。
化合物4 淡黄色针晶,EI/MS 显示有[M]+峰m/z112;结合13C NMR 谱,确定其分子式为C4H4N2O2。1H NMR(600 MHz,DMSO-d6):δ10.98(1H,brs),10.80(1H,brs),7.36(1H,dd,J=7.6,5.7 Hz),5.46(1H,dd,J=7.6,1.2 Hz)。13C NMR(150 MHz,DMSO-d6):δ164.6(C-4),151.6(C-2),142.5(C-6),100.4(C-5)。以上数据与文献[8,9]报道一致,鉴定化合物4 为uracil。
化合物5 白色针状结晶,EI/MS 显示有[M]+峰m/z 126;结合13C NMR 谱,确定其分子式为C5H6N2O2。1H NMR(600 MHz,DMSO-d6):δ10.87(1H,s),10.46(1H,s),7.26(1H,s),1.72(3H,s)。13C NMR(150 MHz,DMSO-d6):δ166.8(C-4),153.4(C-2),109.1(C-5),138.7(C-6),13.1(5-CH3)。以上数据与文献[8,10]报道一致,鉴定化合物5 为thymine。
化合物6 淡黄色粉末,mp.279~281 ℃。ESIMS 显示有[M+H]+峰m/z 243;[M+H]+,265[M+Na]+and 507[2M+Na]+;结合13C NMR 谱,确定其分子式为C12H10N4O2。1H NMR(500 MHz,DMSO-d6):δ11.85(1H,brs,1-NH),11.77(1H,brs,3-NH),7.85(1H,s,H-6),7.68(1H,s,H-9),2.46(3H,s,8-CH3),2.43(3H,s,7-CH3);13C NMR(125 MHz,DMSO-d6):δ161.1(C-4),150.3(C-2),146.5(C-4a),145.4(C-10a),141.4(C-5a),139.3(C-8),138.3(C-7),130.2(C-6),129.1(C-9a),125.8(C-9),20.7(8-CH3),20.1(7-CH3)。以上数据与文献[11,12]报道一致,鉴定化合物6 为7,8-Dimethyl-isoalloxazine。
2.2 讨论
在日本海域和我国台湾省都分布有隋氏蒂壳海绵T.swinhoei。从台湾南部垦丁的该种海绵中已发现含有环肽theonellapeptolidesIa,Id,IId 以及大环内酯swinholideA 等成分[13]。本文尚未从西沙此种海绵中分离到相同的成分,主要获得了5 个嘧啶类化合物和1 个咯嗪类化合物,进一步表明了西沙隋氏蒂壳海绵Tswinhoei 的活性化学成分多样性。本文的研究结果丰富了我国南海海洋天然产物结构,为进一步研究和开发我国南海海洋生物资源提供了参考资料。
1 SugoY,InouyeY,NakayamaN.Structures of nine oxygenated 4-methylene sterols from Hachijome sponge Theonellaswinhoei.Steroids,1995,60:738-742.
2 KhoE,magawaDK,Rohmer M,et al.Sterols in marine invertebrates.22.Isolation and structure elucidation of conicasterol and theonellasterol,two new 4-methylene sterols from the Red Sea sponges Theonellaconica and Theonellaswinhoei.J Organ Chem,1981,46:1836-1839.
3 Aneiros A,GarateixA.Bioactive peptides from marine sources:pharmacological properties and isolation procedures.J Chromatography,2004,803:41-53.
4 FusetaniN,MatsunagaS.Bioactive sponge peptides.Chemical Reviews,1993,93:1793-1806.
5 Mosmann T.Rapid colorimetric assay for cellular growth and survival:Application to proliferation and cytotoxicity assaya.J Immunol Methods,1983,65(1-2):55.
6 MortdcawaT,XieH,Matsuda H,et al.BioactiveConstituentsfrom Chinese Natural Medicines.XVII.Constituents with Radical Scavenging Effect and NewGlucosyloxybenzyl 2-Isobutylmalates from Gymnadeniaconopsea.Chemical & Pharmaceutical Bulletin 2006,54:506-513.
7 DematteN,GuerrieroA,LafargueF,et al.2'-deoxynucleoside uronic acids from the aseidianAplidium(=Amaroucium)fuscum(Drasche,1=883).Comparative Biochemistry and Physiology Part B:Biochem Mol Biol,1986,84(1):11-13.
8 GoldstcinJ H,TarpleyA R.Carbon-13 nuclear magnetic resonance spectra of uracil,thymine,and the 5-halouracils.J Amer Chem Soci,1971,93:3573-3578.
9 Li WL(李文林),Mao SL(毛士龙),Yi YH(易杨华),et al.Studies on the chemical constituents of the sponge phakelliafuscathiele.Chia J Mar Drugs(中国海洋药物),2001,20:9-11.
10 Meng QH(孟艳辉),Su JY(苏镜娱),Zeng LM(曾陇梅).Studies on the chemical constituents from the South China Sea soft coral sarcophtonmolle.Chia J Mar Drugs(中国海洋药物),1999,18(3):1-3.
11 Zhang QH(张起辉),Zhou LD(周莲娣),Lu X(卢轩),et al.Chemical constituents from the marine NigrosporaSphaerica.J Shengyang Pharm Univ(沈阳药科大学学报),2010,27:615-622.
12 Wang FW,Hou ZM,Wang CR,et al.Bioactivemetabolites from Penicillium sp.,an endophyticfungusresiding in Hopeahainanensis.J Microbio Bio Tech,2008,24:2143-2147.
13 Chen QY(陈清雨).Studies on bioactive constituents from Taiwan sponges.National Sun Yat-senUniversity,PhD.2001.
