小改进凸显大思维——一则“原电池原理”引入实验改进的启示
2013-12-28房寿高
房寿高
(江苏省常州高级中学 江苏 常州 213003)
一、问题的提出
苏教版高中化学教材化学2 中演示原电池工作原理的实验很难让全班学生看到, 产生的气体易搅浑溶液,后面的学生看不清气泡产生情况,而且耗液量多。 有人把演示原电池原理的实验改成投影的方式,不仅现象明显,可以让全班同学看到[1]。笔者对后者的实验又稍作改进,改进虽小,但引发了学生的探究欲,大大激活了学生的思维。
二、改进后的实验过程
(1) 在实物投影仪上按照图1 的方式放两个培养皿,用细长铜片(宽约1.5cm,长约15cm)折成如图1 形状放在两培养皿中。
(2) 先在培养皿乙中 加 入1mol/L 的 稀 硫酸浸没过铜片, 然后在其中放入一粒粗锌粒,不与铜片接触, 让学生观察现象。 学生可观察到锌粒表面产生大量气泡,铜片上没有气泡(见图2)。
(3)用塑料镊子把刚才的粗锌粒放在乙中的铜片上再观察现象。学生可观察到: 不仅锌粒上有气泡, 而且浸没在酸中的铜片各处都有气泡(见图3)。学生很好奇,为什么铜片上会有气泡产生? 为什么离锌较远的铜片(与酸接触)上也有气泡? 有部分学生甚至问:“甲中的铜片上(不与酸接触)也会产生气泡吗?”学生的探究欲了得到激发。

图1
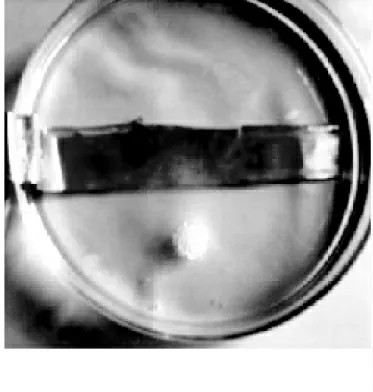
图2
(4) 在探讨了原电池的原理之后, 启发学生思考: 在甲中也倒入同物质的量浓度的稀硫酸,预测发生的现象。这个问题引起了学生的极大争论,有的同学认为:“有气泡,因为锌失去电子到铜片上,铜片上各处都有剩余电子,甲中的铜片上也有剩余电子,H+也会在此处得到电子从而产生氢气。 ”而有的同学认为:“没有气泡产生, 因为如果有气泡产生,H+变成H2逸出, 溶液中的SO42-与哪个离子结合呢?在初中学过,溶液应该是电中性的。 ”在学生争论不分胜负时,教师向甲中倒入稀硫酸,结果发现并没有产生气泡(见图4)。接着进一步启发学生思考为什么没有气泡产生。 在师生、 生生共同对话下,最终能得出“要构成原电池一般必须构成闭合回路”的结论。
三、 改进后的优点与启示
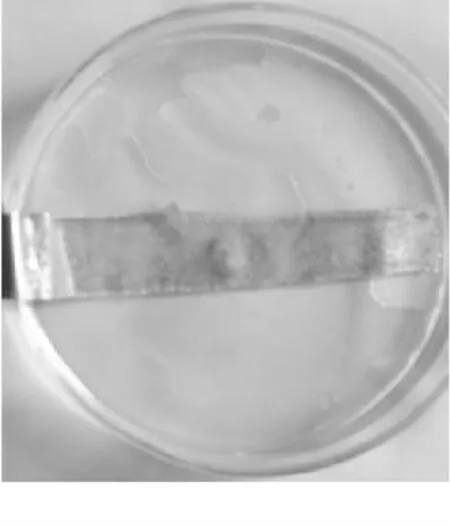
图3

图4
这次实验改进取得了很好的课堂效果,原因有如下三点:其一,由于锌粒的量很少,只有一个锌粒,放出的氢气量较小,没有导致培养皿中溶液的“浑浊不清”,且投影效果非常好,全班学生都能看得到。 其二,实验的改进促进了教学活动的展开。 实验改进的目的不仅仅是为了原料省,现象明和绿色化,更是为课堂学习目标的达成服务。 关于原电池原理, 原电池的3 个构成条件是重要的学习目标之一,步骤(2)到步骤(4)的实施顺利地达成了这一目标。 步骤(2) 让学生感受了锌和铜是两种金属活动性不同的金属;步骤(3)让学生产生了“为什么铜片上会产生气泡”的困惑,促使学生积极去思考,带着好奇心去探究原电池的形成原理;步骤(4)更加促使学生积极思考,讨论热烈,课堂气氛达到高潮。其三,作为引入之用的实验,不能开始一用了之,最好能贯穿课堂始终,这样能给人以前呼后应和整体美之感。 同时也启示我们改进实验应该向装置微型化、操作简单化、排放绿色化、现象明显化、目的目标化和多次利用化等方向发展。
[1] 江丽芬,李胜荣.“化学能转化为电能”教学设计[J].化学教育,2012,(12):64
