低负载量Fe基固体酸催化剂的制备及应用于苯酚羟基化
2013-12-23张敬畅刘海峰曹维良
张敬畅,刘海峰,王 瑞,曹维良
(1. 北京化工大学 现代催化研究所,北京 100029;2. 海南科技职业学院,海南 海口 571126)
苯二酚(邻苯二酚和对苯二酚)是十分重要的化工原料,在农药、医药、香料、染料、橡胶、照相等领域得到广泛应用[1]。传统的苯二酚生产工艺有邻氯苯酚水解法[2]、苯胺氧化法[3]、Rhone-Poulenc法[4-5]、Ube法[6]和Brichima法[7-8]等,这些工艺均以液体强酸为原料或催化剂,存在催化剂分离回收困难、对设备腐蚀严重、后处理工艺复杂[9]等问题,且反应温度过高, 副产物焦油含量高达20%(w)以上。使用TS分子筛固体酸催化剂的Enichem法工艺[10-11],由于催化剂制备工艺复杂、价格昂贵,且TS-1分子筛制备技术的引进费用很高[12],因此限制了它在工业上的应用。
Fe基复合金属氧化物催化剂[13-14]是苯二酚制备研究的热点催化剂,目前报道的该类催化剂活性组分含量高、分散性差、催化剂酸性强,使得苯酚羟基化反应温度难以控制,焦油含量高,催化剂活性组分利用率低。以负载型Fe基复合金属氧化物为催化剂的苯酚制苯二酚工艺还处在研究阶段,未形成工业化生产,我国苯二酚仍依赖进口[15],严重阻碍了二元酚下游产品的生产及相关行业的发展。
本工作采用浸渍法制备出一种酸性可调控、活性组分高分散的低负载量Fe基固体酸催化剂,并提出了苯酚羟基化反应中焦油含量的分析和计算方法,通过调配催化剂的化学组成和含量,优化了催化剂的最佳酸量;同时开发了采用分步滴加H2O2的新工艺,消除了反应过程中产物的次级反应,降低了焦油的含量,为苯二酚的生产开辟了新途径。
1 实验部分
1.1 催化剂的制备
称取1.0 g HZSM-5分子筛载体,置于真空装置中于室温下脱气脱水2 h,按催化剂中活性组分Fe和助剂Cu,Sn,Mg的含量配制Fe(NO3)3,Cu(NO3)2,SnCl2,Mg(NO3)2的混合溶液,并用上述混合溶液浸渍HZSM-5分子筛载体,干燥,在500 ℃下煅烧2 h, 分别得到4种不同化学组成的催化剂:1)Fe/HZSM-5;2)Fe-Cu/HZSM-5;3)Fe-Cu-Sn/HZSM-5;4)Fe-Cu-Sn-Mg/HZSM-5。
1.2 苯酚羟基化反应
在装有温度计和回流冷凝管的100 mL三口瓶中,按一定比例依次加入苯酚、催化剂、水和乙酸,强烈搅拌并加热,待温度升至60 ℃左右时,滴加30%(w)的H2O2溶液20 min,在 60 ℃下反应0.5 h;继续滴加30%(w)的H2O2溶液20 min,待H2O2溶液滴加完毕,继续反应 1 h,停止反应。抽滤,除去催化剂,反应液用乙醚萃取离心分离3次,收集乙醚相和水相。采用气相色谱法分析乙醚相,得到苯酚和苯二酚的含量;水相中的焦油经充分震荡烘干后,称量其实际质量。根据分析结果计算苯酚转化率和产物分布。
1.3 产物的分析方法
乙醚相的分析采用Agilent公司6820N型气相色谱仪,MXT-1色谱柱,柱长15 m,内径0.25 nm。采用氢火焰离子化检测器,升温范围40~285 ℃,气化室、检测室温度均为360 ℃。采用面积归一化法定量。
1.4 苯酚转化率和产物分布的计算方法
苯酚转化率(X)按下式计算:
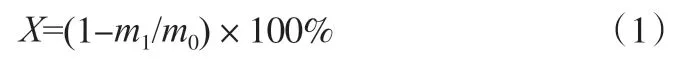
式中,m0是苯酚初始加入量,g;m1是未反应的苯酚量,g。
关联乙醚相和水相,则产物选择性为:

式中,i=2,3,4;m2,m3,m4分别为产物中邻苯二酚、对苯二酚和焦油的质量,g。
1.5 催化剂的XRD表征
XRD分析采用日本理学HR-6000型X射线衍射仪,Cu Kα射线,管电压40 kV,管电流30 mA,扫描范围2θ=10°~80°。
催化剂粒径根据Scherrer公式计算:

式中,d为催化剂粒径,nm;λ为X射线波长,λ=0.154 06 nm;k为常数,k=0.89;θ为衍射角,°;B为衍射峰的半高宽,°。
1.6 NH3-IR法测定催化剂的酸量
NH3-IR表征采用岛津公司Prestige-21型傅里叶变换红外光谱仪,原位漫反射红外附件为Thermo Spectra-Tech公司生产。
准确称量1.00 g KBr和0.05 g催化剂试样混合压片,然后把薄片放入以CaF2为窗口的原位池中。用N2吹扫,程序升温至105 ℃,保持20 min,清除催化剂表面吸附的CO2和水分。降温至80 ℃,切换成NH3,吸附20 min。然后降温至25 ℃,切换成N2,吹扫5 min,清除催化剂表面物理吸附的NH3。扫描试样,得到试样的NH3-IR谱图。根据L酸和B酸酸性位的特征吸收峰面积计算催化剂的表面酸量。
2 结果与讨论
2.1 催化剂制备工艺的优化
2.1.1 载体对催化剂性能的影响
分别以LAY,13X,HY以及硅铝比分别为50,80,100的HZSM-5分子筛为载体,分别制备了活性组分Fe含量(基于载体的质量)为7.45%的一系列催化剂,该系列催化剂的苯酚羟基化反应性能 评价结果见表1。

表1 载体对Fe基催化剂活性和选择性的影响Table 1 Effects of supports on the activity and selectivity of the Fe-based catalysts for the hydroxylation of phenol
由表1可知,以LAY,13X,HY以及硅铝比为100的HZSM-5分子筛为载体时,苯酚转化率较高,均超过46%,但反应副产物焦油选择性也很高,均超过52%,使得这些催化剂上的苯二酚收率均低于24%;而以硅铝比分别为50和80的两种HZSM-5 分子筛为载体的催化剂上副产物焦油选择性较低,分别为32.00%和35.08%,且当载体的硅铝比为80时,苯二酚收率最高,为28.15%。这可能是因为LAY,13X,HY分子筛这3种载体的B酸性较强,而载体的B酸性越强,对其表面的活性组分Fe原子的诱导作用越强,使其呈“电子缺乏性”[16],有利于羟基自由基的生成,因此转化率较高;但酸性过强使产物苯二酚很容易在小孔内发生次级反应,导致焦油含量高。硅铝比为80的HZSM-5分子筛与硅铝比分别为50和100 的HZSM-5及LAY,13X,HY分子筛相比,酸性适中,孔径大小为0.5~0.6 nm,与苯酚和苯二酚的分子直径(0.56 nm左右)相匹配,有利于提高产物的选择性。因此,选择硅铝比为80的HZSM-5分子筛作为苯酚羟基化反应催化剂的载体,以下简写为HZSM-5。
2.1.2 活性组分Fe含量对催化剂性能的影响
以HZSM-5为载体,制备了活性组分Fe含量分别为1.45%,3.45%,5.45%,7.45%,9.45%的一系列Fe/HZSM-5催化剂。该系列催化剂的苯酚羟基化反应性能评价结果见图1。由图1可见,随Fe含量的增加,苯酚转化率和苯二酚选择性均先升高后降低,焦油选择性先降低后升高。这是因为Fe是苯酚羟基化反应的活性中心,随Fe含量的增加,苯酚转化率和邻、对苯二酚的选择性逐渐升高;但Fe含量过高时,催化剂酸量过大,加速了H2O2的分解速率,增加产物次级反应和苯酚脱水成醚反应,生成焦油[17],导致苯酚转化率和苯二酚的选择性下降。当 Fe含量为5.45%时,苯酚羟基化合成苯二酚反应的效果最佳:苯酚转化率达44.83%,产物中邻、对苯二酚的选择性分别达56.07%,16.27%,苯二酚的总选择性为72.34%,焦油选择性为27.66%。因此,选择Fe含量为5.45%较适宜。

图1 Fe含量对Fe/HZSM-5催化剂活性和选择性的影响Fig.1 Effects of Fe content(based on the mass of the support) on the activity and selectivity of the Fe/HZSM-5 catalysts.
2.1.3 助剂Cu含量对催化剂性能的影响
在Fe含量为5.45%的Fe/HZSM-5催化剂上添加助剂Cu,制备了Cu含量(基于载体的质量)分别为1.65%,2.65%,3.65%,4.65%,5.65%的一系列Fe-Cu/HZSM-5催化剂,该系列催化剂的苯酚羟基化反应性能评价结果见图2。由图2可看出,在Fe/HZSM-5催化剂上添加适量Cu,可抑制焦油的生成。这是因为Cu是还原性物质,随Cu含量的增加,产物苯二酚被氧化成苯醌以及进一步被氧化成焦油的几率减小,焦油选择性逐渐降低,苯二酚选择性逐渐升高。此外,Cu也是羟基化反应的活性中心[18],Cu含量过高时,导致H2O2直接分解,使苯酚转化率和苯二酚选择性降低,苯酚、苯二酚缩合成醚的反应加剧,焦油含量逐渐增大[17]。当Cu含量为3.65%时,反应效果最佳:苯酚转化率为46.09%,邻、对苯二酚的选择性分别为60.59%,16.62%,苯二酚的总选择性为77.21%,焦油选择性降至22.79%。因此,选择Cu含量为3.65%较适宜。
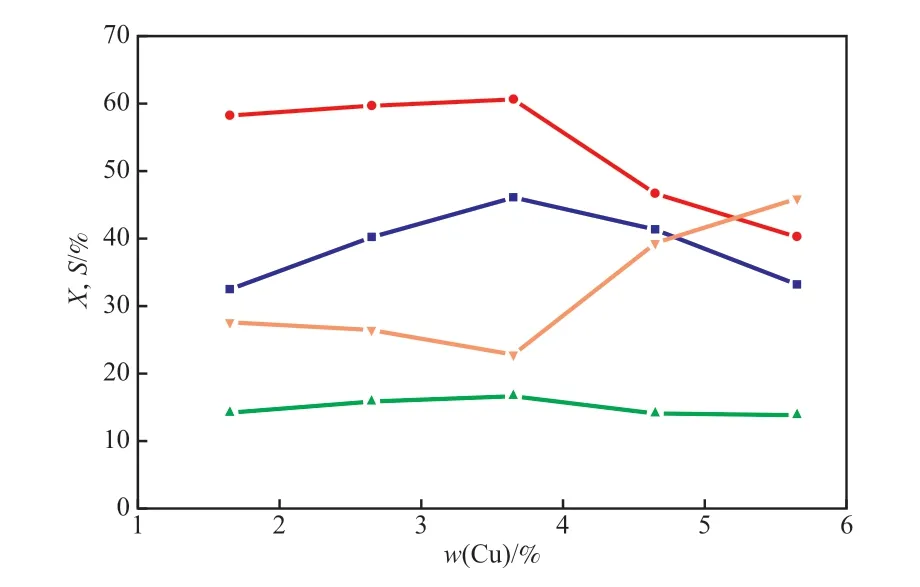
图2 Cu含量对5.45%Fe-Cu/HZSM-5催化剂活性和选择性的影响Fig.2 Effects of Cu content(based on the mass of the support) on the activity and selectivity of the 5.45%Fe-Cu/HZSM-5 catalysts.
2.1.4 助剂Sn含量对催化剂性能的影响
在Fe和Cu含量分别为5.45%,3.65%的Fe-Cu/HZSM-5催化剂上添加助剂Sn,制备了Sn含量(基于载体的质量)分别为0.23%,0.43%,0.63%,0.83%,1.03%的一系列Fe-Cu-Sn/HZSM-5催化剂,该系列催化剂的苯酚羟基化反应性能评价结果见图3。
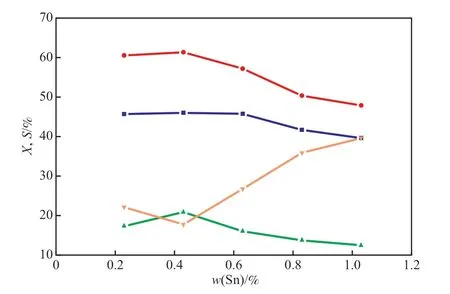
图3 Sn含量对5.45%Fe-3.65%Cu-Sn/HZSM-5催化剂活性和选择性的影响Fig. 3 Effects of Sn content(based on the mass of the support) on the activity and selectivity of the 5.45%Fe-3.65%Cu-Sn/HZSM-5 catalysts.
由图3可看出,添加Sn的作用与Cu相似,但Sn的还原性比Cu更强,当Sn含量由0.23%增至0.43%时,焦油选择性大幅降低。这是因为Sn是强还原性物质,少量Sn的加入在一定程度上抑制了产物苯二酚被氧化成焦油的几率,焦油含量大幅减小,苯二酚的选择性升高。但Sn含量继续增加时,过多的Sn会占据催化剂中Fe和Cu的活性中心,使催化剂的活性降低,苯酚转化率降低,苯酚定向生成邻、对苯二酚的几率减小,产物被H2O2进一步氧化成苯醌的几率增大[17],焦油含量增加。当Sn含量为0.43%时,反应效果最佳:苯酚转化率为46.03%,邻、对苯二酚的选择性分别为61.36%,20.88%,苯二酚总选择性为82.24%,焦油选择性降至17.76%。因此,选择Sn含量为0.43%较适宜。2.1.5 助剂Mg含量对催化剂性能的影响
在Fe, Cu, Sn含量分别为5.45%,3.65%,0.43%的Fe-Cu-Sn/HZSM-5催化剂上添加助剂Mg,制备了Mg含量(基于载体的质量)分别为0.48%,0.68%,0.88%,1.08%,1.28%的一系列Fe-Cu-Sn-Mg/HZSM-5催化剂,该系列催化剂的苯酚羟基化反应性能评价结果见图4。

图4 Mg含量对5.45%Fe-3.65%Cu-0.43%Sn-Mg/HZSM-5催化剂活性和选择性的影响Fig. 4 Effects of Mg content(based on the mass of the support) on the activity and selectivity of the 5.45%Fe-3.65%Cu-0.43%Sn-Mg/HZSM-5 catalysts.
由图4可见,在Fe-Cu-Sn/HZSM-5催化剂上添加适量Mg,在一定程度上也抑制了焦油的生成。随Mg含量的增加,苯酚转化率缓慢降低,苯二酚选择性先升高后降低,焦油选择性先降低后升高。当Mg含量为0.68%时,反应效果最佳:苯酚转化率为45.43%,邻、对苯二酚的选择性分别为64.71%,20.66%,苯二酚的总选择性为85.37%,焦油选择性降至14.63%。这是因为Mg是碱性物质,随Mg含量的增加,催化剂的酸性逐渐减弱,当Mg含量为0.68%时,催化剂的酸量适中,邻、对苯二酚的选择性好,焦油含量低;继续增加Mg含量,催化剂的总酸量继续降低,导致苯酚转化率继续降低,苯二酚的生成速率小于其被氧化成苯醌的次级反应速率,苯二酚选择性下降,焦油含量增加。因此,选择Mg含量为0.68%较适宜。
2.1.6 煅烧温度对催化剂性能的影响
将最佳组成的5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂分别在300,400,450,500,550,600 ℃下煅烧,不同煅烧温度下制得催化剂的苯酚羟基化反应性能评价结果见图5。由图5可看出,随煅烧温度的升高,苯酚转化率和邻、对苯二酚的选择性均先升高后降低,焦油选择性先降低后升高,当煅烧温度为450 ℃时,苯酚转化率达47.06%,邻苯二酚选择性达62.28%,对苯二酚选择性为23.81%,苯二酚的总选择性为86.09%,焦油选择性为13.91%。

图5 煅烧温度对5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂活性、选择性的影响Fig.5 Effects of calcination temperature on the activity and selectivity of the 5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5 catalyst.
这主要是由于煅烧温度对催化剂表面活性相的种类、活性物种的分布和数量等因素的影响造成的[19-20]。低温时,载体上的活性组分还未完全分解,催化剂活性中心少;随煅烧温度的升高,催化剂的活性中心逐渐增多,且活性组分在载体表面高度分散(见图6),苯酚定向生成苯二酚的几率增大,苯酚转化率和邻、对苯二酚的选择性逐渐升高;当煅烧温度过高时,载体晶格结构中的Al以及活性组分Fe的流失,使催化剂的酸性减弱[21-22],苯酚转化率和苯二酚选择性降低。因此,适宜的煅烧温度为450 ℃。
2.1.7 煅烧温度对催化剂结构的影响
5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂在不同煅烧温度下的XRD谱图和粒径变化分别见图6和表2。由图6可看出,在煅烧温度300~600 ℃内,未出现活性组分和助剂的衍射峰,说明活性组分和助剂在载体表面高度分散。由表2可知,当煅烧温度在450 ℃以下时,催化剂的粒径变化不大;当煅烧温度达到450 ℃以上时,催化剂的粒径增加幅度较大;煅烧温度为600 ℃时,催化剂的粒径迅速增大至46.07 nm。因此,煅烧温度为450 ℃时,催化剂活性组分的分散性好,粒径小,催化性能最佳。

图6 不同煅烧温度下5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂的XRD谱图Fig.6 XRD patterns of the 5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5 catalysts calcined at different temperatures.
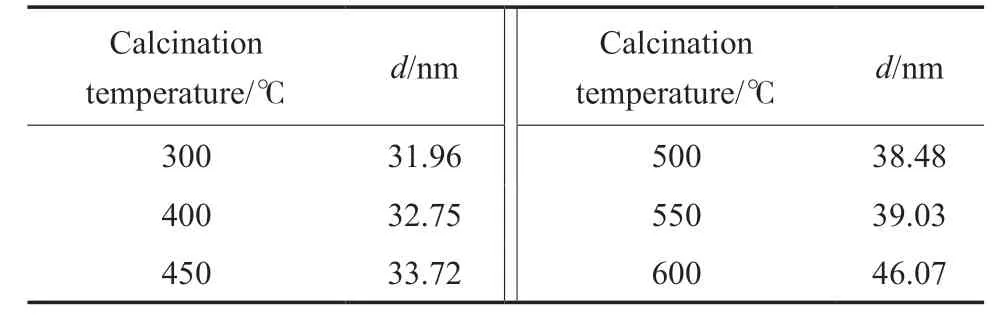
表2 不同煅烧温度下5.45%Fe-3.65%Cu%-0.43%Sn-0.68%Mg/HZSM-5催化剂的粒径Table 2 Particle sizes of the 5.45%Fe-3.65%Cu%-0.43%Sn-0.68%Mg/HZSM-5 catalysts calcined at different temperatures
2.2 催化剂酸量与催化剂性能的关系
4种不同化学组成的催化剂及HZSM-5载体的NH3-IR谱图见图7。由图7可看出,各试样均在1 400~1 600 cm-1和1 600~1 800 cm-1处出现两个峰。这表明各试样表面酸性不均匀,存在B酸和L酸两种酸中心[23-24]。
根据图7得到的催化剂酸量以及催化剂活性评价结果见表3。由表3可见, HZSM-5载体的酸量最低,总酸量为1.58 mmol/g;5.45%Fe/HZSM-5催化剂的酸量最高,总酸量为2.99 mmol/g;添加助剂Cu,Sn,Mg后,催化剂的总酸量由2.99 mmol/g逐渐降至1.98 mmol/g,苯酚转化率由13.09%升至47.06%,苯二酚选择性由66.33%升至86.09%,焦油选择性由33.67%降至13.91%。由此可知,Fe-Cu-Sn-Mg/HZSM-5催化剂的总酸量(1.98 mmol/g)与苯酚羟基化反应相匹配,可有效降低焦油含量。

表3 催化剂酸量与催化性能的关系Table 3 Relationship between the acid amounts on the catalysts and their catalytic performances
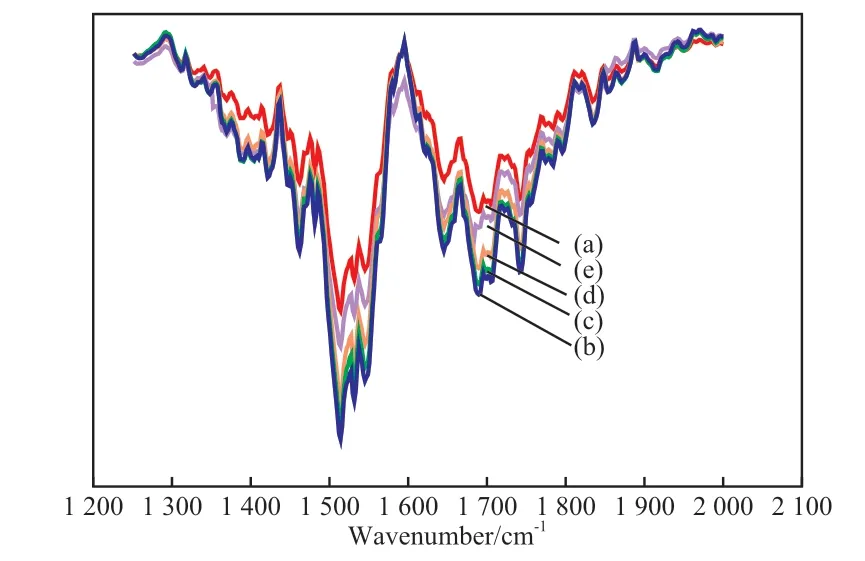
图7 不同化学组成的催化剂和HZSM-5载体的NH3-IR谱图Fig.7 NH3-IR spectra of the HZSM-5 support and the catalysts with different chemical compositions.
3 结论
1)制备了低负载量Fe-Cu-Sn-Mg/HZSM-5固体酸催化剂,当催化剂中的Fe,Cu,Sn,Mg含量分别为5.45%,3.65%,0.43%,0.68%时,在450 ℃下煅烧2 h,苯酚羟基化反应效果最佳:苯酚转化率为47.06%,苯二酚总选择性为86.09%,焦油选择性降至13.91%。
2)XRD表征结果显示,5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂中活性组分Fe和助剂Cu,Sn,Mg在载体表面高度分散,催化剂粒径为33.72 nm。
3)NH3-IR表征结果显示,5.45%Fe-3.65%Cu-0.43%Sn-0.68%Mg/HZSM-5催化剂表面存在L酸和B酸两种酸中心,总酸量为1.98 mmol/g,酸量适中,与苯酚羟基化反应相匹配,表现出较优的催化活性和选择性。
[1] Vicente Rives,Olga Prieto,Amit Dubey,et al. Synergistic Effect in the Hydroxylation of Phenol over CoNiAl Ternary Hydrotalcites[J]. J Catal,2003,220(1):161 - 171.
[2] Dow Chem Co. Pyrocatechol Manufacture from a Chlorophenol:US,3536767[P]. 1970-10-27.
[3] 谭世语,罗婷,朱必珏. 苯胺氧化制对苯二酚中二氧化锰的回收利用[J]. 应用化工,1992,6(10):46 - 50.
[4] Rhone Poulenc Chimie. Hydroxylation of Phenols/Phenol Ethers:US,5245086[P]. 1993-09-14.
[5] Rhone Poulenc Chimie. Catalytic Hydroxylation of Phenols/Phenol Ethers:US,5097078[P]. 1992-03-17.
[6] Ube Industries,Ltd. Process For Preparing Dihydric Phenol Derivates:US,4078006[P]. 1978-03-07.
[7] Rhone Poulenc Chimie. Process for Hydroxylating of Phenolic Compounds:EP,0480800[P]. 1992-04-15.
[8] Brichima Spa. Process for Preparing Diphenols:US,3914323[P]. 1975-10-21.
[9] Joon Ching Juan,Zhang Jingchang,Mohd Ambar Yarmo.Study of Catalysts Comprising Zirconium Sulfate Supported on a Mesoporous Molecular Sieve HMS for Esterification of Fatty Acids Under Solvent-Free Condition[J]. Appl Catal,A,2008,347(2):133 - 141.
[10] Snamprogetti Spa. Preparation of Porous Crystalline Synthetic Material Comprised of Silicon and Titanium Oxides:US,4410501[P]. 1983-10-18.
[11] 王洪生,王祥生. 钛硅选择性氧化催化剂的研究进展[J].石油化工,1998,27(11):844 - 848.
[12] 于剑锋,吴通好. 邻苯二酚与对苯二酚的生产与研究现状[J]. 精细石油化工,1997(6):28 - 34.
[13] Xiong Chunrong,Chen Qinglin,Lu Weiran,et al. Novel Fe-Based Complex Oxide Catalysts for Hydroxylation of Phenol[J]. Catal Lett,2000,69(3/4):231 - 236.
[14] 张敬畅,张信芳,张天巧,等. 负载型铁基复合氧化物催化苯酚羟基化的研究[J]. 分子催化, 2003,17(1):40 - 46.
[15] 张俊梅,冯惠生. 过氧化氢氧化邻苯二酚、对苯二酚反应动力学的研究[J]. 石油化工,2005,34(3):247 - 249.
[16] 黎成勇,黄华. 载体酸性对镍金属催化剂芳烃加氢抗硫性能的影响[J]. 工业催化,2006,14(6):16 - 19.
[17] 张敬畅,张信芳,张光明,等. 苯酚羟基化合成苯二酚反应过程中酚焦油的生成机理[J]. 精细石油化工,2005(5):58 - 63.
[18] Xiao Fengshou,Sun Jianmin,Meng Xianngju,et al. Synthesis and Structure of Copper Hydroxyphosphate and Its High Catalytic Activity in Hydroxylation of Phenol by H2O2[J]. J Catal,2001,199(2):273 - 281.
[19] 王育,戴伟,彭辉,等. 深度托出CO的CuO/ZnO/ZrO2催化剂[J]. 石油化工,2008,37(11):1121 - 1126.
[20] Nagas K,Zheng Y,Kodama Y,et al. Dynamic Study of the Oxidation State of Copper in the Course of Carbon Monoxide Oxidation over CuO and Cu2O[J]. J Catal,1997,187(1):123 - 130.
[21] Lu Jiangyin,Zhao Zhen,Xu Chunming,et al. Effects of Calcinations Temperature on the Acidity and Catalytic Performances of HZSM-5 Zeolite Catalysts for the Catalytic Cracking of n-Butane[J]. J Nat Gas Chem,2005,14(4):213 - 220.
[22] 李晓菲,余定华,初旭明. CuO/SiO2上甘油脱水制α-羟基丙酮[J]. 石油化工,2010,39(8):866-871.
[23] Zhang Jingchang,Mohd Ambar Yarmo,Joon Ching Juan,et al. Supported Zirconium Sulfate on Carbon Nanotubes as Water-Tolerant Solid Acid Catalyst[J]. Mater Res Bull,2007,42(7):1278 - 1285.
[24] 佘励勤,李宣文. 固体催化剂的研究方法[J]. 石油化工,2000,29(8):621 - 635.
