共聚甲基丙烯酸酯纤维对三氯乙烯的吸附动力学及热力学
2013-12-19王成芳
王成芳,封 严,2,赵 健
(1.天津工业大学纺织学部,天津 300387;2.先进纺织复合材料教育部重点实验室,天津 300387;3.天津工业大学材料科学与工程学院,天津 300387)
近些年随着我国工业的快速发展,由各种工业油的泄漏及工业废油的排放造成的严重油污染,对河流和海洋的生态环境构成了严重的威胁[1]。三氯乙烯(TCE)是一种易挥发的有毒化合物,被广泛用作有机溶剂,对环境造成严重污染。因此为了保护生态环境,研究有效地回收污染油技术及材料是十分必要的。作为一种新型的疏水亲油性材料,吸附纤维在含油水处理以及其他相关领域有着很好的应用前景。
共聚甲基丙烯酸酯纤维是一种对氯烃、芳香烃、煤油等油性有机化合物具有良好选择吸附功能的新型高分子材料,可用于水体漏油处理、分离及过滤等环保领域[2-3]。作为新开发的纤维材料,对于其微观结构、吸附模型等基础理论的研究尚不深入。由于该纤维具有化学交联、物理交联和大分子缠结等复杂的网络结构[4],因此基于化学交联聚合物建立的溶胀[5]、吸附模型不能准确模拟油性有机化合物在纤维中的吸附、扩散行为。本文拟从Freundlich吸附模型[6]、Langmuir吸附模型[7]出发,研究三氯乙烯在共聚甲基丙烯酸酯纤维中的吸附热力学;从准一级动力学方程[8],准二级动力学方程[9]和颗粒内扩散方程[10-11]出发,研究三氯乙烯在共聚甲基丙烯酸酯纤维中的吸附动力学,对共聚甲基丙酸酯纤维的吸附机制进行研究。
1 实验部分
1.1 实验原料及仪器
三氯乙烯(TCE),化学纯,天津市光复精细化工研究所;FA2004B电子天平,上海精密科学仪器有限公司;SHA-B型双功能水浴恒温振荡器。
1.2 共聚甲基丙烯酸酯正丁酯纤维的制备
共聚甲基丙烯酸酯正丁酯纤维的制备方法参照文献[1]。采用水相悬浮聚合方法,以甲基丙烯酸正丁酯(BMA)为单体,甲基丙烯酸羟乙酯(HEMA)为潜交联剂合成吸油性能较好的共聚甲基丙烯酸酯,经纺丝成形后,对纤维进行热交联处理,最终制成后交联型的共聚甲基丙烯酸酯吸油纤维。
1.3 三氯乙烯标准溶液的配置
精确量取一定体积的TCE溶液,分别加入4个500 mL容量瓶中,加入去离子水至刻度,使TCE充分溶解,配置质量浓度为15、20、25和30 g/L的三氯乙烯标准溶液。
1.4 对TCE的吸附动力学实验
将一定质量的聚甲基丙烯酸正丁酯纤维分别置于250 mL容量瓶中,瓶中盛有一定浓度的TCE标准液,将容量瓶放入恒温水浴振荡器中,在30℃、200 r/min的转速下,于一定时间段分别称量吸附后纤维的质量,计算不同时刻纤维对TCE的吸附量,研究聚甲基丙烯酸正丁酯纤维对TCE的吸附动力学。
1.5 对TCE的吸附热力学实验
将一定质量的聚甲基丙烯酸正丁酯纤维分别置于250 mL容量瓶中,瓶中盛有质量浓度为25 g/L的TCE 溶液,在20、25、30、35 ℃温度条件下,得到纤维对TCE的饱和吸附量。由不同温度下聚甲基丙烯酸正丁酯纤维对TCE的吸附量分析聚甲基丙烯酸正丁酯纤维对TCE的吸附热力学。
2 结果及讨论
2.1 纤维对TCE的吸附动力学
常见的用于描述吸附过程的模型主要有3种。1)准一级动力学模型
准一级动力学模型是进行固液吸附体系模拟分析的常用模型之一,其吸附方程的线性表达式为
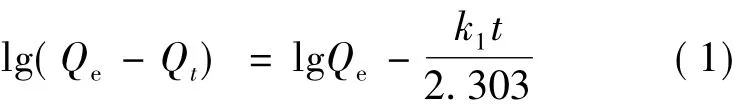
式中:Qe为平衡吸附量,g/g;t为吸附时间,min;Qt为t时刻的吸附量,g/g;k1为准一级吸附动力学速率常数,min-1。
2)准二级动力学模型
准二级动力学模型以吸附速率由吸附剂表面上未被占有的吸附空位数目的平方值决定的假设为基础,其吸附方程的线性表达式为
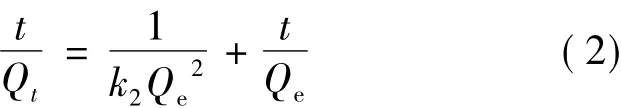
式中:k2为准二级吸附动力学速率常数,g/(g·min)。
3)颗粒内扩散方程表达式为

式中:kid为颗粒内扩散系数。
根据纤维的吸附量与吸附时间的关系,分析纤维对三氯乙烯的吸附动力学,分别绘制lg(Qe-Qt)对t的一级动力学曲线,t/Qt对t的二级动力学曲线,和Qt对t1/2做颗粒内扩散曲线,结果如图1所示,对所有数据进行线性回归分析,计算各个方程的动力学参数以及相关系数,结果如表1所示。
准一级吸附动力学、准二级吸附动力学以及颗粒内扩散方程的拟合结果显示,吸附动力学数据的相关系数R2均表现出显著水平,颗粒内扩散方程和准一级吸附动力学方程的拟合效果不如准二级吸附动力学方程好,准一级吸附动力学拟合得出的平衡吸附量与实验数据有很大差别,可以描述初始阶段的吸附过程,但不适合描述整个吸附过程;准二级吸附动力学方程能准确反应吸附的整个过程,具有较好的拟合性。不同浓度下用准二级吸附动力学模型计算出的Qe为 12.64、14.86、15.70、15.09 g/g,与实验值 11.57,13.44,14.06、14.31 g/g很接近,相对误差不大。从k2值的变化可看出,质量浓度为30 g/L时,k2突然变大,这可能是因为在浓度较低时,其吸附的推动力不是很强,因此刚开始主要集中在大孔和中孔区进行吸附,慢慢地才能渗透进入微孔区,而当浓度增加时,吸附的推动力越大,溶质分子越容易进入微孔区,从而直接被迅速地吸附。
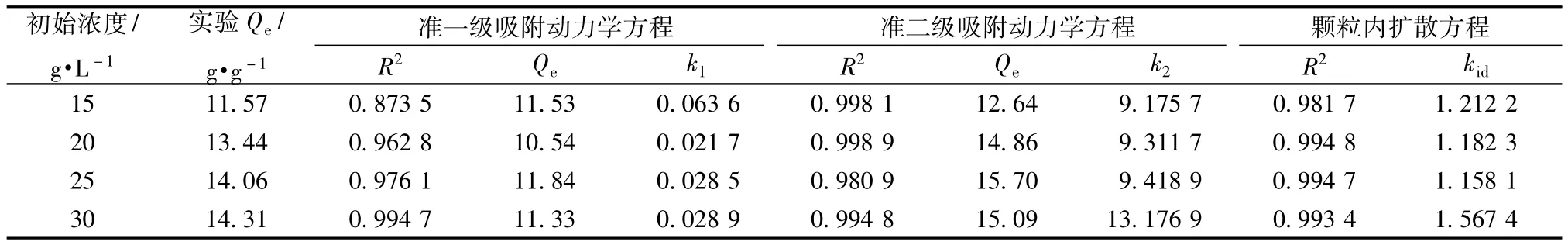
表1 动力学参数Tab.1 Parameters of dynam ics
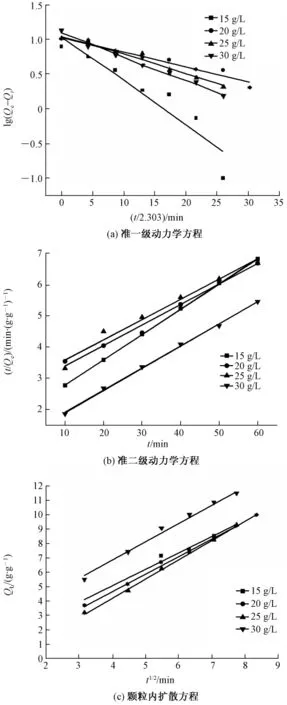
图1 动力学模拟曲线Fig.1 Kinetics curves.(a)Simulated results of pseudofirst-order kinetics;(b)Simulated results of pseudosecond-order kinetics;(c)Simulated results of intraparticle diffusion
2.2 纤维对TCE的吸附热力学
常见的用于描述吸附热力学的模型主要有3种。
1)Langmuir模型
Langmuir方程属于理论推导公式,其线性表达式为
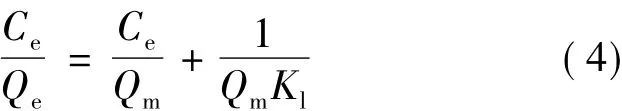
式中:Ce为平衡质量浓度,g/L;Qm为最大吸附量,g/g;Kl为平衡常数。
2)Freundlich模型
Freundlich方程是指数型吸附等温线,属于纯经验公式,一般可以描述非线性的吸附现象,其线性表达式为
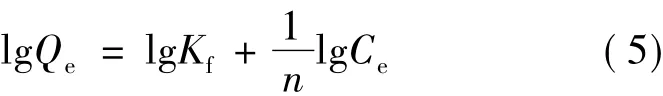
式中:Kf为Freundlich吸附平衡常数,表示吸附作用强度,其值越大表示对该物质的吸附能力越强;n为衡量等温线线性与否的经验常数。
3)Van't Hoff关系式和Gibbs关系式
吸附热力学参数一般可由Van't Hoff关系式及Gibbs关系式[12-14]计算得到。吸附平衡常数K和热力学性质参数△G、△S和△H之间满足Van't Hoff关系式,关系式为
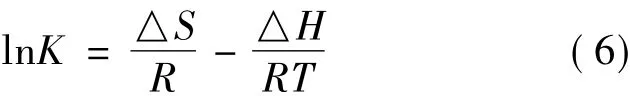
式中:K为等温方程的平衡常数;△H为焓,kJ/mol;△S为熵,kJ/mol。
lnK与1 000/T呈线性关系,从所得的线性关系方程的截距和斜率可得到△S和△H的值。
由Gibbs关系式方程可得到△G的值。
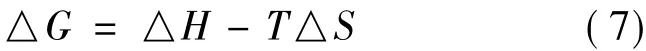
式中:△G为自由能,kJ/mol。
浓度为25 g/L的TCE溶液,在温度为20、25、30、35℃的条件下,在聚甲基丙烯酸正丁酯纤维上的吸附等温线数据进行拟合,不同温度下的吸附等温线见图2。聚甲基丙烯酸正丁酯纤维在不同温度下对三氯乙烯溶液的Langmuir方程、Freundlich方程的拟合结果如表2所示。
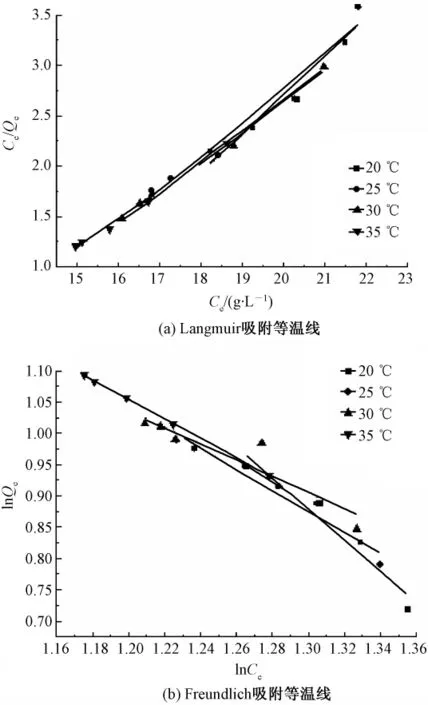
图2 不同温度下的吸附等温线Fig.2 Adsorption isotherm at different temperatures.(a)Adsorption isotherm of Langmuir;(b)Adsorption isotherm of Freundlich
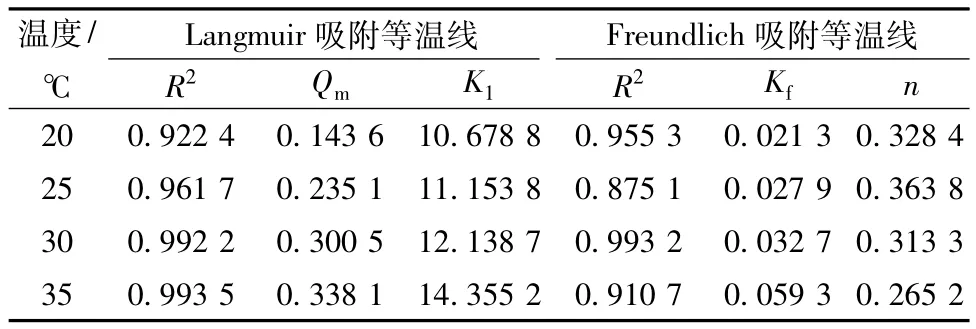
表2 吸附等温线参数Tab.2 Langmuir and Freundlich parameters
4)Van't Hoff和Gibbs方程
对lnKf和1 000/T作图(见图3),即可求得△S和△H。
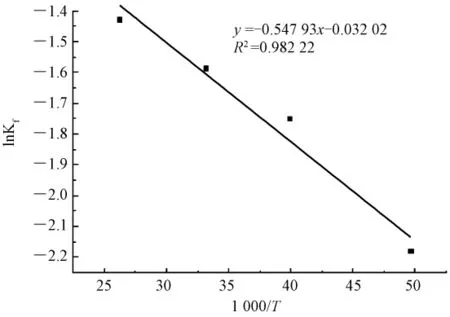
图3 ln K f和1 000/T回归曲线Fig.3 Regression curve of ln K f and 1 000/T
通过Gibbs方程得到△G,各对应值见表3。对比Langmuir和Freundlich吸附等温式可知,共聚甲基丙烯酸正丁酯纤维的吸附符合上述2个方程,比较相关系数R2,可对于Langmuir吸附等温方程的符合程度更好,属于单分子层吸附。随着温度的升高,纤维的饱和吸附量和Langmuir平衡常数Kl也随之增大,因此可看出该吸附属于吸热过程,升高温度有利于吸附的进行。
△G值能够反应吸附过程中推动力的大小,吸附推动力越大,其绝对值越大。从表3中可以看出,随温度升高,△G变大,即吸附推动力增加,使得吸附速率加快。△S>0,表明吸附过程是熵推动为主的过程。△H>0表明该吸附过程为吸热反应,温度升高有利于吸附的进行。
由实验结果可进一步推断TCE吸附过程中的主要分子间作用力。Vonopen等[15]测定了各种作用力引起的吸附热范围,见表4。

表3 热力学参数Tab.3 Thermodynam ic parameters
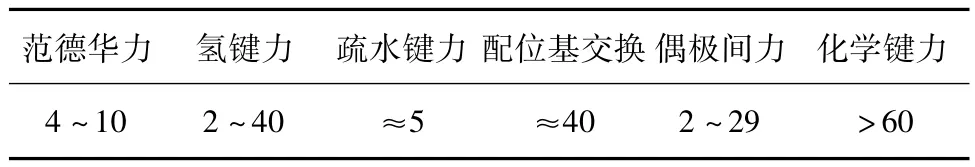
表4 各种作用力引起的吸附热范围Tab.4 Adsorption heat ranges caused by all kinds of forces
由于TCE是极性化合物,结合其热力学参数推断出在共聚甲基丙烯酸正丁酯纤维上的吸附过程中存在范德华力、氢键力、疏水键力、偶极间力等作用力。
3 结论
1)对吸附过程中吸附量随时间的变化进行了准一级、准二级吸附动力学方程和颗粒内吸附方程的线性拟合,结果表明:准二级动力学方程能够更好地模拟整个吸附过程,计算结果更加接近实际情况,其次为颗粒内吸附方程,最次为准一级方程。
2)对吸附过程中平衡浓度随平衡吸附量的变化进行了Langmuir、Freundlich等温方程线性拟合,结果表明:吸附过程对于Langmuir吸附等温方程的符合程度更好,共聚甲基丙烯酸酯纤维的吸附属于单分子层吸附,反应吸热。
3)通过Van't Hoff和Gibbs方程对整个反应过程进行相关热值的探究,结果表明:随着温度升高,吸附速率加快,该吸附过程为吸热反应,吸附过程是熵推动为主的过程。
[1] 柳颖,徐明,柳婧.高吸油性树脂的研究进展[J].化学与黏合,2010,32(1):46-49.LIU Ying,XU Ming,LIU Jing.Research progress of high oil absorption resins[J].Chemistry and Adhesion,2010,32(1):46-49.
[2] 封严,肖长发.聚甲基丙烯酸酯吸油纤维的研究[J].合成纤维工业,2004,27(1):1 -4.FENG Yan,XIAO Changfa.Study on oil-absorbent polymethacrylate fiber[J].China Synthetic Fiber Industry,2004,27(1):1 -4.
[3] RAJAKOVICV,ALEKSIC G,RADETIC M,et al.Efficiency of oil removal from real wastewater with different sorbent materials [J]. J Hazar Mater,2007(143):494-499.
[4] 宋喆,肖长发,徐乃库.甲基丙烯酸正丁酯共聚纤维的结构与性能[J].合成纤维工业,2009(3):18-20.SONG Zhe,XIAO Changfa,XU Naiku.Structure and properties of butyl methacrylate copolymer fiber[J].China Synthetic Fiber Industry,2009(3):18-20.
[5] LIU Xin,CHEN Hou,WANG Chunhua,et al.Synthesis of porous acrylonitrile/methyl acrylate copolymer beads by suspended emulsion polymerization and their absorption properties after amidoximation[J].Journal of Hazardous Materials,2010,175(3):1014 -1021.
[6] SAUCEDO I,GUIBAL E,ROUSSY J,et al.Uranium sorption by glutamate glucan:a modified chitosan:part I:equilibrium studies[J].Water Science and Technology,1993,l9(6):113 -118.
[7] 王雪源,乔旭,严长浩.壳聚糖对Pb(Ⅱ)的吸附及动力学研究[J].化工时刊,2008,22(5):5-9.WANG Xueyuan,QIAO Xu,YAN Changhao.Study on adsorption and kinetics of chitosan for Pb(Ⅱ)[J].Chemical Industry Times,2008,22(5):59.
[8] RENGARAJ S,KIM Y,JOO C K.,et al.Removal of coper from aqueous solution by aminated and protonated mesoporous alumina:kinetics and equilibrium [J].Colloid Interface Sci,2004,273(1):14 -21.
[9] HO Y S.Removal of copper ions from aqueous solution by tree fern[J].Water Research,2003,37(10):2323 -2330.
[10] CHEUNG CW,Porter JF,MCKAY G.Sorption kinetics for the removal of copper and zinc from effluents using bone char[J].Sep Purif Techno1,2000,19(1):55 -64.
[11] CHIRON N,GUILET R,DEYDIER E.Adsorption of Cu(II)and Pb(II)onto a grafted silica:isotherms and kinetic models[J].Water Research,2003,37(13):3079-3086.
[12] LEYVA Ramos J,FUENTES Rubio L,GUERRERO Coronada R M,et al.Adsorption of trivalent chromium from aqueous solutions onto activated carbon[J].J Chem Technol Biotechnol,1995,62(1):64 -67.
[13] HARIBABU E,UPADHYA Y D,UPADHYAY S N,Removal of phenols from effluents by fly ash [J].International Journal of Environmental Studies,1993,43(2):169-176.
[14] HAN R P,ZHANG J H,ZOU W H.Biosorption of copper(II)and lead(II)from aqueous solution by chaff in a fixed-bed column[J].Hazard Mater,2006,133(1 -3):262-268.
[15] VONOPEN B,KORDEL W,KLEIN W.Sorption of nonplus and polar compounds to solis: processes,measurement and experiencewith the applicability of the modified OECD-guideline[J].Chemosphere,1991,22:285-304.
