粘结剂对锂离子电池Si/C复合材料性能的影响
2013-12-14苏明如王志兴郭华军李新海黄思林
苏明如,王志兴,郭华军,李新海,黄思林,甘 雷
(中南大学 冶金科学与工程学院,长沙 410083)
目前,商业化的锂离子二次电池普遍采用各种碳材料作为负极,主要是石墨化碳和无定形碳,如天然石墨、改性石墨、石墨化中间相碳微球、软碳(如焦炭)和一些硬碳等[1]。这类材料嵌脱锂过程中的体积膨胀在 9%以下,表现出较高的库仑效率和优良的循环稳定性能,但却存在比容量低(如石墨理论容量 372 mA·h/g)、易发生有机溶剂共嵌入等缺点[2-3],不能满足高能量密度电池的需求。因此,近年来开发替代碳材料的新型负极备受瞩目。
高容量负极材料的研究主要集中在Si、Sn、Sb、Al和Pb等能与锂电化学合金化的金属,其中硅因为具有最高理论比容量(4 200 mA·h/g)、低嵌脱锂电位(0.02~0.6 V (vs Li+/Li))和丰富的资源而受到广泛的关注[4-5]。但是纯硅材料在高度嵌锂过程中存在非常显著的体积膨胀(>300%),电极材料会逐渐粉化,合金结构被破坏,硅粒子与导电网络之间发生分离,引起材料严重的形态变化,电极内阻增大,容量下降,循环性能变差,从而限制了硅基材料的大规模实用化[4]。
当前,针对高容量硅基材料的研究主要集中在抑制膨胀、改善循环性能方面。具体途径如下:1)减小颗粒尺寸,如纳米化等[6]。纳米材料具有比表面积大、离子扩散路径短、蠕动性强以及塑性高等特点,在充放电过程中电极体积变化小,能够在一定程度上缓解合金类材料的体积效应,并且提高其电化学性能;2)制备硅基复合材料,利用复合材料各组分间的协同效应,达到优势互补的目的[7-8];3)制备硅薄膜,硅基薄膜电极比容量较高,循环寿命也较长[9-11];4)采用新型粘结剂[12-14],如羧甲基纤维素钠(CMC)、苯乙烯-丁二烯橡胶(SBR)以及褐藻酸钠(SA)等。但是,纳米硅在循环过程中的剧烈团聚和电解液的持续分解使其实际应用受到限制,硅基薄膜的高制备成本和低总容量使它很难被广泛应用,而硅碳复合材料有更好的商业化前景。
在硅碳复合材料中,碳是离子与电子的混合导体,不仅在充放电过程中体积变化小,而且具有良好延展性和弹性,有利于改善硅电极的导电性和缓冲硅的体积变化。此外,碳材料与硅的嵌锂电位相近,其复合对材料容量损失相对较小。DATTA等[15-16]将硅、石墨和聚丙烯腈分散在N-甲基吡咯烷酮(NMP)中进行湿法球磨,然后热解制备了硅、石墨和无定形碳的复合物,其可逆容量稳定在660 mA·h/g。他们认为硅分散在石墨网格中,被无定形碳均匀地包覆,是材料稳定循环的重要原因。LEE等[17]利用球磨将硅、石墨和沥青粉末混合,然后通过高温热解沥青粉末得到球状混合物,其可逆容量经50次循环后稳定在700 mA·h/g左右。其实验结论表明:球状结构可有效缓解硅在循环过程体积膨胀对材料结构的破坏。粘结剂也是硅基负极材料的研究热点之一。KOVALENKO 等[14]研究了SA作为粘结剂时硅基材料的性能,材料的容量维持在2 000 mA·h/g左右,循环性能优异。
关于碳硅复合材料的研究很多,但制备材料的前驱体和制备方法明显影响着硅/碳复合材料的电化学性能[18],且不同的粘结剂对硅基材料在充放电过程中的膨胀有不同的抑制和缓解作用,对于硅基材料的循环性能有较大的影响。鉴于鳞片石墨具有形似鱼鳞状的层状结构,能够很好地嵌入纳米硅颗粒,且具有良好的导电性能,将它与硅复合,在一定程度上能改善硅的循环性能。基于以上考虑,本文作者以纳米硅粉(Nano-Si)、鳞片石墨(FG)和柠檬酸为原料,采用高温热解法制备Si/C复合材料,并采用两种不同的粘结剂PVDF和SA系统研究了复合材料的电化学性能。
1 实验
1.1 材料的制备
将柠檬酸(分析纯,天津市科密欧化学试剂有限公司生产)溶于适量无水乙醇中,在磁力搅拌下完全溶解后,向溶液中缓慢加入适当配比的纳米硅(纯度>99.9%,平均粒径约为30 nm,上海水田材料科技有限公司生产)和鳞片石墨(纯度>99%,平均粒径约为0.5 μm,青岛市天合石墨有限公司生产),在25 ℃下强力搅拌2 h,然后在80 ℃下固化,待溶剂完全挥发后,得块状前驱体。将所得前驱体于80 ℃下鼓风干燥12 h后,置于程序控温管式炉中,在高纯氩(99.999%)的保护下于800 ℃煅烧2 h,其中升温速率为5 ℃/min,随炉冷却得到硅/鳞片石墨/热解碳复合材料,各组分的质量分数分别为硅 30%,石墨 60%,柠檬酸热解碳10%,样品标识为Si/C。
1.2 材料的表征
采用日本Rigaku D/max2550VB+18KW转靶X射线衍射仪进行物相分析,分析条件如下:Cu Kα辐射,40 kV,300 mA,步宽 0.02°。采用 JEOL公司的JSM6380扫描电镜观察样品的表面形貌,电子加速电压为20 kV。
1.3 电池的组装与测试
将合成的负极材料、导电炭黑(Super P)和粘结剂(PVDF或 SA)按 8:1:1(质量比)均匀混合,加入 NMP调制成浆后,均匀涂覆在铜箔上,于120 ℃下真空干燥,制备成d=14 mm的负极片。以d=14 mm的金属锂片为对电极,电解液为1 mol/L LiPF6的碳酸乙烯酯(EC)+碳酸二乙酯(DEC)+碳酸甲乙酯(EMC)(1:1:1,体积比)溶液,隔膜为 Celgard2400,在氩气保护的手套箱内装配成CR2025型扣式电池。充放电测试在深圳新威尔公司生产的充放电测试仪上完成,测试温度为常温,充放电电流密度为50 mA/g,充放电截止电压为0.001~2.0 V。循环伏安及交流阻抗测试均在电化学工作站(上海辰华 CHI660A)上完成。循环伏安的扫描速率为0.1 mV/s,电压为0~2.0 V;交流阻抗测试的(正弦波)振幅为5 mV,频率为0.01~105kHz。
2 结果与讨论
2.1 结构和形貌
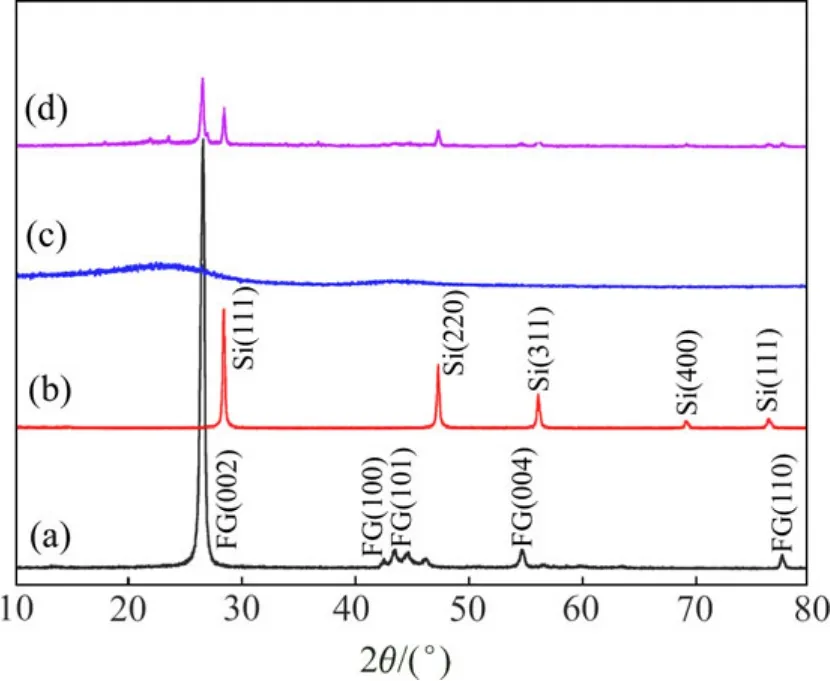
图1 鳞片石墨、纳米硅、柠檬酸热解碳和Si/C复合材料的XRD谱Fig.1 XRD patterns of flake graphite, nano-Si, citratepyrolyzed carbon and Si/C composite: (a)Flake graphite;(b)Nano-Si; (c)Citrate-pyrolyzed carbon; (d)Si/C composite
图1所示为纳米硅、鳞片石墨、柠檬酸热解碳以及高温热解法制备Si/C复合材料的XRD谱。从图1可以看出,在本研究中,采用的原料纳米硅和鳞片石墨具有良好的晶体结构。而复合材料中含有明显的纳米硅粉(衍射峰位于 28.4°、47.3°、56.1°、69.1°和 76.4°,PDF#75—0590)和鳞片石墨(衍射峰位于 26.6°、42.5°、43.5°、54.7°和 77.6°,PDF#26—1080)[19]的特征峰。由于柠檬酸热解碳为非晶态,所以在图中并没有明显的衍射峰,只在2θ=23°处有一个较小的峰,表明复合材料中有残余的碳。且复合材料中没有SiC和SiO2相的衍射峰,表明在该合成条件下,硅与碳之间没有发生化学反应,而是以硅、鳞片石墨和热解碳混合物的形式存在于复合材料中[13]。
图2所示为纳米硅、鳞片石墨和Si/C复合材料的SEM像。由图2可知,实验采用的纳米硅粒度均匀,但是存在一定的团聚现象,鳞片石墨形似鱼磷状,尺寸为0.5 μm。所制备复合材料颗粒尺寸不一,单体颗粒尺寸大多在5 μm以下,填充在大颗粒的空隙中。在材料制备过程中,由于溶剂挥发后,柠檬酸会发生固化,硅和石墨会嵌入块状前驱体的空隙中,包覆在固体颗粒的周围。前驱体经烧结后,柠檬酸会热解碳化,脱去其中的小分子物质(H2O、CO2),收缩形成疏松脆性的复合材料,研磨后为不规则颗粒,反应形成的碳均匀地分布在复合材料的内部或者表面,提供了良好的导电网络。
2.2 电化学性能

图2 纳米硅、鳞片石墨和Si/C复合材料的SEM像Fig.2 SEM images of nano-Si(a), flake graphite(b)and Si/C composite((c), (d))
图3所示为分别使用不同粘结剂(PVDF和SA)时复合材料的首次充放电曲线。硅基负极材料首次嵌锂过程在0.2 V以下有很长的倾斜电压平台,对应复合材料的合金化过程,图中首次放电曲线有明显的电解液分解斜坡和晶体硅的嵌锂平台[20],对应于SEI膜的形成以及材料所消耗的不可逆容量。采用PVDF粘结剂时复合材料的首次充电容量为528.7 mA·h/g,放电容量为759.9 mA·h/g,首次库仑效率为69.57%;采用SA粘结剂时复合材料的首次充电容量为 538.5 mA·h/g,放电容量为849.6 mA·h/g,首次库仑效率为63.38%。比较得知,采用PVDF粘结剂时,材料的首次库仑效率略高于采用SA粘结剂时的,这是因为SA粘结剂是水性粘结剂,难以渗透和吸收电解液,故复合材料在该粘结剂中相对难于活化,首次库仑效率较低。
电压滞后现象是高容量非碳类负极材料普遍存在的问题,对于硅这种高容量、半导体性质的负极材料,其电压滞后现象尤为严重,如图3(a)所示。比较可知,采用PVDF和SA粘结剂的材料在首次充放电过程中均存在电压滞后现象,且二者电压滞后程度相差不多。这是由于电池放电初期,电极反应产生的Li+受到SEI膜的阻碍,使电压滞后。然而经过几次循环后,如图3(b)所示,比较可知,采用SA粘结剂的充电电压平台略高于采用PVDF粘结剂时的,表明其电压滞后状况相对于PVDF略微减轻。
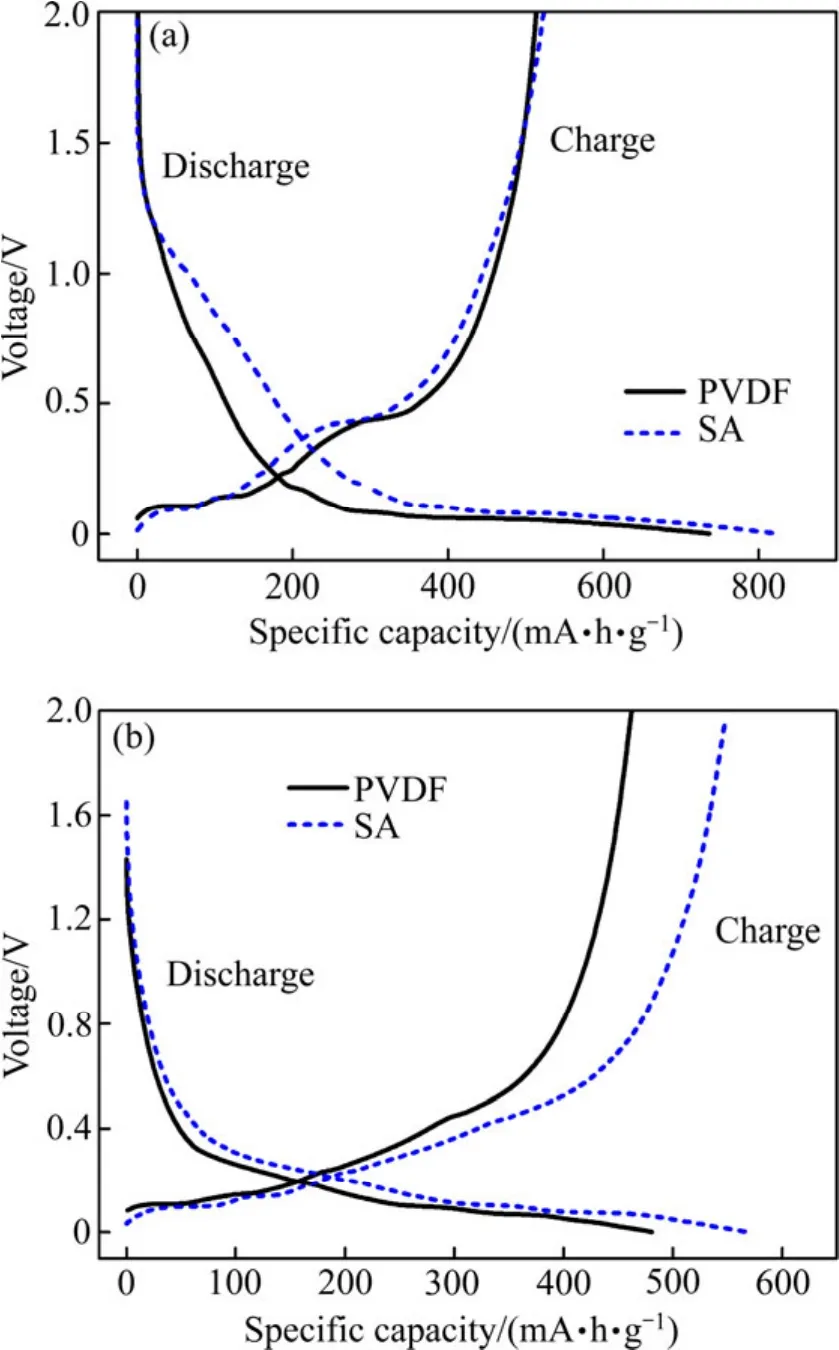
图3 采用不同粘结剂时 Si/C复合材料的首次充放电曲线和第五次充放电曲线Fig.3 Initial(a)and fifth(b)charge/discharge curves using different binders
图4所示为使用PVDF和SA粘结剂Si/C复合材料的循环性能曲线。由图4可知,采用不同粘结剂时材料的库伦效率差异不大,但是使用PVDF作粘结剂时20次循环后材料的容量为297.2 mA·h/g,保持率仅为56.21%。这表明使用PVDF粘结剂对活性物质的缓冲效果较差,导致其逐步粉化,活性材料从集流体脱落,部分电极材料失去了电活性,电极的循环稳定性逐步下降。而使用SA粘结剂的极片,比容量先减小后增加,然后逐渐达到稳定(如图4左下角图所示)。这是由于在最初的几个循环中,部分活性物质没有被充分利用,随着充放电过程的进行,锂离子的扩散通道被打开,使剩余部分活性物质被活化,从而比容量有所提高。采用水性粘结剂SA的极片,其循环性能明显比使用PVDF的极片更好,经过20次循环后,比容量为490.7 mA·h/g,保持率为91.12%。这是由于PVDF是热塑性材料,且PVDF在有机电解质溶液中的溶胀效应较大,同时溶胀后的粘结效果也会降低。而水性粘结剂SA是弹性材料[14],粘力较强,具有很好的延展性,可以承受活性材料较大的体积变化,在充放电时,承受了活性材料的反复膨胀和收缩,更适合用作硅基复合材料的粘结剂。
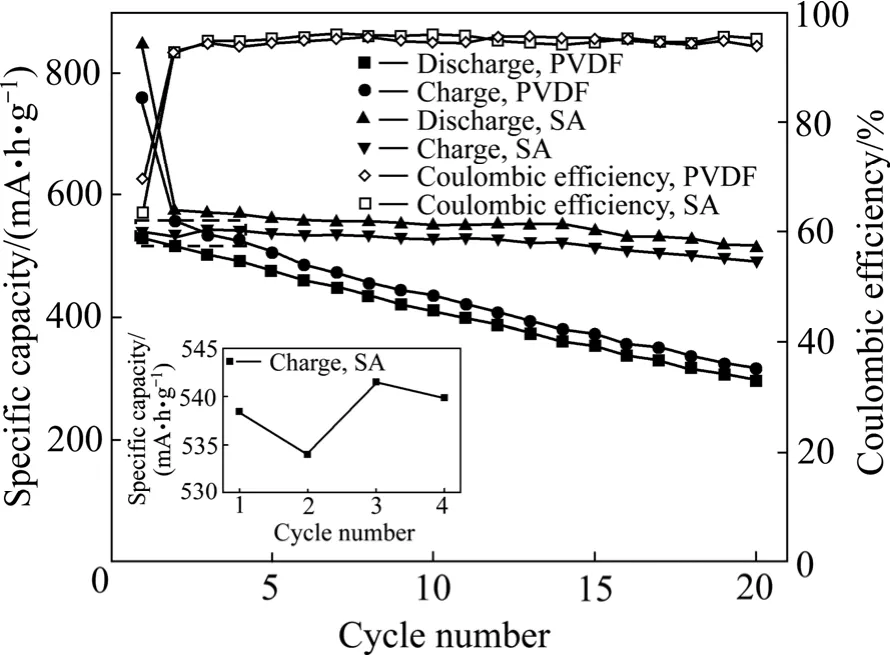
图4 采用不同粘结剂时材料的循环性能和库仑效率比较曲线Fig.4 Comparison of cycle performance and coulombic efficiency using different binders
2.3 电极动力学
本文作者对采用不同粘结剂时材料的电极动力学进行了研究。图5所示为采用PVDF和SA作为电极粘结剂时材料的循环伏安曲线。由图5可知,二者的循环伏安曲线保持一致,说明采用不同的粘结剂,并未改变材料的电极动力学。第一次循环在0.7 V附近有一扁平的还原峰,在第二次循环时消失。这是电解液的分解和材料表面形成固体电解质膜(SEI)造成的。比较得知,采用SA粘结剂时材料的循环伏安曲线较一致,说明采用该粘结剂时材料的循环稳定性优于采用PVDF粘结剂。在图5(b)中,硅有两对氧化还原峰,分别对应于充电(0.28 V、0.45 V)和放电过程(0.23 V、0.08 V)。0.1、0.2和0.25 V出现的氧化峰对应于石墨和无定形碳的脱锂(去合金化)过程,0~0.1 V的还原峰对应于其嵌锂(合金化)过程。循环的氧化峰和还原峰几乎保持一致,说明SA粘结剂对锂离子电池体系是稳定的。随着循环的进行,相应特征峰更加尖锐,说明需要一个活化的过程,材料的电极动力学才能达到最佳状态,这也与材料的循环性能曲线相吻合。
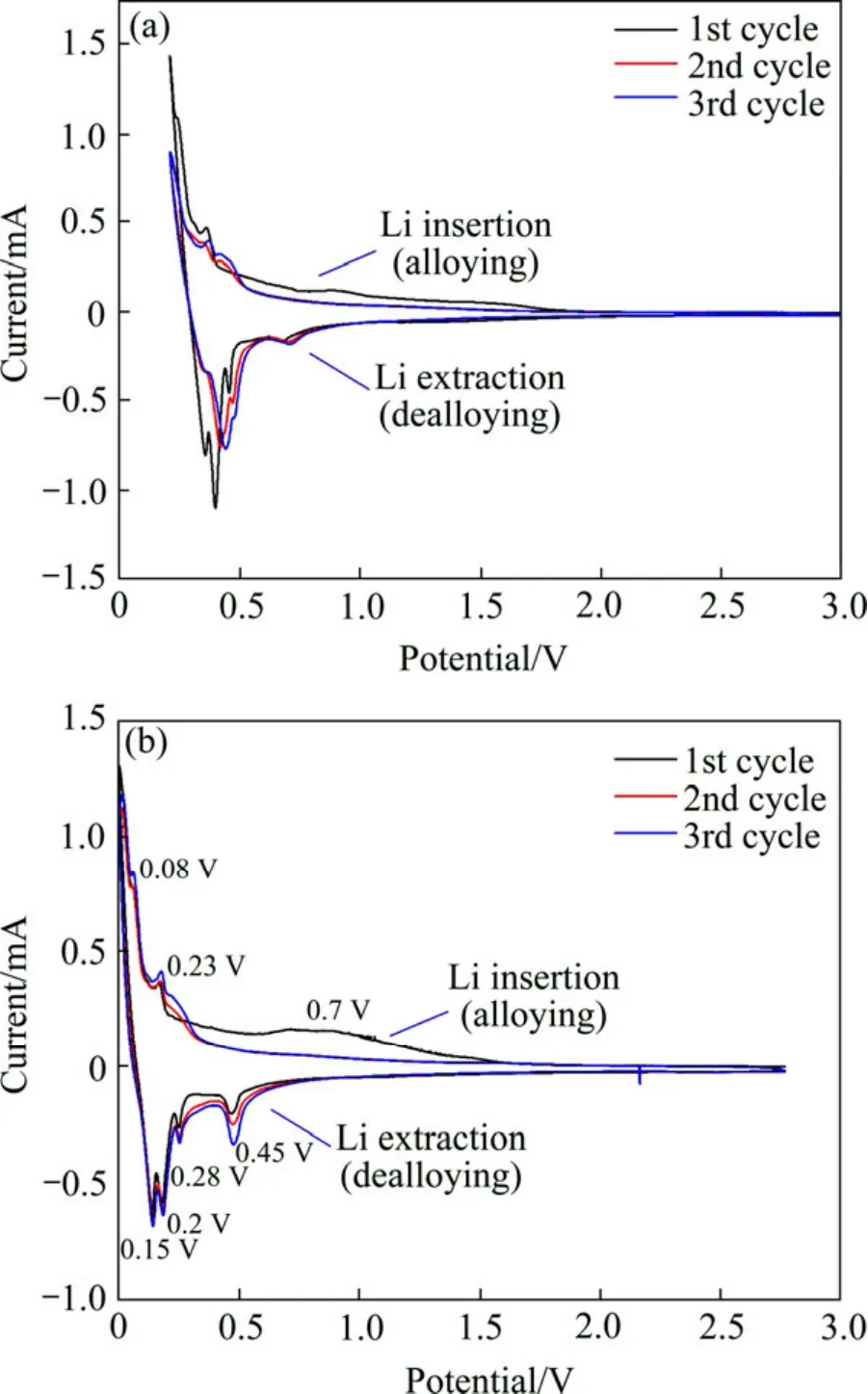
图5 采用不同粘结剂时Si/C复合材料的循环伏安曲线Fig.5 Cyclic voltammetry curves of Si/C composite using different binders (Sweep rate: 0.1 mV/s; Sweep voltage: 0~2.0 V): (a)PVDF; (b)SA
为更好地了解Si/C复合材料电化学性能改善的原因,本文作者采用EIS分析了不同粘结剂时Si/C电极的交流阻抗(EIS)谱,如图6(a)所示。由图可知,各图谱均由一个半圆和一条直线组成,半圆在高频区与实轴的截距代表溶液阻抗(Rs),半圆的直径代表电解质/复合材料界面的电荷转移阻抗(Rct),斜线代表锂离子在电极材料中扩散所引起的 Warburg阻抗(ZW)。采用SA粘结剂的Rct(32 Ω)小于采用PVDF粘结剂的Rct(38Ω),说明SA粘结剂能在一定程度上提高电解质/复合材料界面的电荷转移速率,也使在低频区的斜率增大,即ZW减小,有利于Li+在电极材料中的扩散。较小的Rct和ZW有利于克服放电过程中的动力学限制,使得Li+在Si/C复合材料中的脱/嵌锂深度得到提高,降低Li+在颗粒内部和表面的浓度差,从而有助于材料比容量的提高和循环性能的改善,这也与上述结果保持一致。

图6 采用SA和PVDF粘结剂时Si/C复合材料的交流阻抗曲线Fig.6 EIS curves of Si/C composite using different binders(Testing conditions: 0.01 Hz~100 kHz; amplitude: 5 mV)
3 结论
1)采用高温热解法制备了性能良好的 Si/C复合材料,在一定程度上减小了硅基材料的体积膨胀对电化学性能产生的不利影响。
2)在 Si/C复合材料中,硅和石墨嵌入块状前驱体的空隙中,高温热解后以弥散的形式存在于无定形碳中,无定形碳为复合材料提供了良好的导电网络。
3)相比于采用PVDF粘结剂,使用SA作为粘结剂时复合材料的电压滞后现象得到了一定程度的改善,且电极材料呈现出良好的循环性能,20次循环后,比容量保持率在90%以上。
[1]黄可龙, 王兆翔, 刘素琴.锂离子电池原理与关键技术[M].北京: 化学工业出版社, 2008: 130.HUANG Ke-long, WANG Zhao-xiang, LIU Su-qin.The principle and key technology of lithium ion battery[M].Beijing:Chemical Industry Press, 2008: 130.
[2]MA Hua, CHENG Fang-yi, CHEN Jun, ZHAO Jian-zhi, LI Chun-sheng, TAO Zhan-liang, LIANG Jing.Nest-like silicon nanospheres for high-capacity lithium storage[J].Advanced Materials, 2007, 19(22): 4067-4070.
[3]KIM H, HAN B, CHOO J, CHO J.Three-dimensional porous silicon particles for use in high-performance lithium secondary batteries[J].Angewandte Chemie, 2008, 120(52): 10305-10308.
[4]XIAO Jie, XU Wu, WANG De-yu, CHOI D, WANG Wei, LI Xiao-lin, GORDON L, GRAFF, LIU Jun, ZHANG Ji-guang.Stabilization of silicon anode for Li-ion batteries[J].Journal of the Electrochemical Society, 2010, 157(10): A1047-A1051.
[5]TAO Hua-chao, FAN Li-zhen, QU Xuan-hui.Facile synthesis of ordered porous Si@C nanorods as anode materials for Li-ion batteries[J].Electrochim Acta, 2012, 71(1): 194-200.
[6]WU H, CHAN G, CHOI J W, RYU I, YAO Y, MCDOWELL M T,LEE S W, JACKSON A, YANG Y, HU L B, CUI Y.Stable cycling of double-walled silicon nanotube battery anodes through solid-electrolyte interphase control[J]. Nature Nanotechnology, 2012, 35: 1-6.
[7]LEE J H, KIN W J, LIM S H.Spherical silicon/graphite/carbon composites as anode material for lithium-ion batteries[J].J Power Sources, 2008, 176(1): 353-358.
[8]ZUO Peng-jian, YIN Ge-ping, YANG Zhan-lin, WANG Zhen-bo,CHENG Xin-qun, JIA De-chang, DU Chun-yu.Improvement of cycle performance for silicon/carbon composite used as anode for lithium ion batteries[J].Materials Chemistry and Physics,2009, 115(2): 757-760.
[9]DATTA M K, MARANCHJ J, CHUNG S J, EPUR R,KADAKIA K, JAMPANI P, KUMTAA P N.Amorphous silicon-carbon based nano-scale thin film anode materials for lithium ion batteries[J].Electrochimica Acta, 2011, 56(13):4717-4723.
[10]BOURDERRAU S, BROUSE T, SCHLEICH D M.Amorphous silicon as a possible anode material for Li-ion batteries[J].Journal of Power Sources, 1999, 81/82: 233-236.
[11]ZHANG Y Q, XIA X H, WANG X L, MAI Y J, SHI S J, TANG Y Y, GU C G, TU J P.Three-dimensional porous nano-Ni supported silicon composite film for high-performance lithium-ion batteries[J].Journal of Power Sources, 2012, 213(1):106-111.
[12]MAGASINSKI A, ZDYRKO B, KOYALENKO I,HERTZBERG B, BURTOVYY R, HUEBNER C F, FULLER T F, LUZINOV I, YUSHIN G.Toward efficient binders for Li-ion battery Si-based anodes: Polyacrylic acid[J].Applied Material and Interfaces, 2010, 2(11): 3004-3010.
[13]陈立宝, 谢晓华, 解晶莹, 杨 军.粘结剂对锂离子电池硅/碳复合负极材料循环性能的影响[J].中国有色金属学报,2005, 15(1): 131-134.CHEN Li-bao, XIE Xiao-hua, XIE Jing-ying, YANG Jun.Effect of binder on cycling performance of Si/C anode for lithium ion batteries[J].The Chinese Journal of Nonferrous Metals, 2005,15(1): 131-134.
[14]KOVALENKO I, ZDYRKO B, MAGASINSKI A,HERTZBERG B, MILICEY Z, BURTOVYY R, LUZINOV I,YUSHIN G.A major constituent of brown algae for use in high-capacity Li-ion batteries[J].Science, 2011, 334: 75-79.
[15]DATTA M K, KUMTA P N.Silicon and carbon based composite anodes for lithium batteries[J].Journal of Power Sources, 2006,158(1): 557-563.
[16]DATTA M K, KUMTA P N.Silicon, graphite and resin based hard carbon nanocomposite anodes for lithium ion batteries[J].Journal of Power Sources, 2007, 165(1): 368-378.
[17]LEE J H, KIN W J, KIN J Y, LIM S H.Spherical silicon/graphite/carbon composites as anode material for lithium-ion batteries[J].Journal of Power Sources, 2008, 176(1):353-358.
[18]LI Ming-qi, WANG Cheng-yang, LIU Xiu-jun, ZHENG Jia-ming, WANG Hui.Influence of flake graphite on the microtexture of mescocarbon microbeads[J].New Carbon Materials, 2002, 17(4): 1-6.
[19]李明齐.锂离子电池硅/石墨/蔗糖碳复合负极材料的制备和电化学性能[J].西华师范大学学报: 自然科学版, 2010, 31(1):42-46.
[20]LI Ming-qi.Silicon/graphite/carbon composites as anode material for lithium ion batteries[J].Journal of China West Normal University: Natural Science, 2010, 31(1): 42-46.
