颈椎间盘置换术治疗颈椎病的短期疗效观察
2013-12-01戚小忠徐宏光孙良吕俞宏星
戚小忠,徐宏光,孙良吕,王 弘,刘 平,俞宏星
(1.池州市青阳康平医院 骨科,安徽 青阳 247101;2.皖南医学院附属弋矶山医院 脊柱外科,安徽 芜湖 241001)
颈椎椎间盘退变性疾病是颈椎的疼痛和神经症状的主要原因之一,颈椎病是颈椎退行性疾病中最为常见的一组疾病。通常情况下,颈椎病多采用非手术方法治疗,如果治疗无效,可考虑外科手术。颈前路椎间盘切除融合术(anterior cervical discectomy and fusion,ACDF)一直被视为治疗颈椎病手术的金标准,但因为其常会带来相邻椎间盘退变(adjacent disc degeneration,ADD)加速等并发症[1],故学者们开始寻找一种更好的治疗方式,于是颈椎人工椎间盘置换术逐渐被应用于临床。我们将人工椎间盘应用于颈椎病患者并取得了较好的疗效,现将治疗过程中的体会与随访疗效观察报道如下。
1 临床资料
1.1 一般资料 回顾性分析2010年3月 ~2011年1月期间于皖南医学院附属弋矶山医院就诊并采用Bryan人工椎间盘置换术治疗20例,均为单节段置换,C3/4 2例,C4/5 7例,C5/6 9例,C6/7 2例;其中男性13例,女性7例;年龄为32~50岁,平均年龄(42.5±6.1)岁;所有患者病程时间6个月~4年,平均(22±10.81)个月,均为接受系统的保守治疗但临床症状逐渐恶化者。患者纳入标准:①颈椎退变所致脊髓、神经损害经确诊并保守治疗无效需行前路减压且自愿接受本手术者;②仅行颈前路单节段Bryan人工椎间盘置换术并能良好交流和坚持随访者;③相关术前检查排除手术禁忌症者。排除标准:①明显颈椎屈伸活动不良、退行性节段性不稳定者;②明显椎间隙狭窄或椎管发育性狭窄者;③明显骨质疏松者;④先天性脊柱畸形者;⑤严重基础疾病者;⑦过敏体质者。术后平均随访时间为(18.9±7.23)个月。
1.2 手术方法及技巧 全麻后,仰卧位,肩下垫薄枕,保持自然体位,X线透视下确认手术节段椎间隙平行,常规消毒铺巾后,取右侧颈部横切口,游离颈阔肌瓣,沿胸锁乳突肌内缘到达椎前,切除病变椎间盘组织。确认中线后撑开椎间隙以确认打磨通道,经水平定位放入矢状楔子并确定打磨中心,使用盘状磨钻将上下终板和椎体后缘打磨切除,所有病例均切除后纵韧带,清除后缘和(或)钩椎关节骨赘,部分病例扩大双侧神经根管。测试假体大小,X线透视下确认后最终置入假体。术后24 h拔除引流皮片。
术后第1天可以坐起,第2天可以在软质围领保护下离床活动。围领佩戴1~2周后去除,正常活动并进行项背肌锻炼。
1.3 疗效观察评定标准 患者术前、术后3月及末次随访时颈椎采用日本骨科学会(japanese orthopaedic associatio,JOA)17 分评分法评分标准[2]和 Odom临床疗效评级系统[3]进行临床疗效评价;侧位X线片观察手术节段椎间高度变化,通过测量侧位片上Cobb角度即于C2和C7下缘各划一直线并测量两直线的夹角的变化来观察手术临近节段屈伸活动度(range of motion,ROM),于手术阶段上椎体的上缘和下椎体的下缘各做一直线并测量两直线的夹角,计算过屈过伸位时的差值来观察脊柱功能单位(functional spinal unit,FSU)活动度。
1.4 统计学分析 采用自身治疗前后进行对照,SPSS 13.0统计软件进行统计分析,术前、术后和末次随访JOA评分、手术节段椎间高度、FSU曲度及ROM进行方差分析,若组间存在差异继续采用q检验进行两两比较;以P<0.05作为统计学显著性差异。
2 结果
所有患者术中均未出现明显并发症。术中及术后X线检查显示假体位置良好。所有患者均获(18.9±7.23)个月随访,无人工椎间盘假体松动、移位或脱落等现象发生,椎间高度维持良好,全部患者术后病情良好,均恢复工作,JOA评分术前与术后3月及末次随访比较差异有统计学意义(P<0.05);X线检查观察椎间高度以及ROM术前与术后及末次随访比较显示差异有统计学意义(P<0.05),见表1。末次随访时进行Odom评级显示15例患者疗效优,3例良,2例一般,0例差,优良率达到90%。
表1 颈椎间盘置换术治疗颈椎病临床疗效分析(n=20,±s)
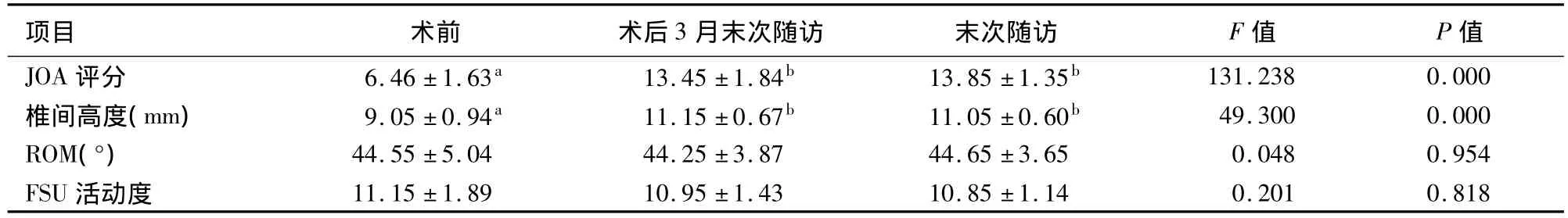
表1 颈椎间盘置换术治疗颈椎病临床疗效分析(n=20,±s)
注:两两比较采用q检验,两组之间字母相同表示P>0.05,两组之间字母不同表示P<0.05
项目 术前 术后3月末次随访 末次随访 F值 P值JOA 评分 6.46 ±1.63a 13.45 ±1.84b 13.85 ±1.35b 131.238 0.000椎间高度(mm)9.05 ±0.94a 11.15 ±0.67b 11.05 ±0.60b 49.300 0.000 ROM(°)44.55 ±5.04 44.25 ±3.87 44.65 ±3.65 0.048 0.954 FSU 活动度 11.15 ±1.89 10.95 ±1.43 10.85 ±1.14 0.201 0.818
3 讨论
3.1 颈椎病手术选择 随着生活节奏和生活方式的改变,近年来颈椎病已经成为骨科的常见病、多发病。颈椎病是颈椎间盘组织退变和退变继发的病理改变累及如神经根、脊髓、椎动脉、交感神经等组织所发生的一组疾病的统称,因目前尚未发现能完全逆转退变和解除压迫的药物,故颈椎病多需进行手术治疗。常用的手术方法分为前路、前外侧路、后路手术等,手术入路的选择取决于被压迫的位置,主要来源于后方的压迫、多节段受累、椎管狭窄、后纵韧带骨化者可选择后路手术;但颈椎病大多为来自前方的压迫,因此颈前路减压植骨融合术(anterior cervical discectomy and fusion,ACDF)成为治疗颈椎病的标准手术方式。但 Hilibrand等[4]报道在进行ACDF后每年约有2.9%的患者出现相邻节段退变的表现,10年后约25%以上的患者出现该问题。Bbaa等[5]根据一项随访8.5年的研究发现,106例行ACDF患者中有17例因邻近节段退变二次手术。多年的临床实践和基础研究发现其原因是由于ACDF融合了病变节段从而增加邻近节段的运动负荷,引起相应椎间盘内环境紊乱从而加速其退变并导致相应临床表现的发生。因此如何在完成前路减压后实现颈椎的生理性重建是解决邻近节段退变的关键问题。基于此,人工椎间盘置换术(artificial disc replacement,ADR)得到了迅速的发展。目前临床上最为常见的颈椎人工椎间盘假体包括Bryan、Pro-disc-C等类型,本研究主要观察Bryan型假体。颈椎ADR与ACDF相比不同的是在减压完成后植入人工椎间盘能保留椎间隙的活动并维持颈椎的生理弯曲和正常活动度,从而预防或延缓邻近节段退变的发生。当然,因为人工椎间盘假体存在机械寿命时间,而且费用昂贵,因此目前治疗颈椎病首选的手术方式仍是ACDF,我们认为在选择应用颈椎ADR时应严格把握手术适应证。
3.2 颈人工椎间盘手术适应证和禁忌症 综合相关因素,笔者认为颈椎ADR的主要适应证为:中青年颈3~7单纯颈椎间盘突出、单或双节段颈椎病,无明显骨性压迫者。禁忌症主要为:①对人工椎间盘材料过敏者;②严重基础疾病如糖尿病或需长期应用类固醇类激素如患风湿免疫类疾病、强直性脊柱炎等疾病者[6];③骨软化和严重骨质疏松[7],骨质疏松情况下有可能使椎间盘假体两端的金属终板陷入相邻近椎体;④颈椎不稳定[8];⑤多节段或伴有椎管狭窄的颈椎病;⑥创伤相关颈椎疾患;⑦活动性感染;⑧脊柱肿瘤转移等。
3.3 人工椎间盘手术疗效观察 自人工椎间盘被应用治疗颈椎病以来,由于其具有可有效减压和维持手术节段ROM从而防止邻近节段退变等优势而被广泛应用。本研究在Bryan颈椎间盘术后平均随访临床症状和影像学的结果,显示本研究中所有患者在行颈人工椎间盘置换术能在彻底减压后很好地缓解临床症状,并在一定程度恢复因椎间盘退变而降低的椎间隙,且因假体在设计时被允许在每个方向上存在11°的ROM[9],故与术前相比基本保留了退变节段活动(P=0.818),且未明显增加临近节段的活动度,颈椎ROM术前术后无明显差异(P=0.954),表明颈椎间盘置换术不会改变颈椎的生物力学,故不会增加临近节段应力负荷,从而降低了临近节段的退变发生率;同时我们观察病例中亦未出现临近节段退行性变现象。因此我们认为严格按照颈椎ADR的适应证和禁忌症选择手术方式,并在术中细心操作,可取得较好临床效果,明显提高患者的生活质量。
3.4 颈椎人工椎间盘置换术的注意事项 虽颈椎ADR手术取得了满意的临床效果,但也存在一定的问题,如颈椎压迫组织减压不彻底、假体下沉、松动和异位骨化与自发性融合等。因此在实行颈椎ADR手术操作过程中必须彻底减压,尤其是神经孔减压,因为人工椎间盘假体对椎间隙的撑开程度有限,故不能间接减压神经孔,所以神经孔的减压彻底与否关系着颈椎ADR的成败。研究表明[10],椎间盘假体松动是因为在终板打磨不够,因此在手术过程中应彻底刮除椎板软骨并选择合适的凹形窝磨钻并打磨到合适的程度,选择合适的假体型号和规格,使邻近椎体终板和假体终板接触充分,从而有利于应力分散和骨胳长入来实现长期固定,从而减少假体下沉、松动。减少假体周围异物是预防异位骨化与自发性融合的关键,故打磨时宜生理盐水反复冲洗,并避免其他物质在假体周围残留。
临床研究的证据已经表明,颈椎人工椎间盘置换术是治疗继发性颈椎间盘退化所导致的疼痛或神经系统症状的一种有前途的新技术,在严格把握其适应证和禁忌症的情况下,值得临床推广。
[1]FEKETE TF,PORCHET F.Overview of disc arthroplasty-past,present and future[J].Acta Neurochir(Wien),2010,152(3):393-404.
[2]NIKAIDO T,KIKUCHI S,YABUKI S,et al.Surgical treatment assessment using the Japanese orthopedic association cervical myelopathy evaluation questionnaire in patients with cervical myelopathy:a new outcome measure for cervical myelopathy[J].Spine(Phila Pa 1976),2009,34(23):2568 -2572.
[3]ODOM GL,FINNEY W,WOODHALL B.Cervical disk lesions[J].J Am Med Assoc,1958,166(1):23 -28.
[4]HILIBRAND AS,CARLSON GD,PALUMBO MA,et al.Radiculopathy and myelopathy at segments adjacent to the site of a previous anterior cervical arthrodesis[J].J Bone Joint Surg Am,1999,81(4):519-528.
[5]BABA H,FURUSAWA N,IMURA S,et al.Late radiographic findings after anterior cervical fusion for spondylotic myeloradiculopathy[J].Spine(Phila Pa 1976),1993,18(15):2167 -2173.
[6]BRYAN VE JR.Cervical motion segment replacement[J].Eur Spine J,2002,11(Suppl 2):S92 -97.
[7]WIGFIELD CC,SKRZYPIEC D,JACKOWSKI A,et al.Internal stress distribution in cervical intervertebral discs:the influence of an artificial cervical joint and simulated anterior interbody fusion[J].J Spinal Disord Tech,2003,16(5):441 -449.
[8]SEKHON LH.Cervical arthroplasty in the management of spondylotic myelopathy[J].J Spinal Disord Tech,2003,16(4):307 -313.
[9]TIAN W,HAN X,LIU B,et al.Clinical and radiographic results of cervical artificial disc arthroplasty:over three years follow-up cohort study[J].Chin Med J(Engl),2010,123(21):2969 -2973.
[10]ZHANG X,ORDWAY NR,TAN R,et al.Correlation of ProDisc-C failure strength with cervical bone mineral content and endplate strength[J].J Spinal Disord Tech,2008,21(6):400 -405.
