吴茱萸粉末醋调敷小鼠皮肤体外透皮吸收研究*
2013-11-04欧水平曹森王森雷小娟袁涛江西中医学院南昌330004成都中医药大学成都60075
★ 欧水平 曹森 王森 雷小娟 袁涛 (.江西中医学院 南昌 330004;2.成都中医药大学 成都 60075)
吴茱萸粉末醋调敷小鼠皮肤体外透皮吸收研究*
★ 欧水平1,2曹森1王森1**雷小娟1袁涛1(1.江西中医学院 南昌 330004;2.成都中医药大学 成都 610075)
目的:考察吴茱萸粉末醋调敷小鼠皮肤的体外透皮吸收特性。方法:采用改良的Franz扩散池,以离体小鼠皮肤为透皮屏障,通过体外透皮吸收实验,用高效液相色谱法检测接收液和皮肤中吴茱萸碱、吴茱萸次碱和吴茱萸内酯的质量浓度,拟合渗透曲线方程,计算累积透过量、渗透速率、皮肤滞留量。结果:吴茱萸碱、吴茱萸次碱和吴茱萸内酯的透皮吸收速率分别为0.64、0.44、4.91μg/(cm2·小时),24小时累积透过量分别为15.05±2.40、10.69±1.04、114.16±6.83μg/cm2,24小时滞留量分别为0.77±0.42、1.66±0.81、4.97±0.69μg/cm2。结论:吴茱萸粉末醋调敷小鼠皮肤,吴茱萸碱、吴茱萸次碱和吴茱萸内酯均可透皮吸收,为吴茱萸醋调敷外治法的研究提供了实验依据。
吴茱萸;透皮吸收;吴茱萸碱;吴茱萸次碱;吴茱萸内酯
吴茱萸,粉末醋调外敷足心涌泉穴,取其滋阴降火、引热下行,发挥药物和穴位的双重作用,用于降压和改善高血压症状,疗效独特[1];研究表明,吴茱萸中的吴茱萸碱和吴茱萸次碱具有降血压的作用[2];据文献[3-5]报导及前期预实验表明,吴茱萸碱和吴茱萸次碱具有一定的经皮渗透性,本实验选取吴茱萸碱和吴茱萸次碱为指标成分,首次研究吴茱萸药材粉末醋调敷豚鼠体外透皮吸收特性,并建立透皮样品的高效液相色谱分析方法,为吴茱萸经皮给药制剂的研究提供参考。
1 仪器与试药
Agilent 1100型高效液相色谱仪(美国安捷伦科技有限公司)、色谱柱 Hypersil ODS2(5μm,4.6×250mm)(大连依利特,柱号:E2115011)、 TT-6B 透皮吸收试验仪(配套改良Franz扩散池,S=1.7663cm2,V=12mL,天津市正通科技有限公司)、BP21ID Sartorius电子天平(北京赛多利斯科学仪器有限公司)、KQ3200E型超声波清洗器(昆山市超声仪器有限公司)。
吴茱萸碱对照品(批号:11802-200606)、吴茱萸次碱对照品(批号:11801-201006)均购于中国药品生物制品检定所。吴茱萸药材(樟树天齐堂中药饮片有限公司,批号:1105004)。乙腈、甲醇为色谱纯,双蒸水自制,其余试剂为分析纯。山西陈醋为市售品(山西陈世家酿业有限责任公司 批号:2011/03/13)。
实验动物:小白鼠,雄性4只,体重18-20g,江西中医学院动物中心。
2 实验方法
2.1 吴茱萸药材前处理
将吴茱萸果实放入60℃烘箱中烘干至恒重,然后用药材粉碎机将其粉碎成粉末,过筛,置干燥器中备用。
2.2 离体鼠皮的制备
将小鼠腹部毛小心剪去,处死后剪下腹部皮肤,小心剥离脂肪及粘液组织,选取完整皮肤,用生理盐水反复冲洗干净,冰箱贮存,1周内备用。
2.3 对照品溶液的配制
各取吴茱萸碱、吴茱萸次碱、吴茱萸内酯对照品约,精密称定,分别加甲醇至mL定容,即得吴茱萸碱、吴茱萸次碱、吴茱萸内酯对照品溶液母液,浓度分别为83.3、110.3、483.6μg/mL。
2.4 色谱条件
采用乙腈-水梯度洗脱,见表1,流速1.0mL/分、柱温25℃、检测波长225nm。
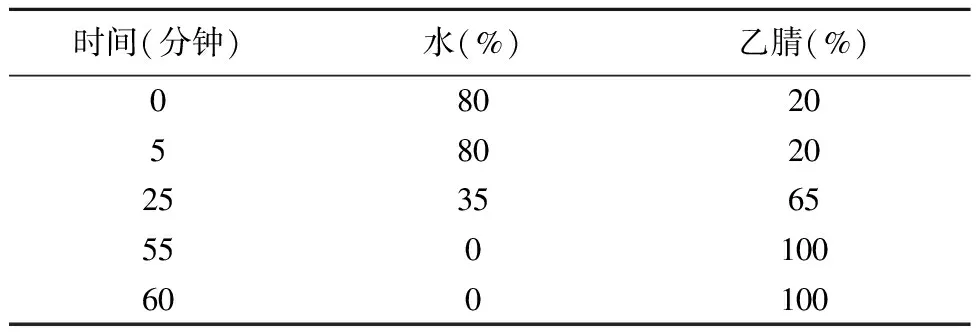
表1 梯度洗脱条件
2.5 吴茱萸药材含量测定
取吴茱萸药材粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入80%乙醇25mL,称定重量,浸泡1小时,超声处理(功率100W,频率40kHz)40分钟,放冷,再称定重量,用80%乙醇补足减失的重量,摇匀,滤过,取续滤液,得供试品溶液[6],按4项下条件精密量取20μL进样测定吴茱萸碱、吴茱萸次碱、吴茱萸内酯含量。
2.6 小鼠体外透皮吸收试验
采用改良Franz扩散池,接收液为PEG400-95%乙醇-水(1∶3∶6)[4]。称取1g 吴茱萸粉末(过120目筛),用食醋3mL调成糊状。将处理好的小鼠腹部皮肤3份,皮肤真皮面向接收池固定于扩散装置的扩散室和接收室之间,在接收室中注满接收液,排尽气泡。磁力搅拌器转速设定为350r/分,水浴温度37℃±0.25℃,扩散池容积12mL,有效扩散面积为1.7663cm2。平衡半小时后,将上述吴茱萸糊紧密贴于皮肤表面,于1、2、4、8、12、24小时取样,同时补充等量新鲜接受液取样时将接收室中的液体全部倒出,经微孔滤膜滤过,即得透皮吸收液样品。平行a、b、c三组空白皮肤样品1份,同法操作。透皮实验结束后,取下皮肤,用新鲜接收液清洗表面残留物,滤纸吸干,剪碎后加入5mL甲醇超声提取2次,每次30分钟,取上清液用微孔滤膜滤过,得皮肤样品。空白皮肤样品1份同法操作。所得样品按2.4项下条件精密量取20μL进样测定吴茱萸碱、吴茱萸次碱、吴茱萸内酯含量。
3 实验结果
3.1 药材有效成分含量
吴茱萸药材中3种主成分吴茱萸碱、吴茱萸次碱、吴茱萸内酯的质量百分数分别为0.779%、0.553%、1.300%,符合药典规定。
3.2 体外经皮渗透性
药物的累积透皮量Qn可由式1计算[7]:
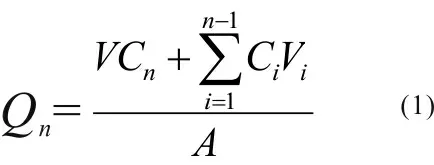
其中,A为有效扩散面积,V为接受液总体积,Cn为第n次取样时接受液中药物的质量浓度,Ci为第i次取样时接受液中药物的质量浓度,Vi为取样体积。以药物的累积透过量Qn(μg/cm2)对取样时间t作曲线(见图1),并由公式(2)对曲线中的直线部分进行线性回归,求出的直线斜率即为稳态透皮速率Js (μg/(cm2·小时)),直线与x轴的交点为时滞tlag (小时)。

药物的皮肤滞留量QS (μg/cm2)可由式3计算:
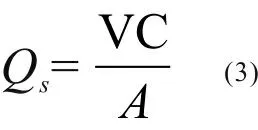
其中,A为有效扩散面积,V为皮肤提取液总体积,C为皮肤提取液中药物的浓度。
吴茱萸醋调敷小鼠透皮成分经皮渗透性结果如下:
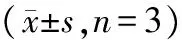
表2 体外透皮吸收结果
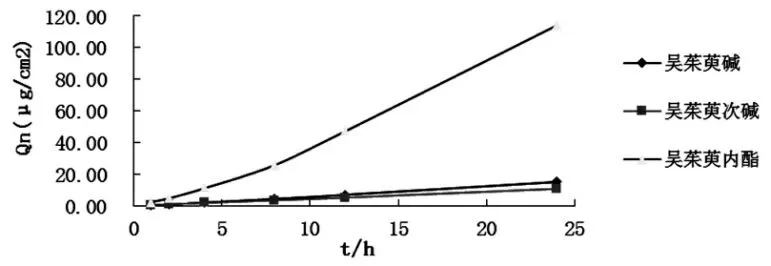
图1 吴茱萸粉末醋调敷小鼠皮肤有效成分渗透曲线
4 小结与讨论
由实验结果可知,指标成分吴茱萸碱、吴茱萸次碱和吴茱萸内酯透皮过程的线性规律明显,透皮速率恒定,符合零级模型,满足制成透皮制剂的前提条件。而本实验中吴茱萸碱和吴茱萸次碱的透皮吸收速率较小[8],而且24小时累积透过量分别占药材含量的1.4%和1.1%,说明皮肤屏障限制了药物的透皮吸收,提示采用各种方法或手段促进有效成分的透皮吸收是提高吴茱萸透皮制剂血药浓度的关键。
结合文献报导[9]及透皮样品在紫外-可见分光亮度计在200-400nm范围内扫描,发现在225nm处有较大的紫外吸收,并且对目标成分的选择性更好,所以本实验选择225nm做为检测波长。并且本实验也优化了流动相比例,使其洗脱能力更强,吴茱萸碱和吴茱萸次碱都能获得基线分离。
实验过程中发现,透皮样品中吴茱萸生物碱成分性质不稳定,对光和热敏感,试验过程中易被破坏,导致含量测定时不易被检出,不能长期保存,与文献[10]报导一致,样品应放在阴凉避光处保存,并在短期内完成检测。应进一步研究生物碱成分不稳定的原因,以科学地指导实验。
[1]冯松杰,陶兴,韦政瑛.吴萸粉外敷涌泉穴治疗肾性高血压44例[J].中医外治杂志,2001,10(1):44.
[2]严春临,张季,薛贵平.中药吴茱萸药理作用研究概况[J].河北北方学院学报,2009,26(1):77-79.
[3]彭丽华,刘淑芝,郭春燕,等.两种巴布剂基质的体外经皮渗透性考察[J].中国实验方剂学杂志,2005,11(5): 1-3.
[4]杜茂波,刘淑芝,李曼玲,等.萸连巴布剂体外释放和透皮行为的研究[J].中国中药杂志,2009,34(8): 969-972.
[5]王冬梅, 李静, 徐月红,等. 宝泻灵提取物的体外透皮吸收研究[J].中草药,2007,38(10):1 487-1 490.
[6]国家药典委员会.中华人民共和国药典﹒一部[S].北京:中国医药科技出版社,2010:160.
[7]郑俊民.经皮给药新剂型[M].北京:人民卫生出版社,2006.
[8]彭丽华.降压巴布剂的透皮吸收与促渗剂筛选研究[D].北京:中国中医研究院中药研究所,2005.
[9]袁金斌,罗习珍,肖锡林,等.HPLC法测定吴茱萸中吴茱萸碱和吴茱萸次碱的含量[J].现代生物医学进展,2008,12(8):2 536-2 537.
[10]甄攀,杨风珍.吴茱萸总生物碱提取条件的考察[J].中国中药杂志,2000, 25( 8) : 504-505.
江西省科技支撑计划项目(项目编号:2010JX00095);南昌市科技支撑计划项目(项目编号:2010-KJZCJH-YYYYLQX-108);江西省研究生创新专项资金项目(项目编号:YC2011-S111)。
**通讯作者:王森,Tel:0791-87118614,E-mail:wangsen912912@126.com。
R 285.5
A
2013-05-17)
