基于离子液体的单滴微萃取-毛细管电泳在线联用测定水体中3种溴酚类化合物
2013-10-22张文慧姜廷福吕志华王远红
张文慧, 姜廷福, 吕志华, 王远红
(中国海洋大学医药学院,山东青岛 266003)
溴酚是一类广泛分布于多种环境介质中的有机污染物,具有持久性和生物累积性,对生态环境和人体健康构成严重威胁[1]。同时,由于溴酚类化合物具有非常低的味觉阀值,在水中或食品中即使以很低浓度存在时,也会产生令人非常反感的气味[2-4]。因此,建立用于检测这类化合物的分析方法显得尤为重要。
目前,测定水体或食品中的溴酚多采用液液萃取和固相萃取对其中的溴酚进行浓缩萃取。da Silva等[5]建立了戊烷-乙醚混合溶剂萃取-高效液相色谱测定海鱼中5种溴酚的方法;Heitz等[6]将溴酚化合物乙酰化,吹扫富集浓缩后利用气相色谱-质谱联用法测定了水中的5种溴酚;Chen等[7]建立了石墨烯固相微萃取-气相色谱联用测定水样中4-溴酚的方法;徐继林等[8]采用乙酸乙酯循环蒸馏的方法对溴酚进行浓缩提取,建立了气相色谱-质谱联用法测定海产品中溴酚类化合物的方法。
毛细管电泳(CE)是上世纪80年代后期发展起来的一种分离分析技术,是分离科学中研究最为活跃的领域之一。但由于CE进样体积小和检测光程短,采用通用的紫外检测时灵敏度较低,从而限制了其在分离分析领域中的应用,所以提高CE检测的灵敏度是一个人们密切关注的前沿课题。
单滴微萃取(SDME)[9]是近年来发展起来的一种萃取装置简单、成本低、溶剂用量少、操作简便快速的一种样品前处理技术。在以往的单滴微萃取技术研究中,通常是将单液滴悬挂在微量进样器针尖,萃取完成后抽回微量萃取器,然后将此液滴直接注射到HPLC或GC中进行分析,整个过程为手动操作,因此不可避免地存在准确性低、重现性差以及操作不便等缺点[10]。同时,SDME的萃取溶剂多为有机溶剂,存在萃取液滴体积小、易挥发、不易高温萃取、萃取维持时间短等缺点。2004年,Choi研究小组[11]首次报道了SDME与CE在线联用的方法。至此,SDME-CE在线联用引起了研究者的关注,并被应用于不同基质中酚类化合物、腺嘌呤、肽的富集与分离[12-14]。离子液体(IL)是一种新型绿色溶剂,具有非挥发性、热稳定性强、黏度和密度大等特点,用作SDME-CE联用的萃取剂避免了传统有机溶剂的缺点[15,16]。因此,本研究利用基于离子液体的单滴微萃取技术-毛细管电泳法(IL-SDME-CE)测定水体中3种溴酚,旨在改进和完善常规CE方法在检测溴酚类化合物方面存在的不足。实验结果显示,本方法简单快速,环境友好,对实际水样的测定结果令人满意。
1 实验部分
1.1 试剂与仪器
4-溴酚(4-BP)、2,6-二溴酚(2,6-BP)、2,4,6-三溴酚(2,4,6-BP)标准品,分析纯,美国 Sigma公司;1-丁基-3-甲基咪唑六氟磷酸盐([C4MIM][PF6])、1-己基-3-甲基咪唑六氟磷酸盐([C6MIM][PF6])、1-辛基-3-甲基咪唑六氟磷酸盐([C8MIM][PF6])和1-丁基-2,3-二甲基咪唑六氟磷酸盐([DC4MIM][PF6]),纯度均为 99%,上海成捷化学有限公司;甲醇、氯化钠、硼砂、氢氧化钠为国产分析纯。
HP3DCE系统,美国Agilent公司;熔融石英毛细管柱,内径50 μm,总长度60 cm,有效长度为51.8 cm,邯郸鑫诺光纤色谱公司;数字酸度计,杭州万达仪器仪表厂;Al104型电子天平,梅特勒-托利多仪器上海有限公司;超声波清洗器,昆山市超声仪器厂。
1.2 实验方法
毛细管电泳离子液体单滴微萃取过程如图1所示。首先,将毛细管柱用含60%(v/v)甲醇的10 mmol/L硼酸盐缓冲液(pH 10.0)冲洗2 min。a.在毛细管入口处用94.5 kPa压力加压3 s,将少量离子液体压入毛细管入口端。b.在毛细管出口处用5 kPa压力加压90 s,使毛细管入口处能够形成离子液体单滴,从而使液滴与样品溶液直接接触并开始进行萃取。c.维持此状态8 min,样品溶液中的分析物会逐渐扩散进入离子液体单滴中。萃取过程中,离子液体单滴由于表面张力会逐渐变小,为了抵消液滴的表面张力,必须在每萃取120 s后,从出口到入口方向以0.6 kPa压力加压60 s。d.萃取完成后,用3 kPa压力在毛细管入口端加压5 s。最后,在30 kV电压下,用20 mmol/L含10%(v/v)甲醇的硼酸盐缓冲液(pH 10.0)运行分离过程。

图1 离子液体单滴微萃取-毛细管电泳联用示意图Fig.1 Scheme of the IL-SDME-CE
1.3 毛细管电泳条件
运行缓冲液为20 mmol/L含10%(v/v)甲醇的硼酸盐缓冲液(pH 10.0);温度20℃;运行电压为30 kV;检测波长为 245 nm。每次进样前用含66.7%(v/v)甲醇的硼酸盐缓冲液(pH 10.0)冲洗2 min。
2 结果与讨论
2.1 离子液体单滴微萃取条件的优化
2.1.1 萃取剂种类的影响
选用的离子液体种类对萃取效率有很大影响。本研究中分别以[C4MIM][PF6]、[C6MIM]-[PF6]、[C8MIM][PF6]和[DC4MIM][PF6]4种离子液体作为萃取溶剂,对比它们在相同条件下的萃取效果,结果如图2所示。

图2 离子液体种类对3种酚类化合物萃取效率的影响Fig.2 Effect of the type of ionic liquids on peak areas of the three bromophenols
从图2中可以看出[C4MIM][PF6]的萃取效率最好。这可能是因为[C4MIM][PF6]的黏度较另外3种离子液体低得多,使[C4MIM][PF6]具有较高的溶质扩散系数。图2显示,对于4-BP而言,不同离子液体对其萃取效率的影响并不明显;而2,6-BP和2,4,6-BP受离子液体种类的影响较大。这可能是由于2位和4位溴的空间位阻影响了BP和离子液体间的氢键作用所致。此外,其他3种离子液体在缓冲溶液中溶解很慢,以致被离子液体萃取的分析物不能充分从液滴中释放出来,这就需要提高缓冲溶液中有机溶剂含量以溶解比[C4MIM][PF6]黏度高的3种离子液体,这同时也会阻碍后续的分离过程。因此,在后续研究中,选定[C4MIM][PF6]作为萃取溶剂。
2.1.2 有机溶剂的影响
研究表明,当SDME与CE在线联用时,缓冲溶液应当能够富集分析物并适用于CE分析。基于此,我们不仅应考虑选择适于CE分离的缓冲液,也需要考虑缓冲液中离子液体的溶解度。如果离子液体不能在短时间内溶解,就会严重影响分离过程和萃取效率。我们考察了润洗缓冲液中甲醇含量在30%~70%范围内变化时对萃取效果的影响。结果表明:在30%~60%范围内,随着甲醇含量的增加,3种酚类化合物的峰面积均呈明显增加趋势,进一步增加甲醇含量,峰值无明显增加。这可能是因为增加甲醇含量,离子液体在缓冲溶液中的溶解度增大,分析物可以从离子液体中更充分地释放出来。但若进一步增加甲醇含量,离子液体会因被甲醇溶解而使单液滴变小,这将会对离子液体单滴的萃取效率产生相反的作用。另外,由于加入大量的甲醇,电渗流将会减小,导致分析时间延长甚至电流中断。综合考虑萃取效率和分析时间,并使离子液体迅速溶解,我们选择使用甲醇含量为60%(v/v)、pH为10的10 mmol/L硼砂缓冲溶液在注入离子液体前冲洗毛细管柱。
2.1.3 单液滴体积的影响
在IL-SDME-CE过程中,离子液体单滴的体积会显著影响萃取效率。对于离子液体单液滴体积的优化,本研究考察了5 kPa压力下加压时间50~150 s范围内不同离子液体液滴体积的影响。结果表明:在50~90 s范围内,3种溴酚的液滴体积越大,峰面积越高。这可能是因为离子液体单滴体积越大,液滴中分析物的量越大,故峰面积越高。然而,离子液体单滴体积越大,越难于操作,且液滴较大时容易脱落。综合考虑3种酚类化合物的萃取效率和操作可行性,后续的实验选择离子液体单滴的注射时间为90 s。
2.1.4 萃取时间的影响
对IL-SDME-CE萃取过程而言,萃取时间对萃取效率的影响至关重要。本研究考察了2~14 min范围内萃取时间对萃取效率的影响。结果表明:萃取时间在2~8 min范围内,3种酚类化合物的萃取效率随离子液体液滴在样品溶液中暴露时间的增加而显著增加,在萃取时间为8 min时峰面积较高;进一步延长萃取时间,峰面积并无明显升高,甚至下降。这一现象可以用两个同时发生的过程来解释:分析物在离子液体单滴中的扩散过程和离子液体在样品溶液中的溶解过程。在2~8 min范围内,随着萃取时间增加,分析物逐渐扩散进入离子液体相,因此峰面积显著增加。若进一步延长萃取时间,离子液体液滴将会部分溶解,液滴中的分析物的量将会随之减少,萃取效率也会因此降低。因此,萃取时间为8 min时峰面积较高是两个同时发生的过程共同作用的结果。同时,离子液体液滴在样品溶液中的暴露时间过长不利于液滴稳定。因此,后续研究中我们选择萃取时间为8 min以得到对3种目标分析物较好的萃取效率。
2.1.5 萃取温度的影响
由于温度对单滴微萃取的热力学和动力学过程均有影响,因此萃取温度是影响萃取效率的一个主要因素。考察了15~35℃范围内萃取温度对目标分析物富集效果的影响,结果见图3。结果表明:在15~20℃范围内,萃取效率随温度升高而增加,这是因为萃取是一个动力学过程,当温度升高时,分子扩散活动更加剧烈,使得分析物进入离子液体单滴的扩散速度增大。但是,进一步升温,峰面积反而明显下降,这是因为分析物在离子液体微滴中的吸收是一个放热过程,分析物在离子液体单滴和样品溶液间的分配系数随着萃取温度的升高而下降。因此,对于特定的待测样品,会有一个最佳萃取温度。实验结果表明,本实验中最佳萃取温度为20℃。
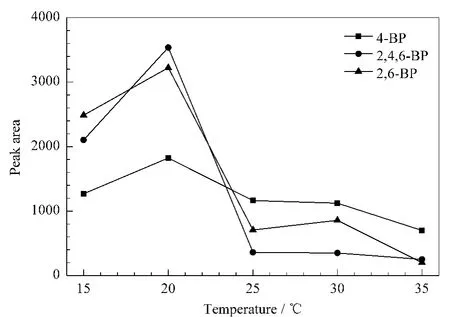
图3 温度对3种酚类化合物萃取效率的影响Fig.3 Effect of the temperature on peak areas of the three bromophenols
2.1.6 样品溶液离子强度的影响
以NaCl为例,研究了水样中盐的含量对萃取效率的影响。结果表明:在所考察的NaCl含量范围(0~50%,质量分数)内,随着NaCl含量的增加,溴酚峰面积先增大后减小,在NaCl含量为10%时,萃取效率最佳。这是由于随着NaCl含量的增加,盐析效应有利于萃取,所以萃取效率增加。而当NaCl含量进一步增加时,样品溶液的黏度有所增加,妨碍了待萃取物进入离子液体液滴,因此萃取率降低。所以,在后续实验中我们选择含10%NaCl的水溶液为样品溶液。
2.1.7 样品溶液pH的影响
弱酸或弱碱的萃取效率取决于pH值。样品溶液的pH值能够影响酚类的存在形式,进而影响其在水中的溶解度和被离子液体单滴萃取的效果。因此,萃取前常把样品溶液调至合适的酸碱度,使酚类化合物去离子化,以分子形式存在,从而减少其在样品溶液中的溶解度,增加萃取效率。本实验考察了pH 2.0~10.0范围内pH值对萃取效率的影响。结果表明:pH越小,3种溴酚的萃取效率越高,pH减小至2.0时,萃取效率显著增加。这是因为此pH条件下,4-溴酚、2,6-二溴酚和 2,4,6-三溴酚均以非离子型的酚为主要存在形式。同时,当样品溶液为酸性时,离子液体的PF-6更倾向于与H+作用,从而减小了PF-6和分析物对咪唑阳离子的竞争作用。综合考虑3种酚类化合物的萃取效率,后续的研究选择pH值为2.0的样品溶液。
图4是在上述优化萃取条件下,IL-SDME-CE与不经富集常规CE进样分析方法比较的电泳图。

图4 (a)IL-SDME-CE与(b)常规CE测定混合标准溶液的电泳谱图Fig.4 Typical electropherograms of standard mixture by(a)IL-SDME-CE and(b)normal CE
2.2 IL-SDME-CE的方法学评价
2.2.1 富集率
从表1可看出,在优化的萃取分离条件下,应用IL-SDME-CE 萃取分离 4-溴酚、2,6-二溴酚和 2,4,6-三溴酚,所得的富集因子(EFs)(即萃取后与萃取前响应值之比)以峰面积比表示分别为115.8、569.8和327.0。显然,与不经富集直接进样的CE分析方法相比,IL-SDME-CE的富集效果显著。

表1 IL-SDME-CE对溴酚的富集因子Table 1 Enrichment factors(EFs)of bromophenols by IL-SDME-CE
2.2.2 方法的线性范围、检出限及精密度
采用将标准溶液逐级稀释的方法,配制成一系列浓度的标准工作液,在上述优化条件下进行萃取分离,以峰面积y对质量浓度x(mg/L)绘制标准曲线,4-溴酚、2,6-二溴酚和 2,4,6-三溴酚在 1 ~ 100 mg/L范围内的线性方程及相关系数如下:4-溴酚,y=19.44x+7.4237(r=0.9939);2,4,6-三溴酚,y=36.57x -124.55(r=0.9970);2,6-二溴酚,y=18.63x+51.601(r=0.9988)。信噪比(S/N)为3时,4-溴酚、2,6-二溴酚和 2,4,6-三溴酚的检出限(LODs)为0.3 mg/L。与文献报道的GC、GC-MS结果[7,8]相比,本方法在灵敏度方面并没有优势;但与我们通过常规CE测定溴酚类化合物相比,从富集因子可以看出本方法的灵敏度有所提高。取4-溴酚、2,6-二溴酚和 2,4,6-三溴酚的混合标准溶液(25 mg/L),在最佳条件下连续进样6次,以相对标准偏差(RSD)表示重现性,3种溴酚峰面积的日内RSD分别为6.47%、5.46%和5.21%,由此可知重现性良好。
2.3 样品分析及加样回收率
对本地区的自来水、河水及湖水用0.45 μm的滤膜过滤后,在最佳实验条件下进行测定,3个水样中的溴酚浓度均低于本方法的检出限,这可能与丰水期取样及水样的周边未被溴酚污染有关。在高、中、低3个加标水平(2、50和100 mg/L)下测定3种溴酚在3个水样中的回收率,3种溴酚在3个水样中的回收率在87.8%~96.7%之间。
3 结论
本文以绿色环保的离子液体为萃取溶剂,建立了单滴微萃取-毛细管电泳在线联用富集分离3种溴酚的方法,并用该方法对本地区的自来水、河水及湖水中的3种溴酚进行了测定。结果表明本方法稳定有效,为水体中溴酚的测定提供了一种切实可行的方法。
[1]Sim W J,Lee S H,Lee I S,et al.Chemosphere,2009,77(4):552
[2]Chung H Y,Ma W C J,Kim J S.J Agric Food Chem,2003,51:6752
[3]Adams J B,Lock S J,Toward M R,et al.Food Chem,1999,64(3):377
[4]Whitfield F B,Drew M,Helidoniotis F,et al.J Agric Food Chem,1999,47:4756
[5]da Silva V M,da Cunha Veloso M,de Oliveira A S,et al.Talanta,2005,68:323
[6]Blythe J W,Heitz A,Joll C A,et al.J Chromatogr A,2006,1102:73
[7]Zou J,Song X H,Ji J,et al.J Sep Sci,2011,34:2765
[8]Xu J L,Yan X J,Xu N J,et al.Journal of Fisheries of China(徐继林,严小军,徐年军,等.水产学报),2004,28(1):100
[9]Liu H,Dasgupta P K.Anal Chem,1996,68(11):1817
[10]Jain A,Verma K K.Anal Chim Acta,2011,706:37
[11]Choi K,Kim Y,Chung D S.Anal Chem,2004,76:855
[12]Xie H Y,He Y Z,Gan W E,et al.J Chromatogr A,2010,1217:1203
[13]Zhu Z F,Zhou X M,Yan N,et al.J Chromatogr A,2010,1217:1856
[14]Park Y K,Choi K,Ahmed A Y B H,et al.J Chromatogr A,2010,1217:3357
[15]Wang Q,Qiu H D,Li J,et al.J Sep Sci,2011,34:594
[16]Wang Q,Qiu H D,Li J,et al.J Chromatogr A,2010,1217:5434
