生物乙醇重整制氢催化剂载体研究进展
2013-10-22李键铭杨文申阴秀丽吴创之
李键铭,郎 林,杨文申,阴秀丽,吴创之
(1.中国科学院 广州能源研究所 中国科学院可再生能源与天然气水合物重点实验室,广东 广州510640;2.中国科学院 研究生院,北京100049)
氢能及燃料电池技术作为先进能源技术领域的重要方向,是当今国际可再生能源产业与低碳经济的研究热点[1-11]。利用醇类液体燃料原位重整制氢供燃料电池发电被认为是近、中期较为现实的燃料电池氢源解决方案之一[2-3,5]。与甲醇等燃料相比,生物乙醇重整制氢以可再生物料为原料,不存在对化石能源的依赖,且具有单位能量高、氢含量高、无毒、易储运等优点,已成为当前低碳能源应用基础研究领域中的热点问题[1-3,5,12]。
生物乙醇重整制氢的效果很大程度上取决于重整制氢催化剂的反应活性。对此已有一些相关的研究报道[13-20],主要集中在对活性组分的筛分与选取,以及对各种活性金属的优劣比较[12,15],一般认为非贵金属中Ni、Cu和Co的效果较好,而贵金属中Rh的效果较好。目前,生物乙醇重整制氢中所使用的催化剂大多为负载型催化剂,载体对重整催化剂的反应活性和寿命均有重要影响。近年来,分子筛等新型载体的引入,加速了生物乙醇重整制氢的发展,显著提高了重整催化剂在低温下的转化率、选择性和稳定性[21-22]。在相同的活性金属和反应条件下,不同载体对催化剂的活性和氢气选择性有较大影响,且存在一定规律性和内在联系。因此,如能对乙醇重整制氢的催化剂载体进行有效的分类与总结,则有望进一步拓宽对生物乙醇重整制氢催化剂的研究范围。但令人遗憾的是,目前尚未见到关于乙醇重整制氢催化剂载体的综述性文献报道。笔者从催化剂载体的角度出发,系统地介绍和分析了目前生物乙醇重整制氢催化剂载体的种类、结构特征、化学特性和催化性能优劣,进而指出了今后生物乙醇重整制氢催化剂载体的发展方向。
1 γ-Al2O3载体
γ-Al2O3的力学性能好,比表面积较大,且价格低廉,是一种常见的催化剂载体,在生物乙醇重整制氢中研究也较多[23-29]。但其积炭问题较为严重,原因可能是γ-Al2O3表面上不完全配位的铝原子产生的L酸位促进了乙醇脱水生成乙烯,乙烯再通过聚合反应形成积炭。积炭不仅会缩短催化剂的寿命,同时也降低了氢气选择性。Vizcaino等[24]研究了 Ni-Cu/γ-Al2O3和 Ni-Cu/SBA-15催化剂对生物乙醇水蒸气重整制氢的催化性能,在反应温度600℃、水与醇摩尔比3.7的条件下,反应进行3h后,Ni-Cu/SBA-15催化剂的积炭率(质量分数,下同)为19.2%,氢气选择性为79.0%,而 Ni-Cu/γ-Al2O3催化剂的积炭率达到59.5%,氢气选择性仅为50.1%。Cavallaro等[29]在研究 Rh/γ-Al2O3催化剂对生物乙醇重整制氢的催化性能时发现,只有在反应温度较高且Rh负载量较大的条件下才能较好地抑制积炭。可见,在相同条件下进行生物乙醇重整制氢时,与其他载体相比,以γ-Al2O3为载体的催化剂普遍存在较为严重的积炭现象。
为较好地解决γ-Al2O3的积炭问题,应尽量克服其酸性位,主要有采用Ca(NO3)2[25]、KOH[26]、Mg(NO3)2[27]和 Zn(NO3)2[28]等对γ-Al2O3进行改性。Marino等[26]采用KOH溶液对γ-Al2O3进行改性,制备了Ni-Cu/K-γ-Al2O3催化剂,在反应温度300℃的条件下取得了较好的重整结果。Zhang等[28]制 备 了 Ni-Cu/γ-Al2O3(NiCu/A)、 Ni-Cu/γ-Al2O3-MgO(NiCu/A-Mg)和 Ni-Cu/γ-Al2O3-ZnO(NiCu/A-Zn)3种催化剂,考察了γ-Al2O3改性对乙醇重整制氢催化剂的影响,结果表明,在400℃、水与醇摩尔比为4的条件下,NiCu/A-Mg和NiCu/A-Zn的氢气选择性分别为68.0%和64.0%,而NiCu/A 仅为 54.0%,NiCu/A-Mg和 NiCu/A-Zn的积炭量分别为0.5g/gcat和0.2g/gcat,而 NiCu/A的积炭量达到2.2g/gcat。由 NH3-TPD 表征 (见图1)可知,NiCu/A-Mg和NiCu/A-Zn的酸量均低于NiCu/A,酸强度也有所降低。虽然经过碱性修饰后,γ-Al2O3的积炭问题可得到有效解决,但也提高了其成本,其价格低廉的优势变得不明显。

图1 30Ni5Cu/γ-Al2O3,30Ni5Cu/γ-Al2O3-MgO和30Ni5Cu/γ-Al2O3-ZnO催化剂的 NH3-TPD曲线[28]Fig.1 NH3-TPD profile of 30Ni5Cu/γ-Al2O3,30Ni5Cu/γ-Al2O3-MgO and 30Ni5Cu/γ-Al2O3-ZnO catalysts
2 稀土氧化物载体
稀土氧化物的碱性较强,可有效地抑制积炭,更为重要的是稀土氧化物具有快速氧交换能力。反应时稀土氧化物所释放的晶格氧有助于促进CO氧化、水煤气变换和CH4水蒸气重整等反应的进行,不仅减少了积炭,还有助于提高氢气选择性[30-37]。在生物乙醇重整制氢的过程中,以稀土氧化物为载体的催化剂表现出了高选择性和高稳定性。
Zhang 等[36]研究了Ni/CeO2,Co/CeO2和Ir/CeO23种催化剂在300~700℃下对生物乙醇水蒸气重整制氢的催化性能,结果表明,Ir/CeO2催化剂表现出了良好的稳定性,当反应温度为650℃时,反应300h后催化剂没有失活。原因可能是Ir和CeO2之间的强相互作用减缓了Ir的烧结,且CeO2的快速氧交换能力有效地抑制了积炭。Zhang等[37]随后系统地研究了Ir/CeO2催化剂对生物乙醇水蒸气重整制氢的催化性能;当反应温度为450℃、水与醇摩尔比为3.2时,产物中H2的摩尔分数为67%,CO2的摩尔分数为17%。Song等[30]研究了氧交换能力对Co/CeO2催化生物乙醇水蒸气重整制氢的影响,Co/CeO2催化剂的氢产率随温度的上升而上升,这与催化剂氧交换能力随温度的变化趋势相一致。因此氢产率提高的主要原因可能是氧交换能力的提高。Sun等[38]研究了Ni/Y2O3催化剂对乙醇部分氧化重整制氢的催化性能。实验中他们制备了不同粒度(9nm、19nm、25nm、38nm)的纳米Y2O3载体,并研究了Y2O3的粒度对催化剂性能的影响,结果表明,Y2O3粒度的减小有助于Y2O3氧交换能力的提高,进而提高了氢气选择性。
虽然对Y2O3、La2O3和CeO2等稀土氧化物作为载体用于生物乙醇重整制氢均有所研究[31,38-48],但由于CeO2的价格相对便宜,工业化应用前景较好,因而研究得较为深入。为进一步提高CeO2的氧交换能力,可在CeO2中掺杂ZrO2。由于Zr4+的离子 半 径 (0.084nm)小 于 Ce4+的离子半径(0.097nm),因此在CeO2的晶格内掺杂一定量的Zr4+可以减小氧化物的晶格常数,形成更多的结构缺陷,进而提高其氧交换能力[46,49-51]。Diagne等[49]在研究Zr含量对Rh/CexZr1-xO2催化生物乙醇水蒸气重整制氢的影响时发现,当Ce与Zr摩尔比为1时,氢气选择性较高,且产物中CO的含量较低。
Breen等[52]比较了 M/γ-Al2O3(M=Rh,Pt,Pd,Ni)和M/CeO2-ZrO2催化剂的生物乙醇重整制氢效果。在相同反应条件下,M/CeO2-ZrO2催化剂的氢气选择性高于M/γ-Al2O3催化剂的,主要原因是M/CeO2-ZrO2催化剂几乎没有产生C2H4,而M/γ-Al2O3催化剂则产生了较多的C2H4。
综上所述,稀土氧化物由于具有较高的氧交换能力,以之为载体的催化剂在生物乙醇重整制氢中具有较高的氢气选择性和良好的稳定性。但由于这种氧交换能力随温度的上升而提高,因而制约了其在低温生物乙醇重整制氢中的应用。
3 分子筛载体
分子筛由于具有特殊的纳米孔道结构,其比表面积较大,且具有离子交换和择形催化等特殊性质,以之为载体可以促进活性组分的分散,提高活性金属的稳定性和催化活性,因此近年来关于分子筛载体用于乙醇重整制氢的研究报道逐渐增多[21-22,53-56]。其主要研究对象可分为以Y型分子筛和ZSM-5分子筛为主的微孔分子筛(孔径<2nm)及以SBA-15分子筛和ITQ-2分子筛为主的介孔分子筛(孔径为2~50nm)。
Vizcaino 等[24]选取了γ-Al2O3、SiO2、 纳 米ZSM-5、MCM-41和SBA-15等5种载体,研究了载体对生物乙醇水蒸气重整制氢的影响。在反应温度为600℃、水与醇摩尔比为3.7的条件下,Ni-Cu/SBA-15催化剂的氢气选择性较高。原因可能是SBA-15分子筛的比表面积较大(926.4m2/g),使得Ni在SBA-15载体上的分散度较高,提高了催化剂的催化活性和热稳定性。此后,Carrero等[55]比较了分别用浸渍法(WI)和直接合成法(DS)制备的Ni-Cu/SBA-15催化剂的性能,实验结果表明,DS法制备的催化剂的催化性能低于WI法制备的催化剂。原因可能是Ni-Cu/SBA-15(DS)中金属颗粒分布在载体的孔道内,堵住了分子筛的孔道(如图2(a)所示),而在 Ni-Cu/SBA-15(WI)中,金属颗粒主要分布在分子筛表面,未发生孔道堵塞现象(如图2(b)所示)。Vizcaino、Calles 和 Lindo等[54,56-57]进一步对Ni-Cu/SBA-15催化剂添加稀土金属、添加碱土金属以及改变分子筛的铝含量等进行了大量的实验研究,在提高氢气选择性和降低积炭等方面取得了一定效果。

图2 Ni-Cu/SBA-15(DS)和Ni-Cu/SBA-15(WI)催化剂的TEM照片[55]Fig.2 TEM micrographs of Ni-Cu/SBA-15(DS)and Ni-Cu/SBA-15(WI)catalysts[55]
Cantao等[21]制备了 Rh-K/NaY催化剂,并在生物乙醇低温重整制氢中取得了较好的结果。在反应温度为300℃、水与醇摩尔比为10和进料速率为2.77g/min的条件下,乙醇转化率接近100%,氢气选择性为68%。与以金属氧化物为载体的铑基催化剂的反应活性相比[14,52,58],在相似的反应条件和反应结果下,将反应温度从450~850℃降低到300℃,因此这是探索低温乙醇水蒸气重整制氢的有效尝试。但需注意的是该报道中贵金属的负载量(质量分数)较大(5%),若将贵金属负载量降低至较低水平(<1%),是否仍能保持较好的催化活性尚待进一步研究。另外,虽然NaY分子筛的酸性较弱,但改性后Rh-K/NaY催化剂的乙醇转化率从80%提高到97%,氢气选择性从63%提高到68%,表明应充分提高分子筛载体的碱性。
Kwak等[59]研究了 Ni-Ga-Mg/NaY催化剂对生物乙醇水蒸气重整制氢的催化性能,结果表明,添加Ga可提高氢气选择性和稳定性;在700℃、GHSV为6470h-1、水与醇摩尔比为3的条件下,乙醇转化率为100%,氢气选择性为87%,并保持了59h。原因主要是Ga可有效促进C—H键断裂,进而将烃类物质中的H释放出来,并且有助于减缓Ni的烧结。
Chica等[22]考察了 M/ITQ-2(M=Ni,Cu)和M/SiO2催化剂在300~600℃对乙醇水蒸气重整制氢的催化性能。为了降低分子筛载体的酸性,该实验采用纯硅ITQ-2分子筛。实验结果表明,M/ITQ-2催化剂的乙醇转化率相对较高,在低温下尤为明显;M/ITQ-2催化剂的氢气选择性也相对较高,其中Co/ITQ-2的氢气选择性较高,且CO选择性较低。在400℃下反应72h后,4种催化剂中都检测到积炭(质量分数3%~5%),但 M/ITQ-2催化剂没有失活,而M/SiO2催化剂出现明显失活,原因可能是活性金属发生了烧结。M/ITQ-2催化剂具有高活性、高选择性和高稳定性的原因可能在于所使用的ITQ-2分子筛的酸性较弱且具有较大的比表面积(>800m2/g)。
关于分子筛载体与γ-Al2O3、SiO2的比较,Vizcaino等[24]较早地从实验上给出了在生物乙醇水蒸气重整制氢中分子筛载体优于氧化物载体的数据,引起了广泛关注。而Cantao等[21]利用Rh-K/NaY催化剂在300℃下取得了较理想的结果,则在低温生物乙醇重整制氢中取得了进步。在对Y型催化剂的继续研究中,主要集中在Ni基和Co基催化剂,关于Rh基催化剂后续的系统研究鲜有报道;在对其他类型分子筛载体的研究中,也较少看到以贵金属为活性组分的报道。但是,Ni和Co在低温下活性不如贵金属催化剂,要真正发挥分子筛载体在低温生物乙醇制氢中的潜力,应加大对贵金属活性组分的研究,特别是应深入研究低贵金属含量的分子筛类重整催化剂。
4 载体物化特性的影响规律
目前用于重整制氢的原料较多,除了乙醇外,还包括甲醇和甲烷等多种化合物[10,60]。虽然此类重整制氢过程均与催化剂密切相关,但由于不同反应物重整制氢体系的催化反应机理差异较大,对催化剂活性组分和载体物化特性的要求也差异显著。如甲醇重整制氢过程不发生C—C断键,因而反应温度较低(200~300℃)[61],反应活性较高,以廉价的Cu为活性组分、ZnO[62-64]或者γ-Al2O3-ZnO[63,65-66]为载体即可取得较好的制氢效果。该过程对载体的物化特性要求相对较低,目前已有商业化的甲醇重整制氢催化剂[66]。然而,对于乙醇重整制氢反应,由于涉及到C—C键断裂,反应活性较低,在较低温度下可能发生的副反应较多,因此不仅对催化剂的催化活性要求较高,而且对催化剂载体的物化特性也提出了更高的要求。为此,笔者对乙醇重整制氢催化剂载体的物理化学性质进行了详细的归纳总结,着重探讨了载体的比表面积、酸碱性和自催化作用等主要影响因素。
载体的比表面积和孔结构影响着活性金属的分散程度,进而制约了活性金属的粒径。活性金属粒径的减小有助于提高催化剂的活性和稳定性[23,28],因此选取高比表面积的载体有利于改善重整制氢的效果。这一点在分子筛类催化剂中表现得较为明显[21-22,24],如表1列出了比表面积较大的ITQ分子筛比SiO2能更有效地减小活性金属的粒径[22];而对于比表面积相对较小的稀土氧化物,则有研究报道了提高稀土氧化物载体的比表面积对生物乙醇重整制 氢 的 影 响[67-69]。Laosiripojana等[69]以 十 六 烷基三甲基溴化铵为阳离子表面活性剂制备了具有较大比表面积的CeO2(HSA)载体,并与用沉淀法制备的CeO2(LSA)载体进行了生物乙醇重整制氢的实验对比。结果表明,在相同的反应条件下,以CeO2(HSA)为载体的催化剂的氢气选择性比CeO2(LSA)提高了约20%,且积炭率仅为后者的一半。
载体的酸碱性也会对生物乙醇重整制氢有影响。一般认为,酸性载体会促进积炭,但某些碱性载体自身也存在易烧结[70-72]和低温下氢气选择性不高[29]的问题,因此有学者对载体酸碱性对催化剂性能的影响进行了深入的研究。Furtado等[73]制备了Ni-Cu/α-Al2O3(NCA)、Ni-Cu/Ce0.6Zr0.4O2(NCCZ)、Ni-Cu/Nb2O5(NCN)和Ni-Cu/ZnO(NCZ)4种催化剂,研究了载体的酸碱性对生物乙醇重整制氢效果的影响。为了能较方便地研究催化剂的失活特性,所选用的空速较高(70000mL/(h·gcat)),所得乙醇转化率随反应时间的变化如图3所示。NCZ的乙醇转化率尽管在开始时达到了近100%,但失活速率较快,6h后已降至15%;其余3种催化剂也有不同程度的失活,其中NCCZ的失活程度较低,并最终稳定在43%。这4种催化剂的酸强度、总酸量、总碱量、强酸量和重整结果如表2所示。NCA和NCN由于含有一定量的强酸,重整产物含有乙烯;NCCZ虽然酸量较大,但均为弱酸,因而产物中没有乙烯,其氢气选择性也较高;而NCZ的总酸量较小,总碱量较大,产物中也没有乙烯,其失活速率却明显快于其余3种催化剂。酸碱性对催化剂失活的影响规律值得探究。Vizcaino等[24]发现,虽然γ-Al2O3和HZSM-5均具有酸性,但由于HZSM-5分子筛具有特殊的孔道结构可以抑制积炭,其积炭率低于γ-Al2O3,可见酸性载体对催化性能的影响可以通过载体自身的其他性质来弥补。
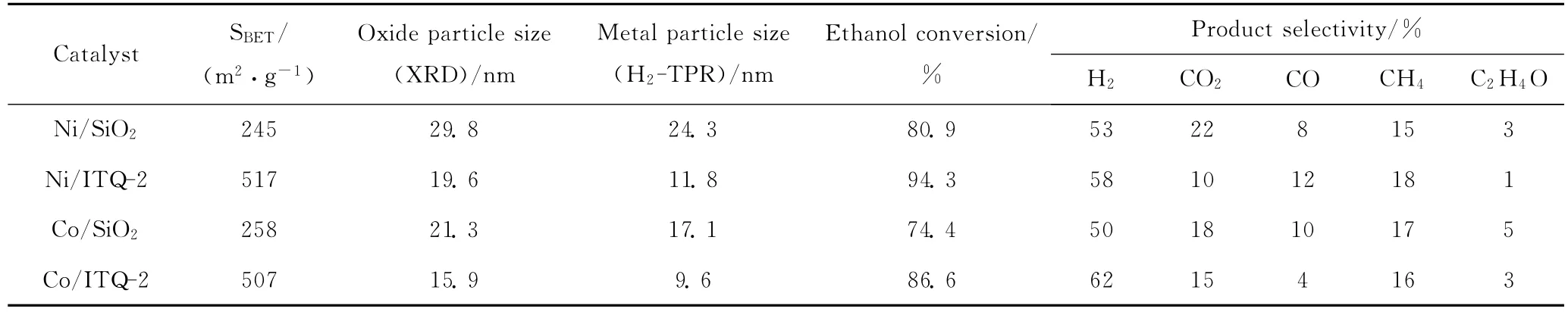
表1 Ni/ITQ-2、Co/ITQ-2催化剂的特性及催化性能[22]Table 1 The properties and performances of Ni/ITQ-2,Co/ITQ-2catalysts[22]
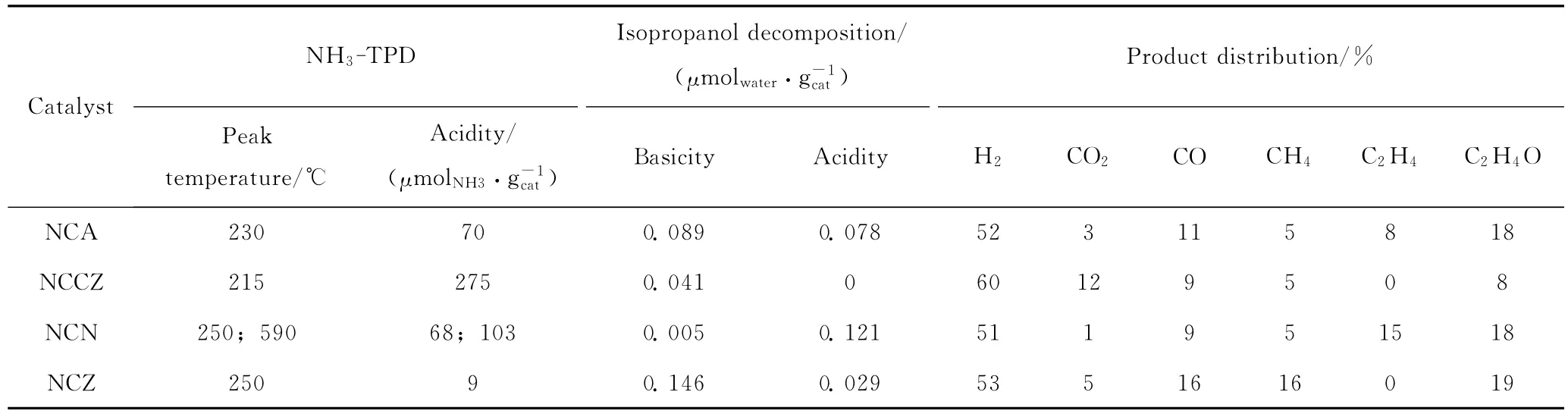
表2 NCA、NCCZ、NCN和NCZ催化剂的NH3-TPD、异丙醇分解表征和催化生物乙醇重整制氢反应结果[73]Table 2 NH3-TPD,isopropanol decomposition results and performances of NCA,NCCZ,NCN and NCZ catalysts for H2production from bio-ethanol reforming[73]
许多金属氧化物载体本身对生物乙醇重整制氢也有一定的活性,具有明显的自催化特性。Llorca等[74]研究了乙醇在一系列金属氧化物上的水蒸气重整制氢效果。在450℃、水与醇摩尔比4、空速5000h-1的反应条件下,V2O5和ZnO能有效催化乙醇水蒸气重整制氢,其中ZnO的乙醇转化率接近100%,氢气选择性达73%。Llorca等[75]随后对Co/ZnO催化剂用于生物乙醇水蒸气重整制氢进行了系统研究,在保持水/醇摩尔比和空速不变的条件下,将反应温度降至350℃后,乙醇转化率为100%,氢气选择性达73%,CH4选择性低于3%,且产物中没有CO,反应75h后仍然保持良好的活性和选择性。

图3 NCA、NCCZ、NCN和NCZ催化生物乙醇重整制氢的乙醇转化率随反应时间的变化[73]Fig.3 Ethanol conversion vs reaction time of H2production by bio-ethanol reforming over NCA,NCCZ,NCN and NCZ[73]
5 总结与展望
目前生物乙醇重整制氢领域中选用的载体主要为γ-Al2O3、CeO2-ZrO2和硅铝分子筛。γ-Al2O3经碱性修饰后效果较好,但成本有所上升,且反应温度普遍较高;稀土氧化物具有较强的碱性和快速氧交换能力,但其氧交换能力受温度的影响较大,制约了其在生物乙醇低温重整制氢中的应用;以分子筛为载体的催化剂在低温下具有较高反应活性和氢气选择性,但其制备工艺尚不成熟,使用成本也相对较高。为早日开发出廉价、高效的生物乙醇重整制氢催化剂,有必要进一步深入研究不同载体催化剂上生物乙醇重整制氢的催化反应机理,尤其是针对载体协同催化作用机理的系统性研究。
[1]DELUGA G A,SALGE J R,SCHMIDT L D,et al.Renewable hydrogen from ethanol by autothermal reforming[J].Science,2004,303(5660):993-997.
[2]FARGIONE J,HILL J,TILMAN D,et al.Land clearing and the biofuel carbon debt[J].Science,2008,319(5867):1235-1238.
[3]LAPOLA D M,SCHALDACH R,ALCAMO J,et al.Indirect land-use changes can overcome carbon savings from biofuels in Brazil[J].Proceedings of the National Academy of Sciences of the United States of America,2010,107(8):3388-3393.
[4]RICHTER B.Using ethanol as an energy source[J].Science,2004,305(5682):340-340
[5]闵恩泽.利用可再生农林生物质资源的炼油厂——推动化学工业迈入“碳水化合物”新时代[J].化学进展,2006, 18(2): 131-141.(MIN Enze. Developing biorefinery by utilizing agriculture and forestry biomass resources:Striding forward the“Carbonhydrate”Era[J].Progress in Chemistry,2006,18(2):131-141.)
[6]张平,于波,陈靖,等.热化学循环分解水制氢研究进展 [J].化学进展,2005,17(6):852-855.(ZHANG Ping,YU Bo,CHEN Jing,et al.Study on the hydrogen production by thermochemical water splitting[J].Progress in Chemistry,2005,17(6):852-855.)
[7]郭坤,张京京,李浩然,等.微生物电解电池制氢[J].化学进展,2010,22(4):748-753.(GUO Kun,ZHANG Jingjing,LI Haoran,et al.Hydrogen production by microbial electrolysis[J].Progress in Chemistry,2010,22(4):748-753.)
[8]李慧青,邹吉军,刘昌俊,等.等离子体法制氢的研究进展[J].化学进展,2005,17(1):69-77.(LI Huiqing,ZOU Jijun,LIU Changjun,et al.Progress in hydrogen generation using plasmas[J].Progress in Chemistry,2005,17(1):69-77.)
[9]温福宇,杨金辉,宗旭,等.太阳能光催化制氢研究进展[J].化学进展,2009,21(11):2285-2302.(WEN Fuyu,YANG Jinhui,ZONG Xu,et al.Photocatalytic hydrogen production utilizing solar energy[J].Progress in Chemistry,2009,21(11):2285-2302.)
[10]吴川,张华民,衣宝廉,等.化学制氢技术研究进展[J].化学进展,2005,17(3):423-429.(WU Chuan,ZHANG Huamin,YI Baolian,et al.Recent advances in hydrogen generation with chemical methods [J].Progress in Chemistry,2005,17(3):423-429.)
[11]晏波,韦朝海.超临界水气化有机物制氢研究[J].化学进展,2008,20(10):1553-1561.(YAN Bo,WEI Chaohai.Hydrogen production from organic compounds by supercritical water gasification[J].Progress in Chemistry,2008,20(10):1553-1561.)
[12]LEUNG D Y C,NI MLEUNG M K H.A review on reforming bio-ethanol for hydrogen production[J].International Journal of Hydrogen Energy,2007,32(15):3238-3247
[13]FISHTIK I,ALEXANDER A,DATTA R,et al.A thermodynamic analysis of hydrogen production by steam reforming of ethanol via response reactions [J].International Journal of Hydrogen Energy,2000,25(1):31-45.
[14]FRENI S.Rh based catalysts for indirect internal reforming ethanol applications in molten carbonate fuel cells[J].Journal of Power Sources,2001,94(1):14-19.
[15]HARYANTO A,FERNANDO S,MURALI N,et al.Current status of hydrogen production techniques by steam reforming of ethanol:A review[J].Energy &Fuels,2005,19(5):2098-2106.
[16]MARINO F J,CERRELLA E G,DUHALDE S,et al.Hydrogen from steam reforming of ethanol.Characterization and performance of copper-nickel supported catalysts [J].International Journal of Hydrogen Energy,1998,23(12):1095-1101.
[17]王卫平,吕功煊.乙醇催化制氢研究进展[J].化学进展,2003,15(1):74-78.(WANG Weiping, LÜ Gongxuan.Advances in catalytic generation of hydrogen from ethanol[J].Progress in Chemistry,2003,15(1):74-78.)
[18]PRAKASH D V A E.Insight into steam reforming of ethanol to produce hydrogen for fuel cells[J].Chemical Engineering Journal,2006,117(1):39-49.
[19]VASUEVA K M N,UMASANKER P,DHINGRA S C.Steam reforming of ethanol for hydrogen production:Thermodaynamic analysis[J].International Journal of Hydrogen Energy,1996,21(1):13-18.
[20]ZHANG Z,VERYKIOS X E.Carbon dioxide reforming of methane to synthesis gas over Ni/La2O3catalysts[J].Applied Catalysis A:General,1996:138(1):109-133.
[21]CANTAO M P,CAMPOS-SKROBOT F C,RIZZODOMINGUES R C P,et al.Novel zeolite-supported rhodium catalysts for ethanol steam reforming[J].Journal of Power Sources,2008,183(2):713-716.
[22]CHICA A,SAYAS S.Effective and stable bioethanol steam reforming catalyst based on Ni and Co supported on all-silica delaminated ITQ-2zeolite[J].Catalysis Today,2009,146(1-2):37-43.
[23]SUN J,QIU X P,WU F,et al.H-2from steam reforming of ethanol at low temperature over Ni/Y2O3,Ni/La2O3and Ni/Al2O3catalysts for fuel-cell application[J].International Journal of Hydrogen Energy,2005,30(4):437-445
[24]VIZCAINO A,CARRERO A,CALLES J.Hydrogen production by ethanol steam reforming over Cu-Ni supported catalysts [J].International Journal of Hydrogen Energy,2007,32(10-11):1450-1461.
[25]CHEN L,CHOONG C K S,ZHONG Z,et al.Carbon monoxide-free hydrogen production via low-temperature steam reforming of ethanol over iron-promoted Rh catalyst[J].Journal of Catalysis,2010,276(2):197-200.
[26]MARINO F,BOVERI M,BARONETTI G,et al.Hydrogen production from steam reforming of bioethanol using Cu/Ni/K/gamma-Al2O3catalysts.Effect of Ni[J].International Journal of Hydrogen Energy,2001,26(7):665-668.
[27]SANCHEZ-SANCHEZ M C,NAVARRO R M,Fierro J L G.Ethanol steam reforming over Ni/MxOy-Al2O3(M=Ce,La,Zr and Mg)catalysts:Influence of support on the hydrogen production[J].International Journal of Hydrogen Energy, 2007, 32(10-11):1462-1471.
[28]ZHANG L,LIU J,LI W,et al.Ethanol steam reforming over Ni-Cu/Al2O3-MyOz(M = Si,La,Mg,and Zn)catalysts [J].Journal of Natural Gas Chemistry,2009,18(1):55-65.
[29]CAVALLARO S,CHIODO V,FRENI S,et al.Performance of Rh-Al2O3catalyst in the steam reforming of ethanol:H2production for MCFC[J].Applied Catalysis A:General,249(1):119-228.
[30]SONG H O,ZKAN U S.Ethanol steam reforming over Co-based catalysts:Role of oxygen mobility[J].Journal of Catalysis,2009,261(1):66-74.
[31]BISWAS P,KUNZRU D.Steam reforming of ethanol for production of hydrogen over Ni/CeO2-ZrO2catalyst:Effect of support and metal loading[J].International Journal of Hydrogen Energy,2007,32(8):969-980.
[32]CAI W,ZHANG B,LI Y,et al.Hydrogen production by oxidative steam reforming of ethanol over an Ir/CeO2catalyst[J].Catalysis Communications,2007,8(11):1588-1594.
[33]GUO Z G,WANG S R,GUO L,et al.Catalytic steam reforming of ethanol for hydrogen production over Ni/CeO2-Zr O2catalysts[J].Bioresources,2011,6(4):4092-4102.
[34]LIU Q H,LIU Z L,ZHOU X H,et al.Hydrogen production by steam reforming of ethanol over copper doped Ni/CeO2catalysts[J].Journal of Rare Earths,2011,29(9):872-877.
[35]MAIA T A,ASSAF J M,ASSAF E M.Steam reforming of ethanol for hydrogen production on Co/CeO2-ZrO2catalysts prepared by polymerization method[J].Materials Chemistry and Physics,2012,132(2-3):1029-1034.
[36]ZHANG B C,TANG X L,LI Y,et al.Steam reforming of bio-ethanol for the production of hydrogen over ceria-supported Co,Ir and Ni catalysts[J].Catalysis Communications,2006,7(6):367-372.
[37]ZHANG B C,CAI W J,LI Y,et al.Hydrogen production by steam reforming of ethanol over an Ir/CeO2catalyst:Reaction mechanism and stability of the catalyst[J].International Journal of Hydrogen Energy,2008,33(16):4377-4386.
[38]SUN G B,HIDAJAT K,WU X S,et al.A crucial role of surface oxygen mobility on nanocrystalline Y2O3support for oxidative steam reforming of ethanol to hydrogen over Ni/Y2O3catalysts[J].Applied Catalysis B:Environmental,2008,81(3-4):303-312.
[39]FAJARDO H V,PROBST L F D,CARRENO N L V,et al.Hydrogen production from ethanol steam reforming over Ni/CeO2nanocomposite catalysts[J].Catalysis Letters,2007,119(3-4):228-236.
[40]SCOTT M,CHIU W,BLACKFORD M G,et al.Hydrogen production from ethanol over Rh-Pd/CeO2catalysts[J].Topics in Catalysts,2008,51(1-4):13-21.
[41]SUN J,LUO D F,XIAO P,et al.High yield hydrogen production from low CO selectivity ethanol steam reforming over modified Ni/Y2O3catalysts at low temperature for fuel cell application[J].Journal of Power Sources,2008,184(2):385-391.
[42]CHEN H Q,YU H,PENG F,et al.Efficient and stable oxidative steam reforming of ethanol for hydrogen production:Effect of in situ dispersion of Ir over Ir/La2O3[J].Journal of Catalysis,2010,269(2):281-290.
[43]CHEN H Q,YU H,YANG G X,et al.Auto-thermal ethanol micro-reformer with a structural Ir/La2O3/ZrO2catalyst for hydrogen production [J]. Chemical Engineering Journal,2011,167(1):322-327.
[44]SUN J,WU F,QIU X P,et al.Hydrogen production from ethanol steam reforming over Ni/Al2O3and Ni/La2O3catalysts at low temperature[J].Chinese Journal of Catalysis,2004,25(7):551-555.
[45]SHI Q J,LIU C WCHEN W Q.Hydrogen production from steam reforming of ethanol over Ni/MgO-CeO2catalyst at low temperature[J].Journal of Rare Earths,2009,27(6):948-954.
[46]ROH H S,PLATON A,WANG Y,et al.Catalyst deactivation and regeneration in low temperature ethanol steam reforming with Rh/CeO2-ZrO2catalysts[J].Catalysis Letters,2006,110(1-2):1-6.
[47]FRUSTERI F,FRENI S,CHIODO V,et al.Steam and auto-thermal reforming of bio-ethanol over MgO and CeO2Ni supported catalysts[J].International Journal of Hydrogen Energy,2006,31(15):2193-2199.
[48]KUGAI J,SUBRAMANI V,SONG C,et al.Effects of nanocrystalline CeO2supports on the properties and performance of Ni-Rh bimetallic catalyst for oxidative steam reforming of ethanol[J].Journal of Catalysis,2006,238(2):430-440.
[49]DIAGNE C,IDRISS H,PEARSON K,et al.Efficient hydrogen production by ethanol reforming over Rh catalysts.Effect of addition of Zr on CeO2for the oxidation of CO to CO2[J].Comptes Rendus Chimie,2004,7(6-7):617-622.
[50]KUNZRU D,BISWAS P.Oxidative steam reforming of ethanol over Ni/CeO2-ZrO2catalyst[J].Chemical Engineering Journal,2008,136(1):41-49.
[51]王阳.Ni/Ce_(0.5)Zr_(0.5)O_2催化剂在乙醇水蒸气重整制氢过程中的研究[D].天津大学,2007.
[52]BREEN J P,BURCH R,COLEMAN H M.Metalcatalysed steam reforming of ethanol in the production of hydrogen for fuel cell applications[J].Applied Catalysis B:Environmental,2002,39(1):65-74.
[53]INOKAWA H,NISHIMOTO S,KAMESHIMA Y,et al.Difference in the catalytic activity of transition metals and their cations loaded in zeolite Y for ethanol steam reforming [J].International Journal of Hydrogen Energy,2010,35(21):11719-11724.
[54]VIZCAíNO A J,CARRERO A,CALLES J A.Ethanol steam reforming on Mg-and Ca-modified Cu-Ni/SBA-15catalysts[J].Catalysis Today,2009,146(1-2):63-70.
[55]CARRERO A, CALLES J A,VIZCAíNO A J.Hydrogen production by ethanol steam reforming over Cu-Ni/SBA-15supported catalysts prepared by direct synthesis and impregnation[J].Applied Catalysis A:General,2007,327(1):82-94.
[56]CALLES J A,CARRERO A,VIZCAÍNO A J.Ce and La modification of mesoporous Cu-Ni/SBA-15catalysts for hydrogen production through ethanol steam reforming[J].Microporous and Mesoporous Materials,2009,119(1-3):200-207.
[57]LINDO M,VIZCAINO A J,CALLES J A,et al.Ethanol steam reforming on Ni/Al-SBA-15catalysts:Effect of the aluminium content[J].International Journal of Hydrogen Energy,2010,35(11):5895-5901.
[58]LIGURAS D K,KONDARIDES D I,VERYKIOS X E.Production of hydrogen for fuel cells by steam reforming of ethanol over supported noble metal catalysts[J].Applied Catalysis B:Environmental,2003,43(4):345-354.
[59]KWAK B S,LEE J S,LEE J S,et al.Hydrogen-rich gas production from ethanol steam reforming over Ni/Ga/Mg/zeolite Y catalysts at mild temperature[J].Applied Energy,2011,88(12):4366-4375.
[60]ZHANG B C,TANG X L,LI Y,et al.Hydrogen production from steam reforming of ethanol and glycerol over ceria-supported metal catalysts[J].International Journal of Hydrogen Energy, 2007, 32(13):2367-2373.
[61]SÁS,SILVA H,BRANDÃOL,et al.Catalysts for methanol steam reforming—A review [J]. Applied Catalysis B:Environmental,2010,99(1-2):43-57.
[62]JEONG H,KIM K I,KIM T H,et al.Hydrogen production by steam reforming of methanol in a microchannel reactor coated with Cu/ZnO/ZrO2/Al2O3catalyst[J].Journal of Power Sources,2006,159(2):1296-1299.
[63]SHISHIDO T,YAMAMOTO Y,MORIOKA H,et al.Active Cu/ZnO and Cu/ZnO/Al2O3catalysts prepared by homogeneous precipitation method in steam reforming of methanol[J].Applied Catalysis A:General,2004,263(2):249-253.
[64]YANG H MLIAO P H.Preparation and activity of Cu/ZnO-CNTs nano-catalyst on steam reforming of methanol[J].Applied Catalysis A:General,2007,317(2):226-233.
[65]HUANG G,LIAW B J,JHANG C J,et al.Steam reforming of methanol over CuO/ZnO/CeO2/ZrO2/Al2O3catalysts[J].Applied Catalysis A:General,2009,358(1):7-12.
[66]PURNAMA H,GIRGSDIES F,RESSLER T,et al.Activity and selectivity of a nanostructured CuO/ZrO2catalyst in the steam reforming of methanol[J].Catalysis Letters,2004,94(1-2):61-68.
[67]LAOSIRIPOJANA N, ASSABUMRUNGRAT S.Methane steam reforming over Ni/Ce-ZrO2catalyst:Influences of Ce-ZrO2support on reactivity,resistance toward carbon formation,and intrinsic reaction kinetics[J].Applied Catalysis A:General,2005,290(1-2):200-211.
[68]LAOSIRIPOJANA N, SUTTHISRIPOK W,ASSABUMRUNGRAT S.Synthesis gas production from dry reforming of methane over CeO2doped Ni/Al2O3:Influence of the doping ceria on the resistance toward carbon formation[J].Chemical Engineering Journal,2005,112(1-3):13-22.
[69]LAOSIRIPOJANA N, ASSABUMRUNGRAT S.Catalytic steam reforming of ethanol over high surface area CeO2:The role of CeO2as an internal pre-reforming catalyst[J].Applied Catalysis B:Environmental,2006,66(1-2):29-39.
[70]FRUSTERI F,FRENI S,SPADARO L,et al.H2production for MC fuel cell by steam reforming of ethanol over MgO supported Pd,Rh,Ni and Co catalysts[J].Catalysis Communications,2004,5(10):611-615.
[71]FRUSTERI F, FRENI S, CHIODO V, et al.Potassium improved stability of Ni/MgO in the steam reforming of ethanol for the production of hydrogen for MCFC[J].Journal of Power Sources,2004,132(1-2):139-144.
[72]FRUSTERI F,FRENI S,CHIODO V,et al.Steam reforming of bio-ethanol on alkali-doped Ni/MgO catalysts:Hydrogen production for MC fuel cell[J].Applied Catalysis A:General,2004,270(1-2):1-7.
[73]FURTADO A C,ALONSO C G,CANTÃOMP,et al.Bimetallic catalysts performance during ethanol steam reforming: Influence of support materials [J].International Journal of Hydrogen Energy,2009,34(17):7189-7196.
[74]LLORCA J,DE LA PISCINA P R,SALES J,et al.Direct production of hydrogen from ethanolic aqueous solutions over oxide catalysts [J]. Chemical Communications,2001,7(7):641-642.
[75]LLORCA J,DE LA PISCINA P R,DALMON J A,et al.CO-free hydrogen from steam-reforming of bioethanol over ZnO-supported cobalt catalysts—Effect of the metallic precursor [J]. Applied Catalysis B:Environmental,2003,43(4):355-369.
