超高效液相-串联质谱法测定鸡肉组织中金刚烷胺残留
2013-10-09魏秀丽高迎春陆庆泉张呈军
魏秀丽,高迎春,陈 玲,陆庆泉,张呈军
(山东省兽药质量检验所,济南 250022)
金刚烷胺是最早用于抑制流感病毒的抗病毒药,国际上于1966年批准作为预防药,1976年在预防药的基础上确认为治疗药[1-2]。国内20世纪90年代末曾在兽医临床上用于动物病毒病的预防和治疗[3]。金刚烷胺作为抗病毒药物应用于兽医临床,缺乏科学规范、安全有效的实验数据,用于动物病毒性疫病不但给动物疫病控制带来不良的后果,而且影响国家动物疫病防控政策,因此2005年10月农业部发布第560号公告[4],同年12月发布《关于清查金刚烷胺等抗病毒药物的紧急通知》[5],规定禁止金刚烷胺等抗病毒兽药的生产和使用。2012年12月18日央视曝光仍有极少数不法养殖场在利益的驱动下违规使用金刚烷胺,严重影响消费者对鸡肉食品安全的信任。我国对于动物源性食品中金刚烷胺残留检测的相关报道极少,无国家标准。为检测鸡肉组织中可能残留的金刚烷胺,保障鸡肉产品安全,解除人们对白羽肉鸡的恐慌,本实验室建立了鸡肉中金刚烷胺残留量测定的超高效液相-串联质谱法(UPLC-MS/MS)。本方法通过优化提取净化条件,优化色谱和质谱条件,提高了分离效果,可以作为定性、定量的确证方法。
1 仪器与试药
1.1 仪器 天平,感量0.01 g;分析天平,感量0.00001 g;Waters Quattro premierXE超高效液相-串联质谱仪;离心机。SPE固相萃取小柱 Oasis MAX(3 cc/60 mg)、0.22 μm 的滤膜均为 Waters公司。
1.2 药品及试剂 金刚烷胺,批号A0309578,含量96%,上海安谱科学仪器有限公司;马来酸氯苯那敏,批号R275,含量99.7%,中国食品药品检定研究院。浓氨水、异丙醇、三氯乙酸均为分析纯;甲酸、乙腈、甲醇均为色谱纯;超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:ACQUITY UPLCTMBEH C18色谱柱(100mm ×2.1 mm,1.7 μm);流动相A:水溶液(0.1%甲酸);流动相B:甲醇(0.1%甲酸);流速:0.3 mL/min;进样量:10μL;柱温:35℃。液相色谱梯度洗脱程序见表1。

表1 液相色谱梯度洗脱程序
2.2 质谱条件 电喷雾离子源;正离子扫描(ESI+);多反应监测(MRM);离子源温度:110℃;脱溶剂温度:320℃;脱溶剂氮气流速:550 L/h;毛细管电压:3 kV;测试药物定性、定量离子对及对应的锥孔电压和碰撞能量见表2。

表2 两种药物的定性离子对、定量离子对、锥孔电压和碰撞能量
2.3 样品制备
2.3.1 阴性样品的制备 取鸡肌肉100 g进行匀浆,自制阴性样品。
2.3.2 标准储备液的制备 精密称取金刚烷胺对照品10 mg,加甲醇至100 mL,制成100 ug/mL的溶液,作为外标储备液,-20℃冰箱保存。精密称取内标马来酸氯苯那敏10 mg,加50%甲醇至100 mL,制成100 ug/mL的溶液,作为内标储备液,4℃冰箱保存。储备液用初始比例流动相适量倍比稀释1000倍,得100 ng/mL的工作液。
2.3.3 标准工作液的制备 取适量标准工作液,用初始比例流动相稀释,制备成含内标20 ng/mL的系列浓度为:1、2、4、10、20 ng/mL 标准工作液,绘制标准曲线。取浓度为4 ng/mL的标准工作液作为UPLC-MS/MS对照品溶液。
2.3.4 阳性添加样品的制备 取100 ng/mL的金刚烷胺和氯苯那敏工作液各适量加入到自制阴性样品中配置成的1、2、5、10 ng/g的阳性添加样品,内标均为10 ng/g。
2.4 提取净化方法
2.4.1 样品提取 取各种样品(2±0.05)g置于50 mL离心管内,加入0.5%的三氯乙酸∶乙腈(1 ∶1,V/V)10 mL,震荡 10 min,10000 r/min 离心10min,取上清液待净化。
2.4.2 SPE流程 固相萃取小柱 Oasis MAX用3 mL甲醇、3 mL水依次活化,把上清液过柱,依次用3 mL 2%甲酸水溶液、3 mL甲醇清洗,挤干,用5%氨化甲醇∶异丙醇(1∶1)洗脱入氮吹管,氮气吹干,用1 mL 0.1%甲酸:甲醇(9∶1)定容,用滤膜滤过,取滤液作为UPLC-MS/MS供试品溶液。
2.5 方法线性考察及添加回收试验结果
2.5.1 标准曲线 在选定的色谱条件下,使用梯度洗脱的方法,可以有效地分离各离子,在1~20 ng/mL的范围内标准曲线方程为Y=0.0892X-0.0345,Y为金刚烷胺定量离子和马来酸氯苯那敏定量离子峰面积的比值,X(ng/mL)为金刚烷胺的浓度,其相关系数R2为0.997,线性良好。
2.5.2 方法的准确度和精密度 鸡肉中添加金刚烷胺以马来酸氯苯那敏为内标物,液质分离良好,无任何干扰,检出限为1 ng/g,定量限2 ng/g;鸡肉的添加浓度分别2、5、10 ng/g,批内批间变异系数均小于20%,阳性添加样品的回收率在85%~125%(表3)。各特征离子质量色谱图见图1-图3。
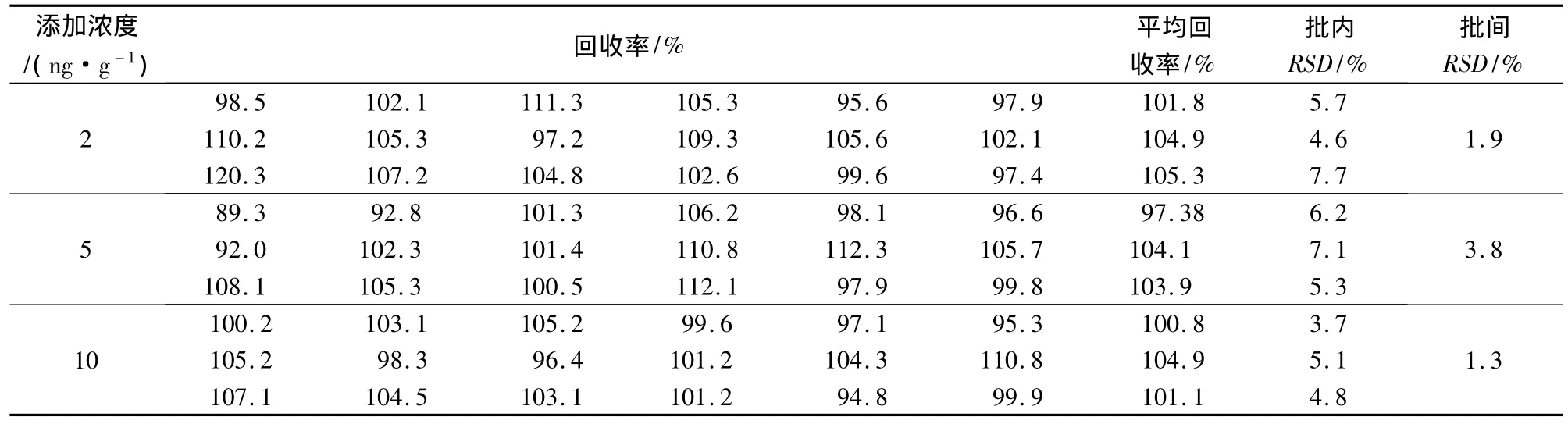
表3 鸡肉中添加金刚烷胺的回收率试验结果(n=6)


图3 2 ng/g阳性添加特征离子质量色谱图
3 讨论
3.1 本实验选择甲醇(0.1%甲酸)和乙腈(0.1%甲酸)为流动相B作比较,发现以乙腈为流动相,其特征离子质量色谱图的峰形和分离度不如用甲醇做流动相好,最终选择了甲醇(0.1%甲酸)为流动相B。
3.2 本实验参考文献方法[1-2]选择了马来酸氯苯那敏作为金刚烷胺的内标物,以内标法计算结果线性良好。因肌肉组织不同于血浆,成分更复杂,重新研究提取方法和净化方法,采用三氯乙酸 ∶乙腈(1∶1,V/V)提取试样中残留的金刚烷胺,并经固相萃取小柱Oasis MAX的净化浓缩,上机检测无干扰,分离度和精密度良好。
3.3 本实验只针对鸡肌肉组织中金刚烷胺的残留检测进行了方法学的考察验证,对鸡的其他组织未进行验证,下一步需要进一步研究鸡肝、鸡肾中金刚烷胺的残留检测方法,为进一步制定国家标准奠定基础。
本方法建立了UPLC-MS/MS法测定鸡肌肉组织中的金刚烷胺残留,采用内标法,对样品进行提取净化后测定,准确性灵敏度高、检测限低。通过方法学考察,本方法完全适合鸡肌肉组织中金刚烷胺残留的定性、定量检测。
[1] 戴晓健,陈笑艳,张 勇,等.液相色谱-串联质谱法同时测定人血浆中金刚烷胺和氯苯那敏[J].药物分析杂志,2006,06:17-21.
[2] 李云巍,周小淳,秦焕杰.同时测定人血浆中金刚烷胺、马来酸氯苯那敏的分析方法[J].中国医药指南,2012,10(26):450-452.
[3] 云 环,张朝晖,罗生亮,等.固相萃取/LC-MS-MS法检测动物源性食品中的金刚烷胺[J].现代仪器,2009,06:42 -45.
[4] 中华人民共和国农业部公告第560号[Z].2005.
[5] 农业部文件农医发[2005]33号关于清查金刚烷胺等抗病毒药物的紧急通知[Z].
