氨曲南的制备新工艺
2013-10-08钟为慧
陈 凯 钟为慧
(浙江工业大学 药学院,杭州 310014)
氨曲南(1)是一种人工合成的单环β-内酰胺类抗生素,由美国施贵宝公司开发,1984年以商品名“Primbactam”在意大利上市,中国于1997年批准进口,2005年后以国内生产为主。氨曲南具有抗菌谱广,疗效确切,对β-内酰胺酶稳定等特点,临床上主要用于治疗敏感革兰阴性菌所致的各种感染,如:尿路感染、呼吸道感染、腹腔感染、生殖道感染,胆道感染、皮肤及软组织感染、骨及关节感染、败血症等[1-3],具有较好的市场前景。现阶段,氨曲南的传统合成工艺是活性酯法:该工艺以头孢他啶侧链活性硫酯,即(Z)-2-[(2-氨基噻唑-4-基)-(苯并噻唑-2-基硫基羰基)亚甲胺基氧基]-2-甲基丙酸叔丁酯 (TAEM)和氨曲南主环(3),即(3S-反式)-3-氨基-4-甲基-2-氧代-1-氮杂环丁烷磺酸为原料,在三乙胺存在下合成叔丁基氨曲南(2),即[2S-[2α,3β(Z)]]-2-[[[1-(2-氨基-4-噻唑基)-2-[(2-甲基-4-氧代-1-磺基-3-氮杂环丁烷基)氨基]-2-氧代亚乙基]氨基]氧代]-2-甲基丙酸叔丁酯,然后在三氟乙酸作用下,60℃,脱去叔丁基,得到氨曲南(1)[4-6],即[2S-[2α,3β(Z)]]-2-[[[1-(2-氨基-4-噻唑基)-2-[(2-甲基-4-氧代-1-磺基-3-氮杂环丁烷基)氨基]-2-氧代亚乙基]氨基]氧代]-2-甲基丙酸。该法原子经济性较差,副产物2-巯基苯并噻唑(MBT)较难除尽,残留的MBT是影响氨曲南质量的重要因素。
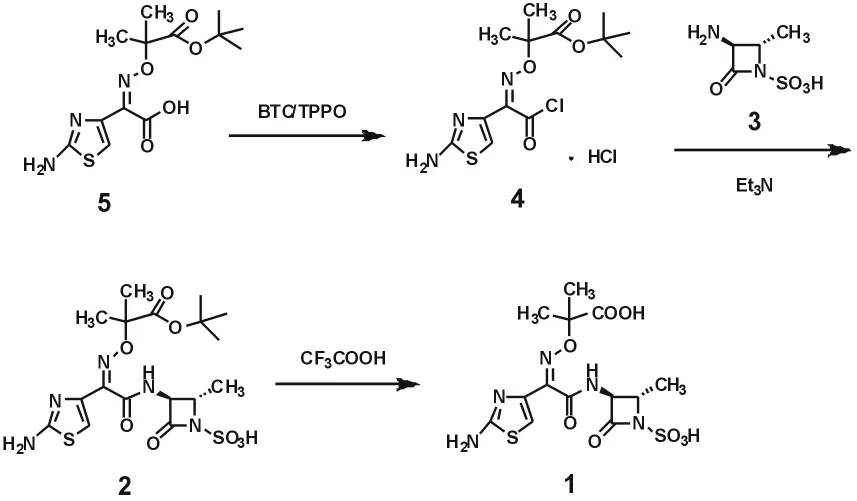
Scheme 1
酰氯法已在合成头孢地尼、头孢呋辛钠和头孢硫脒中得到应用[7-9]。本文使用头孢他啶侧链酸(5), 即 Z-2-(2-氨基噻唑-4-基)-2-[(特-丁氧羰基)异丙氧亚胺基]乙酸为原料,在双(三氯甲基)碳酸酯(BTC)和三苯基氧膦(TPPO)体系作用下,制备酰氯盐酸盐中间体(4),然后在三乙胺作用下与氨曲南主环(3)缩合得到(2),后者再脱去叔丁基保护得到(1)。本方法从源头上避免了MBT的残留,为合成氨曲南提供了一种新的合成方法(Scheme 1)。
1 实验部分
1.1 仪器及试剂
DLSB-3006低温冷却液循环泵;DZF-6050真空干燥箱;Varian NMR-400MHz型核磁共振仪;Frace DSQ FINNGAN质谱仪。
头孢他啶侧链酸、三苯基氧膦、BTC、氨曲南主环等试剂均为市售化学纯。
1.2 合成部分
1.2.1 酰氯盐酸盐中间体(4)的合成
室温下往烧瓶中加入三苯基氧膦 (50.7 g,0.182 mol)和干燥的二氯甲烷(200 mL)。30 ℃下,向烧瓶中滴加溶有双(三氯甲基)碳酸酯(18.1 g,0.061 mol)的二氯甲烷(50 mL)溶液。 滴毕,保温搅拌反应30 min。降温至-15℃,将此溶液快速滴加入装有头孢他啶侧链酸(5)(50.0 g,0.152 mol)和二氯甲烷(150 mL)的另一烧瓶中,保温搅拌反应3 h。然后升温至-5℃,向反应液中加入干燥的石油醚(800 mL),搅拌 15~30 min,有固体析出。减压抽滤,得到白色固体,真空干燥,得到酰氯盐酸盐中间体(4)50.8 g,收率87.3%,产品应密封低温保存。1H NMR(400 MHz,CDCl3)δ 6.63(s,1H,C=CH),3.91 (s,2H,NH2),1.50 (s,6H,C(CH3)2),1.44(s,9H,C(CH3)3)。
母液减压浓缩,残留液用甲苯重结晶,得到三苯基氧膦,回收率90.2%。
1.2.2 叔丁基氨曲南(2)的合成
往烧瓶中加入氨曲南主环 (3)(20.0 g,0.111 mol)和二氯甲烷(200 mL)。 冷却至-10 ℃,向烧瓶中滴加三乙胺(50.5 g,0.500 mol),至反应液变澄清后,分批快速加入中间体 (4)(42.5 g,0.111 mol)。保持温度反应15~20 h后,升温至0~5℃之间,加入200 mL水,静止分层。分离得到的水层用2 mol/L盐酸调节pH至1.5~2.0,静置析晶。抽滤,滤饼真空干燥,得到叔丁基氨曲南(2)36.4 g,收率 66.7%。1H NMR(400 MHz,DMSO)δ 9.25(d,J=7.8 Hz,1H,CONH),6.88(s,1H,C=CH),4.45(dd,J=7.8,2.6 Hz,1H,CHNH),3.69~3.64(m,1H,CHCH3),1.45(s,6H,C(CH3)2),1.40(d,J=6.3 Hz,3H,CHCH3),1.39(s,9H,C(CH3)3)。
1.2.3 氨曲南(1)的合成
往烧瓶中加入叔丁基氨曲南(2)(20.0g,0.041 mol),水(200 mL)和三氟乙酸(60 mL)。 升温至60℃,反应2~3 h。反应完毕后,冰浴冷却,低温下静置至固体析出,抽滤,滤饼用冰水(50 mL)洗涤后,加至冰丙酮(50 mL)中搅拌至均匀。抽滤,滤饼真空干燥得到(1)12.3 g,收率 69.7%,mp:237 ℃~239℃。
1H NMR(400 MHz,DMSO)δ 9.29(d,J=7.9 Hz,1H,CONH),6.89(s,1H,C=CH),4.46(dd,J=7.9,2.5 Hz,1H,CHNH),3.70~3.65 (m,1H,CHCH3),1.47(s,6H,C(CH3)2),1.41(d,J=6.1 Hz,3H,CHCH3)。
2 结果与讨论
本文首次用酰氯法制备氨曲南,关键步骤就是酰氯盐酸盐中间体(4)的合成。本文主要探讨了BTC/TPPO的用量、反应时间、反应温度对中间体(4)合成收率的影响;也考察了反应时间和投料方式对叔丁基氨曲南(2)合成收率的影响。中间体(2)脱叔丁基保护方法较为成熟,本文不作深入研究,具体参考文献[5]和[6]。
2.1 酰氯盐酸盐中间体(4)的制备
2.1.1 BTC/TPPO的用量对(4)合成收率的影响
设定反应温度为-15℃,反应时间为3 h,BTC/TPPO用量对(4)合成收率的影响见表1。实验发现,在头孢他啶侧链酸(5)与BTC、TPPO的投料摩尔比为1:0.4:1.2时,中间体(4)的合成收率最高,可能的原因是,(5)在稍过量的BTC/TPPO作用下,刚好可以消耗完全,在-5℃时向反应体系中加入2倍二氯甲烷体积量的石油醚,恰好能将大部分(4)析出,而三苯基氧膦全部留在溶液中,实现与三苯基氧膦的有效分离。当原料投料比为1:0.33:1时,一方面原料(5)未反应完,在加入石油醚后,剩余的原料(5)也随产品一起析出,产品需进一步纯化,才可投入下一步使用,导致收率较低。继续增加BTC/TPPO的用量(1:0.5:1.5)时,虽然原料(5)消耗完全,但过量的BTC/TPPO会影响产品的析出,导致收率下降。如果再继续增加BTC/TPPO的用量 (1:0.67:2),后处理时无任何固体析出。另外,本文还考察了单独使用BTC和使用BTC/Et3N体系的反应情况。TLC跟踪发现,都不能得到目标产物,此结果表明三苯基氧膦在反应中起到了至关重要的作用。

表1 BTC/TPPO用量对中间体(4)合成收率的影响Table 1 The effect of amount of BTC/TPPO on the yield of 4
2.1.2 反应温度对(4)合成收率的影响
设定投料比5:BTC:TPPO=1:0.4:1.2,反应时间为3 h,反应温度对(4)合成收率的影响见表2。

表2 反应温度对(4)合成收率的影响Table 2 The effect of temperature on the yield of 4
从表2得知,-15℃下反应收率最高。升高或降低温度,都导致收率偏低。-30℃下反应时,析出的固体基本都是原料。如果升高反应温度,反应比较复杂,TLC显示有许多杂质生成,导致产品收率和纯度都降低。
2.1.3 反应时间对(4)合成收率的影响
设定反应温度为-15℃,投料比5:BTC:TPPO=1:0.4:1.2,反应时间对(4)合成收率的影响见表3。

表3 反应时间对(4)合成收率的影响Table 3 The effect of reaction time on the yield of 4
由表3可知,较佳的反应时间为3 h,即可得到较高的收率。延长反应时间至6 h,收率反而降低。如果延长反应时间达到12 h,副反应增加,TLC发现有杂质生成,导致产率降低。
2.2 叔丁基氨曲南(2)的制备
2.2.1 不同的投料方式对叔丁基氨曲南(2)合成收率的影响
设定反应温度为-10℃,反应时间为15 h,不同投料方式对(2)合成收率的影响见表4。

表4 投料方式对(2)合成收率的影响Table 4 The effect of methods of reactants adding on the yield of 2
当向(4)中滴加氨曲南主环(3)与三乙胺的混合溶液时,发现不能得到(2)。TLC显示反应完毕,但最后析晶过程得到的是头孢他啶侧链酸(5)。分析原因,可能是反应液大部分时间呈酸性,钝化了氨曲南主环上3-位氨基,阻碍了酰胺化反应的进行,导致(4)与磺酸基反应形成不稳定的酸酐,该酸酐在后处理加水时又马上分解,于是就又得到了最初的原料(5)。当以第二种方式投料后,反应液始终呈碱性,钝化了磺酸基,促进了酰胺化反应的顺利进行。
2.2.2 不同的反应时间对叔丁基氨曲南(2)合成收率的影响
设定反应温度为-10℃,以第二种方式投料,反应时间对叔丁基氨曲南(2)合成收率的影响见表5。从表5中得知,适当延长反应时间,有助于反应收率的提高,当反应时间为15 h时,收率最高,继续延长反应时间,反而使产率降低。

表5 反应时间对(2)合成收率的影响Table 5 The effect of reaction time on the yield of 2
3 结论
本文探索了一条制备氨曲南(1)的新工艺。以头孢他啶侧链酸为原料,在BTC/TPPO体系作用下得到酰氯盐酸盐中间体,再与氨曲南主环反应得到叔丁基氨曲南,最后脱去叔丁基保护,得到氨曲南,反应总收率约为40.6%。从源头上避免了MBT的残留问题,且使用的试剂经济环保,三苯基氧膦可大部分回收。在药品质量和环境要求趋向严格的新时代,本文提出的工艺为合成氨曲南提供了全新的思路,具有较好的工业化应用前景。
[1]崔红利,陈东风.氨曲南的临床应用[J].现代医药卫生,2008,24(13):1983-1984.
[2]李海滨,廖媛晖.氨曲南的药理作用及临床应用[J].云南民族学院学报(自然科学版),2001,10(2):362-363.
[3]孙玉刚,傅小平.氨曲南的药理作用及临床应用[J].中国医院药学杂志,1991,11(7):307-310.
[4]Domenico F.Process for making aztreonam:US,7601832B2[P].2009-10-13.
[5]邓启华,张宏,黄文才.氨曲南的合成[J].中国医药工业杂志,2009,40(10):728-730.
[6]Gyollai V,Meszaros Sos E,Szabo C,et al.Preparation of aztreonam:WO,2004013133[P].2004-02-12.
[7]林桂春,刘莉,马灵台,等.头孢地尼的合成[J].合成化学,2001,9(5):383-385.
[8]邱民.一种新路线的头孢呋辛钠化合物:CN,101671349[P].2010-03-17.
[9]邱民.一种新路线的头孢硫脒化合物:CN,101704827[P].2010-05-12.
