基于甘氨酸根及邻菲咯啉的锌(Ⅱ)配合物合成、表征、结构及热分解
2013-09-15解凤霞张欣欣
解凤霞 张 丹 张欣欣 华 敏
(西安工程大学环境与化学工程学院,西安 710048)
邻菲咯啉及其衍生物的金属配合物和含有邻菲咯啉的混配金属配合物的研究近年来受到广泛重视,这些配合物已经广泛应用于分子识别、分子催化、自组装、抗肿瘤药物、核酸探针、材料化学等研究领域[1-5]。尽管目前关于邻菲咯啉的研究报道很多,特别是Cu、Co、Zn配位聚合物较多,但是由于邻菲咯啉配体自身的结构特征,通过采用不同的合成方法,改变反应条件和金属-配体间的配比,引入其他配体或客体分子,依旧有新的结构出现[6-10]。
氨基酸是构成生物体内蛋白质、酶等生物大分子的基本结构单元,是同时具有氨基和羧基的双官能团生物小分子配体。由于人体内α-氨基酸的含量大大高于β-氨基酸的含量,人们对α-氨基酸金属配合物的兴趣更为浓厚。α-氨基酸常作为二齿配体,利用其α-碳上的羧基和氨基作为配位基团同金属离子作用,形成较稳定的五元环鳌合物。生物体中的金属元素往往不是以自由离子的形式存在,而是经常与蛋自质、核酸等生物大分子配体形成金属配合物。蛋白质的基本结构就是氨基酸,所以生命体是一个多金属离子、多生物配体的集合体。氨基酸金属配合物等小分子生物配体的配合物不仅具有重要的生物功能,也是金属蛋白、金属酶等生物大分子维持其结构和功能所必需的活性中心[11-13]。因此,研究以氨基酸为配体的金属配合物具有重要意义。本文以邻菲咯啉、甘氨酸(Hgly)为配体,采用溶剂扩散法,合成出了含有2个配位单元的配合物[Zn(gly)(phen)(H2O)2]2·2OH·SO4·4H2O,并对其进行结构和性质报道。
1 实验部分
1.1 试剂和仪器
邻菲咯啉,甘氨酸,七水合硫酸锌,氢氧化钠以及其它试剂均为分析纯,使用前未进一步纯化。VarioELIII型元素分析仪;Shimadzu FTIR-8400型红外光谱仪(KBr压片,测量范围为400~4 000 cm-1);Bruker APEX-II CCD X-射线单晶衍射仪;f-4500型荧光分光光度计;TGA/SDTA851e型热重/差热同步热分析仪。
1.2 配合物[Zn(gly)(phen)(H 2O)2]2·2OH·SO4·4H 2O的合成
称取邻菲咯啉 (1 mmol,0.198 7 g)、 甘氨酸(1 mmol,0.075 9 g)、七水合硫酸锌(1 mmol,0.287 4 g)溶于 10 mL 蒸馏水;氢氧化钠(0.5 mmol,0.021 8 g)溶于5 mL蒸馏水;在搅拌下将两者混合。用磁力搅拌器将混合液加热至50℃并搅拌,1 h后,停止加热,自然冷却至室温。放置2个月之后,得出适于进行单晶结构分析的无色透明晶体,产率约为31%。元素分析按C28H44N6O18SZn2计算,实测值(括号内为计 算 值)(%):C,36.75(36.73);H,4.93(4.84);N,9.16(9.18)。溶解性测试结果显示:配合物易溶于水、乙醚;微溶于热甲醇、吡啶、苯、丙酮;不溶于N,N-二甲基甲酰胺、乙醇、二甲基亚砜。
1.3 晶体结构的测定
选用尺寸为 0.30 mm×0.25 mm×0.21 mm 配合物单晶,用Bruker APEX-II CCD衍射仪进行衍射实验,在 296 K 下用 Mo Kα 射线(λ=0.071 073 nm)辐射为光源,以φ-ω扫描方式收集衍射数据,并用SADABS方法进行半经验吸收矫正,在2.335 5°≤θ≤28.246 5°收集 24352 个衍射点,其中独立衍射点6 412 个(Rint=0.027 0),5 679 个 I>2σ(I)的可观察衍射点用于结构分析和结构修正。晶体结构解析分别使用 SHELXS-97[14]、SHELXL-97程序[15]完成。 对氢原子和非氢原子分别采用各向同性和各向异性热参数,用全矩阵最小二乘法进行结构修正,精修采用SHELXL-97程序[14]完成。最后偏离因子R1=0.0421和 wR2=0.1082,w=1/[σ2()+(0.0519P)2+5.8854P],其中P=()/3。结构解析表明:配合物属三斜晶系,空间群 P1。 其晶胞参数为:a=1.171 63(9)nm,b=1.280 22(10)nm,c=1.348 49(10)nm,α=74.480 0°,β=85.424 0°,γ=69.807 0°,V=1.828 9(2)nm3,Z=2,Dc=1.661 g·cm-3,μ=1.455 mm-1,F(000)=946。配合物的部分键长和键角见表1。
CCDC:876328.
2 结果与讨论
2.1 配合物的红外光谱
用KBr压片法测定标题配合物 [Zn(gly)(phen)(H2O)2]2·2OH·SO4·4H2O 在 500~4 000 cm-1范围内的的红外光谱。红外光谱显示:自由邻菲咯啉有C-H面外弯曲,振动位于734、860 cm-1,形成配合物后分别移至 727.8、852.9 cm-1,面内弯曲振动由 1 470 移至1 427.1 cm-1,邻菲咯啉的环伸缩振动由1 561移至1 518.5 cm-1,这些变化都可认为是邻菲咯啉的氮原子与Zn(Ⅱ)配位引起的。在配合物的谱图中没有发现质子化羧基的特征峰,说明配合物中甘氨酸配体中的羧酸质子已经完全被脱去,这与配合物的单晶结构相一致,1 622.1 cm-1为配合物中游离水的特征吸收。1 210~1 040 cm-1处的吸收峰为硫酸根的吸收。 3 343.94 cm-1处的宽缝属于-OH、H2O、和甘氨酸氨基上的N-H的吸收。616.3 cm-1为酰胺的弯曲振动吸收。
2.2 晶体结构描述
图1给出了配合物[Zn(gly)(phen)(H2O)2]2·2OH·SO4·4H2O的晶体结构配位环境图,晶体结构表明配合物为二聚体,二聚体结构中包含2个配位单元,2个配位单元的配位环境、配位方式是一致的。以Zn(1)中心原子来分析,Zn(Ⅱ)分别与1个邻菲咯啉分子中的2个氮原子(N(1)、N(2))、1个甘氨酸根分子中N(3)、O(1)以及 2 个水分子中氧原子(O(3W)、O(4W))配位,形成1个6配位的畸变八面体配位构型,其中N(1)、N(2)、N(3)、O(4W)处 于 八 面 体 的 赤 道 位 置 ,O(3W)、O(1)处于轴向位置。 N(1)-Zn(1)-O(4W)、N(3)-Zn(1)-N(2)、N(3)-Zn(1)-O(4W)和 N(1)-Zn(1)-N(2)的键角分别为 89.11(10)°,97.99(11)°、95.50(11)°、77.48(10)°,键角总和为 360.09°,接近 360°,表明 N(1)、N(2)、N(3)、O(4w)组成一个近似平面。轴向位置的O(3W)与处于赤道位置的原子之间的键角为:O(3W)-Zn(1)-N(1)、O(3W)-Zn(1)-N(2)、O(3W)-Zn(1)-N(3)和 O(3W)-Zn(1)-O(4W)分 别 为 101.71(10)°、88.67(10)°、94.91(10)°和91.84(9),它们稍偏离 90°。处于轴向位置的 O3W、O(1)和八面体中心 Zn(Ⅱ)的夹角 O(3W)-Zn(1)-O(1)为172.34(9),偏离 180°。

表1 配合物的部分键长和键角Table1 Selected bond lengths(nm)and bond angles(°)of the complex

图1 椭球几率为30%配合物的分子结构Fig.1 Molecular structure of the complex with thermal ellipsoide at 30%probability level
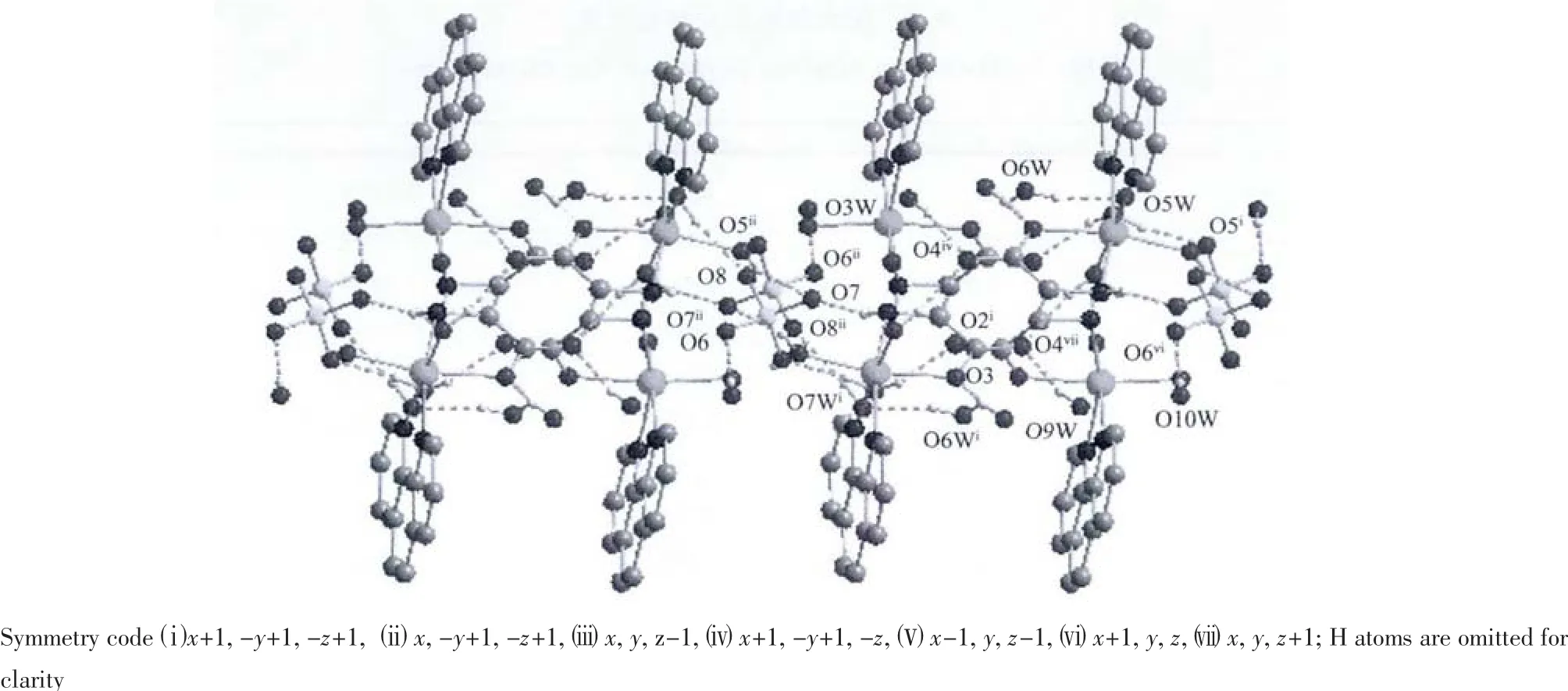
图2 配合物的氢键图Fig.2 Hydrogen bonds of the complex
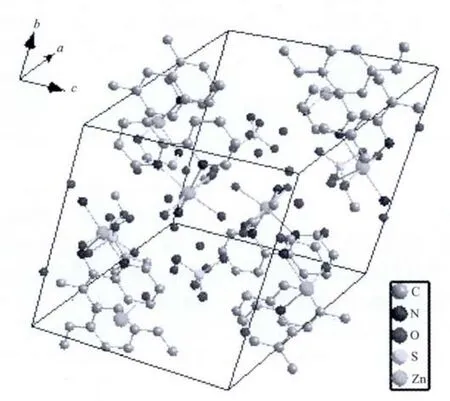
图3 配合物的晶胞堆积图Fig.3 Cell packing diagram of the complex
Zn-O 键长在 0.2084(2)~0.2155(2)nm 范围内,Zn-N 键长在 0.211 6(3)~0.219 0(3)nm 范围内。来自邻菲咯啉的 2个氮原子N(1)、N(2)与 Zn(1)的键长(0.213 4(3)、0.219 0(3)nm)大于来自于甘氨酸的N(3)-Zn(1)的键长(0.2116(3)nm)甘氨酸中的氨基氧与Zn(1)离子的键长(O(1)-Zn(1)0.215 5(2)nm)比来自配位水中氧的距离(O(3W)-Zn(1)0.208 4(2)nm;O(4W)-Zn(1)0.212 6(2)nm)键长大。晶体结构中还包含2个游离的水分子和1个含有负电荷的抗衡阴离子硫酸根离子,这样,2个配位单元分子间通过羧基氧与游离水,硫酸根中的氧与配位水及游离水中氧之间的氢键形成1个二聚体。
在晶体中,存在着丰富的O-H…O、N-H…O型氢键,主要的氢键数据列于表2。参与氢键的原子主要有:配体甘氨酸上羧基氧原子、氢氧根中的羟基氧原子、水上的氧原子游离水和配位水中的羟基氧原子以及硫酸根中的氧原子。形成氢键的类型:游离水之间、游离水与配位水、羧基氧原子与游离水、羧基氧原子与配位水、羟基氧原子与羧基氧原子、羟基氧原子与游离水、硫酸根与游离水、硫酸根与配位水,这些丰富的氢键将相邻的配位单元连接起来形成三维网状结构。

表2 配合物的主要氢键数据Table 2 Hydrogen-bonding parameter for the complex
2.3 配合物的荧光光谱分析
Zn2+离子为d10电子组态,不会发生d-d电子转移,因此Zn2+离子经常和一些具有共轭结构的有机配体形成很好的发光材料[16-17]。在温度为293 K条件下,用荧光分光光度仪记录了配体和配合物的浓度均为5×10-5mol·L-1溶液的发射光谱。以300 nm为激发波长,测得邻菲咯啉配体和配合物在300~550 nm的发射光谱(图4)。

图4 配体及配合物的荧光光谱图Fig.4 Fluorescence emission spectra of the complex and ligand
从图4看出在激发波长λ=300 nm时配合物在370 nm处出现强的宽的吸收峰,这种光谱被称为电荷转移光谱,属于LMCT光谱带[18-19]。和配体的吸收光谱相比较发现:甘氨酸本身是没有荧光性的;邻菲咯啉在370 nm左右有吸收峰,强度为260;而配合物吸收峰的强度很大,达到了3000,说明没有荧光性质的甘氨酸在与锌(Ⅱ)发生配位作用以后形成的五元环加强了配体邻菲咯啉的共轭度,从而使配合物的结构刚性增强,荧光强度显著增强。
2.4 配合物的热重分析
在氮气流速为20 mL·min-1、升温速度为10℃·min-1的实验条件下测定了配合物的热重曲线。
2.4.1 热解特性

图5 配合物的TG、DTG曲线Fig.5 TGand DTGcurves of the complex
图5 为配合物的TG-DTG曲线。TG曲线上的3个失重台阶表明配合物的分解经过的3个阶段:第一步分解发生在80~130℃范围内,失重率5.65%,根据失重率推测应该为结晶水的失去 (理论失重率5.79%);在179~330℃之间配合物经历第二步分解,失重率10.17%;在340~860℃之间有一个大的失重台阶,失重率55.79%,这是由于配合物的主体骨架结构发生分解;860℃以后,样品质量趋于平衡,配合物的分解过程结束,根据样品剩余质量为25.39%,推测出标题配合物在氮气气氛中最终分解为碳酸锌和氢氧化锌的混合物 (理论值24.55%),分解产物通过红外光谱实验得到进一步验证。
2.5.2 动力学分析
对30个不同的机理函数f(α),运用微分Achar法和积分Coats-Redfern法,对其不同阶段的热分解反应动力学参数E、ln A进行了计算。两种方法中以计算得到E、ln A值接近且相关系数均较大的f(α)和G(α)为该反应可能的机理函数的机理函数以及机理函数的积分式[20]。

表4 配合物第三步热分解Achar法和Coats-Redfern法计算结果Table 4 Results between the calculation results of Achar method and Coats-Redfern method for the third decomposition step the complex

表5 配合物的热分解过程的动力学参数Table 5 pyrolysis kinetic parameters of complex

式中:f(α),微分机理函数;G(α),积分机理函数;T,温度;E,活化能;A,指前因子;R,气体常数(8.314 J·mol-1·K-1);β,线性升温速率(℃·min-1)。
为了简便起见,表4仅给出第3步分解过程的的计算结果。分析表4实验结果,发现用两种方法处理第13个函数得到的E、ln A值接近且相关系数R均大于0.988,因此判断第13个函数f(α)=1/4(1-α)[-ln(1-α)]-3为第三步分解过程的机理函数,相应的机理函数积分式G(α)=[-ln(1-α)]4。标题配合物在不同阶段热分解的动力学参数见表5。
[1]Jin V X,Ranford JD.Inorg.Chem.Acta,2000,304:38-44
[2]Ye B H,Tong M L,Chen X M,et al.Coord.Chem.,Rev.,2005,249:545-565
[3]Zhang QL,Liu JG,Chao H,et al.J.Inorg.Biochem.,2001,83:49-55
[4]Wan Y H,Zhang L,Jin L P,et al.Inorg.Chem.,2003,42(16):4985-4994
[5]Zheng SL,Zhang JP,Wong W T,et al.J.Am.Chem.Soc.,2003,125(23):6882-6883
[6]LIU Jian-Feng(刘建风),CHEN Ji-Fei(陈吉妃),ZHAO Guo-Liang(赵国良).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(1):100-106
[7]HE Qi-Zhuang(何其庄),YU Hui(郁慧),ZHOU Mei-Feng(周美峰).Journal of the Chinese Rare Earth Society(Zhongguo Xitu Xuebao),2007,25(2):150-156.
[6]TIAN Li(田俐),CHEN Lin(陈琳),ZHANG Xin(张馨),et al.Chemical Research(Huaxue Yanjiu),2006,17(3):13-15
[9]WANG Qian-Qian(王倩倩),LIU Chun-Bo(刘春波),LI Xiu-Ying(李秀颖).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2012,28(3):619-625
[10]Yokoyama K,Wakabayashi A,Noguchi K,et al.Inorg.Chim.Acta,2006,359(3):807-814
[11]GAOSheng-Li(高胜利),YANG Xu-Wu(杨旭武),CHEN San-Ping(陈三平),et al.Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),2003,24(2):195-199
[12]ZHANG Xin(张 欣),DU Cong(杜 聪),CHEN Dan(陈 丹 ),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(3):489-494
[13]XIE Hai-Quan(谢海泉),DANG Yuan-Lin(党元林),ZHUO Li-Hong(卓立宏),et al.Chinese Journal of Synthetic Chemistry(Hecheng Huaxue),2007,15(3):362-364
[14]Sheldrick G M.SHELXS-97,Program for the Solution of Crystal Structures,University of Göttingen,Germany,1997.
[15]Sheldrick G M.SHELXL-97,Program for the Refinement of Crystal Structures,University of Göttingen,Germany,1997.
[16]Allendorf M D,Bauer C A,Bhakta R K,et al.Chem.Soc.Rev.,2009,38:1330-1352
[17]Fang Q R,Zhu G S,Xue M,et al.Dalton Trans.2004,14:2202-2207
[18]Bordiga S,Lamberti C,Ricchiardi G,et al.Chem.Commun.,2004,(20):2300-2301
[19]Cheng J K,Yin P X,Li Z J,et al.Inorg.Chem.Commun.,2007,10(7):808-810
[20]HU Rong-Zu(胡荣祖),GAO Sheng-Li(高胜利),ZHAO Feng-Qi(赵凤起),et al.Thermal Analysis Kinetics.2nd Ed(热分析动力学.2版).Beijing:Science Press,2008:54-117
