C/MgAl水滑石复合材料为前驱物所制催化剂在柠檬醛-丙酮缩合反应中的催化性能
2013-09-15刘秀芳范彬彬高升成李瑞丰
刘秀芳 范彬彬 高升成 李瑞丰
(太原理工大学精细化工研究所,太原 030024)
MgAl水滑石(Hydrotalcite)是一种层状双羟基复合金属氢氧化物,其分子通式为[Mg1-x2+Alx3+(OH)2]x+[An-]x/n·y H2O,其中An-为层间阴离子,x为水滑石中Al3+的摩尔数,y为层间水分子数目。MgAl水滑石自身不具有碱催化功能或碱催化功能很弱,将水滑石焙烧可形成具有高比表面的MgAl复合金属氧化物,该复合金属氧化物在水环境下,可水合重构形成插层阴离子为OH-的MgAl水滑石(meixnerite)。经焙烧水合重构形成的meixnerite水滑石是优良的具有Brönsted碱性位的催化剂,可用于烷基化反应、双键异构化反应、Knoevenagel缩合反应以及aldol缩合等多种反应[1-3]。水滑石经焙烧水合后形成的meixnerite催化剂的碱催化性能受水滑石自身镁铝比、焙烧水合条件、碱金属的引入及水滑石前驱物的合成条件、相关后处理等因素的影响[4-9]。然而,目前对水合重构meixnerite水滑石催化性能的调变多集中在改变镁铝比、焙烧和水合条件上,而对水滑石前驱物的合成条件对水合重构后所形成meixnerite水滑石碱催化性能影响的研究较少。
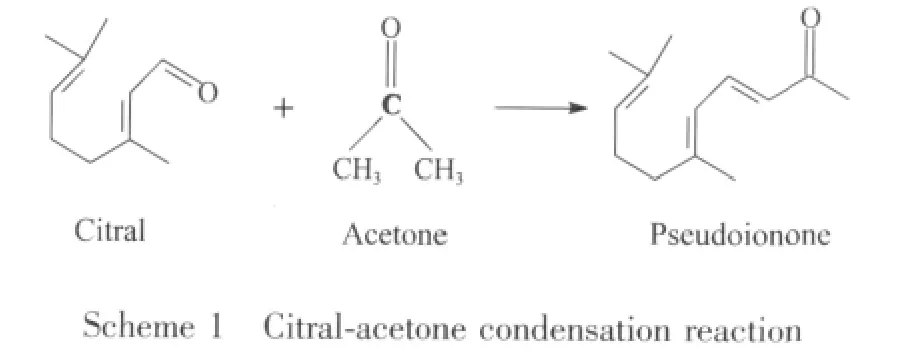
本工作在水滑石合成体系中引入不同量的葡萄糖,利用葡萄糖在所采用的合成条件下可原位碳化的特性[10],通过共沉淀法制备了一系列C/MgAl水滑石复合材料,并以所制备的C/MgAl水滑石复合材料为前驱物,经焙烧和水合制备了系列meixnerites水滑石催化剂,选择柠檬醛-丙酮缩合这一具有重要工业背景的典型碱催化反应为探针反应,详细考察了所制备的meixnerites水滑石的催化性能,旨在通过上述研究,为基于水滑石的固体碱催化性能的改进提供新的路线和思路。
1 实验部分
1.1 C/MgAl水滑石复合材料的制备
系列nMg/nAl=3的C/MgAl 水滑石样品均采用共沉淀法在含葡萄糖的合成体系中于恒定温度和pH值条件下制备。具体制备过程如下:首先在室温并剧烈搅拌下,将100 mL含5.5 g K2CO3的水溶液A加入 到含 14.4 g Mg(NO3)2·6H2O、7.0 g Al(NO3)3·9H2O与不同量葡萄糖的50 mL水溶液B中,以1 mol·L-1KOH溶液调节混合液的pH值,使之始终稳定在10左右;随后将上述混合液转移至带有聚四氟乙烯内衬的高压釜中,于120℃条件下晶化24 h;最后将所得棕色固体经用去离子水洗涤至中性、抽滤后,于80℃下干燥过夜。所制得样品记为C/MgAl-HT-x(x为合成体系中加入葡萄糖的质量百分数:x=mmglucose/(mMg(NO3)2·6H2O+mAl(NO3)3·9H2O))。在相同合成条件无葡萄糖存在体系中得到的样品记为MgAl-HT。
将所制MgAl-HT和C/MgAl-HT-x样品在空气气氛中于550℃焙烧3 h,得到MgAl复合金属氧化物样品,分别记为MgAl-HT-C和MgAl-HT-x-C。在含水的反应体系中经水合后得到的样品分别记为MgAl-HT-rh和 MgAl-HT-x-rh。
1.2 样品表征
X射线衍射(XRD)测试采用日本Simadzu XRD-6000 型 X 射线衍射仪,Cu Kα 靶(λ=0.154 18 nm),石墨单色器,电压 40 kV,电流 30 mA,扫描范围 5°~70°, 扫 描 速 度 4°,DS(divergence slit) 为 1°,RS(scatter slit)为 1°,SS(receiving slit)为 0.15 mm;低温N2吸附/脱附测试采用美国NOVA1200型比表面积和孔径测试仪,测试前样品经80℃抽真空(至10.64 Pa)活化4 h;元素分析采用美国热电公司产IRIS intrepidⅡ型电感耦合等离子体原子发射光谱仪进行。
样品的碱量通过Hammett指示剂测定,所使用的指示剂为酚酞 (p Ka=9.3)。具体测试方法如下:将0.05 g样品悬浮于2 mL含指示剂的乙醇溶液和3 mL H2O 的混合溶液中,使用 0.05 mol·L-1的苯甲酸乙醇溶液进行滴定,观察指示剂的颜色变化,滴至终点时根据苯甲酸用量计算样品中的碱量。
1.3 催化评价
柠檬醛-丙酮缩合反应在50 mL聚四氟乙烯瓶中进行。称取0.1 g催化剂加入瓶中,再加入0.6 g的柠檬醛和4.6 g丙酮,最后再加入3 mL去离子水(煮沸去除CO2),密封后置于60℃下进行反应3 h。反应产物使用日本岛津GC-2014C型气相色谱仪进行分析,FID检测器,色谱柱为RTX-1毛细管柱(30 m×0.25 mm,×0.25 μm), 进样口温度与检测器温度均为300℃,分流进样,分流比为50,N2为载气,载气流速为40 mL·min-1。色谱分析采用程序升温,初始柱温为100℃,在此温度下保持4 min,然后以20℃·min-1速率升温到160℃,并保持8 min。
2 结果与讨论
2.1 不同水滑石样品及其焙烧衍生物的XRD表征
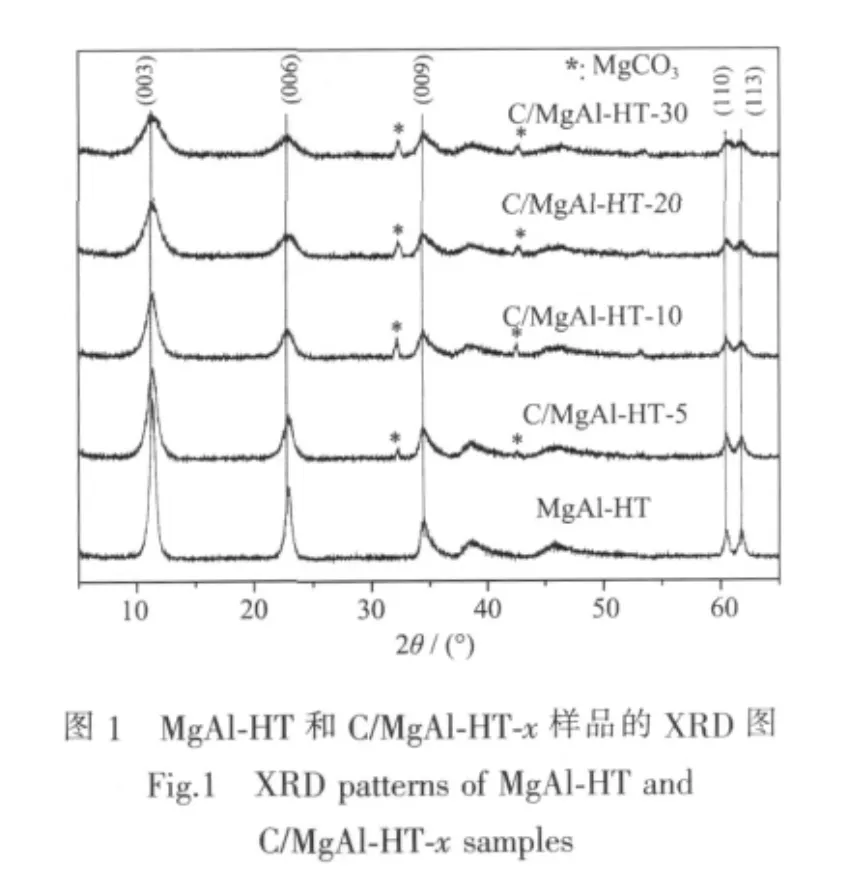
在含葡萄糖的合成体系中所制得的样品经水和乙醇充分洗涤后仍为棕色,表明在所采用的水热合成条件下,葡萄糖原位发生了芳构化和碳化,相似的结果已于复合材料NiAl-LDH/C[10]的制备研究中被报道。图1为在含不同量葡萄糖的合成体系中所制备的C/MgAl水滑石复合材料的XRD图,从图中可以看出,各样品均显示了对应于水滑石的特征衍射峰,但同MgAl-HT相比,在含葡萄糖的合成体系中所得到的C/MgAl-HT-x样品的衍射峰的强度变弱、峰形宽化,出现了MgCO3杂晶相(PDF 86-2348),且随着合成体系中葡萄糖含量的增加,所制样品衍射峰强度进一步变弱、峰形进一步宽化,MgCO3杂晶含量进一步增多。MgCO3杂晶相的产生是由于引入到合成体系中的葡萄糖在芳构化和碳化过程中伴随有部分CO2的生成[11],随着葡萄糖引入量的增加,CO2生成量增大,进而导致MgCO3杂晶量的增加。C/MgAl-HT-x复合材料XRD衍射峰强度减弱和峰形宽化可能由以下3个主要原因所导致:一是水滑石合成体系中由葡萄糖碳化形成的碳充当了MgAl-HT结晶相的“稀释剂”[10];二是原位生成的碳抑制了HT微晶的生长,从而使得C/MgAl-HT-x的晶粒尺寸减小[10];三是其它晶相的形成。
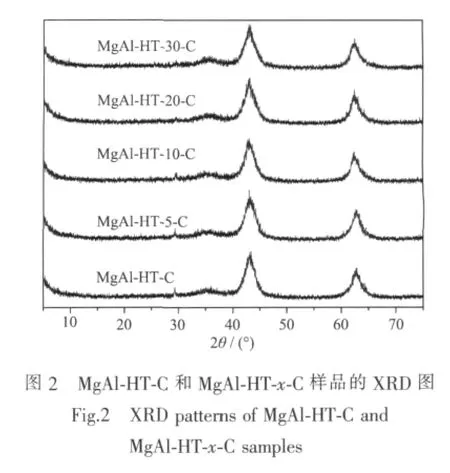
在550℃于空气气氛下焙烧3 h后,C/MgAl-HT-x样品的颜色由起始棕色变为白色,表明在此焙烧条件下可将在水热条件下形成的碳有效除去。图2为焙烧后样品的XRD图。从图中可以看出,经焙烧后所制不同样品的水滑石特征衍射峰均消失,同时在2θ=43°和63°两处出现了镁铝复合金属氧化物的衍射峰。
2.2 焙烧再水合后不同样品的表征
尽管在柠檬醛-丙酮缩合反应中所使用的催化剂为水滑石的焙烧产物,但由于所选用的反应体系中含水,焙烧后的水滑石衍生氧化物在该反应体系中会水合重构为插层阴离子为OH-的水滑石,因此对焙烧样品在丙酮和水(20 mL丙酮和3 mL水)混合物中的重构样品进行了XRD、N2吸附-脱附和碱性能表征。XRD测试(图3)表明,经水合后所得样品的XRD图中均出现了水滑石的特征衍射峰,表明不论以何种体系下合成的HT为前驱物,经焙烧所形成的MgAl混合氧化物在所采用的水合条件下均能有效地水合,恢复其层状结构。但同MgAl-HT经焙烧水合后所形成的水滑石相比,以C/MgAl-HT-x为前驱物所得样品的XRD(003)和(006)衍射峰强度明显减弱,峰宽变大,并随着前驱物中碳含量的增加,这些变化趋于更加显著。对于水滑石材料来说,(003)和(006)衍射峰的强度大小通常同其层板排列的有序度相关[12],(003)和(006)衍射峰强度的降低和衍射峰宽化表明以C/MgAl-HT-x为前驱物所得MgAl-HT-x-rh样品的层状结构发生扭曲,层状结构的有序度下降。不同于(003)和(006)衍射峰的变化,对于以C/MgAl-HT-x为前驱物所得样品,表征其水滑石层板二维晶体结构有序性和层板组成的(110)衍射峰的位置和强度,与以MgAl-HT水滑石为前驱物所得到的样品相比,并未发生明显变化。
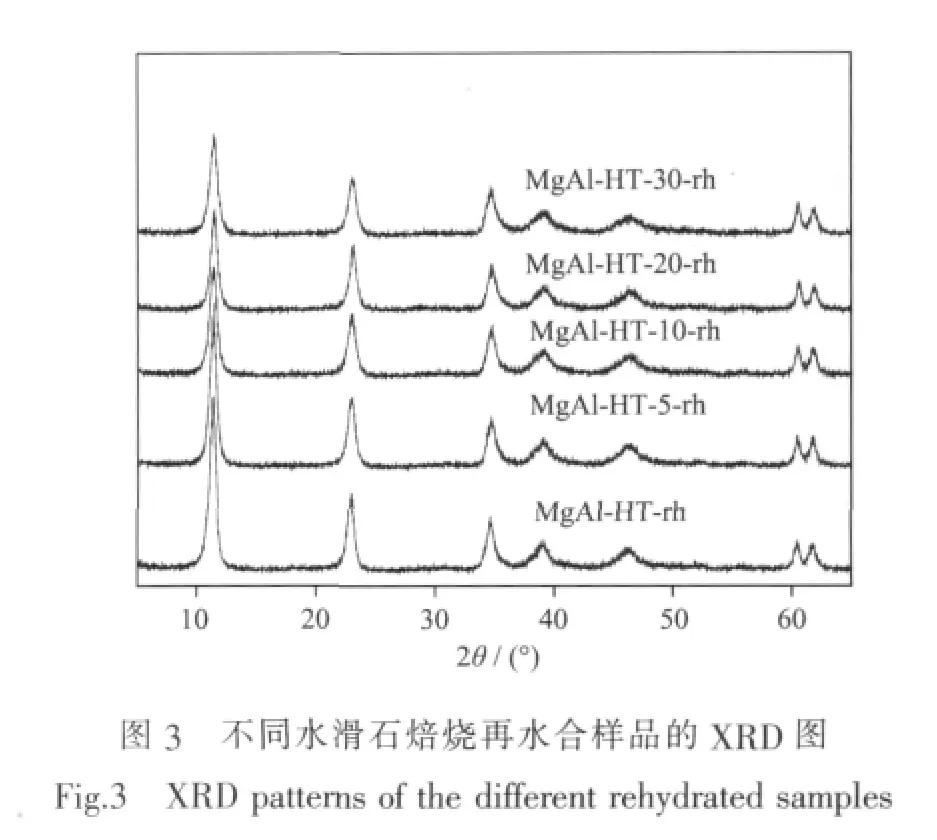
表1为以不同MgAl水滑石为前驱物所制备的meixnerite样品的物化性能。ICP元素分析结果表明,所制备水滑石经焙烧后的MgAl复合金属氧化物样品中镁铝物质的量的比接近于3,这与其前驱体水滑石合成过程中原料加入时的Mg/Al物质的量的比十分接近,这表明在葡萄糖存在的水滑石合成体系中镁铝两种盐均匀且完全沉淀。N2吸附-脱附测试结果表明,所制得的水合产物其比表面积和孔结构表现出较大区别。样品MgAl-HT-x-rh的比表面积均大于MgAl-HT-rh,且随着前驱物中碳含量的增加而呈现最佳值,其中MgAl-HT-20-rh样品具有最大的比表面积,比表面的增加,可提高暴露的OH-的数目。从各焙烧产物在水中测得的pH值可看到,不同水合样品的碱强度十分相近,表明MgAl水滑石前驱物的性质的不同并不会对其焙烧水合产物的样品的碱强度产生显著影响,但从苯甲酸滴定结果可看到,水滑石前驱物的性质对其焙烧水合产物的碱性位的数目有很大影响。碱性位数也随着前驱物中碳含量的增加而呈现最佳值,其中MgAl-HT-20-rh的可测得的碱性位数目最多,这一现象同 Winter等[7]的报道结果相一致。他们采用焙烧水合法和离子交换法制备了meixnerite样品,通过测定CO2在水合活化样品碱性位上的吸附量和吸附焓来表征样品的碱量和碱强度,结果表明不同的活化手段主要影响样品碱性位的可接近性,而不影响所制活化样品的碱强度。对于经焙烧水合重构的水滑石样品其碱性位的数目同样品中Al3+的数目相关,Al3+的数目与补偿阴离子(compensating anions)的数目成正比。ICP测试表明,以不同MgAl水滑石为前驱物所制备的样品的Al含量相当,因而其所检测到碱量的显著差异同碱性位的可接近性相关,对以C/MgAl-HT-x为前驱物所制备的样品,其较高的碱性位数目同其较大的比表面积和水合后的层状结构的有序度下降相关。
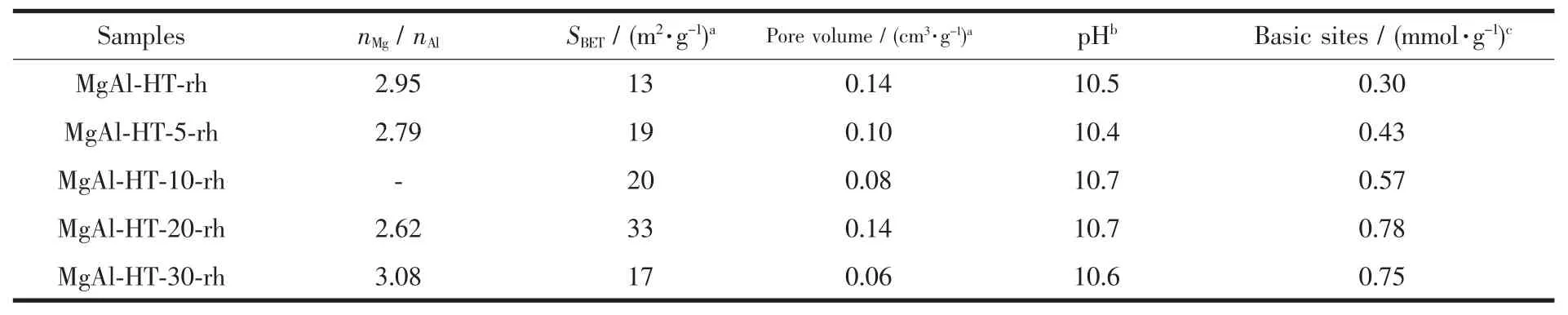
表1 MgAl-HT-rh和MgAl-HT-x-rh样品的物理化学性质Table 1 Physicochemical properties of MgAl-HT-rh and MgAl-HT-x-rh samples
2.3 催化性能
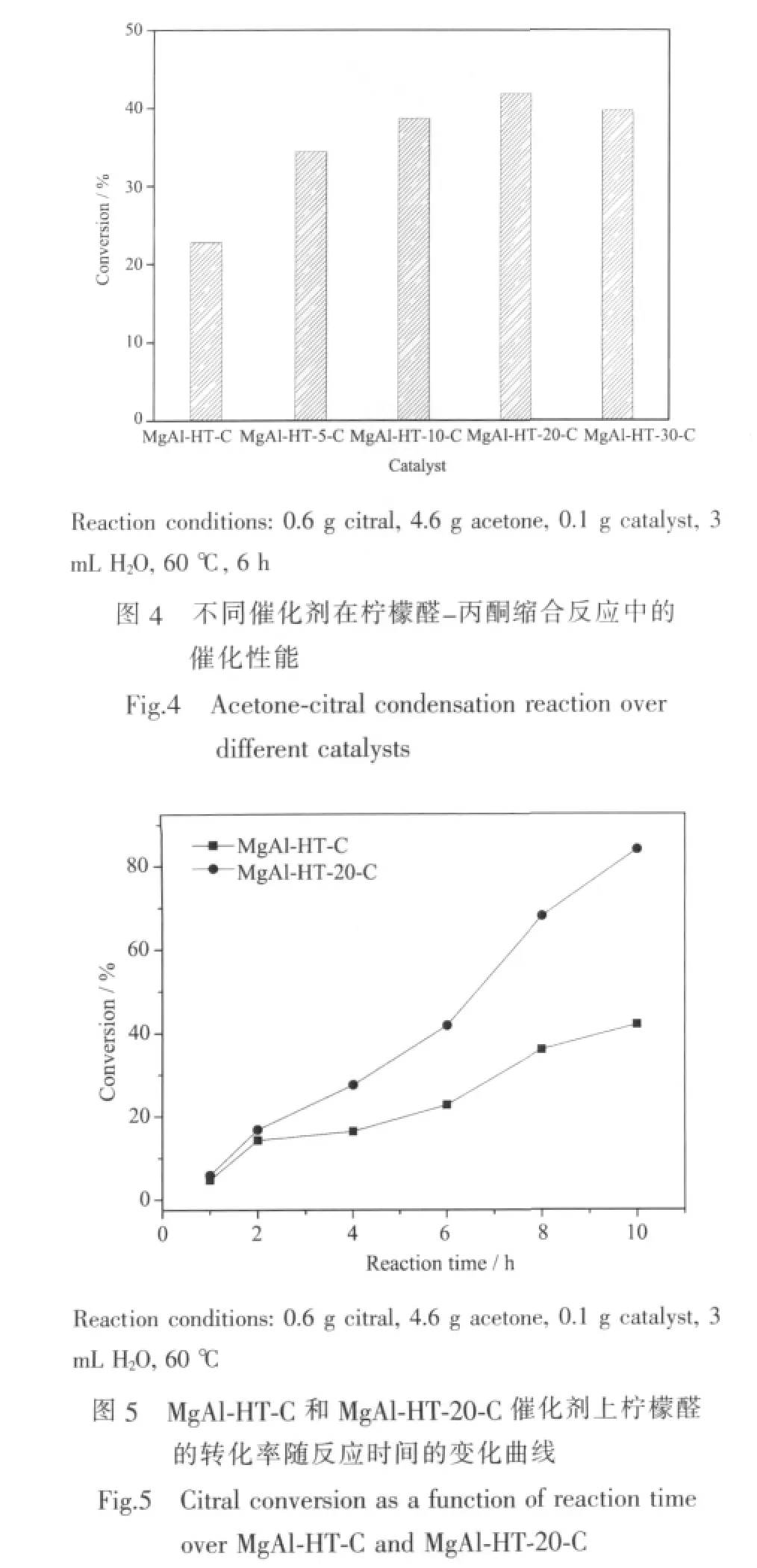
图4为以C/MgAl-HT-x和MgAl-HT为前驱物所制MgAl复合金属氧化物在含水的反应体系中对柠檬醛-丙酮缩合反应的催化结果。由图可见,合成体系中葡萄糖的引入对所制MgAl水滑石的焙烧水合产物的催化性能有很大影响。在相同的反应条件下,以C/MgAl-HT-x为前驱物所制系列催化剂的催化活性明显高于以MgAl-HT为前驱物所制备的催化剂,且随着合成体系中葡萄糖引入量的增加出现最佳值。以C/MgAl-HT-20为前驱物所制备的催化剂在反应中表现出最高的催化活性,柠檬醛的转化率达到42%,而以MgAl-HT为前驱物所制备的催化剂参加反应时,柠檬醛的转化率仅为23%左右。不同催化剂的催化活性的高低同其比表面积和可接近的碱性位数目的多少基本相一致。
以C/MgAl-HT-x和MgAl-HT为前驱物所制MgAl复合金属氧化物在含水的反应体系中对柠檬醛-丙酮缩合反应催化活性的差异随着反应的不断进行趋于更加显著。图5为反应时间对不同催化剂样品在柠檬醛-丙酮缩合反应中催化活性的影响。由图可以看出,MgAl-HT-20-C和MgAl-HT-C两种催化剂的催化活性均随反应时间的变化趋势也有所差异,虽然二者的反应活性均随反应的不断进行呈现递增趋势,但以MgAl-HT-20-C为催化剂时柠檬醛转化率递增的幅度要明显大于以MgAl-HT-C作为催化剂时的转化率增幅,前者几乎呈线性增加。当反应时间达到10 h时,MgAl-HT-20-C催化剂的反应活性达到84%,而MgAl-HT-C在10 h时活性仅为42%。在所采用的反应条件下,假紫罗酮的选择性基本不随反应时间的变化而变化并始终保持在90%以上。
3 结 论
在含不同量葡萄糖的合成体系中可制备C/MgAl水滑石复合材料,以C/MgAl水滑石复合材料为前驱物所制备的焙烧产物在含水的柠檬醛-丙酮缩合反应体系中的催化活性高于以常规的MgAl水滑石为前驱物所制备的催化剂。这是由于同以常规MgAl水滑石为前驱物经焙烧和水合所形成的产物相比,以C/MgAl水滑石复合材料为前驱物所制备的水合产物的比表面增大和层状结构的有序度下降,这些导致以C/MgAl水滑石复合材料为前驱物所制备的水合产物具有更多的可接近的碱性位。
[1]Reichle WT.J.Catal.,1985,94(2):547-557
[2]Beres A,Palinko I,Kiricsi I,et al.Appl.Catal.A:Gen.,1999,182(2):237-247
[3]Choudary B M,Kantam M L,Reddy C R V,et al.J.Mol.Catal.A:Chem.,1999,146(1/2):279-284
[4]Díez V K,Di Cosimo J I,Apesteguía C R.Appl.Catal.A:Gen.,2008,345(2):143-151
[5]Fraile J M,García N,Mayoral J A,et al.Appl.Catal.A:Gen.,2009,364(1/2):87-94
[6]AbellóS,Medina F,Tichit D,et al.Appl.Catal.A:Gen.,2005,281(1/2):191-198
[7]Winter F,Xia X Y,Hereijgers B PC,et al.J.Phys.Chem.B,2006,110(18):9211-9218
[8]Sharma S K,Parikh P A,Jasra R V.Appl.Catal.A:Gen.,2010,386(1/2):34-42.
[9]NI Zhe-Ming(倪哲明),FU Xiao-Wei(付晓微),XUE Ji-Long(薛继龙)et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2012,28(3):471-476
[10]Xiang X,Hima H I,Wang H,et al.Chem.Mater.,2008,20(3):1173-1182
[11]Wang J,Jing X Y,Wang J,et al.Solid State Sci.,2010,12(12):1934-1940
[12]Chimentão R J,AbellóS,Medina F.J.Catal.,2007,252(2):249-257
