空腹血糖水平与胰岛素抵抗关系的分析
2013-09-14仲彬
仲彬
南京市市级机关医院内分泌科,江苏南京 210000
糖尿病(diabetes mellitus)是一组以慢性血葡萄糖(简称血糖)水平增高为特征的代谢疾病群,其患病率随着人民生活水平的提高,生活方式的改变迅速增加,已成为发达国家中继心血管病和肿瘤之后的第3大非传染性疾病,它可引起多系统损害,导致眼、肾、神经、心脏、血管等组织的慢性进行性改变,引起功能缺陷及衰竭,严重威胁着人类健康,因此早期及时发现糖尿病易患人群,尽早采取相应的干预措施显得尤为重要,这样就可以降低糖尿病的患病率,降低糖尿病大血管及微血管并发症的发生率。
胰岛素抵抗和胰岛B 细胞分泌缺陷是2型糖尿病(T2DM)发病机制中重要的病理生理改变[1-2]。糖耐量低减(IGT)/空腹血糖受损(IFG)同属于正常糖代谢和糖尿病之间的中间状态,被称为糖尿病前期[3]。任何一个糖尿病者在发病过程中均可经过IFG/IGT 阶段,只是或长或短而已。作为不同的糖调节受损类型,IFG 和IGT 都存在胰岛素抵抗和胰岛B 细胞分泌缺陷,但是二者的代谢缺陷不同,其中IFG 与基础胰岛素分泌缺陷和肝脏胰岛素抵抗更相关,而IGT 与外周组织(脂肪、肌肉等)胰岛素抵抗和胰岛B 细胞早时相分泌缺陷关系更密切。IFG的早期诊断对于糖尿病和心血管疾病的防治十分重要,确立IFG的诊断标准更是意义深远。本文主要研究:①比较不同空腹血糖人群代谢特征的差异;②比较不同空腹血糖人群胰岛素抵抗和胰岛B 细胞分泌功能的差异;③空腹血糖受损与胰岛素抵抗和胰岛B 细胞分泌功能的相关关系。
表1 不同空腹血糖人群的临床特征的比较(±s)
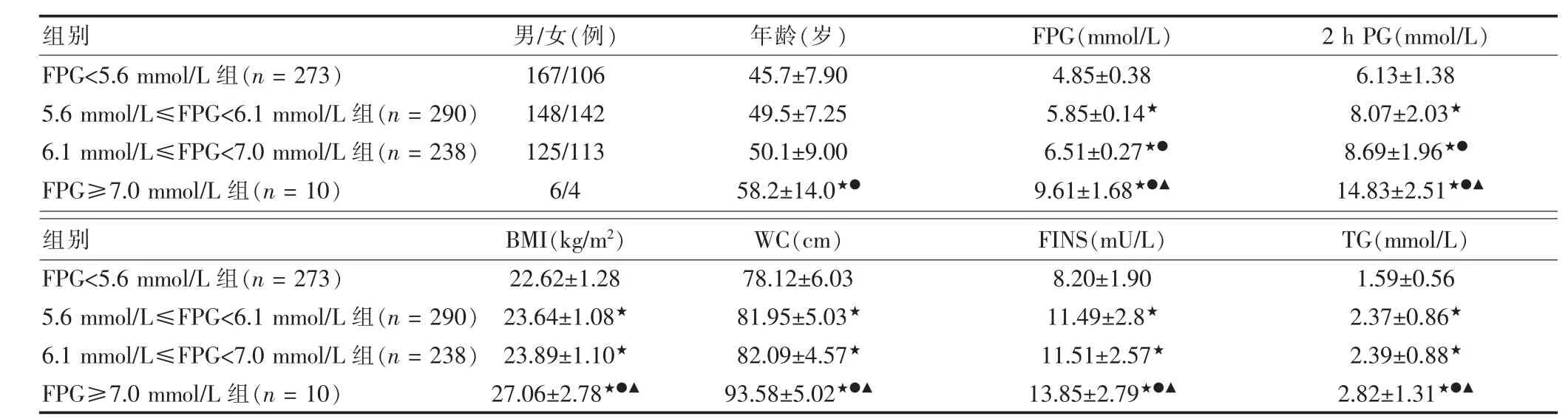
表1 不同空腹血糖人群的临床特征的比较(±s)
注:与FPG<5.6 mmol/L 组比较,★P<0.05;与 5.6 mmol/L≤FPG<6.1 mmol/L 组比较,●P<0.05;与 6.1 mmol/L≤FPG<7.0 mmol/L 组比较,▲P<0.05;FPG:空腹血糖;2 hPG:餐后 2 h 血糖;BMI:体重指数;WC:腰围;FINS:空腹胰岛素;TG:三酰甘油
组别 男/女(例)年龄(岁)FPG(mmol/L)2 h PG(mmol/L)FPG<5.6 mmol/L 组(n=273)5.6 mmol/L≤FPG<6.1 mmol/L 组(n=290)6.1 mmol/L≤FPG<7.0 mmol/L 组(n=238)FPG≥7.0 mmol/L 组(n=10)组别FPG<5.6 mmol/L 组(n=273)5.6 mmol/L≤FPG<6.1 mmol/L 组(n=290)6.1 mmol/L≤FPG<7.0 mmol/L 组(n=238)FPG≥7.0 mmol/L 组(n=10)167/106 148/142 125/113 6/4 BMI(kg/m2)22.62±1.28 23.64 ±1.08★23.89 ±1.10★27.06±2.78★●▲45.7±7.90 49.5±7.25 50.1±9.00 58.2±14.0★●WC(cm)78.12±6.03 81.95±5.03★82.09±4.57★93.58±5.02★●▲4.85±0.38 5.85±0.14★6.51±0.27★●9.61 ±1.68★●▲FINS(mU/L)8.20±1.90 11.49 ±2.8★11.51±2.57★13.85±2.79★●▲6.13±1.38 8.07±2.03★8.69±1.96★●14.83±2.51★●▲TG(mmol/L)1.59±0.56 2.37±0.86★2.39±0.88★2.82±1.31★●▲
1 资料与方法
1.1 一般资料
对象为2008年1月~2009年1月于江苏省盐城市第一人民医院体检中心接受体检的人群,其中口服糖耐量试验(OGTT)资料完整且既往无糖尿病者共811例,其中,男446 例,女 365 例;年龄 25~78 岁,平均(48.5±8.4)岁。入选标准:所有入选者行75 g 口服葡萄糖耐量试验,自愿参加。排除标准:排除继发性糖尿病、1型糖尿病、妊娠和哺乳者、严重的肝肾功能障碍、口服影响糖代谢的药物。
1.2 主要仪器与试剂
血浆葡萄糖测定采用葡萄糖氧化酶法,血脂测定应用酶法。胰岛素测定由江苏省盐城市第一人民医院核医学实验室以化学发光法测定,药盒由北京原子能科学研究所提供,检测过程严格按照试剂说明书进行。
1.3 方法
1.3.1 研究设计 受检者常规测量身高、体重,测定腰围(WC):受试者取立位,双脚分开 25~30 cm,使体重均匀分配,用一根没有弹性、最小刻度为1 mm的软尺放在右侧腋中线髂嵴上缘与第12 肋骨下缘连线的中点,沿水平方向围绕腹部1周,紧贴而不压迫皮肤,在平静呼吸末测量WC的长度,WC 读数精确至1 mm。所有研究对象早晨7∶00(空腹 8 h 后)测定空腹血糖(FPG)、空腹胰岛素(FINS)、三酰甘油(TG),接受 OGTT 试验,测定餐后 2 h 空血糖(2 h PG)。
1.3.2 分组 空腹血糖(FPG)正常组A:FPG<5.6 mmol/L组,共 273 例,其中,男 167 例,女 106 例;平均年龄(45.7±7.9)岁。新增 FPG 受损组 B:5.6 mmol/L≤FPG<6.1 mmol/L组,共290 例,其中,男 148 例,女 142 例;平均年龄(49.5±7.2)岁。传统 FPG 受损组 C:6.1 mmol/L≤FPG<7.0 mmol/L组,共238 例,其中,男 125 例,女 113 例;平均年龄(50.1±9.0)岁。糖尿病组D:FPG≥7.0 mmol/L组,共10例,其中,男6例,女 4 例;平均年龄(58.2±14.0)岁。
1.3.3 有关参数的计算方法 体重指数(BMI)=体重(kg)/身高(m2);用稳态模型胰岛素抵抗指数(HOMA-IR)=(FPG×FINS)/22.5,作为胰岛素抵抗指标,胰岛B 细胞功能指数(HOMA-B)=20×FINS/(FPG-3.5)作为基础胰岛素分泌指标。
1.4 统计学方法
采用SPSS 11.0 统计软件进行统计分析。所有计量资料进行正态性、方差齐性检验,非正态及方差不齐者,进行对数转换,计量资料数据以均数±标准差(±s)表示,多组计量资料间差异性研究用方差分析,相关分析采用偏相关分析。以P<0.05 为差异有统计学意义。
2 结果
2.1 不同空腹血糖人群的临床特征的比较
4组性别分布相似。随着FPG水平的升高,年龄、BMI、WC、TG、FINS、2 h PG 逐步上升,与 FPG <5.6 mmol/L 组比较,差异均有统计学意义(均P<0.05),进一步与5.6 mmol/L≤FPG<6.1 mmol/L 组比较显示:6.1 mmol/L≤FPG<7.0 mmol/L组与 5.6 mmol/L≤FPG<6.1 mmol/L 组,BMI、WC、TG、FINS、2 h PG 无明显差异(P>0.05);FPG≥7.0 mmol/L组 BMI、WC、TG、FINS、2 h PG 明 显 高 于 5.6 mmol/L≤FPG<6.1 mmol/L组。见表1。
2.2 不同空腹血糖人群胰岛素抵抗和胰岛B 细胞分泌功能的比较
胰岛素抵抗:校正年龄、性别、BMI后,随着空腹血糖的升高,HOMA-IR 呈上升趋势,两两比较显示,5.6 mmol/L≤FPG<6.1 mmol/L组与 6.1 mmol/L≤FPG<7.0 mmol/L组HOMA-IR 高于 FPG<5.6 mmol/L组(P< 0.05),其中以糖尿病组 HOMA-IR 最高(P<0.05),而 5.6 mmol/L≤FPG<6.1 mmol/L组与 6.1 mmol/L≤FPG<7.0 mmol/L组 间HOMA-IR 无明显差异(P>0.05)。基础胰岛素分泌:校正年龄、性别、BMI、HOMA-IR后,随着空腹血糖的升高,HOMA-B 呈逐渐降低趋势,各组间差异均有统计学意义(均P<0.05)。两两比较显示,5.6 mmol/L≤FPG<6.1 mmol/L组低于FPG<5.6 mmol/L组(P<0.05), 其中以糖尿病组HOMA-B 最低(P<0.05)。见表2。
表2 不同空腹血糖人群胰岛素抵抗和胰岛素分泌功能的比较(±s)

表2 不同空腹血糖人群胰岛素抵抗和胰岛素分泌功能的比较(±s)
注:与 FPG<5.6 mmol/L 组比较,★P<0.05;与 5.6 mmol/L≤FPG<6.1 mmol/L组比较,●P<0.05;与 6.1 mmol/L≤FPG<7.0 mmol/L组比较,▲P<0.05;FPG:空腹血糖;HOMA-IR:稳态模型胰岛素抵抗指数;HOMA-B:胰岛B 细胞功能指数
组别 HOMA-IR HOMA-B FPG<5.6 mmol/L 组(n=273)5.6 mmol/L≤FPG<6.1 mmol/L 组(n=290)6.1 mmol/L≤FPG<7.0 mmol/L 组(n=238)FPG≥7.0 mmol/L 组(n=10)0.24±0.09 0.46±0.10★0.51±0.10★0.76±0.06★●▲2.09±0.13 1.97 ±0.09★1.87 ±0.08★●1.66±0.19★●▲
2.3 新切点下的FPG 受损(5.6 mmol/L≤FPG<7.0 mmol/L)与HOMA-IR、HOMA-B的相关关系
相关分析发现新切点下的空腹血糖受损与HOMA-IR具有显著的正相关(r=0.52,P<0.01),而与 HOMA-B 呈负相关(r=-0.34,P<0.01),说明胰岛素抵抗与糖代谢紊乱密切相关。
3 讨论
在代谢综合征(metabolic syndrome,MS)及胰岛素抵抗的定义中,血糖异常都有其特殊重要的意义[4]。而对FPG正常值的切点(cut point)定义均采用了美国糖尿病协会(ADA)1997年提出的6.1 mmol/L 标准,我国糖尿病学会也于1999年10月采用了这一标准。随着近年来糖尿病研究的进展,ADA 糖尿病诊断与分类专家委员会于2003年年底再次对糖尿病的诊断提出了新的建议,就是将IFG 受损的FPG 切点值从6.1 mmol/L 降至5.6 mmol/L。从发病机制上来看,T2DM的病因和发病机制是包括遗传及环境因素在内的多种因素共同作用的结果。胰岛素抵抗和胰岛B 细胞功能缺陷是T2DM 发病机制的两大机制,同时也有多项研究表明,胰岛B 细胞的异常可能是T2DM 发病的中心环节[5-6]。胰岛素抵抗是T2DM 发生的始动因素,而胰岛B 细胞功能正常与否则是T2DM是否发生的决定因素。胰岛素抵抗的发生启动了T2DM的发病历程,但如果胰岛B 细胞能保持其代偿能力,T2DM 并不会发生,一旦其代偿能力下降,则T2DM 逐渐发生。Huan等在对174名非糖尿病年轻美国黑人进行纵向研究中采用高胰岛素。正葡萄糖钳夹技术评价胰岛素抵抗程度。随访8年,证实胰岛素抵抗组较胰岛素敏感(IS)组高血压(包括舒张压及收缩压)、血脂谱异常(低密度脂蛋白明显增高)的患病风险加大,胰岛素抵抗不仅可预示该类人群今后有糖代谢异常及糖尿病患病风险.同时心血管疾病患病风险也明显增高。文献报道研究显示HOMA-IR 和心血管事件的发生有很好的相关性[33]。本研究结果显示新切点下的空腹血糖受损人群已经可出现HOMA-IR的升高,提示应当重视对该人群心血管事件的防治工作,同时也再次佐证了在中国人群中将IFG诊断下限值从6.1 mmol/L 降至5.6 mmol/L的合理性与必要性。
本研究中相关性研究发现随着FPG的增加,HOMAIR 呈线性升高,HOMA-B 呈线性降低,且HOMA-IR 相关系数要高于HOMA-B,说明胰岛素抵抗与糖代谢紊乱密切相关。本研究中,5.6 mmol/L≤FPG<6.1 mmol/L 人群和FPG<5.6 mmol/L 人群比较,其 BMI、WC、TG 已出现了明显的差异,可以推测空腹血糖受损切点下调至5.6 mmol/L,已出现明显胰岛素抵抗,其可能的原因为肥胖、高TG。高TG血症往往与肥胖相伴而生,脂肪细胞肥大、增生,使胰岛素受体数目和活性相对下降,表现为胰岛素抵抗。国外文献报道,血TG/高密度脂蛋白胆固醇(TG/HDL-C)比值与胰岛素抵抗之间有显著关系,TG 及TG/HDL-C 比值与HOMAIR 存在密切的相关性,是反映胰岛素抵抗的理想血脂指标[7-8]。
综上所述,胰岛素抵抗是空腹血糖受损的独立危险因素。越来越多的研究证实了胰岛素抵抗在糖尿病、心脑血管病前瞻性研究中的重要性,而利用空腹血糖、空腹胰岛素及HOMA-B等简单指标进行宣教尤为重要[9],它对指导人们改变不合理饮食结构和生活习惯,更多地进行锻炼,保持良好的体态,避免发生代谢异常,从而降低糖尿病、心脑血管疾病的患病率,具有十分重要的社会意义。
[1]Cheal KL,Abbasi F,Lamendola C,et al.Relationship to insulin resistance of the adult treatment panelⅢdiagnostic criteria for identification of the metabolic syndrome [J].Diabetes,2004,53(5):1195-1200.
[2]Gazzaruso C,Solerte SB,De Amiei E,et al.Association of the metabolic syndromeand insulin resistance with silent myocardial is chemia in patients with type 2 diabetesmellitus[J].Am J Cardiol,2006,97(2):236-239.
[3]The Expert committee on Diagnosis and Classification of Diabetes Mellitus.Follow-up report on the diagnosis of diabetes mellitus[J].Diabetes Care,2004,27:s5-s10.
[4]Crundy SM,Brewer HB,Cleeman J,et al.Defimtion of metabolic syndrome:report of the National Heart,Lung,and Blood Institute American Heart Association conference on scientitle issues related to definition[J].Circulation,2004,109(3):433-438.
[5]Gerasi E.胰岛素生成,胰岛素分泌及2型糖尿病:问题的核心在于B 细胞[J].中华内分泌代谢杂志,2005,21(3):194-198.
[6]赵家伟,马凤海,罗梅,等.胰岛B 细胞胰岛素抵抗的证据[J].中华内分泌代谢杂志,2005,21(4):4-5.
[7]Henning B,Meerarani P,Ramadass P,et al.Fattyacidmediated activation endothelial cells[J].Metabolism,2000,49(10):1006-1013.
[8]Braschi S.Postprandial hyperlipdemia small and dense LDL-HDL sub-fractions[J].Ann Med Intern,2001,152(3):162-168.
[9]Goodman E, Daniels SR,Lawrence M.et al.Socioeconomic disparities in insulin resistance:results from the princeton school district study[J].Psychosom Med,2007,69:61-67.
