达里诺尔湖沉积物中无机碳的形态组成
2013-09-11孙园园吕昌伟樊明德任丽敏
孙园园,何 江,2,* ,吕昌伟,2,王 维,2,樊明德,2,任丽敏,麻 涛
(1.内蒙古大学环境与资源学院,呼和浩特 010021;2.内蒙古大学环境地质研究所,呼和浩特 010021)
碳是最主要的生源要素,它以CO2、CH4、碳酸盐及有机化合物等多种形式在环境中不断循环。碳循环是生物圈健康发展的重要标志,是全球变化研究的热点[1]。湖泊碳循环是陆地生态系统碳循环的重要组成部分。湖泊是流域内降水和冲刷物质(面源)、排放物质(点源)和悬浮物质(雨水吸附)的集聚地,是流域产生的溶解碳、颗粒碳及各种营养盐的最终汇集场所[2]。湖泊生态系统具有生物地球化学过程活跃、生物生产力高、生物泵功能强大等特点[3]。
沉积物是全球碳的重要源与汇,在碳循环中起重要作用。无机碳在沉积物中占有相当份额,在全球碳循环中扮演重要角色。沉积物在碳循环中的作用与沉积物中无机碳的形态分布密切相关。不同形态无机碳在碳循环中的作用及再循环能力不同,沉积物中无机碳形态及其变化对湖泊水-沉积物界面的碳通量及碳过程起关键控制作用,无机碳形态研究是探讨无机碳在碳循环中作用的基础和前提[4]。沉积物中无机碳主要以不同形态的碳酸盐矿物存在(如方解石、文石、白铅矿、角铅矿、菱锌矿、菱镁矿、菱锰矿、菱钴矿等)[5],根据其在不同pH介质中的溶解能力将沉积物中的无机碳分为NaCl相、NH3·H2O相、NaOH相、NH2OH·HCl相和HCl相无机碳,不同形态的无机碳在沉积物中的结合强度不同。近年来,国内外学者取得了沉积物中无机碳总量及其空间分布等一系列研究成果[6-7],虽然无机碳总量研究对恢复和重建地质历史时期古气候环境演化等是必要的,但不能为沉积物中无机碳的变化过程及其在碳循环中作用的研究提供有价值信息[8]。
内蒙古高原湖区地处内陆干旱半干旱区,地表径流对湖泊的补给水量少而蒸发量大,湖泊不断向咸水湖或盐湖方向演化[9]。内蒙古高原湖泊湿地资源丰富,类型多样,在我国湖泊湿地整体研究中占有重要位置。本文以地处半湿润半干旱区的达里诺尔湖(Dali Lake,DLNE)为研究对象,开展了沉积物中无机碳的形态组成研究,综合分析了表层沉积物与沉积柱芯中无机碳的形态分布特征,探讨了沉积物中不同形态生源要素与无机碳的相互关系,以期为探讨无机碳形态对湖泊生态系统碳循环的贡献,评价内蒙古高原区湖泊沉积物的碳源汇功能和强度,厘定内蒙古高原湖泊碳的时空分布格局,合理开发与保护利用湖泊湿地资源提供科学依据,为湖泊湿地碳循环研究积累基础资料。
1 研究区域与研究方法
1.1 研究区概况
达里诺尔湖(E116°26'—116°45',N43°13'—43°23')位于内蒙古自治区赤峰市克什克腾旗西部,南依浑善达克沙地,是内蒙古四大湖泊之一。湖泊面积约228 km2,湖盆东浅西深(图1),平均水深6.8 m,最大水深13 m,储水量约1.6×109m3。湖区位处中温带半湿润和半干旱区过渡带,年降水量350—400 mm,年蒸发量1287 mm[10]。达里诺尔湖属堰塞湖,无外流河流,湖泊补给水源主要来自贡格尔河、沙里河、耗来河、亮子河等入湖河流(图2)及地下水和雨水,湖水的主要损耗方式为蒸发。该湖为碳酸盐型半咸水湖泊,水质类型为碳酸钠Ⅰ型水,盐分以碳酸盐为主,总碱度高达53.57 mmol/L,pH值9.3—9.6。近年来,由于气候干旱和人类活动的影响,水位连年下降,湖泊面积逐年萎缩,水质盐碱度不断增高,富营养化程度日益加剧[11-13],对达里诺尔国家自然保护区内的珍稀候鸟、渔业生产以及周边区域的可持续发展构成了潜在威胁和风险。
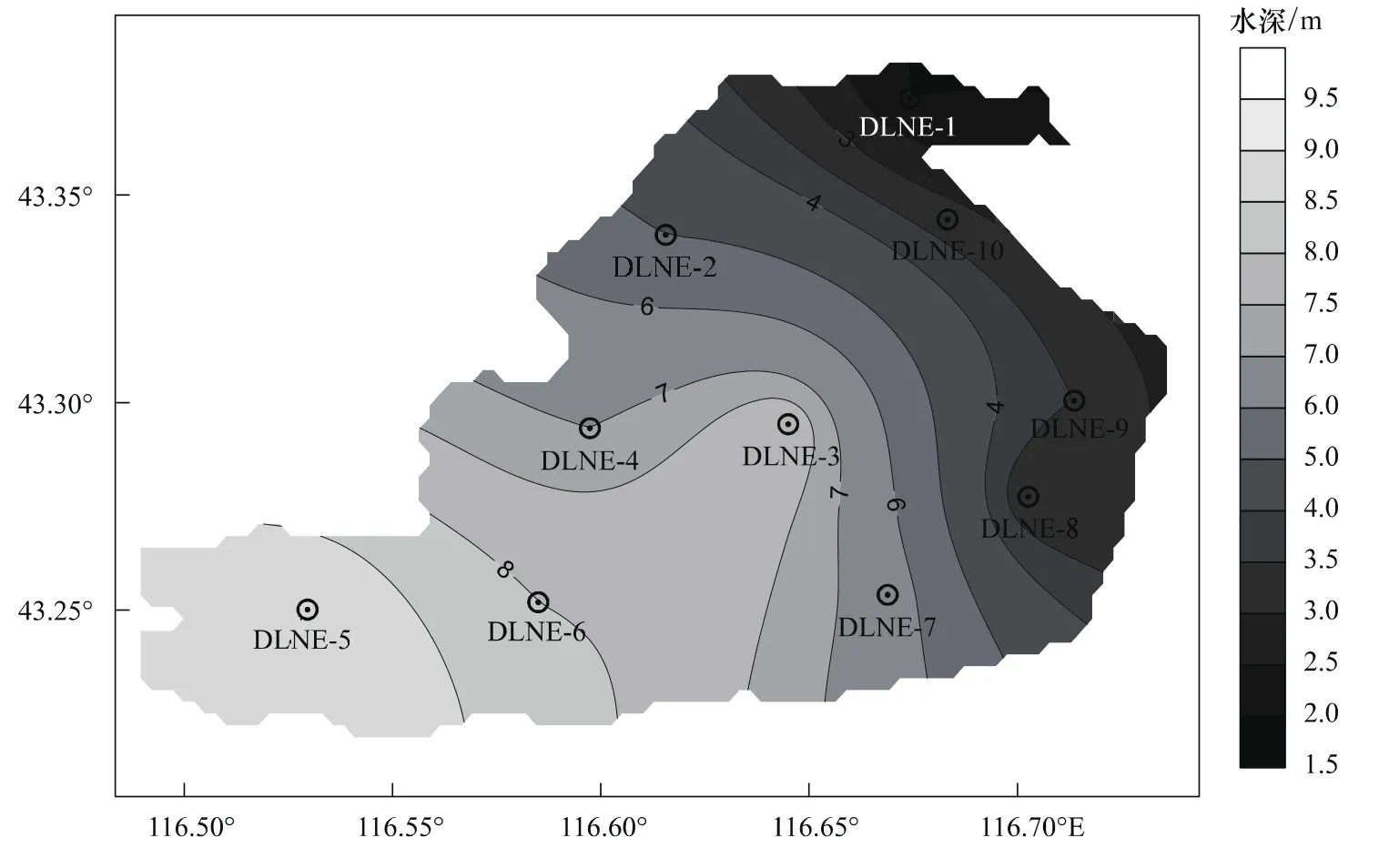
图1 达里诺尔湖水深分布图Fig.1 The water depth gradient of Dali Lake
1.2 样品采集及分析方法
依据《湖泊生态系统观测方法》,针对达里诺尔湖现有水域面积及湖泊生态系统类型设置采样点。于2008年8月对达里诺尔湖进行了系统的现场监测和样品采集(图2)。沉积物柱芯样视湖泊深度分别用挪威Swedaq公司产KC mod A och B型无扰动采样器和荷兰Eijkelkamp公司产SA Beeker型沉积物原状采样器采集,现场以2 cm间隔分层。沉积物样品装入封口聚乙烯塑料袋后冷藏保存,回实验室于-24℃冷冻保存。采样点用GPS定位。
无机碳的形态提取按文献[14]的方法进行,具体步骤见表1。实验在25℃下进行,CO2含量用容量法测定。实验过程中同时进行空白样和平行样测定,相对标准偏差均<10%。上覆水钙的测定采用原子吸收分光光度法(GB11905-89),碱度的测定采用酸碱指示剂滴定法(HZHJSZ0130),pH值的测定采用玻璃电极法(GB6920-86),其它营养盐指标为本小组前期研究成果。表层沉积物中各指标的空间分布图均用Surfer 8.0完成,相关性分析用SPSS 16.0完成,其它数据处理均用Excel 2003完成。

表1 沉积物中无机碳的形态提取Table 1 Sequential extraction method of inorganic carbon in sediments

图2 达里诺尔湖流域水系及采样站位分布图Fig.2 Locations of sampling points in the Dali Lake
2 结果与讨论
2.1 表层沉积物(0—10 cm)中无机碳形态的分布特征
表层沉积物中各形态无机碳含量见表2。NH2OH·HCl相为表层沉积物中无机碳的主导形态,占总量的百分比范围在 72.20%—90.69%,平均82.77%,占绝对优势,其余4相无机碳含量均较低,四者之和占总无机碳的百分比不足20%(图3)。表层沉积物中各形态无机碳的平均含量序列为NH2OH·HCl相>HCl相>NaCl相>NH3·H2O 相>NaOH 相,与本小组前期对乌梁素海及岱海的研究结果类似[4]。与武汉东湖[15]、辽东湾[8]及渤海湾北部和西部[16]相比,达里诺尔湖表层沉积物中无机碳的含量高于前者。武汉东湖、辽东湾及渤海湾北部和西部均属我国湿润半湿润气候区,区内接受来自周边河流的大量物质输入,地表冲刷作用均强于位于内陆的达里诺尔湖,陆源物质的输入稀释了沉积物中的无机碳而导致无机碳含量较低。此外,达里诺尔湖位于半湿润和半干旱区过渡带,水体蒸发浓缩作用强烈,从而导致湖水对碳酸钙过饱和度增加及较多的湖泊自生碳酸盐沉淀。

图3 达里诺尔湖表层沉积物中无机碳的形态分布特征Fig.3 Speciation distribution of inorganic carbon in surface sediments

表2 达里诺尔湖表层沉积物中不同形态无机碳的含量(n=9)Table 2 Speciation concentration of inorganic carbon in surface sediments
贡格尔河、沙里河是湖泊第一和第二大供给河流,分别从湖区东北部和东部入湖,但无机碳的空间分布却呈现东低西高的趋势(图4)。大量碎屑沉积物的注入对碳酸盐沉淀具有较强的稀释作用,从而不利于湖泊自生碳酸盐沉淀[17]。统计分析结果表明,水深与无机碳具有良好的正相关性(R2=0.86,P<0.01),即随水深增大,离湖岸距离越远,陆源碎屑物质逐渐减少,碳酸盐含量逐渐增大。这与湖盆西深东浅(图1)及无机碳空间分布的客观事实相一致,揭示入湖河流携带的陆源物质对沉积物无机碳具有稀释作用。

图4 达里诺尔湖表层沉积物中各形态无机碳的空间分布/(mg/g)Fig.4 Pattern of horizontal distribution of inorganic carbon speciation in surface sediments from DLNE Lake
碳酸钙过饱和是天然水体中碳酸盐沉淀的必要条件,常用离子活度积(Ionic Activity Product,IAP)与平衡常数Ksp的关系作为判断湖水碳酸钙饱和性的依据,以饱和系数IAP/Ksp表示[6]。

式中,(Ca2+)和()分别是Ca2+和的离子活度和rHCO-3分别是Ca2+和的活度系数;[Ca2+]为湖水Ca2+的浓度;K2是H2CO3的二级离解常数;Alk是湖水总碱度;(H+)为H+的活度(pH=-lg(H+))。若IAP/Ksp>1,则湖水碳酸钙达过饱和。
计算结果(表3)表明,达里诺尔湖水碳酸钙饱和系数远大于1(31.59<IAP/Ksp<166.92),揭示该湖泊具备了自生碳酸盐沉淀的必要条件。
2.2 柱状沉积物中无机碳形态的分布特征
DLNE-3、DLNE-5、DLNE-8和 DLNE-10沉积柱芯中各形态无机碳含量见表4。4个沉积柱芯中,NH2OH·HCl相无机碳均为无机碳的主导形态,占无机碳总量的80%以上。各沉积柱芯中,NaCl相含量接近且变化不大;NH3·H2O相含量在0—8 cm内随深度递增,8—26 cm内波动较大,26 cm以下趋于稳定;NaOH相含量在0—8 cm内随深度递增,8—26 cm内波动不大,DLNE-8沉积柱芯在26—34 cm随深度递减,34 cm以下呈微弱递增趋势;HCl相含量在0—24 cm内波动较大,24 cm以下较为稳定;NH2OH·HCl相与总无机碳的变化趋势相一致,在所有沉积柱芯中含量波动不大(图5),这可能与NH2OH·HCl相为4个沉积柱芯中无机碳的主导形态,是无机碳的主要组成部分有关。
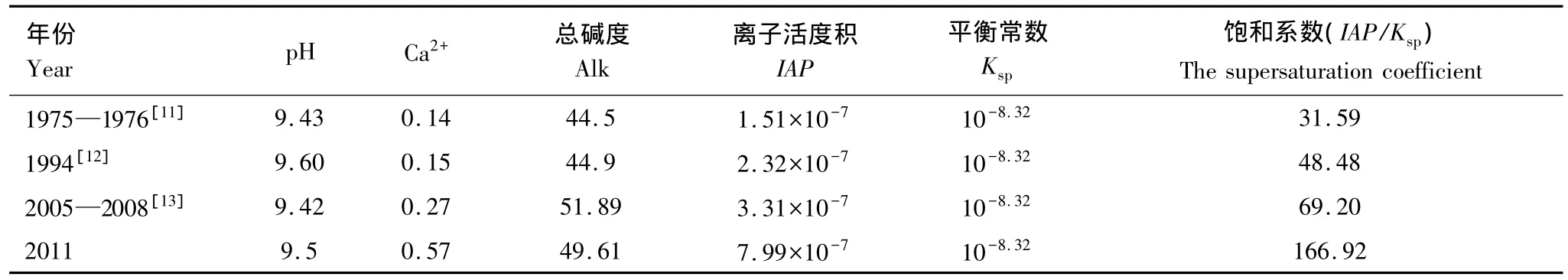
表3 达里诺尔湖不同年份湖水中碳酸钙的饱和系数Table 3 The supersaturation coefficients of Calcium carbonate of different year in the water of Dali Lake

表4 达里诺尔湖沉积柱芯中不同形态无机碳的含量(n=62)Table 4 Speciation concentration of inorganic carbon in sediment cores form Dali Lake
DLNE-3和DLNE-5柱芯中NH2OH·HCl相无机碳含量明显高于DLNE-8和DLNE-10,这可能与前2个柱芯位处深水区(图1),受陆源输入稀释作用影响较弱从而有利于碳酸盐的沉淀,以及后2个柱芯位处浅水区(图1),受陆源输入稀释作用影响较强从而不利于碳酸盐的沉淀有关。
2.3 无机碳与生源要素相互关系分析
研究表明,沉积物中有机碳与各形态无机碳均不存在显著相关关系,表明有机质的降解与矿化对无机碳的影响较小。沉积物中TN、Org-N、TP、活性磷、有机磷和生物硅等营养盐与各无机碳形态均呈正相关关系(表5),揭示营养盐含量的增加可促使无机碳各形态含量增加。除大量碎屑沉积物的注入对碳酸盐沉淀有重大影响外,碳酸盐的发育与藻类的大量繁殖密切相关[17]。营养盐含量的增加,可促使藻类等浮游植物的繁育,藻类增殖大量吸收CO2及部分藻类对水体中有机酸的吸收和重碳酸盐的利用等均可导致水体pH值升高从而有利于碳酸盐沉淀[18-19]。达里诺尔湖硅藻资源极为丰富[20],水质具有高碱度和高pH值特点,藻类的光合作用对水体理化性质的改变可能是导致碳酸钙过饱和进而导致碳酸盐沉淀的重要因素之一。

图5 达里诺尔湖沉积柱芯无机碳垂向分布Fig.5 Vertical distribution of inorganic carbon speciation in sediment cores

表5 沉积柱芯中各形态无机碳与生源要素间的相关性(n=62)Table 5 Correlations between inorganic carbon speciation and trophic element in sediment cores
3 结论
达里诺尔湖表层沉积物中各形态无机碳含量平均值排序为:NH2OH·HCl相>HCl相>NaCl相>NH3·H2O相>NaOH相。NH2OH·HCl相无机碳为表层沉积物和沉积柱芯中无机碳的主导形态,约占无机碳总量的80%。空间分布上,湖心区为各形态无机碳的高值区,东部和北部湖区为低值区。近30余年来,达里诺尔湖水碳酸钙饱和系数均远大于1(31.59<IAP/Ksp<166.92),揭示达里诺尔湖具备形成自生碳酸盐沉淀的条件。
沉积柱芯中氮、磷和生物硅与无机碳的相互关系反映了营养水平升高可促进水体对碳酸钙过饱和条件的形成,藻类的光合作用对水体理化性质的改变可能是导致碳酸盐沉淀的重要因素之一。
[1] Reay D S.Climate change for the masses.Nature,2008,452(7183):31-31.
[2] Yan G A,Liu Y D.Aquatic ecosystems:carbon cycle and as atmosphere CO2sink.Acta Ecologica Sinica,2001,21(5):827-833.
[3] Yu G R.Global Change,Carbon Cycle and Storage in Terrestrial Ecosystem.Beijing:Meteorology Press,2003:1-6,109-119.
[4] Lü C W.Geochemistry Character of Carbon(Nitrogen,Phosphorus,Silicon)in Lakes in West Inner Mongolia Plateau[D].Hohhot:Inner Mongolia University,2008.
[5] Helmke J P,Banch H A.Glacial-interglacial relationship between carbonate components and sediment reflectance in the North Atlantic.Geo-Marine Letter,2001,21(1):16-22.
[6] Chen J A,Wan G J,Wang F S,Huang G R,Zhang F,Zhang D D,Schmidt R.Environmental records of carbon in modern sediments of Lake.Science in China(Series.D),2002,32(1):73-80.
[7] Wan G J,Bai Z G,Wang H R,Huang R G.The geochemical records of C-N-S-P in recent sediments of Lake Erhai.Geochimica,2000,29(2):189-197.
[8] Niu L F,Li X G,Song J M,Yuan H M,Li N,Dai J C.Forms of inorganic carbon in Liaodong Bay core sediments.Marine Sciences,2006,30(11):17-22.
[9] Zeng H A,Wu J L.Lake status of water quality and the changes in Inner Mongolia-Xinjiang Plateau.Journal of Lake Sciences,2010,22(6):882-887.
[10] Xiao J L,Si B,Zhai D Y,Shigeru Itoh,Zaur Lomtatidze.Hydrology of Dali Lake in central-eastern Inner Mongolia and Holocene East Asian monsoon variability.Journal of Paleolimnology,2008,40(1):519-528.
[11] He Z H,Xie Z H,Lei Y Z.Study on the hydrochemistry and hydrobiology of Dali lake.Acta Hydrobiologica Sinica,1981,7(3):341-357.
[12] He Z H,Jiang H,Bi F S.Restudies on the hydrochemistry and hydrobiology of Dali lake.Journal of Dalian Fisheries College,1996,11(2):2-13.
[13] Ding Z J.Dalinuoer Lake environmental problems and prevention measures.Journal of Chifeng University(Natural Science Edition),2009,25(4):57-58.
[14] Li X G,Li N,Song J M.Determination for the different combined-form inorganic carbon in marine sediments.Chinese Journal of Analytical Chemistry,2004,32(4):425-429.
[15] Yang H,Yi C L,Xie P,Xing Y P,Ni L Y.Vertical distribution of carbon,nitrogen and phosphorus of sediments at Stations I and II in Lake Donghu,Wuhan.Geochimica,2004,33(5):507-514.
[16] Wang Y Z,Gao X L,Yang Y W.Fractionation of inorganic carbon in the surface sediments of northern and western Bohai Bay.Marine Sciences,2011,35(2):52-57.
[17] Xia Q S,Tian J C,Ni X F.Lacustrine carbonate rocks in China:an overview.Sedimentary Geology and Tethyan Geology,2003,23(1):106-112.
[18] Xu H,Liu Z P,Yuan L,Yang L Z.Effect of pH on growth of several freshwater algae.Environmental Science and Technology,2009,32(1):27-30.
[19] Liu C G,Jin X C,Sun L,Zhong Y,Dai S G,Zhuang Y Y.Effects of pH on growth and species changes of algae in freshwater.Journal of Agro-Environment Science,2005,24(2):294-298.
[20] Li Z M,An M,Li Y P.Investigation on the phytoplankton of Dali Lake.Inner Mongolia Agricultural Science and Technology,2007,(S1):210,212.
[21] Wang X L.A Study of Transportion Behaviors of Inorganic Carbon in Huanghe Estuary[D].Qingdao:Ocean University of China,2005.
[22] Zhang B L.The Characteristics of Phosphorus Behavior at Sediment-Water Interface and Environmental Risk Assessment from Shallow Lakes[D].Shanghai:East China Normal University,2004.
参考文献:
[2] 严国安,刘永定.水生生态系统的碳循环及对大气CO2的汇.生态学报,2001,21(5):827-833.
[3] 于贵瑞.全球变化与陆地生态系统碳循环和碳蓄积.北京:气象出版社,2003:1-6,109-119.
[4] 吕昌伟.内蒙古高原湖泊碳(氮、磷、硅)的地球化学特征[D].呼和浩特:内蒙古大学,2008.
[6] 陈敬安,万国江,汪福顺,黄荣贵,张峰,Zhang D D,Schmidt R.湖泊现代沉积物碳环境记录研究.中国科学(D辑),2002,32(1):73-80.
[7] 万国江,白占国,王浩然,黄荣贵.洱海近代沉积物中碳-氮-硫-磷的地球化学记录.地球化学,2000,29(2):189-197.
[8] 牛丽凤,李学刚,宋金明,袁华茂,李宁,戴纪翠.辽东湾柱状沉积物中无机碳的形态.海洋科学,2006,30(11):17-22.
[9] 曾海鳌,吴敬禄.蒙新高原湖泊水质状况及变化特征.湖泊科学,2010,22(6):882-887.
[11] 何志辉,谢祚浑,雷衍之.达里湖水化学和水生生物学研究.水生生物学集刊,1981,7(3):341-357.
[12] 何志辉,姜宏,毕风山.达里湖水化学和水生生物学再调研.大连水产学院学报,1996,11(2):2-13.
[13] 丁子军.达里诺尔湖水环境问题及防治措施.赤峰学院学报(自然科学版),2009,25(4):57-58.
[14] 李学刚,李宁,宋金明.海洋沉积物中不同结合态无机碳的测定.分析化学,2004,32(4):425-429.
[15] 杨洪,易朝路,谢平,邢阳平,倪乐意.武汉东湖沉积物碳氮磷垂向分布研究.地球化学,2004,33(5):507-514.
[16] 王允周,高学鲁,杨玉玮.渤海湾北部和西部海域表层沉积物中无机碳形态研究.海洋科学,2011,35(2):52-57.
[17] 夏青松,田景春,倪新锋.湖相碳酸盐岩研究现状及意义.沉积与特提斯地质,2003,23(1):105-112.
[18] 许海,刘兆普,袁兰,杨林章.pH对几种淡水藻类生长的影响.环境科学与技术,2009,32(1):27-30.
[19] 刘春光,金相灿,孙凌,钟远,戴树桂,庄源益.pH值对淡水藻类生长和种类变化的影响.农业环境科学学报,2005,24(2):294-298.
[20] 李志明,安明,李岩平.达里湖浮游植物调查.内蒙古农业科技,2007,(S1):210,212.
[21] 王晓亮.黄河口无机碳输送行为研究[D].青岛:中国海洋大学,2005.
[22] 张斌亮.浅水湖泊沉积物-水界面磷的行为特征与环境风险评价[D].上海:华东师范大学,2004.
