硝酸N-正丁基吡啶(BPNO3)离子液体的合成与表征
2013-09-04赵石楠
赵石楠
(公安消防部队昆明指挥学校,云南 昆明 650500)
离子液体是指在室温范围内呈液态并完全由离子所组成的盐,也称为低温熔融盐,一般由有机阳离子和无机阴离子、有机阴离子所组成。离子液体除具有制备简单、导电性良好、较宽的电化学窗口等特性外,还具有特殊的溶解性,且多数可以任意比例均相混合;高极性而不发生配位作用;与非极性有机溶剂不相溶、可作为非水的极性替代物;热稳定性好、不挥发、蒸汽压为零、不会对环境产生污染等优良特性,而且其物理化学性质可以通过对阳离子的修饰或改变阴离子进行调节,因此离子液体是传统挥发性溶剂的理想替代品。
一、实 验
1.仪器试剂
(1)部分试剂处理
丙酮提纯:在圆底烧瓶中,加入100mL丙酮、0.5g高锰酸钾,水浴加热回流,直到紫色不再消失为止,用无水碳酸钾干燥1h。将干燥好的丙酮倾入蒸馏装置,水浴加热蒸馏,收集55.0~56.5℃馏分,此法用于除去丙酮中含有的还原性杂质。
吡啶提纯:在圆底烧瓶中,加入200mL吡啶、5g氢氧化钾、回流0.5h,然后换成蒸馏装置隔绝潮气蒸出吡啶(收集115~117℃馏份)。因干燥的吡啶吸水性强,应将容器口用石蜡封好保存。
乙腈提纯:在圆底烧瓶中,加入5g五氧化二磷、100ml乙腈回流2h,然后换成蒸馏装置蒸出,以除去乙氰中水分。在馏出的乙腈中加入少量的碳酸钾再进行蒸馏,可以除去痕量的五氧化二磷(收集81~82℃馏份)。
(2)主要仪器及设备
主要仪器及设备:BUCHI旋转蒸发仪(瑞士BUCHI实验仪器公司),Varian XL-300核磁谱仪(美国Varian公司),WGH-30/6红外光谱仪(天津光学仪器厂),8100型电子熔点测定仪(上海亚荣生化仪器厂)。
2.室温离子液体中间体的合成
氯化N一正丁基吡啶(BPC)的合成反应为:
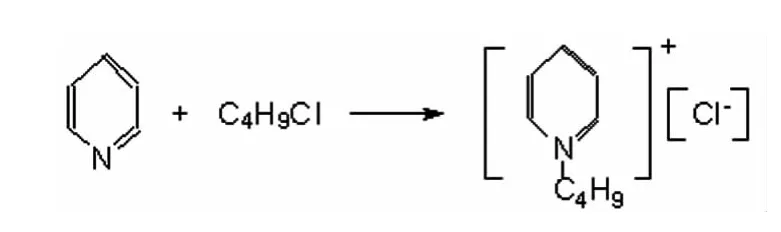
将0.5moL氯代正丁烷与0.5mol吡啶加入到250mL单口烧瓶中,在黑暗中油浴回流,控制温度为100℃,半小时后出现浑浊,烧瓶中有白色晶体出现,继续反应48h。冷却后,真空抽滤,滤饼用乙腈重结晶2~3次,真空干燥,得白色氯化N一正丁基吡啶(BPC)晶体,获得产物迅速放入试剂瓶中,置于真空干燥皿中保存。经测量,BPC产量为65.13 g,产率 76%,熔点 131.5~133℃ (文献值 131.7~133℃)
3.硝酸N一正丁基吡啶(BPNO3)室温离子液体的合成
合成反应为:
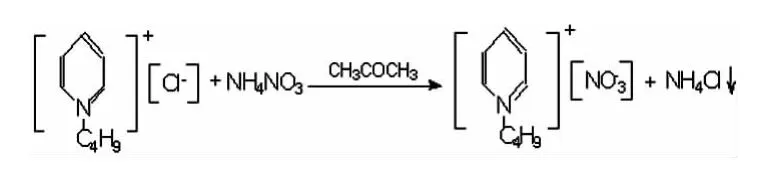
准确称取0.05mol的NH4NO3和0.05mol的 BPC加入到锥形瓶中,在搅拌条件下,加入60.0mL丙酮,反应2h后过滤,用旋转蒸发仪蒸出滤液中多余丙酮,干燥至质量不变.得到产物为无色透明液体,产量8.1g,产率为85.0%.
4.BPNO3中氯离子含量的测定
(1)硝酸银溶液的标定
准确称取0.2922g基准NaCl,定量转移至500mL容量瓶中,配制成浓度为0.0100mol/L的NaCl标准溶液。取此溶液25mL三份,按照莫尔法,以K2CrO4为指示剂,用配制好的AgNO3溶液滴定到终点,并以CaCO3饱和溶液为背景进行空白实验。
(2)BPNO3中氯离子含量的测定
称取2.1477g的硝酸N-正丁基吡啶,加入少量去离子水溶解,定量转移到500mL容量瓶中,稀释至刻度。取此溶液25mL三份,分别置于250mL锥形瓶中,加25mL去离子水及1mL 5%K2CrO4指示剂,用0.0101mol/L的 Ag-NO3溶液滴定至终点,消耗AgNO3的体积记为VT。在同样的条件下以CaCO3饱和溶液为背景进行空白实验,消耗溶液体积记为V0,则标定实际消耗的AgNO3溶液体积为VT-V0。
5.BPNO3的纯化
于100mL锥形瓶中称取10.0032gBPNO3(Cl-含量0.206%,0.56mmol)和 0.1020gAgNO3(0.60mmol),在搅拌条件下,再加入20mL丙酮,反应5分钟后过滤,滤液蒸发除去多余丙酮,真空干燥,得到无色透明液体9.2085g。用去离子水溶解少量产物,滴加AgNO3溶液后无白色沉淀生成,说明产物中无可测定量Cl-。再用去离子水溶解少量产物,滴加纳氏试剂后无褐色沉淀生成,说明无可测定量NH4+。
二、结果与讨论
1.硝酸N一正丁基吡啶(BPNO3)离子液体的合成
1HNMR 核磁共振数据(CDCl3,TMS):δppm=9.570(2H2,6,吡啶),δppm=8.418(1H4,吡啶),δppm=8.283(2H3,5,吡啶),δppm=4.963(2H,N -CH2-),δppm=2.057~0.938(2H,-CH2CH2CH3)。
IR测定,KBr压片,将离子液体涂于其上,数据为:3058~2780 cm -1(-C4H9),1632cm -1、1488 cm-1(吡啶),1348 cm -1.829 cm-1(NO3-)。
结果表明,在实验的误差范围内,其实验核磁共振谱与文献值基本一致,同时在IR图谱中,观测到NO3-峰的存在,证明已合成目标化合物BPNO3。
2.硝酸N一正丁基吡啶(BPNO3)中氯离子含量的测定与纯化
在合成过程中,因有NH4Cl的产生,故BPNO3中混有少量cl-和NH4的存在,而BPNO3室温下为吸水性液体,进行元素分析有一定困难,故实验采用莫尔法测得新合成BPNO3中cl-含量,结果为 cl-平均含量为0.206%,0.
56mmol,见表 1。
并通过AgNO3对产物进行纯化,通过AgNO3溶液及滴加纳氏试剂检测,结果表明纯化后的BPNO3中无可测定量的Cl-和NH4+的存在,证明所合成的BPNO3纯度较高。
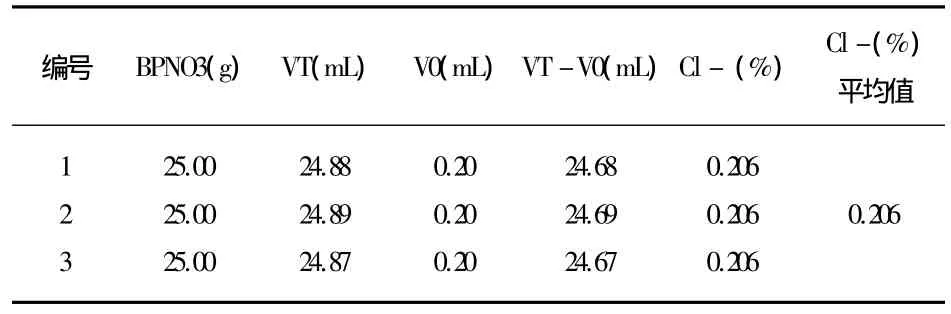
表1 硝酸N-正丁基吡啶(BPNO3)中氯离子含量的测定
在莫尔法经典空白实验中,因滴定过程生成的AgCl沉淀对Cl-的吸附作用,且AgNO3标准溶液消耗体积较小,难以校正Cl-所带来的误差。其次在测定过程中,K2CrO4指示剂的用量和AgNO3滴定液的浓度对测定结果均有影响,因此一般加入一定量的CaCO3作为沉淀背景,使得水样与空白滴定终点色调变化基本一致,以此校正终点误差。
三、结 论
实验通过室温离子液体中间体氯化N一正丁基吡啶(BPC)与NH4NO3在丙酮条件下的复分解反应,合成出了硝酸N一正丁基吡啶(BPNO3)室温离子液体,并通过IR、1HNMR等手段对其结构进行了鉴定,结果与文献值一致,表明已经合成了目标化合物BPNO3。同时,根据实验结果用硝酸银对BPNO3进行了进一步纯化,纯化后的BPNO3经AgNO3溶液和纳氏试剂检验,结果表明并无可测定量的Cl-和NH4+存在,证明所合成的BPNO3纯度较高。
[1]吕子健.BP-NO3和BP-BF4离子液体物理化学性质和光谱性质研究[D].沈阳:沈阳师范大学,2010.
[2]王荐辕,张沙艳.N-烷基吡啶类室温离子液体BPNO3、BPBF4的合成研究[J].辽宁师专学报(自然科学版),2008,(2):103.
[3]张建民,孙荣印,尹懿敏等.莫尔法测定水中氯离子终点误差校正[J].石家庄铁道学院学报,1996,(3).
[4]赵永志.AgNO3滴定水中 Cl-终点误差的校正[J].环境监测管理与技术,2000,(6)
