利用化学酯交换法制备蛋挞专用油
2013-09-04朱晨曦李伟伟黄训端江明星张部昌1
朱晨曦,李伟伟,程 兴,黄训端,江明星,范 伟,郑 洋,张部昌1,2,,4,*
(1.安徽大学健康科学研究院,安徽合肥230601;2.安徽康尔美油脂有限公司,安徽霍山237200;3.安徽大学生命科学学院,安徽合肥230601;4.安徽大学康尔美生物技术研发中心,安徽合肥230601)
油脂理化性质与脂肪酸种类和脂肪酸在甘三酯上的分布直接相关[1]。进行油脂改性,可以得到理化性质好的可塑性油脂产品[2]。化学酯交换是通过交换甘三酯分子内和分子间的脂肪酸位置,从而得到含有特定脂肪酸的具有药用和营养价值的油脂产品[3]。此外,随着人们对反式脂肪酸安全问题的关注不断加深,酯交换等技术被用于新产品开发[4]。同时,化学酯交换技术被用于替代部分氢化技术,已用于起酥油和人造奶油的生产[5]。Farmani等[6]通过利用棕榈油、低芥酸菜子油和葵花油酯交换反应制备零反式脂肪酸的人造黄油。而含丰富的γ-亚麻酸和亚油酸的特种油脂已通过酯交换反应得到[7]。最新营养学证据表明富含营养均衡的脂肪酸油脂能促进人体健康[3]。理想油脂的脂肪酸组成应含有适量的饱和脂肪酸(saturated fatty acids,SFA)、单不饱和脂肪酸(monounsatu-rated fatty acids,MUFA)和多不饱和脂肪酸(unsaturated fatty acids,PUFA)[8]。然而,天然油脂中没有这样的理想油脂,因此对油基进行改性是必须的。蛋挞是一种高热量甜点,蛋挞皮的制作对油脂延展性和可塑性要求高。本研究为解决该问题利用椰子油(cocoanut oil,CNO)、大豆油(soybean oil,SBO)、棕榈硬脂(palm stearic,ST)和棕榈油(palm oil,OL)化学酯交换法制备蛋挞专用油油基。棕榈硬脂和棕榈油由于其不饱和度低而提高了混合油基的热稳定性[9]。大豆油的多不饱和脂肪酸可以提高酯交换产品的可塑性[10],而添加椰子油是为了改善由于其它油基中中碳链脂肪酸含量缺乏造成的营养方面的不足[8]。本文以上述四种油基进行化学酯交换,制备蛋挞专用油。
1 材料与方法
1.1 材料与仪器
棕榈油和棕榈硬脂 康尔美油脂公司提供;椰子油、大豆油 上海益海嘉里产品。
日立L-2000型高效液相色谱仪(HPLC)日本日立株式会所;Alltech3300型蒸发光检测器(ELSD)美国Alltech公司;气相色谱仪(GC)、DSC-60A型差示扫描热量仪 日本岛津株式会所;核磁共振仪德国Bruker公司;MB3600FT-NIR红外分析仪德国ABB公司。
1.2 实验方法
1.2.1 油基混合 四种油基按不同比例混合,如表1所示。根据理化指标,综合产品口感和成本,第七组较为适合做蛋挞专用的备选油基。
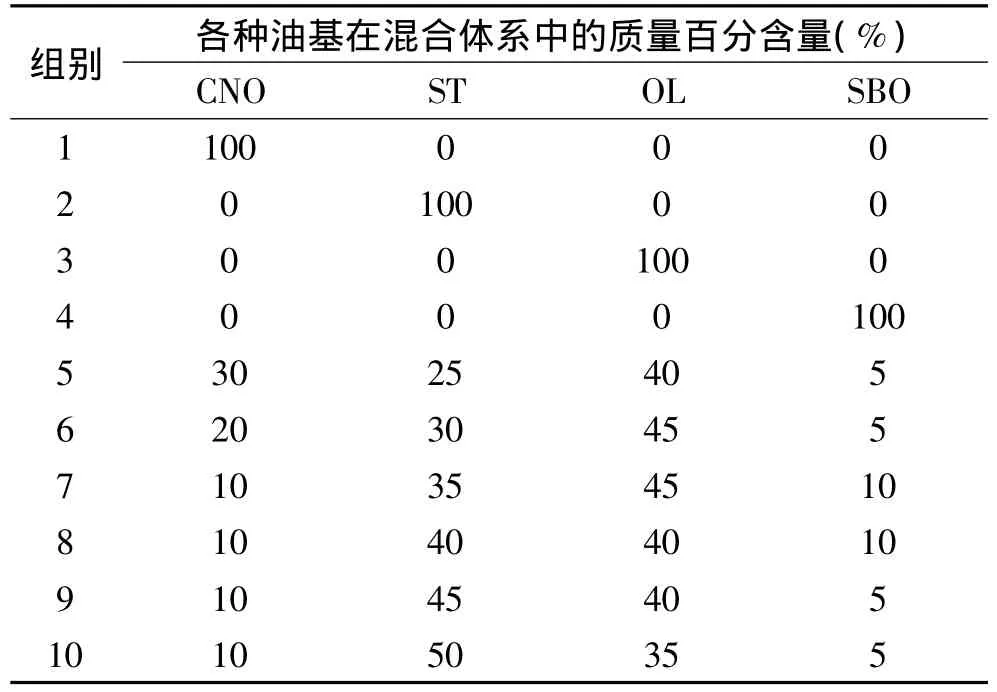
表1 混合油基的成分设计(w/w)Table 1 Composition design of the blends(w/w)
1.2.2 化学酯交换 称取100g混合油基于反应三角烧瓶中,110℃下真空脱水脱气30min,迅速加入甲醇钠反应。反应终止立即加入开水和1g柠檬酸水洗,水洗3~4次过滤除水,得酯交换油脂。
1.2.3 碘值测定 使用MB3600FT-NIR红外分析进行碘值测定。
1.2.4 动脉硬化指数 动脉硬化指数参考 Kim[11]提出的计算公式进行计算。公式为:
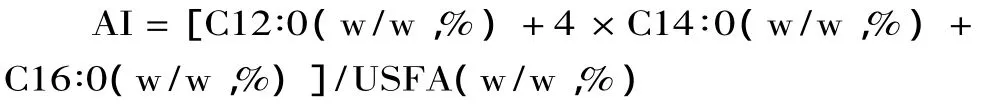
式中,AI表示动脉硬化指数,C12∶0表示月桂酸在油基总体脂肪酸中的相对百分含量(%),C14∶0表示豆蔻酸在油基总体脂肪酸中的相对百分含量(%),C16∶0表示棕榈酸在油基总体脂肪酸中的相对百分含量(%),USFA表示总不饱和脂肪酸在油基总体脂肪酸中的相对百分含量(%)。
1.2.5 熔点测定 参照国标 GB/T24892-2010[12]。本实验采用开口毛细管法,-20℃下冷冻15min后测定。
1.2.6 酸值测定 参照国标 GB/T5530-2005[13]。
1.2.7 过氧化值测定 参照国标 GB/T5538-2005[14]。1.2.8 差示扫描量热法测定油基焓变 测量条件为从室温起以5℃/min升温至60℃,低熔点油基从-60℃起升温,记录油基焓变曲线。
1.2.9 固脂含量测定 采用脉冲核磁共振法测定油基的固脂含量。称取4g左右的样品,每样做两个平行。样品需进行预处理,预处理温度程序如下:60℃恒温水浴0.5h使样品完全融化,0℃恒温水浴1h,再将样品分别放置在20、25、30、35、45℃水浴锅中恒温0.5h,测定 SFC值。以温度为横坐标,绘制 SFC-T曲线[15]。
1.2.10 脂肪酸组成测定 制备脂肪酸甲酯:取约0.06g油样,溶于8mL正己烷中,充分溶解,再加入2mL 0.2mol/L KOH-CH3OH饱和溶液反复震荡混匀,静置30min,分层后吸取上层溶液进行脂肪酸组成分析。
气相色谱条件:RT-2560强极性毛细管气相色谱柱(100m × 0.25mm,i.d.0.2μm,Varian),检测器为FID,载气为N2,燃烧气为 H2和空气。进样口温度260℃,柱前压 278.6kPa,柱温 160℃ 保留 5min,以4℃/min升温至220℃保留10min,再以4℃/min升温至240℃保留20min。检测器温度260℃,H2压力60kPa,空气压力 50kPa,进样量 1μL,进样模式:不分流[15]。
1.2.11 甘三酯组成测定 液相色谱条件:Alltima C18(5μm,250mm ×4.6mm),流动相为乙腈∶二氯甲烷 =65∶35,流速为 1.2mL/min,柱温为 30℃,ELSD 漂移管检测温度为70℃,载气为N2,压力300kPa,流量为1.5L/min[15]。
1.2.12 X射线衍射分析(XRD)样品于18℃放置2h,取1g左右均匀涂于载样板中的测量槽中,然后进行测量。测定条件为:起始角为2°,终止角为30°,以1°/min进行扫描。结果使用 Parallel Distributed Processing(PDP)软件进行分析。
2 结果与讨论
2.1 油基基本参数
酯交换前后油基过氧化值、酸值、碘值和熔点,结果如表2所示。
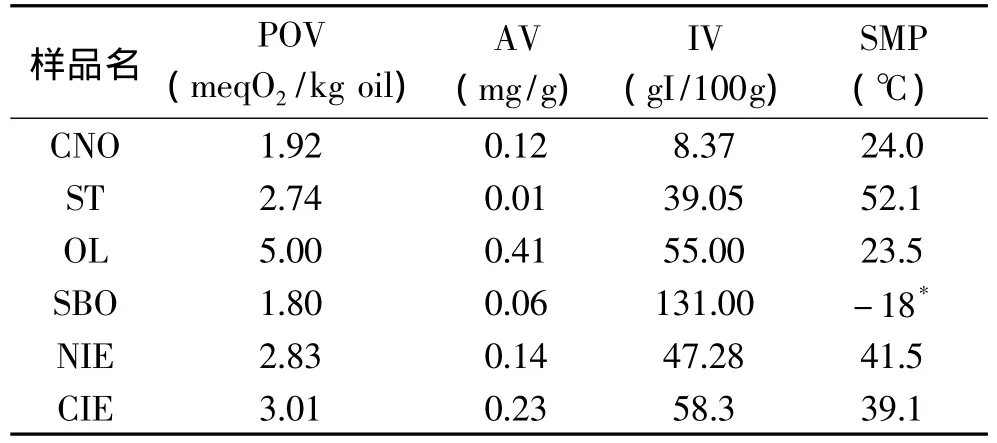
表2 油基基本参数Table 2 Basic parameter of oils
由上表可知,各种基料油及反应前后混合油基的指标均符合国标 GB 15196-2003[16],可以进行酯交换实验,并可应用于蛋挞生产。
2.2 酯交换反应对油基热学性质的影响
熔点是评价酯交换反应是否达到平衡的一个重要参数。混合油基酯交换前后熔点从41.5℃降到39.1℃。这个结果和 Soares等[17]的研究结果化学酯交换前后熔点没有显著变化相一致。即当与含高比例的硬脂肪混合物进行化学酯交换,其对熔点的影响较小。
通过DSC测定发现,反应前后油基焓变曲线都是非常平滑的,如图1。但反应前后对比发现在31℃左右的特征焓变峰反应后要比反应前峰型更尖锐。同时平行实验组2、3两组焓变峰出峰要比反应前晚1℃出峰。这个变化趋势和熔点变化减低趋势相一致。这表明酯交换中甘三酯相对含量变化与其焓变曲线变化有直接关系。因此通过 DSC曲线变化趋势,可以间接判断脂肪酸在甘三酯位置上随机交换后的变化情况。化学酯交换造成了重排的脂肪酸在甘油骨架由较高的熔点骨架(如SSU)向新的较低的熔点骨架(如UUU和UUS)转变,如表3。
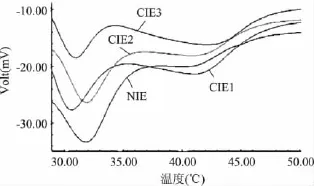
图1 酯交换前后油基焓变曲线对比图Fig.1 The transesterification of oil before and after radical enthalpy curve contrast diagram
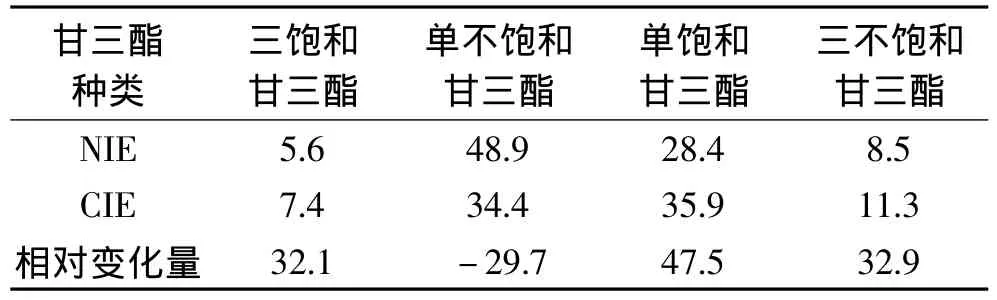
表3 反应前后不同甘油三酯相对含量(%)变化对比Table 3 Distribution of triacylglycerols in native blended and interesterified oils(%)
2.3 酯交换反应对油基晶型的影响
通过X射线衍射测定反应前后晶型变化情况。依据 Ap PH 等[18]的晶型理论:同时在 3.8Å 和 4.2Å出现两个峰才能说明测定样品存在β'晶型;在4.6Å出现峰说明测定样品存在β晶型。根据峰型所占的相对比例可以大致确定各晶型所占比例。对反应前后油基中β'和β的峰型所占的相对比例可以大致确定各晶型所占比例。对反应前后油基中β'和晶型相对比例分析发现,反应前后油基中均含有这两种晶型。反应前β'晶型占42.8%,β晶型占57.2%。而反应后 β'晶型占73.9%,β 晶型占26.1%。一般来说,β'晶型是涂抹黄油的小晶体的理想晶型,因为较大的β晶型会使硬度增大而降低了黄油的延展性[19]。

图2 酯交换前混合油基X射线衍射晶型图Fig.2 X-ray diffraction spectrum for non-interesterified blends
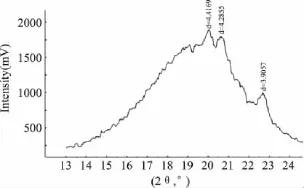
图3 酯交换后混合油基X射线衍射晶型图Fig.3 X-ray diffraction spectrum for interesterified blends
2.4 酯交换反应对脂肪酸组成的影响
各油基和混合油基及酯交换反应后油基脂肪酸组成和AI指数见表4。
由表4知,反应前反式脂肪酸含量为0.5%,反应后反式脂肪酸含量为0.4%,均低于大多数国家反式脂肪酸含量的标准。在上表中反应前后,油酸和硬脂酸的脂肪酸含量分别增加了8.4倍和7倍,而月桂酸和花生酸分别降低了97.6%和97.0%。这说明酯交换反应中还可能伴有其他副反应发生。总之,脂肪酸的变化间接显示出化学酯交换具有一个明显的脂肪酸偏好,这个原因可能是副反应皂化反应引起的。
β'晶型在棕榈酸含量较高的起酥油中更具稳定性。同时,高棕榈含量不仅可以使油基更耐氧化,也提高了油基的延展性使其更适于应用在蛋挞中。较低的熔点和较低的不饱和脂肪酸比例可以使椰子油特别适用于低水分食品的油脂产品中。适当添加大豆油于混合油基中可降低饱和脂肪酸含量,增加PUFA、MUFA含量。反应前后对比发现,反应前混合油基中32.3%的亚油酸作为主要的不饱和脂肪酸,而油酸含量小于5%。多不饱和脂肪酸和饱和脂肪酸(P/S)反应前后比分别约为0.52和0.32。这符合食品和农业组织/世界卫生组织(FAO/WHO)和欧盟委员会提出的最小的P/S比值[20]。

表4 各油基及混合油基反应前后脂肪酸组成(%)及AI指数Table 4 The base oil and mixed oil base reaction of fatty acid composition(%)and AI index

表5 酯交换反应前后甘三酯相对含量比较Table 5 TAG composition(%peak area)of NIE and CIE.
动脉硬化指数是评价一个油脂产品是否符合营养学健康标准的一个重要参数[21]。较低的值表示该油脂是一个“健康”的脂肪组合物。反应后的混合产物的该指数明显低于反应前,表明反应后的混合油基比反应前的更加健康。这个结果可能与SFA含量显著降低而USFA含量增加有关。因此反应后得到的混合油基更适宜作蛋挞专用油。
2.5 酯交换反应对甘三酯组成的影响
甘三酯种类和结构决定了油脂的生化特性和理化性质[21]。酯交换反应前后各种甘三酯相对含量如图4、图5所示。酯交换反应前后对比发现,LLL、POP和 OOP 相对含量减低,而 PPL、PPP、POL、OOL和OOO相对含量增加。其中POL和OOL含量分别增加了126.9%和354.5%。混合油基甘三酯理化性质主要是由近50%的二饱和甘三酯提供。化学酯交换后,SSU含量降低了29.7%。相反,UUU、SSS和UUS增加了 32.9% ,32.1% 和47.5%,见表3。由此可推断出反应前后混合油基的理化性质变化是由于脂肪酸随机酯交换造成的。熔点范围广的甘三酯的混合油基,通常可塑性更好,在油脂产品中的应用也更为广泛。
2.6 酯交换反应对固脂含量的影响
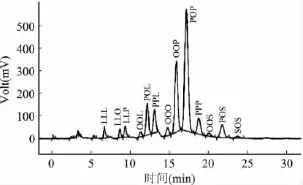
图4 酯交换反应前混合油基甘三酯组成HPLC图谱Fig.4 Triacylglycerol molecular species of non-interesterified blends(NIE)showed through HPLC Chromatograms

图5 酯交换反应后混合油基甘三酯组成HPLC图谱Fig.5 Triacylglycerol molecular species ofinteresterified blends(CIE)showed through HPLC Chromatograms
固脂含量对油脂产品晶型结构影响很大。反应前后的SFC值如图6所示。反应前混合油基表现为在各温度下的固脂含量都高于反应后的混合油基的SFC值。酯交换后混合油基SFC值的下降是由于高熔点甘三酯的比例下降造成的。经过化学酯交换反应,伴随着混合油基SFC值的变化,混合油基中甘三酯组成也发生变化。这表明通过酯交换反应SFC值的变化会显著影响甘三酯组成。由于其甘三酯组成发生变化,导致反应后混合油基的结晶时间延长。总之,酯交换工艺可以改善混合油基SFC的温度分布。

图6 酯交换前后反应SFC含量变化Fig.6 SFC profiles of blends before and after chemical interesterification
根据 Kim 等[11]研究表明,在10℃ 时 SFC值 <32%可以使油脂产品在冰箱温度下储存仍具有良好的延展性。由图6可知,酯交换前后混合油基在25℃和40℃时SFC值均降低。这使得酯交换后的混合油基具有更好的可塑性,同时风味也更好。
3 结论
本研究得到的蛋挞专用油基是通过添加CNO、OL、ST和 SBO进行复配得到的,具有适合 SFA/USFA比例。混合油基进一步通过酯交换反应随机化重组甘三酯,得到熔点、脂肪酸组成、动脉硬化指数、甘三酯、晶型结构和SFC值均优于酯交换反应前。反应后的混合油基SFC值小于反应前使其具有更好的可塑性。以上这些都为我们提供了其作为合适的蛋挞专用油的理由。其次,酯交换后的混合油基拥有更低的动脉硬化指数使其更具营养价值。
[1]Kris-Etherton P,Griel A,Psota T,et al.Dietary stearic acid and risk of cardi-ovascular disease:Intake,sources,digestion,and absorption[J].Lipids,2005,40:1193-1200.
[2]Krishna DB,Dahyabhai PJ.Modification of palm oil by chemical and enzyme catalyzed interesterification[J].J Oleo Sci,2010,59:293-298.
[3]Reena MB,Reddy SY,Lokesh BR.Changes in triacylglycerol molecularspecies and thermalproperties ofblended and interesterified mixtures of coconut oil or palm oil with rice bran oil or sesame oil[J].Eur J Lipid Sci Technol,2009,111:346-357.
[4]Costale RR,Gibon V,Verhe R,et al.Chemical and Enzymatic Interesterification of a Blend of Palm Stearin:Soybean Oil for Low trans-Margarine Formulation[J].J Am Oil Chem Soc,2009,86:681-697.
[5]Adhikari P,Shin JA,Lee J,et al.Production of trans- free margarine stock by enzymatic interesterification of rice bran oil,palm stearin and coconutoil[J].JournalScience Food Agricultural,2010,90:703-711.
[6]Farmani J,Safari M,Hamedi M.Application of palm olein in the production of zero-trans Iranian vanaspati through enzymatic interesterification[J].Eur J Lipid Sci Technol,2006,108:636-643.
[7]Lumor SE,Akoh CC.Incorporation of γ-linolenic and linoleic acids into a palm kernel oil/palm olein blend[J].Eur J Lipid Sci Technol,2005,107:447-454.
[8]SoaresFA,daSilvaRC,HazzanM,etal.Chemical interesterification of blends of palm stearin,coconut oil,and canola oil:physicochemical properties[J].J Agric Food Chem,2012,60:1461-1469.
[9]Saadi S,Ariffin AA,Ghazali HM,et al.Effect of blending and emulsification on thermalbehavior,solid fatcontent,and microstructure properties of palm oil- based margarine fats[J].J Food Sci,2011,76:C21-30.
[10]LaiO,GhazaliH,Chong C.Effectofenzymatic transesterification on the melting points of palm stearin-sunflower oil mixtures[J].J Am Oil Chem Soc,1998,75:881-886.
[11]Kim BH,Lumor SE,Akoh CC.Trans- free margarines prepared with canola oil/palm stearin/palm kernel oil-based structured lipids[J].J.Agric.Food Chem,2008,56:8195-8205.
[12]GB/T24892-2010.动植物油脂测定标准[S].北京:中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会,2010.
[13]GB/T5530-2005.动植物油脂测定标准[S].北京:中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会,2005.
[14]GB/T5538-2005.动植物油脂测定标准[S].北京:中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会,2005.
[15]孟宗,刘元法,徐振波,等.酯交换法改善牛油基起酥油起砂的初步研究[J].中国油脂,2008,33(6):28-32.
[16]GB 15196-2003.人造奶油卫生标准[S].北京:中华人民共和国卫生部,中国国家标准化管理委员会,2003.
[17]Soares FASDM,Silva RC,Silva KCG,et al.Effects of chemical interesterification on physicochemicalpropertiesof blends of palm stearin and palm olein[J].Food Res.Int,2009,42:1287-1294.
[18]Ap PH,de-Man JM,de-Man L.Polymorphism of palm oil and palm oil products[J].J Am Oil Chem Soc,1989,66:693-697.
[19]Rousseau D,Hodge SM,Nickerson MT,et al.Regulating the β'→β polymorphic transition in food fats[J].J Am Oil Chem Soc,2005,82:7-12.
[20]Petrauskaite V,Greyt DW,Kellens M,et al.Physical and chemical properties of trans-free fats produced by chemical interesterification of vegetable oil blends[J].J.Am.Oil Chem.Soc,1998,75:489-495.
[21]Bracco U.Effect of triglyceride structure on fat absorption[J].Am J Clin Nutr,1994,60:1002-1009.
