新型对叔丁基杯[4]芳烃1,3-二酮衍生物的合成*
2013-09-01罗再刚徐雪梅史永健张晓梅
罗再刚,马 超,徐雪梅,史永健,张晓梅
(安徽理工大学化学工程学院,安徽 淮南 232001)
杯芳烃是对位取代的苯酚或其衍生物与甲醛在碱性条件下反应,苯酚单元在羟基邻位通过亚甲基或类似的基团联接起来的大环化合物,是继冠醚和环糊精之后出现的“第三代超分子化合物”[1]。三十年来,通过对杯芳烃的结构进行修饰所得的大量杯芳烃衍生物在分子识别、分子组装、酶模拟、化学传感器等领域得到了广泛的研究和应用[2~4]。
到目前为止,将1,3-二酮结构片段连接到杯[4]芳烃上还未见文献报道。本文以对叔丁苯酚(1)为原料,经聚合反应得对叔丁基杯[4]芳烃(2);在碳酸钾和乙腈体系中,2与氯乙酸乙酯经醚化反应得对叔丁基杯[4]芳烃-1,3-二乙酸乙酯(3);利用氢化钠夺取苯乙酮中乙酰基上的α-H形成的碳负离子进攻3的酯羰基从而构建1,3-二酮结构,合成了1个新型的对叔丁基杯[4]芳烃1,3-二酮衍生物(4,Scheme 1),其结构经1H NMR,13C NMR和MS表征。
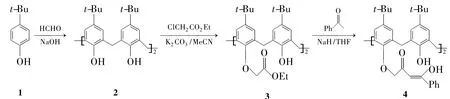
Scheme 1
1 实验部分
1.1 仪器与试剂
X-4型显微熔点仪(温度未校正);Bruker Avance-400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Esquire 6000型质谱仪。
2[5]和 3[6]按文献方法合成;柱层析用硅胶,200目~300目,青岛海洋化工厂;其余所用试剂均为分析纯,其中THF使用前经无水处理。
1.2 合成
(1)4的合成
氮气保护,在冰浴冷却的反应瓶中加入THF 5 mL和氢化钠90 mg(2.1 mmol),搅拌使其完全溶解;滴加苯乙酮0.24 g(2 mmol)的THF(5 mL)溶液,滴毕,反应 5 min;滴加3 0.82 g(1 mmol)的THF(5 mL)溶液,滴毕,回流反应至终点(TLC监测)。冷却至室温,倒入含有1 mL浓盐酸的冰水中,用乙酸乙酯(3×15 mL)萃取,合并萃取液,用盐水洗涤,无水硫酸镁干燥,旋蒸脱溶后经快速硅胶柱层析[洗脱剂:V(乙酸乙酯)∶V(石油醚)=9∶1]纯化得白色固体 4 0.56 g,收率 58%,m.p.198 ℃~200 ℃;1H NMR δ:0.95(s,18H,CH3in t-Bu),1.31(s,18H,CH3in t-Bu),3.42(d,J=13.2 Hz,4H,ArCH2Ar),4.30(d,J=13.2Hz,4H,ArCH2Ar),4.55(s,4H,ArOCH2),6.83(s,4H,ArH),7.13(s,4H,ArH),7.29(s,2H,COCH),7.35(t,J=7.6 Hz,4H,ArH),7.50(t,J=7.6 Hz,2H,ArH),7.58(s,2H,ArOH),7.88(d,J=7.6 Hz,4H,ArH),15.34(s,2H,OH);13C NMR δ:192.1,183.3,150.4,148.9,147.9,142.3,133.7,132.7,132.2,128.1,127.7,127.6,125.9,125.2,94.1,34.0,33.9,31.7,31.4,30.9;ESI-MS m/z:991.4{[M+Na]+}。
2 结果与讨论
在THF溶液中,用氢化钠夺取苯乙酮中乙酰基上的α-H形成碳负离子,紧接着进攻3中的酯羰基从而得到1,3-二酮结构。考虑到在此碱性条件下,3中26,28-位上裸露的酚羟基可能不利于反应的进行,起初我们尝试将26,28-位酚羟基先保护后再在碱性条件下构建1,3-二酮结构。但实验发现,控制氢化钠的用量,3的26,28-位酚羟基不需要保护也能进行缩合反应。氢化钠若过量可能会使部分3中裸露的酚羟基成盐,从而影响该反应的进行。在对反应条件进行优化后发现,当n(氢化钠)∶n(苯乙酮)∶n(3)=2.1 ∶2 ∶1时,收率最高(经柱层析纯化后可达58%)。另外,若THF干燥不彻底,会损耗掉部分氢化钠转变为氢氧化钠,同时在加热回流条件下部分3中的酯基水解成羧基而降低反应活性,进而影响4的最终收率,因此该反应对无水条件的控制比较苛刻。
4的1H NMR分析表明,1,3-二酮之间的亚甲基质子峰基本消失,在7.29和15.34处分别出现烯氢和羟基氢的信号峰,而在碳谱中94.1处出现烯碳的信号峰,这表明4在氘代氯仿溶液中以醇式构象为主。
[1] 刘育,尤长城,张衡益.超分子化学——合成受体的识别与组装第1版[M].天津:南开大学出版社,2001.
[2] Liu S Y,He Y B,Wu J L,et al.Calix[4]arenes containing thiourea and amide moieties:Neutral receptors towards α,ω-dicarboxylate anions[J].Org Biomol Chem,2004,2:1582-1586.
[3] Liu Y,Chen Y,Li L,et al.Cooperative multiple recognition by novel calix[4]arene-tethered β-cyclodextrin and calix[4]arene-bridged bis(β-cyclodextrin)[J].J Org Chem,2001,66(21):7209-7215.
[4] Baur M,Frank M,Schatz J,et al.Watersoluble calix[n]arenes as receptor molecules for non-polar substrates and inverse phase transfer catalysts[J].Tetrahedron,2001,57:6985-6991.
[5] Kim J S,Shon O J,Rim J A,et al.Pyrene-armedcalix[4]azacrowns as new fluorescent ionophores:“molecular taekowndo”process via fluorescence change[J].J Org Chem,2002,67:2348-2351.
[6] 蒋忠良,王修智,段辉.25,26,27,28-羟乙氧基-杯[4]芳烃的合成[J].合成化学,2009,17(6):716-721.
[7] 杨发福,蔡秀琴等,新型杯[4]芳烃衍生物的合成及其氨基酸萃取性能[J].分子科学学报,2006,22(2):96-99.
