新型四核铜配合物{[Cu4L2(N3)2(μ2-N3)2]·CH3OH}的合成及其晶体结构*
2013-09-01郭越新马红翠段漓童张卫国侯红卫樊耀亭
郭越新,马红翠,段漓童,张卫国,程 翔,侯红卫,樊耀亭
(1.河北联合大学 药学院,河北 唐山 063000;2.郑州大学化学系,河南 郑州 450052)
多吡啶配体及衍生物构筑的金属-有机配合物具有众多的配位原子和较为特殊的分子构型,在配位过程中可采取多样化的配位方式,有可能构筑出具有新颖拓扑结构的配合物[1]。1994年,Fujita等[2]报道4,4'-联吡啶(4,4'-bipy)和 Cd 在混合溶剂(H2O-EtOH)中形成具有二维平面结构的配位聚合物{[Cd(4,4'-bipy)2](NO3)2}n;2006,Lah等[3]报道了通过设计多吡啶三脚架配体而制得两个具有大孔洞的金属笼状配合物,两个笼的内径分别达到13.6 Å和14.4 Å。同时,该类配合物在分子识别、分子交换、电子传递和选择性催化等方面具有着潜在的应用前景[4]。2000年Kitagawa[5]等报道的多孔配位聚合物[CuSiF6(4,4'-bipy)2]·8H2O,每个 Cu 与四个 4,4'-bipy配位,形成二维平面结构,在c轴方向有8×8 Å孔道,而在a和b轴方向有6×21 Å的孔道,并在298 K和0 kPa~3.65×103kPa内测定了其甲烷吸附特性,具有良好的吸附效果;Yaghi等许多课题组所制得的大孔洞化合物在气体储存应用上展示了相当可观的潜力[6]。
本文以钳形多吡啶化合物H2L[N,N'-二(3-甲基吡啶基)-2,6-吡啶二酰胺]为配体,与醋酸铜Cu(OAc)2·H2O反应合成了一种新颖的四核铜配位化合物——[Cu4L2(N3)2(μ2-N3)2]·CH3OH(1),其结构经IR、元素分析和X-射线单晶衍射表征。
1 实验部分
1.1 仪器与试剂
X-4型显微熔点仪;Nicolet NEXUS 470-FT-IR型红外光谱仪(KBr压片);MOD 1106型元素分析仪;Rigaku SATURN-724型单晶衍射仪(XRD)。
H2L按文献[7]方法制备;2,6-吡啶二甲酸,Aldrich公司;其余试剂均为化学纯或分析纯。
1.2 1 的合成
在反应瓶中依次加入 H2L 17 mg(0.05 mmol)的DMF(4 mL)溶液和Cu(OAc)2·H2O 20 mg(0.1 mmol)的甲醇(8 mL)溶液,搅拌使其溶解;于室温反应5 min。缓慢滴加 NaN313 mg(0.20 mmol)的甲醇(4 mL)溶液,滴毕,反应 2 min。过滤,滤液(澄清暗绿色)于室温静置14 d得暗绿色棒状晶体1,产率64%(以Cu计算);Anal.calcd for C19H15N11O3Cu2:C 39.86,H 2.64,N 26.92;found C 40.55,H 2.31,N 26.15。
1.3 晶体结构测定
将单晶1(0.25 mm ×0.21 mm ×0.11 mm)置衍射仪上,采用单色化的 MoKα射线 (λ=0.710 73 Å),于 293(2)K 以 ω -2θ方式扫描(3.21°≤θ≤27.48°)共收集衍射点 14 188 个。晶体结构采用直接法解出,并且用傅立叶技术扩展,按各向异性进行修正。最后采用全矩阵最小二乘法,依据可观察的衍射数据和可变参数进行校正,所有数据经LP因子校正。所有的计算均使用程序 SHELX-97[8]。CCDC:932 126。
2 结果与讨论
2.1 1 的表征
1的元素分析结果表明,其组成为C19H15N11O3Cu2,其中Cu与配体H2L的比例为2∶1,晶体结构证实1含有六个配位叠氮根,这与铜离子通常是四配位或六配位的情况相符。
1的IR谱图分析表明,3 389 cm-1和2 924 cm-1处较强的吸收谱带归属为酰胺的振动,1 660 cm-1处的强吸收谱带归属为羰基的吸收峰;1 608 cm-1和1 582 cm-1处的吸收峰可归为吡啶环的特征吸收峰,说明配合物中存在吡啶环的配位。
2.2 1的晶体结构
1的分子结构见图1,主要键长和键角见表1。晶体结构解析表明,1属单斜晶系,空间群C2/m,晶胞参数 a=15.774(3)Å,b=15.062(3)Å,c=10.724(2)Å,β =114.91(3)°,V=2 344.0(8)Å3,Z=4,Dc=1.736 mg·cm-3,μ =1.869 mm-1,R1=0.120 1,ωR2=0.298 4。
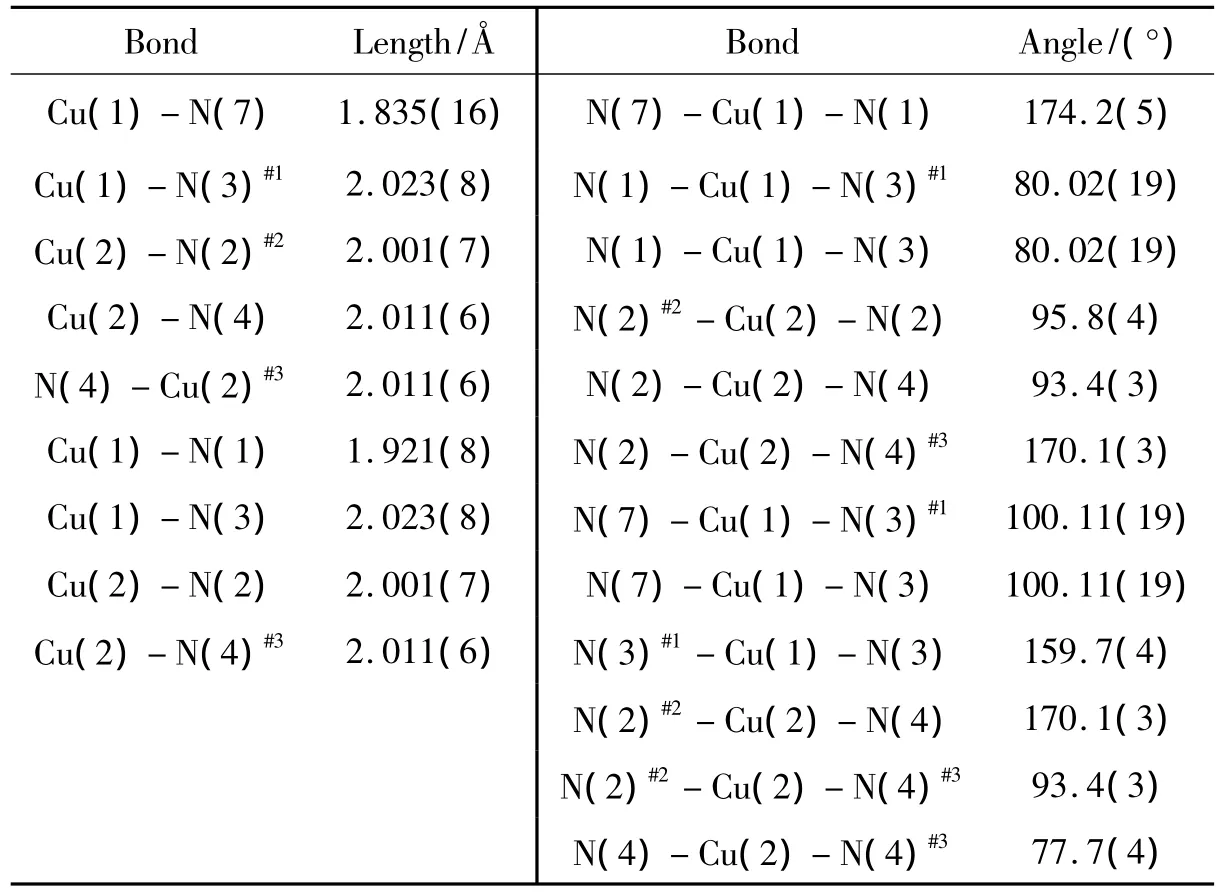
表1 1的主要键长和键角Table 1 Selected bond lengths and angles of 1

图1 1的分子结构图Figure 1 Molecular structure of 1
由图1和表1可见,配体L表现为五齿配位模式,两个L配体被两个Cu(Ⅱ)连接在一起形成了一个环状的结构。四个金属铜原子通过两个L配体和四个N3-连接在一起,形成了一个奇特的四核铜结构。在1中,有两种配位构型不同的金属铜原子。其中Cu1和Cu1A分别与三个来自L配体的氮原子和一个来自N3-的氮原子配位形成平面四边形构型,金属铜原子位于平面四边形的中心。Cu2和Cu2A分别与来自两个L配体的氮原子和两个来自边桥μ2-N3-的氮原子配位形成平面四边形构型,使两个L配体连接在一起形成了一个环状的结构;而两个N3-孤对电子被两个铜原子共用,桥联着Cu2和Cu2A,使整个分子呈现一个“双环”结构,金属中心Cu(2)-Cu(2A)距离为3.133 Å,而且该“双环”结构采用的是稳定的椅式构象。
3 结论
以多吡啶化合物H2L为配体,与醋酸铜反应合成了一种新的四核铜化合物1。1中的H2L存在两个亚甲基,造成了“钳形”多吡啶配体“双臂”上配位点距离的加大,更易形成较大的环结构,同时,该配体也因此具有一定柔性的特点,造成了其配位模式的多样性,在1中表现为五齿配位模式,形成了一个新颖的具有“双环”的四核铜结构。
另一方面,阴离子N3-参与了配位。由于N3-基团体积较小,配位灵活,两个μ-N3-将两个金属铜原子连在一起形成了一个较小的四边形的环状结构。可见,在金属-有机配合物的构筑中,阴离子除了起到平衡电荷作用外,还在结构新颖配合物的构筑中起到了重要作用。
[1] 沈家骢,孙俊奇.超分子科学研究进展[J].中国科学院院刊,2004,19:420-424.
[2] Zhang J P,Lin Y Y,Huang X C,et al.Copper(Ⅰ)1,2,4-Triazolates and related complexes:Studies of the solvothermal ligand reactions,network topologies,and photoluminescence properties[J].J Am Chem Soc,2005(127):5495-5506.
[3] Fujita M,Kwon Y J,Washizu S.Preparation,clathration ability,and catalysis of a two-dimensional square network material composed of cadmium(Ⅱ)and 4,4'-bipyridine[J].J Am Chem Soc,1994(116):1151-1152.
[4] Moon D,Kang S,Park J,et al.Face-driven cornerlinked octahedral nanocages:M6L8 cages formed by C3-symmetric triangular facial ligands linked via C4-symmetric square tetratopic PdⅡIons at truncated octahedron corners[J].J Am Chem Soc,2006(128):3530-3531.
[5] Noro S I,Kitagawa S,Kondo M,et al.A new,methane adsorbent,porous coordination polymer [{CuSiF6(4,4'-bipyridine)2}n][J].Angew Chem Int Ed,2000(39):2081-2084.
[6] Hou H W,Meng X R,Song Y L,et al.Two-dimensional rhombohedral grid coordination polymers[M(bbbt)2(NCS)2]n(M=Co,Mn or Cd;bbbt=1,1'-(1,4-butanediyl)bis-1H-benzotriazole):Synthesis,crystal structures,and third-order nonlinear optical properties[J].Inorg Chem,2002(41):4068-4075.
[7] Qin Z Q,Jennings M C,Puddephatt R J.Self-assembly in Palladium(Ⅱ)and Platinum(Ⅱ)chemistry:The biomimetic approach[J]Inorg Chem,2003,42:1956-1965.
[8] Sheldrick G M.SHELX-97.Program for the solution and refinement of crystal structures[K].University of Göttingen:Goöttingen,Germany,1997.
