核-壳和中空多面体二氧化钛制备、表征及光催化
2013-08-20何明明莫茂松
何明明 莫茂松
(北京有色金属研究总院 先进电子材料研究所,北京 100088)
0 引 言
二氧化钛(TiO2)作为光催化剂具有以下优势:首先,TiO2是N 型宽带隙(3.2 eV)半导体材料,其价带电子暴露于波长不大于387.5 nm 光照下会被激发到导带形成电子-空穴对,这些激发态电子具有比同类催化剂更高的激发态能量,能与空气中O2和H2O 更好地作用生成具有极高活性的·O2和·OH 自由基;其次,TiO2是环境友好材料,对环境无损害,可以利用钛白粉来净水,这比一些环境污染型的硫化物和其它重金属氧化物作为光催化剂更具优势;再次,TiO2稳定、易得且廉价[1-3]。一直以来,为了进一步提高TiO2的光催化活性,科学家们尝试了许多策略和方法,从形貌控制到过渡金属掺杂,从负载贵金属到做成异质结等特殊结构。在众多研究报道中,TiO2高活性晶面的可控暴露制备是近年来的研究热点[4-6]。Yang 等制备出了具有高活性面的多面体TiO2,高活性面的存在能有效提高TiO2的光催化效率[7-8];Han 等进一步将这些暴露的高活性晶面百分比提高到90%以上[9]。目前,如何调控提高多面体暴露高活性面的比表面以进一步提高TiO2的光催化效率是一个挑战性的难题。考虑到核-壳和中空结构具有大幅提高的比表面积,因此控制制备核-壳或中空纳米结构的TiO2是挑战性的研究方向之一。迄今为止,文献报道的核-壳或中空结构TiO2大多是微球状形貌的多晶结构[10-11],多面体单晶TiO2的中空或核-壳结构鲜见文献报道。
本文尝试采用二步水热法成功控制制备了核-壳和中空结构多面体单晶TiO2,所得两种结构的TiO2均有较大比表面积,且都为单晶结构,其光生电子有较大的平均自由程,这样可以避免光生电子与空穴的快速复合,保证电子能被顺利传导出TiO2表面,实现与环境有机污染物的有效结合,从而达到较高的光催化效率[12-14]。实验结果证实,利用目前方法得到的核-壳和中空结构多面体单晶TiO2具有优异的光催化性能,它们对亚甲基蓝的光催化降解效率能达到商业光催化剂P25 的最佳催化水平,且在加入一定量过氧化氢(H2O2)后,二者的催化效率能得到进一步提升。
1 实验部分
1.1 实验试剂
Ti 粉(Aladdin,300 目,纯度99.99%)、硫脲(国药集团化学试剂北京有限公司,AR)、硫胺(国药集团化学试剂北京有限公司,AR)、氨水(国药集团化学试剂北京有限公司,AR)、过氧化氢(Aladdin,30%,AR)、氢氟酸(Aladdin,40wt%,AR)、乙醇(国药集团化学试剂北京有限公司,AR)、超纯水(18 MΩ·cm)。所有试剂均未经进一步提纯处理。
1.2 样品制备
称量0.2 mmol 钛粉并置于容量为50 mL 的内衬聚四氟乙烯的不锈钢反应釜中,按顺序分别加入27 mL 超纯水、0.1~0.15 mL 氢氟酸。将反应釜密封后置于180 ℃的数字式烘箱中保温8 h 制备不同厚度实心多面体TiO2,待反应釜自然冷却到室温后,开釜并向溶液中加入1 mmol 硫脲和3 mL 过氧化氢,再次将反应釜密封后置于180 ℃条件下保温8~12 h,将产物用离心机分离收集,用超纯水和乙醇各洗涤3 次后,置于60 ℃空气中烘10 h,以供表征。
1.3 样品表征
采用日本岛津XRD-6000 型X 射线衍射仪(XRD)对样品相结构和相组成进行表征(Cu 靶Kα 辐射,λ=0.154 18 nm,加速电压40 kV,电流40 mA,扫描范围10°~90°,扫描速率为2°·min-1,步宽0.033°)。采用Hitachi S-4800 冷场发射扫描电子显微镜(FESEM) 来观察样品的微观形貌。采用美国Tecnai G2F20 场发射透射电子显微镜(TEM/HRTEM)观察样品的微观结构和晶型。
1.4 光催化性能测试
本文利用8 组实验来测试不同结构TiO2对亚甲基蓝溶液的降解率,分别为:(1)H2O2(1 mL);(2)P25(0.05 g);(3)实心厚多面体TiO2(0.05 g);(4)实心薄多面体TiO2;(5)核-壳多面体TiO2(0.05 g);(6)中空多面体TiO2(0.05 g);(7)核-壳多面体TiO2(0.05 g)+H2O2(1 mL),(8)中空多面体TiO2(0.05 g)+H2O2(1 mL)。文中用来测试的TiO2均经过500 ℃煅烧2 h 处理以除去表面F-和其它配位基团[15]。实验前将8 组样品先进行10 min 超声处理,使样品中的颗粒分散均匀,然后分别分散到50 mL 浓度为10 mg·L-1的亚甲基蓝溶液中,将得到的悬浊液暴露于30W 的紫外灯下,每隔30 min 采1 次样,用离心分离法去除样品中TiO2,再用日本岛津UV-1800 紫外可见分光光度计测量离心分离后所得上清液中亚甲基蓝溶液的吸光度,通过吸光度的变化来观测亚甲基蓝溶液浓度的变化。本研究之所以选用H2O2作为辅助光催化试剂,是由于H2O2本身对亚甲基蓝的降解作用极其微弱,可以忽略不计[16-17],且H2O2在光催化反应中不仅能提供活性氧分子使TiO2表面的e-/h+得到有效分离(Equ.1),还能有效抑制亚甲基蓝溶液自身被还原而造成的溶液褪色情况发生。低浓度范围内亚甲基蓝吸光度和浓度之间有很好的线性关系,且遵守Lambert-Beer 定律,因此可以用脱色率来衡量亚甲基蓝的降解程度。试样的脱色率η 用下式计算:
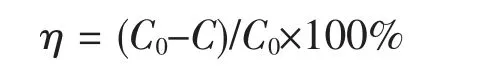
式中C0:亚甲基蓝溶液的初始浓度(mg·L-1);C:不同光照时间亚甲基蓝溶液的浓度(mg·L-1)。
Equ.1:
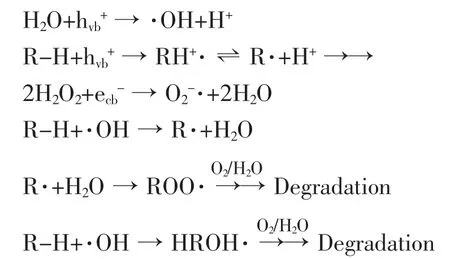
其中R-H 代表有机染料,hvb代表空穴,e 代表电子,·OH 代表活性氢氧根自由基[18]。
2 结果与讨论
2.1 样品SEM 表征结果分析


图1 不同结构多面体TiO2 的SEM 图Fig.1 SEM images of thick polyhedral TiO2 (a) thin polyhedral TiO2(b), core-shell polyhedral TiO2(c), and hollow polyhedral TiO2 (d)

值得注意的是,(001)氟离子先被拉出的地方会优先发生腐蚀形成凹坑,而后被拉出的地方则会腐蚀滞后,这两个过程同时作用可能对核-壳和中空多面体TiO2最终结构的均匀性产生一定影响。
应当注意的是,在第一步钛粉与氢氟酸反应的过程中若氢氟酸含量较少(0.1~0.13 mL),则少部分生成的实心多面体TiO2可能会发生团聚,团聚的粒子将不利于第二次水热中配位和弱酸性腐蚀反应的进行,结果是影响产物最终的均匀性。增加氢氟酸量(0.13~0.15 mL)可以有效防止实心多面体TiO2团聚,但过多的氢氟酸会部分溶解生成的TiO2产物,不利于最终产品的收集。因此,如何有效防止第一步水热中实心多面体TiO2团聚同时又不影响最终产物的收集是一个值得继续深入研究的方向。另外,多面体(101) 侧面上的6 配位钛离子也有较小可能发生配位和弱酸性腐蚀,使原本分散性较好的粒子在第二步水热过程中团聚,影响产物最终均匀性。
2.2 样品XRD 和TEM 表征结果分析
图2 给出所制备两种特殊结构TiO2与标准锐钛矿晶型TiO2的XRD 对比图。从图中我们可以得出如下信息:(1) 核-壳和中空结构多面体TiO2的衍射峰与标准锐钛矿的衍射峰对应的非常好,说明核-壳和中空多面体TiO2是锐钛矿晶型的晶体;(2)XRD 谱图中,所有锐钛矿晶型特征峰都非常明显,没有其它杂峰,表明制备过程中残留在核-壳和中空多面体TiO2中的其它反应物已去除干净;(3) 核-壳和中空结构多面体TiO2XRD 谱图中峰值出现的位置相对于体相锐钛矿有轻微的角度偏移,这可能源于二者特殊的内部结构。
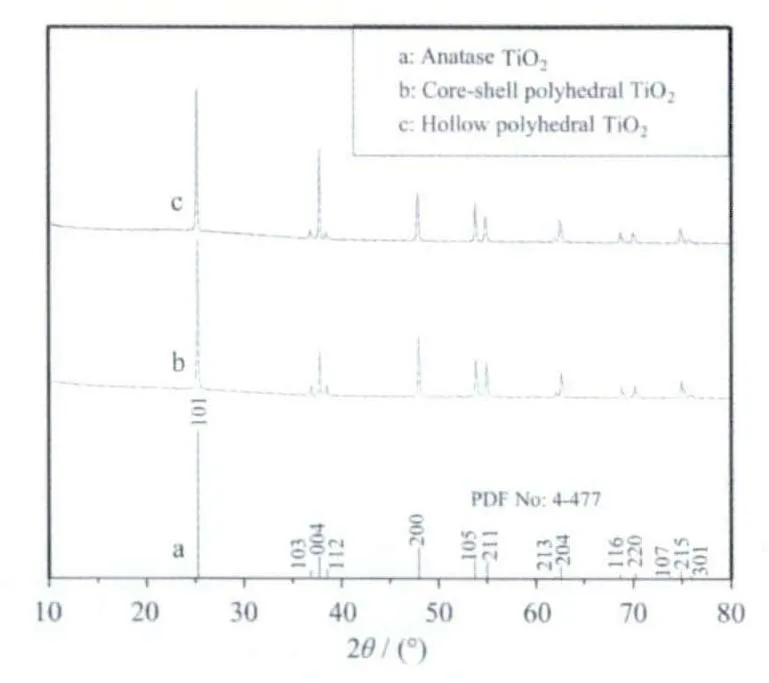
图2 不同结构TiO2 的XRD 图Fig.2 XRD patterns of TiO2 with different structures

2.3 多面体TiO2 制备过程中的影响因素
2.3.1 配位和弱酸性腐蚀作用时间的影响

图3 不同结构TiO2 的TEM 和SAED 图Fig.3 TEM and SAED images of TiO2 with different structure

表1 配位和弱酸性腐蚀共同作用时间对核-壳和中空多面体TiO2 结构的影响Table 1 Effect of complexing and weak acid etching time to core-shell and hollow polyhedral TiO2

图4 不同HF 加入量和配位腐蚀时间所制TiO2 的SEM 图及TiO2 形貌演变示意图Fig.4 SEM images of TiO2 and schematic illustration of TiO2 with different structure
在配位和弱酸性腐蚀共同作用过程中,观察产物结构随反应时间的变化有助于了解整个反应过程。扫描电镜观察结果显示: 氢氟酸加入量为0.1 mL 的样品在加入过氧化氢和硫脲经5 h 配位腐蚀和弱酸性环境作用后,(001)/(001)会生成大面积的凹坑(图4a),部分凹坑边缘还能观察到明显的斜面,继续延长配位和弱酸性腐蚀共同作用时间至12 h,凹坑不是均匀地沿垂直于[001]方向伸展,而只是在靠近边缘处继续往里深透,最终生成核-壳结构多面体TiO2(图1a),再继续延长保温时间对最终结构影响不大,并且由于配位和弱酸性腐蚀共同作用的不均匀性还可能导致核-壳结构碎裂,不利于最终结果的观察。

2.3.2 不同配位剂的影响

在制备中空多面体TiO2的实验中,只有过氧化氢与硫脲同时加入才能制备得到中空结构多面体TiO2,用硫胺和氨水替代硫脲则得不到中空结构的多面体TiO2,这也说明过氧化硫脲提供的配位和弱酸性腐蚀共同作用对最终结构的形成至关重要。

表2 不同配位剂对产物最终结构的影响Table 2 Effect of different complexing agents to final structure

图5 不同配位剂制得的TiO2Fig.5 TiO2 prepared by different complexing agents
2.4 不同结构多面体TiO2 光催化性能测试结果分析
洞开的核-壳和中空结构多面体TiO2展示了异常高效的光催化性能。图6 是八组光催化实验数据的UV-Vis 吸收光谱曲线图。图6a 是只加H2O2而不加任何TiO2的亚甲基蓝吸收光谱图,从图中可以看出经120 min 光催化反应后,只加H2O2的实验组亚甲基蓝的光吸收峰值基本不变,这表明H2O2本身对亚甲基蓝并没有降解作用,光催化降解主要是依靠TiO2的催化效果。图6b 是商业光催化剂P25 对亚甲基蓝降解作用的UV-Vis 吸收光谱,由图可知,经30 min 催化降解,亚甲基蓝的光吸收峰值已经降到0.5 左右,降解效率接近70%,继续延长P25 的光催化时间,降解效率不再有大的变化,120 min 光催化反应后,亚甲基蓝的吸收峰值从最初的1.5 降到了0.3 左右,降解率达到80%,这证明P25 具备较好的光催化效率,能在短时间内达到较高的光催化降解值,并且由于P25 粒子的小尺寸效应,图6b 中亚甲基蓝的吸收光谱还出现了微弱的蓝移现象。具体的P25 光催化效率与P25 的颗粒剂量,溶液PH 及溶氧量还有关系[24]。
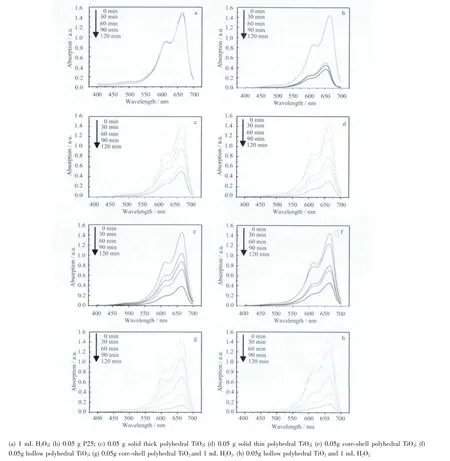
图6 不同结构TiO2 对亚甲基蓝进行催化降解的紫外可见吸收光谱图Fig.6 UV-Vis spectra of Methylene Blue by using different structured TiO2 to carry out photocatalysis
为考察核-壳和中空结构对光催化效率的影响,将第一步水热中制备的实心厚多面体TiO2和核-壳结构多面体TiO2作为一组对比二者的光催化性能(图6c,6e),将第一步水热中制备的实心薄多面体TiO2和中空结构多面体TiO2作为另一组对比二者的光催化性能(图6d,6f)。结果表明:实心厚多面体TiO2经120 min 催化降解,亚甲基蓝的吸收峰值降到了0.4 左右,而核-壳结构多面体TiO2经120 min 催化降解,亚甲基蓝的吸收峰值降到了0.3 左右,二者最终的降解效率差别在0.1 左右,这可能是由于核-壳结构虽然增大了TiO2的比表面积,但同时高活性(001)面的消失会部分抵消掉这种增大效果,导致最终二者的光催化活性相差不大,核-壳结构多面体TiO2的光催化活性只比实心厚多面体TiO2高10%左右。实心薄多面体TiO2由于高能量的(001)所占比例较大,经120 min 光催化降解后,亚甲基蓝的吸收峰值能降到0.3 左右,形成中空结构后,经120 min 光催化反应,亚甲基蓝的吸收峰值也降到了0.3 左右,与核-壳结构略微增大实心厚多面体TiO2光催化活性的机理相似,这可能是由于高活性(001)的洞开使光催化活性降低,而中空结构使多面体比表面积增大,比表面积增大的正作用与(001)消失的负作用相抵消,使得中空结构多面体TiO2的光催化效率与实心薄多面体TiO2相比较变化不大。
由上述实验可知: 核-壳和中空结构多面体TiO2的光催化效率略优于商业光催化剂P25,这可能一方面是由于核-壳和中空多面体TiO2的特殊内部结构,另一方面还可能与核-壳和中空结构多面体TiO2制备过程中用到的硫脲有关,有研究表明[25-26],硫脲可以对TiO2起到改性的作用,硫可以S4+的形式进入TiO2的晶格并取代部分Ti4+位,改性后的TiO2拥有更优异的光催化性能。
H2O2具有增强TiO2光催化效率的作用。图6g是加入1 mL H2O2之后核-壳结构多面体TiO2对亚甲基蓝的催化吸收光谱,与图6e 对比可知: 没加H2O2时亚甲基蓝在670nm 光频段处的最低吸收值为0.3,而加入H2O2后,经相同时间的催化降解,亚甲基蓝在670 nm 光频段处的最低吸收峰值可降到0.2 以下(0.1 左右),降解率超90%,表明核-壳多面体TiO2在加入H2O2做辅助催化后光催化性能得到了提升。同样,从图6f 和图6h 的对比中,我们也可以看出H2O2对TiO2光催化效率的提升作用。一方面,这可能是由于少量H2O2的加入改变了溶液的pH 值,在酸性条件下生成的·OH 量要远高于其他情况; 另一方面,H2O2有助于捕获催化降解反应过程中产生的电子,产生·OH 参与反应。对于不同剂量的催化剂,H2O2加入量还存在一个最佳值[27]。
此外,从图6f 和6h 的对比中还可以看出:两组实验中前60 min 亚甲基蓝在670 nm 光频段处的吸光度相差不多,90 min 后6h 中加入H2O2的光催化优势开始显现出来,在加入H2O2后,即使亚甲基蓝浓度降到非常低的水平,中空多面体TiO2依然可以保持对亚甲基蓝的高降解速率,表明H2O2不仅能提高TiO2的光催化效率,还能对TiO2的光催化特性进行优化。
以上8 组实验结果表明,核-壳和中空结构多面体TiO2具有优异的光催化性能,二者略优于P25的光催化活性,而加入H2O2能进一步提高核-壳和中空结构多面体TiO2的光催化性能,使它们的光降解能力得到明显提升(效率90%以上)。
图7 是亚甲基蓝溶液浓度随时间变化的关系曲线,由图中可以看出核-壳和中空结构多面体TiO2的光催化性能略优于P25,而加入了H2O2以后,形成的TiO2-H2O2复合光催化体系则能进一步提高核-壳和中空结构多面体TiO2的光催化效率。
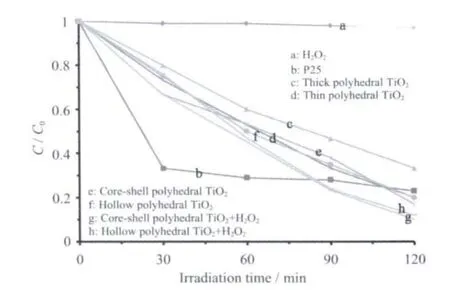
图7 不同样品使亚甲基蓝浓度随时间变化的关系曲线Fig.7 Variation of Methylene Blue concentration by photochemical reaction with different structured TiO2
3 结 论
本文以简单的水热法合成了核-壳和中空结构的多面体单晶TiO2,并对它们进行了结构表征和光催化性能测试。主要结论如下:
(1) 在温和的水热条件下,借助硫脲配位和弱酸性腐蚀的共同作用,可以制备得到洞开的核-壳和中空结构多面体TiO2;
(2) 核-壳结构和中空结构的多面体单晶TiO2具有优异的光催化性能,核-壳和中空结构多面体TiO2的光催化效率略优于P25,这可能一方面与洞开的多面体壳层结构提高了产物的比表面积有关,另一方面则与硫脲对TiO2的光催化改性有关;
(3) 加入H2O2可以进一步提高核-壳和中空结构多面体TiO2的光催化性能。
[1] Hironori A, Michele A, John N A, et al. Chem. Rev., 2001,101:953-996
[2] Fujishima A, Honda K. Nature, 1972,238:37-38
[3] Chen X B, Samuel S M. Chem. Rev., 2007,107:2891-2959
[4] ZANG Dan-Wei(臧 丹 炜), YANG Ya-Jun(杨 亚 君). Chem.Ind. Eng.(Huaxue Gongye Yu Gongcheng), 2010,27(1):79-83
[5] Jiang H B, Qian C, Wen C Z, et al. Angew. Chem. Int. Ed.,2011,50:3764-3768
[6] Wen C Z, Jiang H B, Qiao S Z, et al. J. Mater. Chem., 2011,21:7052-7061
[7] Yang H G, Sun C H, Qiao S Z, et al. Nature, 2008,453:638-642
[8] Yang H G, Liu G, Qiao S Z, et al. J. Am. Chem. Soc., 2009,131:4078-4083
[9] Han X G, Kuang Q, Jin M S, et al. J. Am. Chem. Soc., 2009,131:3152-3153
[10]CHANG Lin(常琳), LIU Jing-Bing(刘晶冰), WANG Jin-Shu(王金淑),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(5):744-748
[11] Liu B, Zeng H C. Small, 2005,1(5):566-571
[12]JIA Jin-Yi(贾进义), LIU Jing-Bing(刘晶冰), ZHANG Wen-Xiong(张 文 熊), et al. J. Inorg. Mater.(Wuji Cailiao Xuebao),2009,24(4):671-674
[13]XIAO Yao-Ming(肖尧明), WU Ji-Huai(吴季怀), YUE Gen-Tian(岳 根 田), et al. Acta Phys.-Chim. Sin.(Wuli Huaxue Xuebao), 2012,28(3):578-584
[14]XUE Hong-Xin ( 薛 红 星). Thesis for the Masterate of Zhejiang University(浙江大学硕士论文). 2011.
[15]ZHANG Xiu-Ling(张秀玲), SUN Dong-Feng(孙东峰), HAN Yi-Dang(韩 一 丹), et al. Chinese J. Inorg. Chem.(Wuji Huaxue Xuebao), 2011,27(7):1373-1377
[16]Su M H, He C, Virender K S, et al. J. Hazard. Mater., 2012,212:95-103
[17]Guo Z C, Chen B, Mu J B, et al. J. Hazard. Mater., 2012,219:156-163
[18]Chen C C, Ma W H, Zhao J C. Chem. Soc. Rev., 2010,39:4206-4219
[19]Serge A S, Reuben H S, Sergei V M. J. Chem. Soc., Dalton Trans., 2000,4:511-514
[20]Michele L, Andrea V, Annabella S. Phys. Rev., 2001,63(15):155409(1-9)
[21]Michele L, Annabella S. Phys. Rev. Lett., 2001,87(26):266105(1-4)
[22]Yang X H, Yang H G, Li C Z. Chem. Eur. J., 2011,17:6615-6619
[23]Pan J, Liu G, Lu G Q, et al. Angew. Chem. Int. Ed., 2011,50:2133-2137
[24]LIU Jin-Song(刘 劲 松),DAI Zhi-Ming(戴 智 铭). Chem.Produ. Technol.(Huagong Shengchan Yu Jishu), 2006,13(2):26-29
[25]SUN Ming(孙鸣), YU Zhan-Jiang(于占江), ZHANG Ya-Ting(张 亚 婷), et al. Appl. Chem. Ind. (Yingyong Huagong),2008,37(5):472-474
[26]ZHOU Wu-Yi(周武艺), CAO Qing-Yun(曹庆云), TANG Shao-Qiu(唐 绍 裘). J. Inorg. Mater.(Wuji Cailiao Xuebao),2006,21(4):776-782
[27]JI Xiu-Ying(吉秀英), QIU Yan(邱雁), XU Xuan(徐璇),et al. Chinese J. Environ. Eng.(Huajing Gongcheng Xuebao),2008,2(6):743-747
