A型产气荚膜梭菌滤液的质控标准研究
2013-08-14章振华景小冬陈小玲史爱华张建伟黄凤军姜北宇
章振华,李 林,沈 佳,景小冬,陈小玲,史爱华,张建伟,黄凤军,姜北宇
(北京市农林科学院畜牧兽医研究所,北京100097)
A型产气荚膜梭菌滤液系用A型产气荚膜梭菌菌株接种适宜培养基,收获培养液离心后取上清过滤而成。通常认为A型产气荚膜梭菌滤液中含有磷酸酯酶C[1-2],可用其取代价格昂贵的商品化磷酸酯酶C来处理鸡传染性支气管炎病毒(IBV),使该病毒表现出血液凝集(HA)活性,从而制备出IBV血凝抑制试验(HI)抗原[3-5]。IBV HI抗原用来检测鸡传染性支气管炎(IB)疫苗免疫后鸡群的HI抗体水平。目前国内IB灭活疫苗的效价检验都用进口IBV HI抗原来测定,我国还没有商品化的IBV HI抗原。课题组近年来一直研究如何制备出特异、敏感、稳定的IBV HI抗原,而作为制备IBV HI抗原一种重要的原材料,A型产气荚膜梭菌滤液质量的好坏直接关系到IBV HI抗原的质量。因此,建立A型产气荚膜梭菌滤液质控标准对于生产出合格的IBV HI抗原产品至关重要。一般认为磷酸酯酶C是使IBV呈现HA活性的酶类物质,只要测定A型产气荚膜梭菌滤液中磷酸酯酶C的含量,就能够确定A型产气荚膜梭菌滤液的准确加入量,从而建立起可靠的制备IBV HI抗原用A型产气荚膜梭菌滤液的质控标准。对A型产气荚膜梭菌滤液中的卵磷脂酶C进行含量测定有两种方法,一是小鼠致死性试验,由于卵磷脂酶C(α毒素)是A型产气荚膜梭菌培养过程中产生的最主要的外毒素[6-8],其含量的多少与小鼠致死性直接相关,因此,测定滤液对小鼠的最小致死剂量(MLD)可间接反应卵磷脂酶C的含量;二是卵磷脂酶活性试验,采用蛋黄琼脂平板培养基直接测定A型产气荚膜梭菌滤液中卵磷脂酶C的含量,其原理是卵磷脂酶C在钙、镁离子存在的条件下,迅速水解卵黄中的卵磷脂,生成甘油二酸酯和磷酸胆碱;在加有滤液的孔周围产生混浊环,卵黄被分解产生的游离脂肪和卵黄磷蛋白反应而产生沉淀[5,9]。利用卵磷脂的水解试验可证明卵磷脂酶C的存在,以及通过将滤液作不同稀释后进行测定,确定滤液中卵磷脂酶C含量。
本研究对29批次A型产气荚膜梭菌滤液进行了小鼠致死性试验、卵磷脂酶活性试验、处理IBV后的其HA活性试验及滤液最小加入量试验,观察A型产气荚膜梭菌滤液的小鼠最小致死量、磷酸酯酶C含量与滤液处理过的浓缩IBV的HA效价之间的相关关系,从而以滤液的小鼠最小致死量或磷酸酯酶C含量为基础单位确定A型产气荚膜梭菌滤液最佳使用量,以此作为菌滤液质控标准。如果这两个指标不能作为滤液的质控标准,可考虑直接以滤液处理IBV后的其HA活性达到要求的抗原效价作为质控标准,通过这些试验筛选出一个A型产气荚膜梭菌滤液的质控标准。
1 材料与方法
1.1 材料
A型产气荚膜梭菌滤液共29批次,由北京市农林科学院畜牧兽医研究所动物免疫与预防研究室采用A型产气荚膜梭菌BZ株接种厌氧肉肝汤培养基或厌氧肉肝胃酶消化汤培养基制备而成;卵磷脂酶试验培养基按参考文献[5]方法自制;100倍浓缩IBV M41株病毒液(批号为20120511),SPF鸡血清,IBV阳性血清,NDV阳性血清,H9亚型禽流感病毒阳性血清,HA缓冲液,10mL/L的鸡红细胞悬液,250g/L的高岭土悬液,均由本研究室自制。
卵磷脂酶C(批号061M8623V,125U/瓶),购自SIGMA公司;16g~20g昆明雄性小鼠,购自军事科学院实验动物中心。
A型产气荚膜梭菌兔阳性血清(批号20090715)及A型产气荚膜梭菌α毒素单因子血清(批号20080611),中国兽医药品监察所细菌室蒋玉文研究员惠赠。
1.2 方法
1.2.1 小鼠致死性试验 先将A型产气荚膜梭菌滤液用灭菌生理盐水作倍比稀释,从1∶2稀释至1∶4或1∶8或1∶16;然后,以A型产气荚膜梭菌滤液原液及不同稀释度的滤液经尾静脉途径接种16g~20g的昆明小鼠,每批次滤液原液及不同稀释度滤液均各接种2只,每只0.2mL,接种后观察2d,记录死亡小鼠数,测定相同培养方法制备的不同批次A型产气荚膜梭菌滤液对小鼠的最小致死量(MLD)。
1.2.2 卵磷脂酶活性试验 先将A型产气荚膜梭菌滤液用灭菌生理盐水作倍比稀释,从1∶2稀释至1∶256;然后,在卵磷脂酶试验培养基上用打孔器(直径为3mm)打孔,取A型产气荚膜梭菌滤液原液及不同稀释度的滤液分别加入到培养基相应孔中,每孔加0.25mL,加完后放37℃温箱孵育,观察72h,以出现卵磷脂水解而孔周围形成混浊环的滤液最高稀释倍数作为判定终点。
1.2.3 处理后IBV的HA活性试验 分别取不同批次的A型产气荚膜梭菌滤液0.05mL加入到0.45mL 100倍浓缩的IBV M41株病毒液中,充分混匀,放37℃恒温振荡器感作2h,取出置2℃~8℃条件下48h,测定其HA效价。
1.2.4 制备IBV HI抗原的滤液最小加入量 从被检29批次A型产气荚膜梭菌滤液中选出10批次,分别以20%、10%、5%、2.5%、1.25%的量加入到100倍浓缩的IBV M41株病毒液中,充分混匀,放37℃恒温振荡器感作2h,取出置2℃~8℃条件下48h,测定其HA效价;观察A型产气荚膜梭菌滤液的加入量与IBV M41株抗原血凝价的关系。
1.2.5 商品化卵磷脂酶C处理后IBV的HA活性试验 将商品化卵磷脂酶C用HA缓冲液配制0.125U/mL~4U/mL的溶液,以不同酶含量加入到IBV浓缩病毒液中,加完后充分混匀,放37℃恒温振荡器感作2h,取出置2℃~8℃条件下48h,测定其HA效价。
1.2.6 卵磷脂酶C处理IBV获得血凝活性的试验试验分为3组,第1组用A型产气荚膜梭菌滤液和A型产气荚膜梭菌抗血清等量混合,第2组用A型产气荚膜梭菌滤液和产气荚膜梭菌α毒素单因子血清等量混合,第3组用A型产气荚膜梭菌滤液和HA缓冲液等容量混合。将上述3组混合样品在37℃条件下中和50min;分别将上述中和样品用灭菌生理盐水作倍比稀释,从1∶2稀释至1∶256,取中和样品原液及不同稀释度的中和样品分别加入到卵黄琼脂平板培养基相应孔内,观察卵磷脂酶效价,进行卵磷脂酶活性试验;然后,每组各取0.4mL浓缩IBV分别与0.1mL的1组~3组中和样品进行混合,制备IBV HI抗原,同时,设1个对照组(第4组)将0.4mL浓缩IBV与0.1mL HA缓冲液混合,进行处理浓缩IBV HA活性试验,通过试验观察卵磷脂酶C在使IBV获得血凝活性中所起的作用。
2 结果
2.1 A型产气荚膜梭菌滤液小鼠最小致死量、卵磷脂酶效价、处理IBV后其HA效价试验结果
对29个批次的A型产气荚膜梭菌滤液进行了小鼠致死活性试验、卵磷脂酶活性试验、处理后IBV的HA活性试验。从表1试验结果来看,不同批次的A型产气荚膜梭菌滤液对小鼠致死活性存在较大差异,从原液0.2mL/只不致死,到8倍稀释液0.2mL/只全部致死,滤液对小鼠的最小致死量(MLD)最低为小于 5MLD/mL,最高达到 40 MLD/mL;不同批次的滤液卵磷脂酶效价也存在较大差异,最低为1∶2,最高为1∶64;分别用29个批次A型产气荚膜梭菌滤液,以10%的加入量处理浓缩IBV,制备IBV HI抗原,其抗原的HA效价均≥7log2。同批滤液小鼠MLD低,其卵磷脂酶效价也低,而滤液小鼠MLD高,其卵磷脂酶效价也高。表中第6、8、11、13、14、16、21、22、23、29批滤液没有测出小鼠MLD,这些批次的滤液卵磷脂酶效价也较低,仅在1∶2~1∶8之间;滤液小鼠最小致死量为5MLD/mL时,卵磷脂酶效价在1∶16~1∶32之间;滤液小鼠最小致死量为10MLD/mL时,卵磷脂酶效价达到1∶32;滤液小鼠最小致死量高于20 MLD/mL时,卵磷脂酶效价达到1∶64。证明A型产气荚膜梭菌滤液的小鼠MLD与卵磷脂酶效价之间存在着明显的正相关关系。而不论滤液的小鼠MLD和卵磷脂酶效价高或是低(在1∶2~1∶64之间),不同批滤液处理后IBV的HA活性均较好,其抗原HA效价均≥7log2,证明滤液处理IBV的HA活性与小鼠MLD和卵磷脂酶效价没有明显的关系。

表1 29批A型产气荚膜梭菌滤液小鼠最小致死量、卵磷脂酶效价、处理IBV后其HA效价试验结果Table 1 Test results of minimum lethal dose in mice,lecithinase activity,HA activity of the treated IBV in 29batches of the culture filtrate of Clostridium perfringens type A
2.2 A型产气荚膜梭菌滤液最小加入量试验
从29批A型产气荚膜梭菌滤液中选出10批,分别以1.25%~20%的量加入到100倍浓缩的IBV M41株病毒液中制备IBV HI抗原。从表2可以看出,A型产气荚膜梭菌滤液的加入量与IBV M41株抗原血凝价存在相关关系,滤液加入量为1.25%时,IBV抗原效价在3log2~6log2之间;滤液加入量为2.5%时,IBV抗原效价基本均为6log2;滤液加入量为5%~20%时,IBV抗原效价在7log2~8log2之间。以5%~20%的A型产气荚膜梭菌滤液处理浓缩的IBV M41株病毒液,均可制备出符合要求的IBV HI抗原,A型产气荚膜梭菌滤液的最小加入量为2.5%~5%。

表2 A型产气荚膜梭菌滤液加入量与IB HI抗原HA效价的关系Table 2 The relationship between the adding amount of the filtrate of type AClostridium perfringens and HA titer IB HI antigen
2.3 商品化卵磷脂酶C处理IBV的HA活性试验
3次不同酶加入量试验结果显示,卵磷脂酶C的加入量为0.125U/mL至4U/mL均可制备出效价符合要求的抗原。分别用卵磷脂酶C及A型产气荚膜梭菌滤液处理制备出的2种抗原测定血清IBV HI效价,结果,IBV阳性血清均为阳性,SPF鸡血清及其它病原阳性血清均为阴性,且用这2种抗原所测定出的IBV HI效价结果完全相同。
2.4 卵磷脂酶C处理IBV获得血凝活性的试验结果
将A型产气荚膜梭菌滤液分别与A型产气荚膜梭菌抗血清和产气荚膜梭菌α毒素单因子血清在37℃条件下中和50min后,进行卵磷脂酶活性试验及处理后IBV的HA活性试验。表3结果显示,A型产气荚膜梭菌滤液加等量HA缓冲液组(即滤液对照组)的卵磷脂酶效价为1∶32,处理IBV后出现了血凝活性,其HA价达到8log2,而两种血清中和组样品的卵磷脂酶效价均为0,证明两种血清可有效地中和A型产气荚膜梭菌滤液中的卵磷脂酶C,然而,A型产气荚膜梭菌滤液与A型产气荚膜梭菌抗血清中和的样品处理IBV后,未出现血凝活性,而A型产气荚膜梭菌滤液与产气荚膜梭菌α毒素单因子血清中和的样品,虽然卵磷脂酶效价为0,但处理浓缩IBV后,也出现了血凝活性,HA价达到6log2,提示可能还存在产气荚膜梭菌α毒素(卵磷脂酶C)之外引起IBV抗原具有血凝活性的物质。
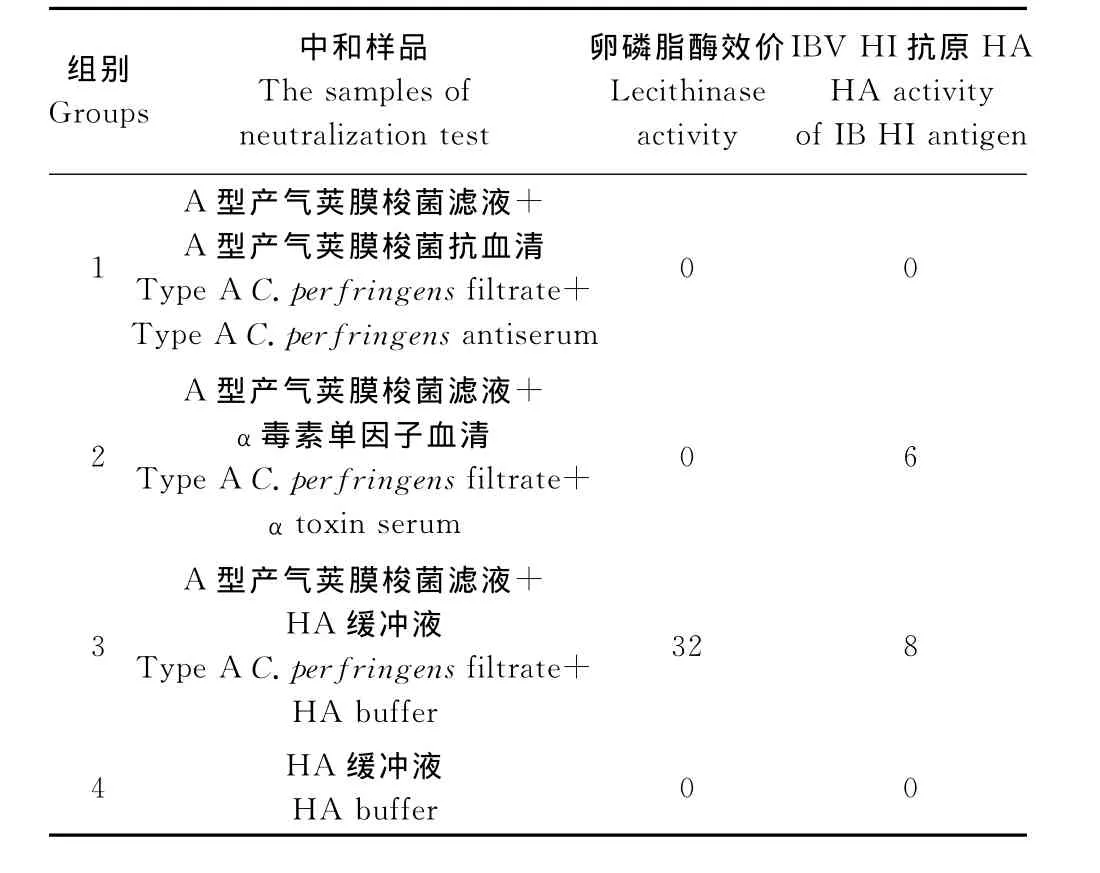
表3 滤液抗血清、α毒素单因子血清与滤液的中和试验结果Table 3 Results of neutralization test of the antiserum of the filtrate and theαtoxin with the filtrate
3 讨论
对29批A型产气荚膜梭菌滤液进行了小鼠致死性试验、卵磷脂酶活性试验、处理后IBV的 HA活性试验及制备IBV HI抗原的滤液最小加入量等试验,结果显示虽然不同批次的A型产气荚膜梭菌滤液的MLD、卵磷脂酶效价存在较大差异,但制备的IBV HI抗原的HA效价均达到了≥7log2,而且滤液最小加入量基本相同。这提示滤液中的卵磷脂酶C的含量与滤液使浓缩IBV获得HA活性没有明显的相关关系,卵磷脂酶C可能不是使浓缩IBV获得HA活性的物质,而是滤液中其它未知的成分。“陆生动物诊断试验和疫苗手册(哺乳动物、禽鸟与蜜蜂)第五版,2004”第799页中介绍,“最初发现商品化的Ⅰ型卵磷脂酶C可促进HA活性,似乎是一个污染的酶而不是卵磷脂酶在发挥作用”[10]。根据这一推测我们对卵磷脂酶C在使IBV获得血凝活性中所起的作用进行了研究,结果证明尽管A型产气荚膜梭菌滤液中的卵磷脂酶C被中和掉了,但其使IBV出现血凝活性的物质仍然存在。试验结果看起来与商品化卵磷脂酶C能使IBV呈现血凝活性的事实不符,然而,进一步了解得知商品化卵磷脂酶C也是由产气荚膜梭菌制备的,我们推测在卵磷脂酶C的制备过程中可能由于纯化不彻底,保留了能使IBV出现血凝活性的成分,从而直接导致了卵磷脂酶C能使IBV获得血凝活性的假象。因此,以卵磷脂酶C的含量即小鼠MLD与卵磷脂酶效价来建立制备IBV HI抗原所用滤液的质控标准,看来是不可行的。
用29个批次的A型产气荚膜梭菌滤液,以10%的加入量处理浓缩IBV,制备IBV HI抗原,其IBV HI抗原的HA效价均达到≥7log2,均符合要求,这证明所制备的A型产气荚膜梭菌滤液的质量是稳定的,可以充分保证所制备出的IBV HI抗原的质量。根据以上结果,我们建立了制备IBV HI抗原所用滤液的质控标准,即滤液处理IBV后的HA活性试验为滤液质控标准:取A型产气荚膜梭菌滤液0.05mL加入到0.45mL 100倍浓缩的IBV M41株病毒液中,充分混匀,放37℃恒温振荡器感作2h,取出置2℃~8℃条件下48h,测定其HA效价,其IB HI抗原的HA效价应≥7log2。该方法简单可靠,可直接反应滤液使IBV获得血凝活性的能力。
致谢:本研究得到了中国兽医药品监察所细菌室蒋玉文主任的精心指导及大力帮助,在此表示深深的感谢!参考文献:
[1] 姜 平.兽医生物制品学[M].2版.北京:中国农业出版社,2003:359-361.
[2] 陆承平.兽医微生物学[M].4版.北京:中国农业出版社,2007:191-195.
[3] 林 雪,辛朝安.微量血凝抑制试验检测鸡传染性支气管炎抗体的研究[J].中国兽医科技,1995,25(6):8-10.
[4] 姜北宇,郑世兰,刘月焕,等.鸡传染性支气管炎HA抗原的制备及HI试验方法的建立[J].实验动物科学与管理,1998,15(3):13-17.
[5] 陈天寿.微生物培养基的制造与应用[M].北京:中国农业出版社,1995:407.
[6] 吕存女,张敬友,赵 红,等.微量法测定产气荚膜梭菌α毒素[J].兰州大学学报:自然科学版,2000,36(6):101-104.
[7] 郭明章,何正礼,董亚芳.对A型产气荚膜梭菌生长和产生毒素的观察[J].中国兽医科技,1991,21(9):20-22.
[8] 蒋玉文.产气荚膜梭菌α毒素研究进展[J].中国兽药杂志,2001,35(6):41-45.
[9] 费恩阁,李德昌,丁 壮.动物疫病学[M].北京:中国农业出版社,2004:637-643.
[10] 世界动物卫生组织.陆生动物诊断试验和疫苗手册:哺乳动物、禽鸟与蜜蜂 [M].5版.农业部兽医局/中国动物卫生与流行病学中心,译.世界动物卫生组织,2004:799.