Box-Behnken响应面法优化黄芩素微丸的缓释包衣处方
2013-07-25黄廼奇杨春欣吕迁洲
沈 熊, 梁 健, 黄廼奇, 杨春欣, 吕迁洲
(复旦大学附属中山医院药剂科,上海200032)
黄芩素 (Baicalein)异名:黄芩苷元,黄芩黄素,为唇形科Labiatae黄芩属Scutellaria多年生草本中药植物黄芩Scutellaria baicalensis Georgi的干燥根中提取的黄酮类化合物,是黄芩的最主要活性成分之一,具有抗菌、抗病毒、抗炎、抗氧化、抗肿瘤、抗纤维化及心脑血管、神经元保护等药理作用,提示黄芩素具有多层次、多途径、多靶点的药理活性作用[1]。黄芩素在胃和小肠中吸收良好,在结肠中有少量吸收,提示适宜制成缓控释制剂[2,3]。微丸作为多单元剂型,具有受生理因素影响小、胃肠道分布广、释药变异小等优点,因此是缓控释和靶向制剂的优良剂型[4]。
Eudragit RS与Eudragit RL属于水不溶性成膜材料,在水中可溶胀,Eudragit RS比Eudragit RL渗透性和溶胀性小,将二者配合使用,可有效调节包衣型缓释制剂的释药速率[5]。本研究应用Box-Behnken试验设计法优选出释放效果理想的缓释包衣处方,并检验模型的预测性。
1 材料与仪器
黄芩素原料 (陕西慈缘生物技术有限公司),黄芩素对照 (中国食品药品检定研究院,批号1115952200604);微晶纤维素丸芯 (Celphere 507,日本旭化成公司);Eudragit RS 30D与Eudragit RL 30D(上海罗姆公司药用树脂部);聚乙烯吡咯烷酮 (PVP K29/32,国际特品公司);羟丙甲纤维素 (HPMC,6cps,上海卡乐康包衣技术有限公司);柠檬酸三乙酯 (TEC,美国Morflex公司),甲醇、乙腈为色谱纯,其它试剂均为分析纯。
气流粉碎机 (JGM-H50型,华东理工大学),流化床包衣机 (GPCG 1,Glatt,德国);智能溶出仪 (ZRS-4型,天津大学无线电厂);Agilent 1200高效液相色谱系统 (美国)。
2 方法和结果
2.1 黄芩素缓释微丸的制备
2.1.1 载药微丸的制备 用气流粉碎机对原料药物进行微粉化。以25%PVP水溶液为黏合剂,搅拌下将微粉化的黄芩素 (粒径2~10 μm)分散于其中制成混悬液。将空白丸芯至于包衣机中,采用底喷法,丸芯在流化状态下预热5 min,工艺条件见表1,包衣过程中需对包衣液持续搅拌。包衣完成后,再包一层HPMC层作为隔离层,增加质量2%。
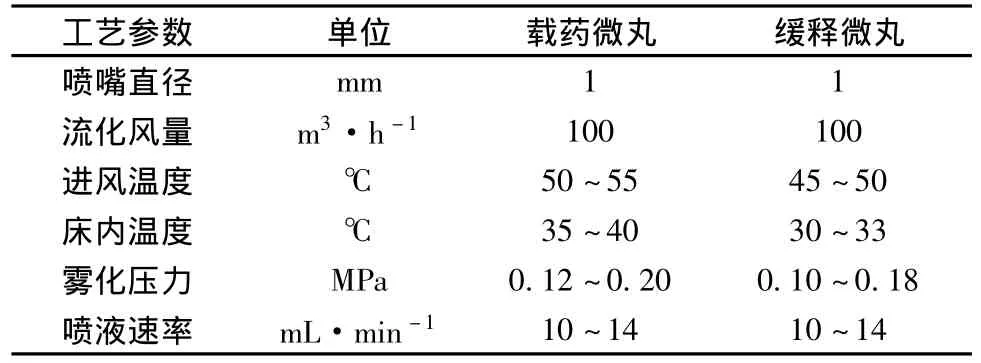
表1 黄芩素载药微丸和缓释微丸制备工艺参数Tab.1 Process parameters for baicalein layering and the sustained release coating of layered pellets
2.1.2 缓释微丸的制备 分别称取Eudragit RS 30D与Eudragit RL 30D两种水分散体,按预定比例混合,加水适量,搅匀。将滑石粉、柠檬酸三乙酯和消泡剂 (甲基硅油)加入适量水中,混匀。将此混悬液缓慢倒入上述水分散体中,搅匀,过80目筛,即得缓释包衣液。取黄芩素载药微丸适量至于包衣机中,采用底喷法,按表1工艺参数制备,包衣结束后同样包一HPMC隔离层。
2.2 黄芩素缓释微丸含量测定方法
2.2.1 色谱条件 Phenomenex Luna C18色谱柱(150 mm×4.6 mm,5 μm),流动相为0.05%三氟乙酸-乙腈-甲醇 (55∶20∶25);体积流量 1.0 mL/min;检测波长272 nm;柱温30℃,进样量20 μL。
2.2.2 测定方法 取黄芩素对照品适量,精密称定,加流动相制成每1 mL含500 μg的溶液,作为对照品溶液。取黄芩素微丸适量,研细,精密称取细粉500 mg(约相当于黄芩素5 mg),置10 mL量瓶中,加流动相9 mL,超声处理30 min,加流动相稀释至刻度,混匀,用0.45 μm微孔滤膜滤过,作为供试品溶液。
取对照品溶液和供试品溶液,按2.2.1项下操作,记录色谱图,按外标法以峰面积计算。
2.3 黄芩素缓释微丸体外释放度测定
2.3.1 标准曲线的制备 精密吸取上述对照品溶液2、10、20、30、40 μL进样,按上述色谱条件测定其峰面积值。以峰面积值X对进样量Y(μg)进行回归,得回归方程为Y=64696X+5689,r=0.9999(n=5),表明黄芩素进样量在1.00~20.00 μg范围内与峰面积呈良好的线性关系。
2.3.2 精密度试验 精密吸取对照品溶液20 μL,于同日内连续进样6次,记录峰面积,黄芩素的RSD为0.82%(n=6)。
2.3.3 稳定性试验 取同一供试品溶液分别于0、2、4、6、8、12 h进样20 μL,记录峰面积,黄芩素的RSD为2.83%,表明处理后的样品溶液室温放置12 h内稳定性良好,符合实验测试要求。
2.3.4 重复性试验 取微丸 (批号120117)研匀,精密称取6份,每份约500 mg,按2.2.2项下方法制备,再按2.2.1项下的色谱条件测定,黄芩素的RSD为1.60%。
2.3.5 加样回收率 精密称取2.3.4项下已测定含量的微丸6份,每份约500 mg,精密加入对照品适量,按2.2.2项下方法制备,再按2.2.1项下的色谱条件测定,黄芩素的平均回收率为98.21%,RSD为1.92%。
2.3.6 体外释放度测定 根据中国药典2010年版二部附录X D第一法,采用溶出度测定法 (附录X C)第一法的装置,称取黄芩素微丸适量 (含黄芩素约10 mg),以脱气的新鲜纯化水900 mL为介质,温度为 (37±0.5)℃,转速为75 r/min,依法操作,分别于2、6、12 h取样5 mL,同时补充(37±5)℃同体积的释放介质,样品经0.45 μm微孔滤膜滤过,测定含量,计算累积释放度。
2.4 Box-Behnken设计-响应面法优化缓释微丸处方
2.4.1 Box-Behnken设计 在单因素考察的基础上,选取对缓释微丸系统释药影响较明显的3个因素,即增塑剂 (TEC)在包衣液中的质量分数、聚合物比例 (Eudragit RS 30D:Eudrgit RL 30D)以及包衣增重,分别记为X1、X2和X3,在3个水平上进行了优化研究,以2、6、12 h的释放度为响应值,分别记为Y1、Y2和Y3,建立数学模型,优化黄芩素缓释微丸处方。试验中每个因素的3水平分别记作-1、0、+1,见表2,试验设计及结果见表3。
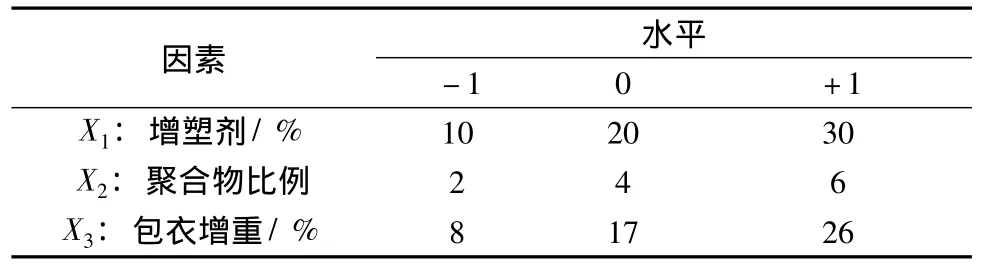
表2 Box-Behnken设计的因素和水平Tab.2 Independent variables:factors and their levels for Box-Behnken design
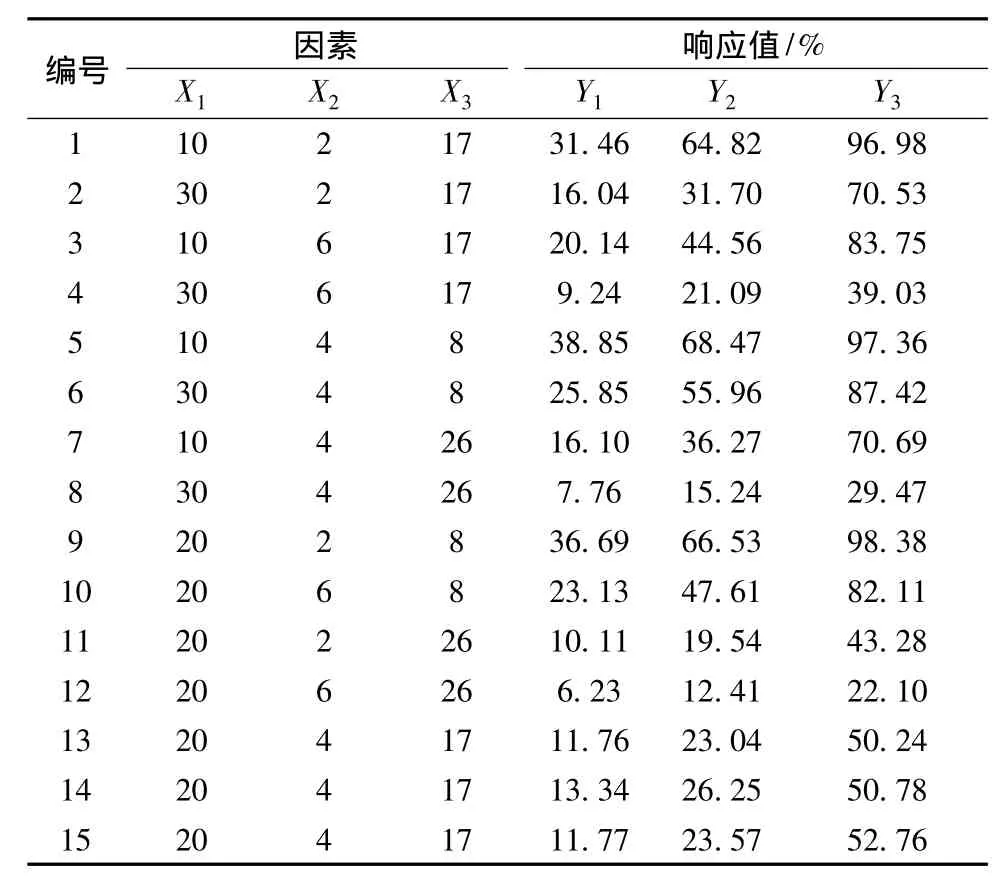
表3 Box-Behnken设计及响应值Tab.3 Experimental runs and observed values of responses for Box-Behnken design
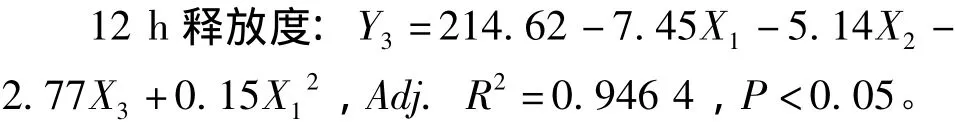
其中,Adj.R2为校正后的决定系数 (Adjusted R-Squared),结果表明,缓释微丸在2、6、12 h的释放度与增塑剂质量分数、聚合物比例、以及包衣增重三因素各水平的非线性拟合效果较好,相关系数较大 (Adj.R2>0.94)。
2.4.3 处方优化和预测 应用Design Expert 7.0进行拟合作图,得响应面图和等高线图,可直观反应各因素和响应值、以及各因素之间的交互作用,以响应值Y2为例,列举了各因素和响应值的三维图。
为了确定黄芩素缓释微丸优化模型的取值区域,根据缓释制剂指导原则,对3个取样点的释放度分别设定目标范围,其中2 h为10%~30%,考察药物是否有突释;6 h为40%~60%,用于确定释药特性;12 h为90%以上,用于考察释药是否基本完全,此3点可用于表证体外缓释制剂药物释放度[6]。经Design Expert7.0软件计算,得到最优处方为:X1为11%,X2为4%,X3为12%,响应值的预测值分别为:Y1为28.34%,Y2为58.56%,Y3为95.00%。
2.4.4 验证性试验 根据上述最优处方组成,增塑剂柠檬酸三乙酯在包衣液中的质量分数为11%,聚合物比例 (Eudragit RS∶Eudragit RL)为4∶1,包衣增重为11%,按表1工艺参数制备3批黄芩素缓释微丸,考察释放度,得3个指标的实测值,将实测值与预测值比较,根据以下公式计算偏差:偏差=(实测值-预测值)/预测值×100%,偏差越小,表明所建立的模型预测性越好。结果见表4。结果显示制得微丸的释放度实测值与预测值基本一致,说明所建立的拟合模型具有较高的可靠性,预测性良好。
各因素与响应值 (Y2)的三维图见图1。
2.4.2 Box-Behnken设计-响应面法优化试验结果运用Design Expert 7.0,经多元线性及非线性回归处理并适当简化,得拟合方程:
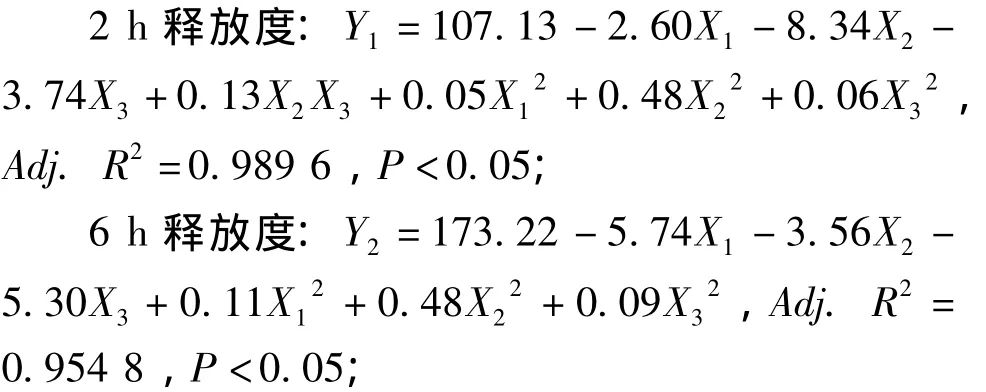
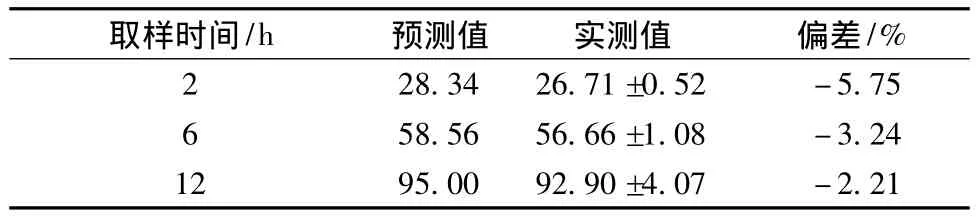
表4 预测值与实测值的偏差Tab.4 Bias between predicted and observed values
3 讨论
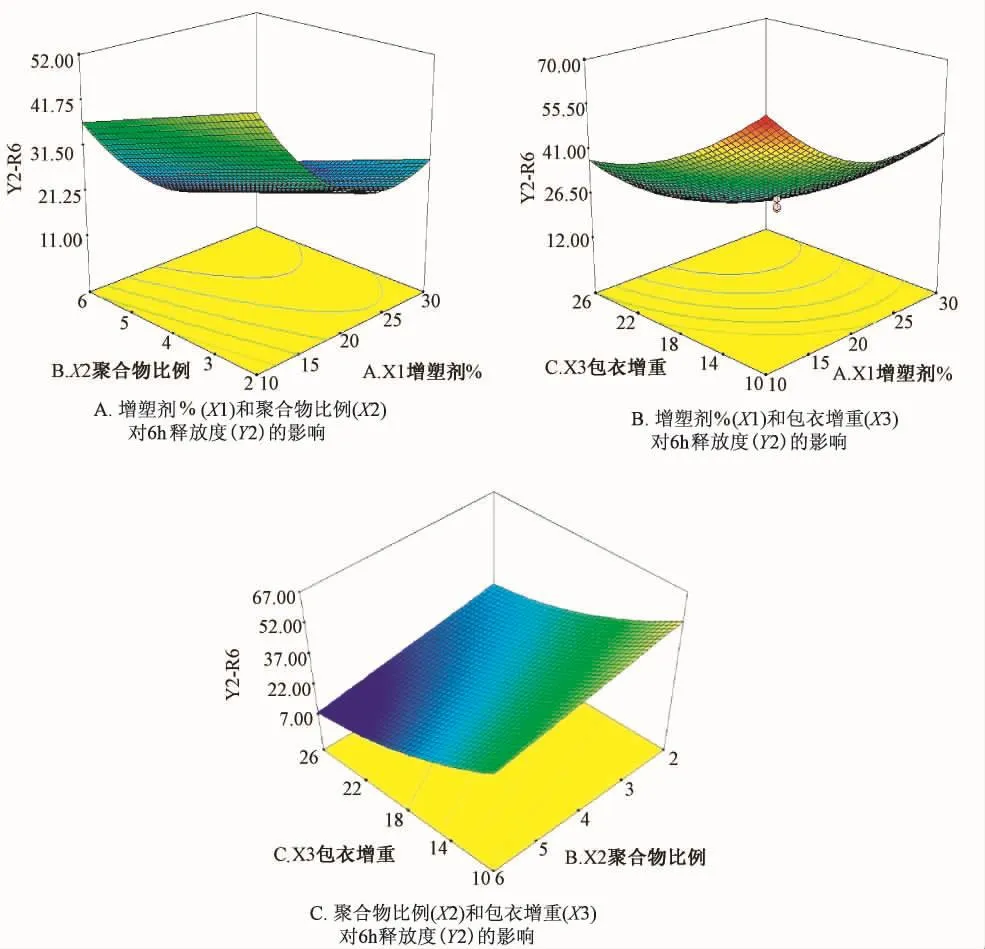
图1 各因素与响应值 (Y2)的三维图Fig.1 Three-dimensional response surface plot showing effect of independent factor Y2 on response values
本实验制备的黄芩素缓释微丸,体外释放度主要取决于包衣液中增塑剂质量分数、包衣液中聚合物比例、以及包衣增重。通过Box-Behnken设计-响应面优化,得到最优处方,制得包衣微丸可以达到缓释的目的。根据参考文献[7,8],采用高效液相色谱法测定缓释微丸中黄芩素的量和释放度,方法准确、简便、重现性好。
Box-Behnken试验设计法是响应面设计法的一种,它可以提供多因素、三水平的实验设计及分析,目前已被广泛的应用于中药提取[9]和药物制剂处方筛选和优化[10,11]等药学研究领域。
评价模型拟合度时,向模型中增加没有统计学意义的变量,决定系数R2值仍会增大,校正后的决定系数 (Adj.R2)克服了自变量个数的影响,当模型中增加的变量没有统计学意义时,校正决定系数会减小,计算公式如下:

其中,n为观测值个数,p为解释变量个数,Adj.R2越大,模型拟合越好[12]。
为简化方程求解,在保证拟合度的前提下,进行了相应的方程简化。以响应值Y1为例,拟合得到完整的二次多项式为:Y1=116.02-3.05X1-9.47X2-4.00X3+0.06X1X2+0.01X1X3+0.13X2X3+0.05X12+0.48X22+0.06X32,P < 0.0001。根据方差分析结果,除X1X2项和X1X3项外,其余各项均为显著项 (P<0.05)或以上,本实验在置信度P=0.05水平上简化方程,舍去P>0.05的项,得到简化的拟合方程为 Y1=107.13-2.60X1-8.34X2-3.74X3+0.13X2X3+0.05X12+0.48X22+0.06X32,R2=0.9896,P <0.05,同理简化了Y2和Y3两个响应值的拟合方程,并验证简化模型的预测性,结果显示预测准确可靠。上述结果显示,Box-Behnken设计-响应面法具有良好的预测性,可有效应用于黄芩素缓释微丸的处方筛选和优化。
[1]彭 蕾,顾振纶,薛仁宇,等.黄芩素对大鼠高脂血症性脂肪肝的防治作用研究[J].中成药,2011,33(3):414-418.
[2]刘太明,蒋学华.张梅娟,等.黄芩苷和黄芩素的大鼠在体肠吸收特性[J].中国药学杂志,2006,41(23):1784-1787.
[3]刘太明,蒋学华.黄芩苷和黄芩素大鼠在体胃、肠动力学研究[J].中国中药杂志,2006,31(12):999-1001.
[4]沈 熊,吴 伟,徐惠南,等.5-氟尿嘧啶结肠定位释药微丸的研制及释药特性[J].中国医药工业杂志,2004,35(3):146-149.
[5]韩海岭,王建新.药用丙烯酸树脂在中药缓控释制剂中的应用[J].中成药,2009,31(1):112-115.
[6]国家药典委员会.中华人民共和国药典:2010年版二部[S].北京:中国医药科技出版社,2010,附录 XIX D:201.
[7]王艳伟,宋立言,代雪平,等.双黄连注射液HPLC指纹图谱研究[J].中成药,2011,33(9):1461-1464.
[8]姚亚红,张立伟.黄芩素稳定性研究[J].光谱实验室,2006,23(2):346-348.
[9]陈 京,姜春波,熊耀康.基于RSM法优化补骨脂中总呋喃香豆素的提取工艺[J].中成药,2011,33(6):1065-1067.
[10]魏 萍,尹蓉莉,李东芬,等.Box-Behnken设计-效应面法优化淫羊藿总黄酮微孔渗透泵片处方[J].中成药,2010,32(7):1124-1128.
[11]郝吉福,王建筑,郭丰广,等.基于Box-Behnken实验优化龙血竭固体脂质纳米粒的制备[J].中成药,2011,33(10):1713-1718.
[12]应用线性回归[M].2版.北京:中国统计出版社,1998,55-57.
