培养基加温溶解次数对医院制剂微生物检测结果的影响分析
2013-07-01王琦
王 琦
(南阳市第一人民医院,河南 南阳473000)
培养基加温溶解次数对医院制剂微生物检测结果的影响分析
王 琦
(南阳市第一人民医院,河南 南阳473000)
目的探讨培养基加温溶解次数对医院制剂微生物检测结果的影响。方法选择玫瑰红钠琼脂培养基、青枯菌半选择性培养基进行金黄色葡萄球菌和白色念珠菌培养,培养基分别溶解3次。结果随着溶解次数的增加,培养基上的金黄色葡萄球菌与白色念珠菌数都呈下降趋势,不过对比差异不明显。随着溶解次数的增加,培养基上的pH值呈现明显下降趋势,对比差异明显(P<0.05)。结论培养基加温溶解次数能影响医院中成药制剂的微生物检测数与pH值,要尽量减少溶解次数,保证检测的准确性。
培养基;加温溶解次数;药剂;微生物
在当前医疗环境下,医药中成药制剂质量直接关系到用药者的安全和疗效[1]。而微生物限度检查在中成药制剂质量控制方面起着重要的质量评估作用,其准确与否直接关系到患者用药的安全性和有效性[2]。但是在检测过程中,很多含琼脂类培养基的多次加温溶解,造成培养基内的成分被破坏和丢失,导致微生物检测的不准确[3,4]。本文为此具体探讨了培养基加温溶解次数对医院中成药制剂微生物检测结果的影响,现报道如下。
1 材料与方法
1.1 仪器与试药
玫瑰红钠琼脂培养基、青枯菌半选择性培养基、金黄色葡萄球菌[CMCC(B)26003]、白色念珠菌[CMCC(B)44102]均购自中国药品生物制品检定所。无菌磷酸盐缓冲液(pH 7.2)购自北京三药科技开发公司。培养皿、吸管均按2005年版《中国药典》要求合理清洗、消毒与高压灭菌。
1.2 方法
1.2.1 菌检率分析
将金黄色葡萄球菌、白色念珠菌分别按2005年版《中国药典》要求配制成100个/mL的供试菌液。另将已配制好的玫瑰红钠琼脂培养基和青枯菌半选择性培养基溶解,冷至约45℃后各取25mL分别对应倾注在2个培养皿中,35℃培养48h和25℃培养72h后行计数。从培养基冷却到加温溶解循环3次,并记录每次菌落数的变化。
1.2.2 pH值考察
取10%葡萄糖溶液300mL于三角烧瓶中,置水浴上加温,沸后冷却至室温,测定其pH值。并将从葡萄糖冷却到加温至沸循3次,记录各次的pH值变化。
1.3 统计分析
使用SPSS19.0数据库进行分析,菌数与pH值数对比采用卡方对比检验,P<0.05代表有显著性差异。
2 结 果
2.1 细菌生长数的变化
经过观察,随着溶解次数的增加,培养基上的金黄色葡萄球菌与白色念珠菌数都呈下降趋势,不过对比差异不明显。见表1。
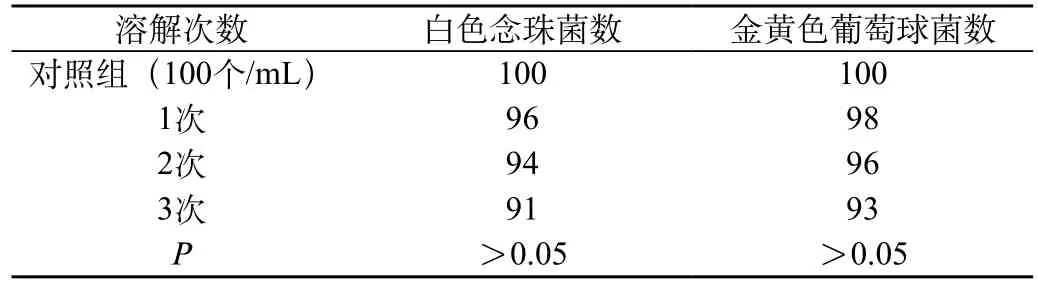
表1 不同加温溶解次数对细菌生长数的影响结果
2.2 pH值的变化
经过观察,随着溶解次数的增加,培养基上的pH值呈现明显下降趋势,对比差异明显(P<0.05)。见表2。

表2 不同加温溶解次数对pH值的影响结果
3 讨 论
当前中成药确切的临床疗效和较低廉的价格越来越得到认可,使用的人群越来越多,但伴随而来中成药的安全性比以往则更需要引起重视[5]。中成药安全性问题究其来源是多方面的,主要与中成药本身特性和药品受细菌污染程度等相关。中成药细菌数测定是微生物的定量检查,是用来判断药品被细菌污染程度和卫生质量评价的指标,也是检测中药药品质量的指标之一。在检测方法中,培养基稀释法是利用扩大培养基的使用量或增加样品的稀释倍数,减少单位体积供试品的量,以达到降低供试品抑菌作用的目的。培养基稀释法操作也较简便,所需时间短,尤其适用于中成药的微生物种类[6]。
但是在培养基检测方法中,其加温溶解次数过多将造成检测的误差。有调查显示,10%葡萄糖溶液经过1~6次加温,溶液逐渐浓缩,pH值会明显下降。而微生物也是一个生命体,在反复多次的加温中,大量的矿物质、蛋白质和水分都被破坏和丢失,在这样一个没有充足营养的培养基中微生物不能生长繁殖[1]。经过观察,随着溶解次数的增加,培养基上的金黄色葡萄球菌与白色念珠菌数都呈下降趋势,不过对比差异不明显。为此培养基的溶解数次不得>3次,否则微生物限度检查虽进行了培养,但很难检查出样品中的菌量数。pH值是微生物检测的重要影响因素,不同的检测样品具有不同的pH值,如果忽略pH值对反应的影响,必然会使检测结果产生偏差。本文经过观察,随着溶解次数的增加,培养基上的pH值呈现明显下降趋势,对比差异明显(P<0.05)。在预防中,首先要严格热水定容原则,溶解后都要对培养基进行热水定容,预防营养成分浓度不均。其次要检测pH值的变化,确保pH值的稳定性。
总之,培养基加温溶解次数能影响医院中成药制剂的微生物检测数与pH值,要尽量减少溶解次数,保证检测的准确性。
[1] 王琳琳,丁安伟,耿径军.药品微生物学检查方法学验证执行现状[J].医药导报,2007,26(5):569-571.
[2] Malekazadeh HE,Hsasnifar M,Shahamat,Antibacterial activity of black mymbalan(Terminalia chebula Retz)against Helicobacter pylori[J].Int J Antimicr Agents,2010,8(10):85-88.
[3] 马文漪,杨柳燕.环境微生物工程.南京:南京大学出版社,2008: 45-47.
[4] 舒柏华,赵志耀,徐顺清,等.利用生物发光分析技术快速检测微生物的方法学研究[J].发光学报,2009,20(1):77-80.
[5] 中国药品生物制品检定所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2005:45-47.
[6] 张崇生,申遂扬.加味藿香正气丸的微生物限度的检查[J].医药导报,2007,26(1):76-77.
R37
B
1671-8194(2013)11-0071-02
