不同主盐对羟基亚乙基二膦酸体系镀铜的影响
2013-06-17黄崴曾振欧谢金平李树泉
黄崴,曾振欧, *,谢金平,李树泉
(1.华南理工大学化学与化工学院,广东 广州 510640;2.广东致卓精密金属科技有限公司,广东 佛山 528247)
钢铁基体打底镀铜的传统工艺为氰化物镀铜。由于氰化物具有很强的生物毒性,以氰化物为电镀液的镀铜工艺曾被经贸委第32 号令列为2003年底为限期的 淘汰工艺名单,如今在发改委的《产业结构调整指导目录》中属于“暂缓淘汰”。HEDP(羟基亚乙基二膦酸)溶液体系镀铜是南京大学和邮电部电镀组在20世纪70年代攻关研究的无氰碱性镀铜工艺[1],是目前较为成熟和应用较早的无氰镀铜工艺,镀液均镀能力好,所得铜镀层韧性和结合力好。目前报道的HEDP 体系镀铜工艺的主盐不尽相同,主要有CuSO4·5H2O[2-3]和Cu2(OH)2CO3[4-5],也有采用CuCl2和CuCO3[6-7]作主盐。本文在笔者前期研究[8]所得最佳镀液组成和工艺条件的基础上,通过赫尔槽试验和方槽试验探讨了几种常见铜盐对HEDP 溶液体系镀铜过程及镀层性能的影响。
1 实验
1.1 镀液组成与配制
镀液组成为:HEDP 160 g/L,Cu2+10 g/L,K2CO360 g/L,pH = 9.0。提供Cu2+的主盐为CuSO4·5H2O、Cu2(OH)2CO3、Cu(NO3)2·3H2O、Cu(CH3COO)2·H2O 和CuCl2·2H2O。镀液的配制如下:
(1) 称取160 g HEDP(质量分数为50%)于1 L 烧杯中,加入适量去离子水后,再加入含10 g Cu2+的铜盐。
(2) 缓慢加入KOH 浓溶液并不断搅拌至pH 稍高于7.0,此过程应将烧杯置于冷水中,以防止中和放热反应太激烈。随后加入适量K2CO3使溶液pH 达9.1,待其完全溶解后加去离子水稀释至1 L,此时pH 刚好为9.0。若pH 有少许偏差,可用少量HEDP 或K2CO3进行微调。
1.2 工艺流程
(1) 黄铜片:除油─弱酸[w(HCl)= 10%]活化─水洗─电镀铜─水洗─钝化(30 g/L K2CrO4,25 °C,10 s)─清水冲洗─吹干─镀层测试。
(2) 镀锌铁片:退锌[w(HCl)= 50%]─清水冲洗─弱酸[w(HCl)= 10%]活化─水洗─电镀铜─水洗─钝化(30 g/L K2CrO4)─清水冲洗─吹干─镀层测试。
1.3 赫尔槽试验与方槽试验
赫尔槽试验采用BH 赫尔槽试验仪(广州市二轻工业科学技术研究所)和267 mL 赫尔槽(250 mL 镀液),以10.0 cm × 6.5 cm 的黄铜片为阴极,电解铜板为阳极,电流为0.2~1.0 A,空气搅拌,时间10 min,温度50 °C。
方槽试验采用容积为1 L(10 cm × 10 cm × 15 cm)的自制电镀槽,阳极为电解铜板,必要时用致密的阳极布包裹,防止阳极溶解产物污染镀液,阴极为7.7 cm × 6.5 cm 的镀锌铁片,空气搅拌,时间60 min,温度50 °C。
1.4 电流效率测定[9]
采用铜库仑计法测定电流效率,铜库仑计与被测镀液槽串联。实验前后称量库仑计试片和被测试片的质量,按下式计算电流效率η。

式中Δm0、Δm1分别为库仑计试片、被测试片的增重量。每组测2 次,取平均值。
1.5 镀层性能测定
1.5.1 厚度与镀速
采用牛津的CMI 900 型测厚仪测量镀层厚度,每个试样测5 个不同点,取平均值。镀层厚度除以电镀时间 即为镀速。
1.5.2 表面形貌
采用JSM-6510 型扫描电子显微镜(日本日立公司)观察镀层的表面形貌。1.5.3 结合力
以黄铜片为基体,依次用HEDP溶液预镀铜5 min、酸性镀铜加厚、镀光亮镍后,分别采用弯曲试验法、划格试验法和热震试验法进行结合力测试[10]。
2 结果与讨论
2.1 镀液置换Cu 的时间
室温下,镀锌铁片经退锌、电解除油后置于不同主盐体系的镀铜液中,记录铁片表面出现置换铜层的时间。结果表明,一周内所有镀液中的铁片都未出现置换铜层,10 d 时,置于CuCO3Cu(OH)2·H2O、Cu(CH3COO)2·H2O、CuCl2·2H2O 主盐体系镀液中的铁片出现微弱的红色,即发生了轻微置换。以CuSO4·5H2O、Cu(NO3)2·3H2O 为主盐时,置换铜所需的时间更长。
2.2 赫尔槽试片外观
主盐不同时,赫尔槽试片外观如表1所示。

表1 不同主盐所得赫尔槽试片外观随电流的变化Table 1 Appearance of Hull cell test coupon obtained at different currents when using different main salts
从表1可知,电流为0.2 A 时,5 种主盐体系的HEDP 镀铜液均能得到整片呈半光亮的试片。Cu(NO3)2·3H2O 作主盐时,在电流为0.2~1.0 A 内,赫尔槽试片都为整片半光亮。进一步实验表明,电流为4 A 时,Cu(NO3)2·3H2O 为主盐的HEDP 镀铜液仍可得到整片半光亮的试片,其他主盐的HEDP 镀铜液所得试片都呈大面积烧焦。这就说明以Cu(NO3)2·3H2O 为主盐时,HEDP 镀铜液的允许电流密度范围最大。因此,单从赫尔槽试片外观及允许电流密度范围看,Cu(NO3)2·3H2O 应是主盐的最佳选择。
2.3 主盐对沉积过程和镀层性能的影响
2.3.1 厚度和镀速
主盐不同、电流密度为1 A/dm2时,镀层厚度与时间的关系如图1所示。
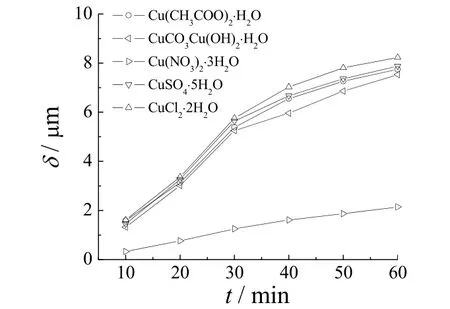
图1 镀层厚度随电镀时间的变化Figure 1 Variation of coating thickness with plating time
从图1可知,Cu(NO3)2·3H2O 为主盐时,镀层厚度最小,其他几种主盐的镀层厚度较接近。在1 A/dm2下电镀30 min 后,从CuSO4·5H2O 为主盐的镀液中所得镀层厚度达5.76 μm,从Cu(NO3)2·3H2O 为主盐的镀液中所得镀层厚度仅1.25 μm。
以不同物质作主盐,在不同电流密度下对黄铜片电镀30 min,镀速与电流密度的关系如图2所示。

图2 镀速随电流密度的变化Figure 2 Variation of deposition rate with current density
从图2可知,Cu(NO3)2·3H2O 为主盐时镀速最慢,其他几种主盐的镀速较接近。以CuSO4·5H2O 作主盐,电流密度1 A/dm2时镀速为0.192 μm/min,3 A/dm2时镀速达0.447 μm/min;以Cu(NO3)2·3H2O 为主盐,电流密度为1 A/dm2和3 A/dm2时对应的镀速分别为0.042 μm/min 和0.058 μm/min,远远低于以CuSO4·5H2O作主盐时的镀速。
综合图1和图2可知,阴极电流密度越大,镀层越厚,镀速越高;电镀时间越长,镀层厚度越大,但镀速减小;Cu(NO3)2·3H2O 为主盐时,HEDP 镀铜液的镀速远远小于其他铜盐作主盐时的镀速,约为其他铜盐时的1/5。
2.3.2 阴极电流效率
采用不同主盐体系HEDP 镀铜液,在1 A/dm2下电镀20 min,不同主盐体系的电流效率见表2。

表2 主盐对电镀铜电流效率的影响Table 2 Effect of main salt on current efficiency of copper plating
从表2可知,CuSO4·5H2O 主盐体系HEDP 镀铜液的电流效率为92.48%,Cu(CH3COO)2·H2O 作主盐时的电流效率最高(97.56%),Cu(NO3)2·3H2O 主盐体系HEDP 镀铜液的电流效率最低。
2.3.3 表面形貌
采用不同主盐体系HEDP 镀铜液,在1 A/dm2下电镀1 h,所得镀层的SEM 照片如图3所示。从图3可知,CuSO4·5H2O 或CuCl2·2H2O 作主盐时,所得镀层表面紧密细致,结晶颗粒细小;而以Cu(NO3)2·3H2O或C4H6CuO4·H2O 作主盐时,所得镀层表面较粗糙,结晶颗粒粗大。

图3 不同主盐所得镀层的SEM 照片Figure 3 SEM images of the coatings obtained by using different main salts
2.3.4 镀液稳定性
实验过程中发现,长时间电镀后,5 种主盐体系的HEDP 镀铜液都由浅蓝色变为深蓝色, 用Cu(NO3)2·3H2O 作为主盐时尤其明显。另外,CuCl2·2H2O 作主盐时,阳极会附着一层绿色的阳极泥,使阳极溶解变得极不正常。在1 A/dm2下电镀1 h 后阴、阳极的质量变化见表3。

表3 采用不同主盐时阴、阳极的质量变化Table 3 Weight changes of cathodes and anodes when using different main salts
从表3可知,除Cu(NO3)2·3H2O 外,其他3 种主盐的阴、阳极质量变化量都较接近,阳极溶解的速率与阴极沉积的速率相近。由于镀液中Cu2+离子含量变化越小则镀液越稳定,不同主盐体系镀液的稳定性顺序依次为:CuCO3Cu(OH)2·H2O > CuSO4·5H2O > Cu(CH3COO)2·H2O > CuCl2·2H2O > Cu(NO3)2·3H2O。Cu(NO3)2·3H2O 为主盐时,阳极质量减小0.86 g,远大于阴极的增加量0.25 g,即阳极溶解速率远大于阴极沉积速率,致使镀液中Cu2+离子含量明显升高而不稳定,镀液维护困难。
观察不同主盐体系的HEDP 镀铜液发现,长期自然静置后,镀液均未发生浑浊、变色现象,长时间的电镀过程中,pH 较稳定,只有微小变化,用HEDP 或KOH 溶液(30 g/L)调节即可。
2.3.5 镀层与钢铁基体的结合力
对从不同主盐体系HEDP 镀液中所得镀层进行划格试验,均无翘起或剥离现象;弯折试验中弯折部位的镀层与基体金属一起断裂,均无脱皮现象;将铜镀层经300 °C 烘烤1 h 后进行热震试验,均无起泡现象。结合力试验结果表明,采用不同主盐体系HEDP 镀液电镀所得铜镀层均与钢铁基材结合良好,结合力差别不大。
3 结论
(1) 采用不同铜盐作HEDP 镀液的主盐时,由于主盐的阴离子不同,对电镀过程和镀层性能都有一定影响。CuCO3Cu(OH)2·H2O 作主盐时,低电流密度区出现白雾;Cu(NO3)2·3H2O 作主盐时,允许的电流密度范围最宽,但电流效率低、镀速慢且镀液稳定性差;CuCl2·2H2O 作主盐时,阳极附着一层绿色物质而不能正常溶解;Cu(CH3COO)2·H2O 作主盐时,在低电流密度区镀层容易产生白雾,结晶较粗糙。
(2) 采用CuSO4·5H2O 作HEDP 镀液的主盐时,镀速为0.18 μm/min,电流效率为92.5%,所得镀层结晶细致、表面平整,与钢铁基体之间的结合力良好。
[1]南京大学化学系络合物研究所电镀组,邮电部邮电工业无氰电镀攻关组.通用电镀络合剂的研究II──钢铁件HEDP 直接镀铜[J].材料保护,1979 (4): 1-9.
[2]钱全录,王世荣,藏广忠,等.HEDP 一次镀铜[J].电镀与精饰,1982 (4): 37-38.
[3]PECEQUILO C V,PANOSSIAN Z.Study of copper electrodeposition mechanism from a strike alkaline bath prepared with 1-hydroxyethane-1,1-diphosphonic acid through cyclic voltammetry technique [J].Electrochimica Acta,2010,55 (12): 3870-3875.
[4]袁诗璞,毛茂财,汪小英.采用两级跳间歇镀电源的无氰碱铜研究[J].电镀与涂饰,2008,27 (1): 7-10.
[5]袁诗璞.无氰镀铜的实验研究与生产应用进展(二)[J].电镀与涂饰,2009,28 (12): 9-13.
[6]崔继民,孙敦清,韩学君.HEDP 镀铜[J].环境保护科学,1980 (1): 34-39.
[7]杨磊.HEDP 在金属防腐中的应用[J].电镀与涂饰,1989 (3): 38-41.
[8]张强,曾振欧.徐金来,等.HEDP 溶液钢铁基体镀铜工艺的研究[J].电镀与涂饰,2010,29 (3): 5-8.
[9]袁诗璞.第七讲—电镀液的电流效率[J].电镀与涂饰,2009,28 (2): 39-42.
[10]张景双,石金声,石磊,等.电镀溶液与镀层性能测试[M].北京: 化学工业出版社,2003.
