骨松强骨颗粒的醇提取工艺研究
2013-06-05杜志谦牛琼琼夏华玲
杜志谦牛琼琼夏华玲
(1河南省洛阳正骨医院中心实验室,洛阳,471002;2河南中医学院,郑州,450008)
中药研究
骨松强骨颗粒的醇提取工艺研究
杜志谦1,2牛琼琼2夏华玲1
(1河南省洛阳正骨医院中心实验室,洛阳,471002;2河南中医学院,郑州,450008)
目的:优选骨松强骨颗粒的醇提最佳工艺。方法:以提取液中淫羊藿苷含量,人参皂苷Rg1含量及总固体得率为指标,采用正交实验法,优选醇提工艺。结果:处方药材的最佳醇提工艺为70%乙醇10倍量,提取3次,1.5 h/次。结论:优选的提取工艺稳定可行。
正交实验法;骨松强骨颗粒;醇提工艺
骨松强骨颗粒处方是河南省洛阳正骨医院的经验方,由淫羊藿、三七、黄芪、骨碎补、葛根、附子、鹿角霜、何首乌组成,具有益气补肾、强筋壮骨、温阳通脉、理气止痛作用。该处方在临床应用10余年,疗效显著,安全性高,按新药开发拟制成颗粒剂。用于治疗原发性、继发性骨质疏松及骨软化症。根据所含的化学成分和药理作用结合功能主治,淫羊藿、三七、骨碎补、葛根4种药材采取醇提的方法。淫羊藿补肝肾,强筋骨[1]。淫羊藿所含的淫羊藿苷可促进骨细胞的分化成熟,促进成骨细胞的增殖[2],为治疗骨质疏松的有效化学成分[3]。三七为贵重药材,三七所含的人参皂苷Rg1为其主要成分[4],且含量较高。人参皂苷Rg1可增强机体免疫力[5]。因此,以淫羊藿苷含量和人参皂苷Rg1的含量及总固体得率为指标来优选提取条件,从而为制定生产工艺提供依据。
1 仪器与试药
1.1 仪器 Agilent1100 series液相色谱系统(美国安捷伦),XS205DU电子分析天平(瑞士梅特勒),HH-6金坛市科兴仪器厂水浴锅。
1.2 试药 淫羊藿、三七等药材均购自洛阳康鑫中药饮片有限公司,经河南中医学院董成明教授鉴定符合《中华人民共和国药典》2010版一部规定;淫羊藿苷对照品(110737-200415)、人参皂苷Rg1对照品(703-8903)购自中国食品药品检定研究院;乙腈、甲醇为色谱纯,其余为分析纯;水为超纯水。
2 方法与结果
2.1 醇提液的制备 采用加热回流的提取方法[6],选用L9(34)正交进行实验,以加醇量(A),提取时间(B),提取次数(C),醇浓度(D)为考察因素,进行4因素3水平的正交实验。因素水平见表1,一次称取处方量药材50 g,分别称取药材共9份,按表2加醇液提取,药液经过滤即得1~9号样品。

表1 因素水平表
2.2 淫羊藿苷含量的测定[7]
2.2.1 色谱条件[8-9]色谱柱安捷伦C18柱;乙腈∶水(28∶72)为流动相;检测波长270 nm;柱温35℃;理论塔板数淫羊藿苷峰计算应不低于1500。
2.2.2 标准曲线的绘制 精密称取淫羊藿苷1.9 mg对照品,置10 mL容量瓶中,加甲醇至刻度,制成0.19 mg/mL的溶液,分别精密吸取0.1 mL,0.2 mL,0.3 mL,0.4 mL,0.5 mL,0.6 mL,0.7 mL上述溶液,用甲醇分别稀释至1mL。过滤后分别吸取20μL注入液相色谱仪。按上述色谱条件测峰面积。以淫羊藿苷的浓度(x)为横坐标,峰面积积分值(Y)为纵坐标线性回归,得回归方程为Y=39532X+66.986,R2=0.9998,表明淫羊藿苷在0.019~0.133mg/mL范围内线性良好。
2.2.3 供试品溶液的制备[10]按处方量称取药材提取,精密移取提取液2 mL,蒸干,加稀乙醇,定容至10 mL。
2.2.4 对照品溶液的制备 取淫羊藿苷对照品1.6 mg,加甲醇定容至10 mL容量瓶中,制成每0.16 mg/mL的溶液。
2.2.5 阴性溶液的制备 称取处方量缺淫羊藿的其余药材提取,照供试品的制备方法制备阴性溶液。
2.2.6 含量测定 分别精密吸取过0.45μm滤膜的对照品溶液,供试品溶液、阴性溶液各20μL注入液相色谱仪。HPLC图见图1,结果见表2。
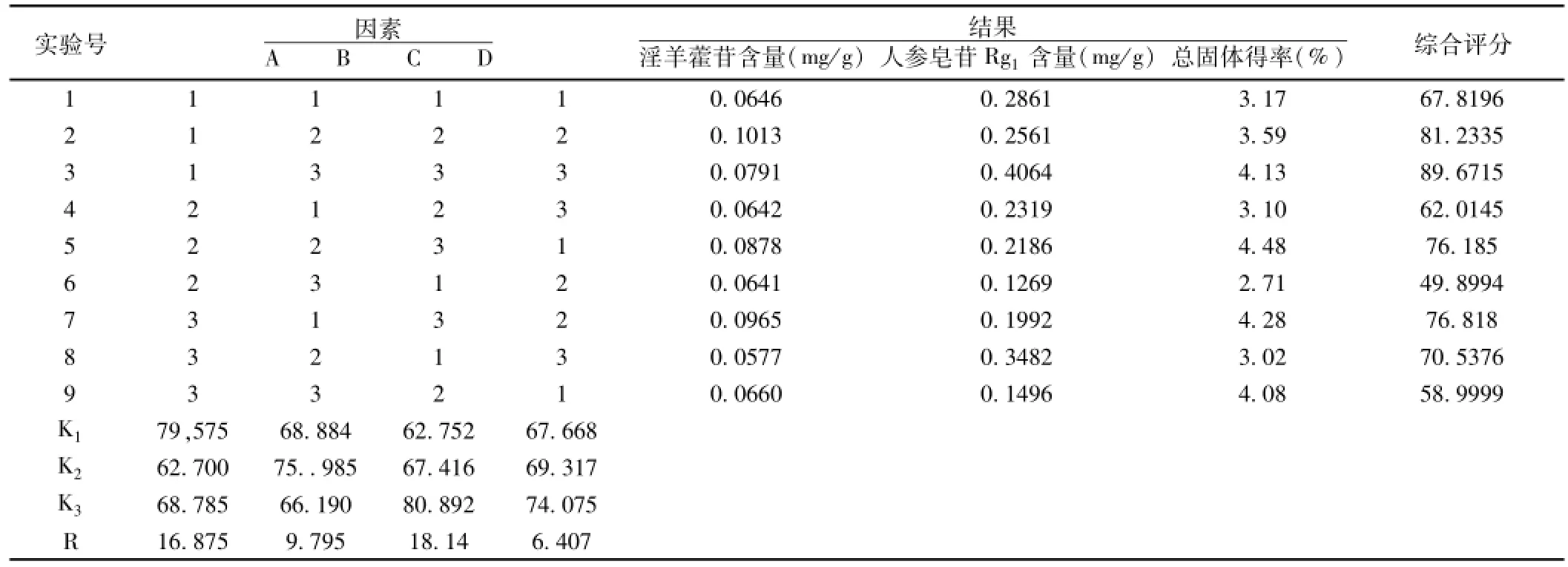
表2 L9(34)正交实验表
2.3 三七中人参皂苷Rg1含量测定[11]
2.3.1 色谱条件[12-13]色谱柱安捷伦C18;乙腈为流动相A,水为流动相B;检测波长为203 nm,柱温35℃;流动相比例如下图表3,理论板数按人参皂苷Rg1算应不低于4000。

表3 流动相比例
2.3.2 标准曲线的绘制 精密称取人参皂苷Rg1标准品12.5 mg,放入10 mL容量瓶中,加甲醇至刻度,制成1.25 mg/m L的溶液,分别精密吸取0.1 mL,0.2 mL,0.3 mL,0.4 mL,0.5 mL,0.6 mL,0.7 mL的上述溶液加甲醇至1 mL。分别精密吸取20μL,按上述色谱条件注入液相色谱仪。以人参皂苷Rg1的浓度(X)为横坐标,峰面积(Y)为纵坐标线性回归,回归方程为Y=7421.7X+105.86,R2=0.9997,表明人参皂苷Rg1在0.125~0.875 mg/mL范围内线性良好。
2.3.3 供试品溶液的制备[14]按处方量称取药材50 g提取,精密量取乙醇提取液10 mL,蒸干加20 mL水溶解,水溶液用水饱和的正丁醇萃取3次,每次20 mL,合并正丁醇液,弃水液,用正丁醇饱和的氨试液洗涤2次,每次20 mL,合并正丁醇液,用正丁醇饱和的水液洗涤1次,每次60 mL,取正丁醇层,蒸干,用甲醇溶解并定容至10 mL容量瓶中。
2.3.4 对照品溶液的制备 精密称取人参皂苷Rg1对照品4.7 mg,加甲醇定容至10 mL容量瓶中。制成含人参皂苷Rg10.47 mg/mL的溶液。
2.3.5 阴性溶液的制备 按处方量称取缺三七的其余药材提取,照供试品的方法制备阴性溶液。
2.3.6 含量测定 精密吸取过0.45μm滤膜的对照品溶液,供试品溶液、阴性溶液各20μL注入液相色谱仪。HPLC图见图2,结果见表2,方差分析见表4。
2.4 总固体得率的测定[15]精密量取样品液30 mL至恒重的蒸发皿中,水浴蒸干后在105°C干燥箱中干燥5 h,于干燥器内冷却至室温,待恒重时精密称定,计算总固体得率,见表2。
2.5 结果 分析极差值知因素对结果影响大小顺序为:煎煮次数>加水量>煎煮时间>乙醇浓度。由方差分析知各影响因素对结果影响都不显著,由直观分析知最佳组合为A1B2C3D3.即10倍醇液,每次煎煮1.5 h,煎煮3次,乙醇浓度为70%。

图1 为淫羊藿的HPLC图(注:A为淫羊藿苷的对照品溶液;B为样品溶液;C为阴性溶液;1为淫羊藿苷)
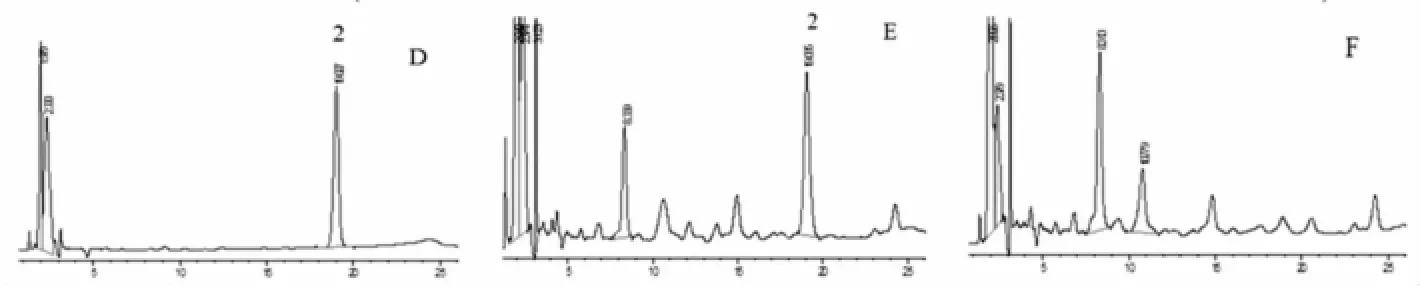
图2 三七的HPLC图(D为三七中人参皂苷Rg1的对照品溶液;E为样品溶液;F为阴性溶液图;2为人参皂苷Rg1)
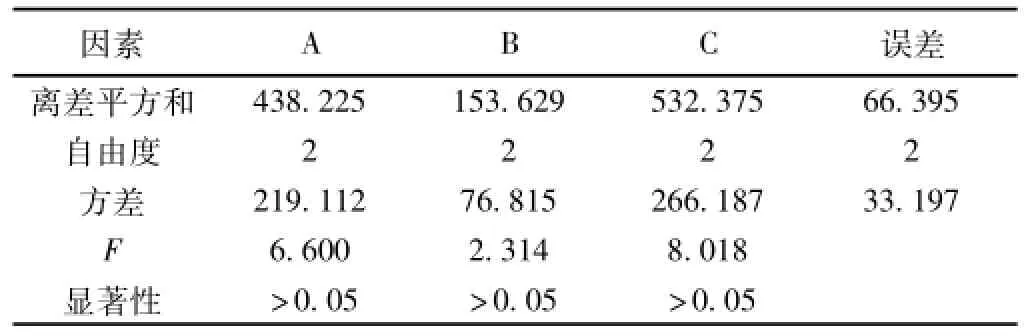
表4 方差分析表
2.5.1 验证实验 分别称取药材以最优的工艺提取,按“2.2”和“2.3”项下测定淫羊藿苷含量和三七中人参皂苷Rg1的含量,测定总固体得率。验证3批结果差异无统计学意义。
3 讨论
淫羊藿苷含量测定时参照《中华人民共和国药典》2010版方法,由于复方组成的干扰,对流动项的比例进行了选择,调整为乙腈∶水为28∶72,就得到理想的峰形和保留时间。三七中人参皂苷Rg1的含量测定时供试品溶液的制备方法进行了优选:1)以乙醇提取液取10 mL,蒸干加甲醇溶解并定容至10 mL;2)先将乙醇提取液取10 mL蒸干加20 m L水溶解,水溶液用水饱和的正丁醇液萃取3次,每次20 mL,弃水液,正丁醇液合并,用正丁醇饱和的水液60 mL洗涤正丁醇液,取正丁醇液蒸干,加甲醇溶解并定容至10 mL;3)先将乙醇提取液10 mL蒸干加20 mL水溶解,水溶液用水饱和的正丁醇萃取3次,每次20 mL,弃水液,正丁醇液合并,用正丁醇饱和的氨试液洗涤2次,每次20 mL,合并正丁醇液,用正丁醇饱和的水洗涤1次,每次60 mL,取正丁醇层,蒸干,用甲醇溶解并定容至10 mL。经比较第3种方法色谱图简洁,分离度好,保留时间合适,选择该方法为供试品溶液的制备方法。人参皂苷Rg1的含量测定经比较,优选了流动相比例,以流动相B为例,0~12 min为19,12~60 min为19~36;0~6 min为19,6~30 min为19~26;0~6 min为22,6~28 min为22~26;最终又改为比例0~6 min为21,6~28 min为21~26。
[1]孟宁,孔凯,李师翁.淫羊藿属植物化学成分及药理活性研究进展[J].西北植物学报,2010,30(5):1063-1073.
[2]孙晓玲,短小群.淫羊藿苷及衍生物药理作用研究进展[J].华夏医学,2010,23(6):807-810.
[3]李娌,王学美.淫羊藿苷药理作用研究进展[J].中国中药杂志,2008,33(23):2727-2731.
[4]谢清春,陈燕忠,吕竹芬,等.三七中人参皂苷Rg1的提取及含量测定[J].中国医药导报,2010,7(34):40-41.
[5]冯陆冰,潘西芬,孙泽玲.三七的药理作用研究进展[J].中国药师,2008,11(10):1185-1187.
[6]谭银合,孙维广,谭弘.丹龙抗痴胶囊提取工艺研究[J].中国中医药信息杂志,2008,15(5):56-59.
[7]中国药典委员会.中华人民共和国药典[M].2010版一部.北京:化学工业出版社,2010:306.
[8]林雪英,黄君曦.高效液相色谱法测定前列舒乐胶囊中淫羊藿苷含量[J].海峡药学,2010,22(12):73-75.
[9]叶咸钰,杨水新,曹恒斌.hPLC测定强筋合剂中淫羊藿苷的含量[J].浙江中医药大学学报,2010,34(6):920-921.
[10]申强,吕竹芬,谢清春,等.高效液相法测定祛痹舒肩丸中淫羊藿苷的含量[J].中国实验方剂学杂志,2008,14(4):16-18.
[11]毕晓黎,罗文汇,李素梅.HPLC-ELSD法测定三七止血胶囊中三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量[J].中国实验方剂学杂志,2011,17(1):75-77.
[12]王雁.不同商品规格三七中3种皂苷的高效液相色谱法含量测定[J].中药材,2005,28(1):33-34.
[13]魏莉,杜奕,周浩.不同产地和生长年限三七花蕾中总皂苷及单体皂苷的含量测定[J].上海中医药杂志,2008,42(4):76-78.
[14]姚育端,傅钰,蒋平,等.高效液相色谱法测定三七伤药片中3组分的含量[J].中国药房,2007,18(3):206-207.
[15]于佳,刘瑶,张建玲,等.正交试验法优选舒郁煎膏水提工艺[J].中国实验方剂学杂志,2012,18(8):31-33.
(2013-04-28收稿)
Study on the Alcohol Extraction Process for Gusong Qianggu Granule
Du Zhiqian1,2,Niu Qiongqiong2,Xia Hualing1
(1 Henan Luoyang Orthopedic Hospital,Luoyang 471002,China;2 Henan University of Traditional Chinese Medicine,Zhengzhou 450008,China)
Objective:To optimize the alcohol extraction process of GuSong QiangGu Granule.M ethods:Orthogonal test was employed for selecting the optimum of alcoholextraction process by the indexes of the contents of ginsenoside Rg1 and total solidmatters.Results:Ten times amount of70%ethanol concentration,extracting 3 timeswith 1.5 hours for each time was considered the optimum alcohol extraction process of Gusonng Qianggu Granule.Conclusion:The optimum alcohol extraction process condition was stable and feasible. Key W ords Orthogonal test;GuSong QiangGu Granule;Alcohol extraction process
10.3969/j.issn.1673-7202.2013.11.028
牛琼琼,女,在读硕士,研究方向:中药质量标准的研究,E-mail:niuqiongqiongmengjin@126.com
