腹腔镜在中低位直肠癌手术中的应用
2013-05-16吕泽坚张育超苏正来伟潘子豪陈双
吕泽坚,张育超,苏正,来伟,潘子豪,陈双
(1.中山大学附属孙逸仙纪念医院胃肠外科, 广州 510120; 2.中山大学附属孙逸仙纪念医院肝胆外科, 广州 510120)
中低位直肠癌是指位于距齿状线10 cm以内、腹膜反折下的肿瘤,约占直肠癌的70%~75%[1],发病率高且患者较年轻[2]。其治疗强调以手术为主、包括放化疗在内的多学科综合治疗,旨在根治肿瘤的同时尽可能保留患者肛门功能和保护自主神经功能。常规开腹手术一直被视为其经典的治疗方法。近年来随着腹腔镜设备及技术的发展,临床上越来越多地应用腹腔镜治疗中低位直肠癌。本文回顾性分析2010年1月~2012年1月中山大学附属孙逸仙纪念医院胃肠外科收治的接受两种不同手术方式的82例中低位直肠癌患者的临床资料,探讨腹腔镜在中低位直肠癌手术的应用价值。
1 临床资料
1.1 一般资料
2010年1月~2012年1月采用腹腔镜手术治疗中低位直肠癌患者42例,男性23例,女性19例;年龄30~85岁,平均(60.34±13.07)岁;肿瘤分化程度:低分化6例,中分化20例,高分化16例;Dukes分期: A期6例, B期21例, C期12例,D期3例;肿瘤距离肛缘3~10 cm,平均(6.64±1.02)cm。同期行开腹手术治疗中低位直肠癌患者40例,男性23例,女性17例;年龄33~82岁,平均(59.33±14.69);肿瘤分化程度:低分化3例,中分化19例,高分化18例; Dukes分期: A期2例, B期20例, C期14例,D期4例;肿瘤距离肛缘4~10 cm,平均(6.82±1.13)cm。所有病例术后均由病理结果证实为恶性,并按照NCCN 2012年诊疗指南进行TNM分期及按照中国抗癌协会大肠癌专业委员会制定的“大肠癌诊治指南”进行Dukes分期。两组患者一般资料见表1,组间比较差异均无统计学意义(P>0.05)。
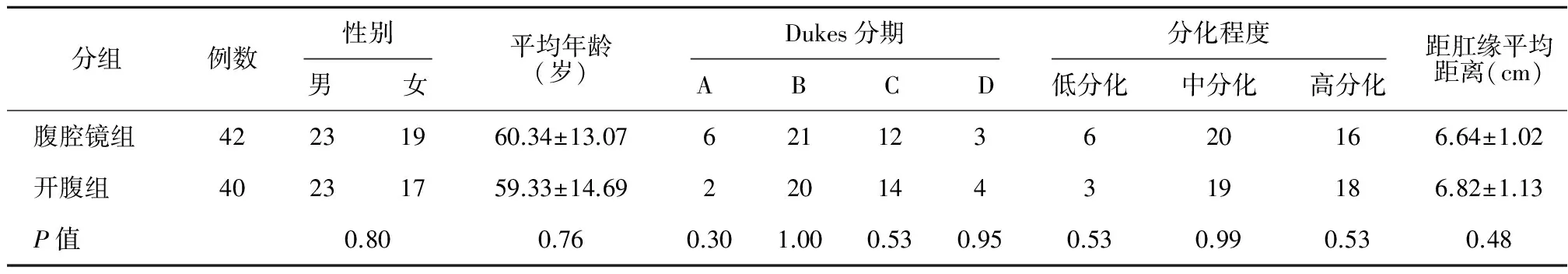
表1 腹腔镜组与开腹组患者一般资料
1.2 方法
两组患者术前准备(包括肠道准备)及术后治疗原则相同;手术均采用气管插管全身麻醉联合连续硬膜外麻醉;手术由同一组医生完成;所有手术均严格遵循肿瘤根治原则和无瘤原则。
开腹组患者按中国抗癌协会大肠癌专业委员会制定的 “大肠癌诊治指南” 所制定的手术规范进行手术操作。腹腔镜组气腹压力控制在12~15 mmHg(1 mmHg=0.133 kPa),脐上10 mm观察孔置入30°腹腔镜,左、右脐旁腹直肌外缘及左下腹行5 mm戳孔安置操作器械,右下腹行12 mm戳孔作为主操作孔。按照全直肠系膜切除(total mesorectal excision,TME)的标准,游离并切断肠系膜下动脉或直肠上动脉及其伴行静脉,直视下沿着直肠固有筋膜与盆壁筋膜的间隙锐性分离直肠及其系膜至肿瘤下方至少3 cm(低位直肠肿瘤的骶前分离应至尾骨尖部及双侧肛提肌平面)。对于保肛患者,在肿瘤下方约3 cm处用腹腔镜切割闭合器切断直肠,取下腹部正中切口约5 cm进入腹腔,用塑料袋保护好切口,将带肿瘤的近端直肠乙状结肠拉出腹腔外,切除病变肠段,将圆形吻合器砧座放入近端结肠并回纳腹腔,重新建立气腹,经肛门置入吻合器在腹腔镜直视下行乙状结肠-直肠端端吻合;对于腹腔镜会阴联合直肠癌切除患者,按无菌要求腹腔内用线形切割器或体外直接切断乙状结肠,环绕肛门作皮肤梭形切口,广泛切除坐骨直肠窝脂肪组织,切断肛尾韧带和肛提肌,向前牵拉肛管,横行切开提肛肌上筋膜,进入直肠后骶前间隙,并将已游离、切断的乙状结肠及直肠从骶前拉出,以利直肠前壁的分离,切断肛门外括约肌深部向前的交叉纤维,剪断直肠前的附着肌肉,将直肠切除,并在左下腹适当位置作永久性腹壁造口。
1.3 观察指标
观察比较两组患者的手术时间、术中出血量、淋巴结清扫范围、肿瘤距下切缘距离、切除标本长度、并发症发生率、胃肠功能恢复时间、术后住院时间等指标。
1.4 统计学处理
2 结 果
两组患者实施中低位直肠癌手术均获得成功,无手术死亡病例。腹腔镜组2例由于肿瘤明显侵犯周围组织而中转开腹,顺利完成手术。腹腔镜组37例行Dixon术,5例行Miles术,共8例行预防性或永久性造口; 开腹组30例行Dixon术, 8例行Miles术, 2例行Hartmann术,共12例行预防性或永久性造口。腹腔镜组6例出现并发症,其中吻合口瘘2例,切口感染、造口疝、造口旁疝、直肠阴道瘘各1例;开腹组10例出现并发症,其中吻合口瘘3例,切口感染3例,盆底静脉出血、造口疝、直肠阴道瘘及下肢深静脉血栓形成各1例。两组在术中出血量、淋巴结清扫数目、肿块距下切缘距离、切除肠管长度、并发症发生率等方面比较,差异均无统计学意义 (P>0.05); 腹腔镜组手术时间长于开腹组, 胃肠功能恢复时间、 术后住院时间等明显短于开腹组, 差异均有统计学意义(P<0.05)。术后随访至今, 腹腔镜组局部复发3例 (7.14%), 远处转移2例 (4.76%), 死亡1例 (2.38%); 开腹组局部复发3例 (7.50%), 远处转移2例 (5.00%), 死亡2例(5.00%)。详见表2。
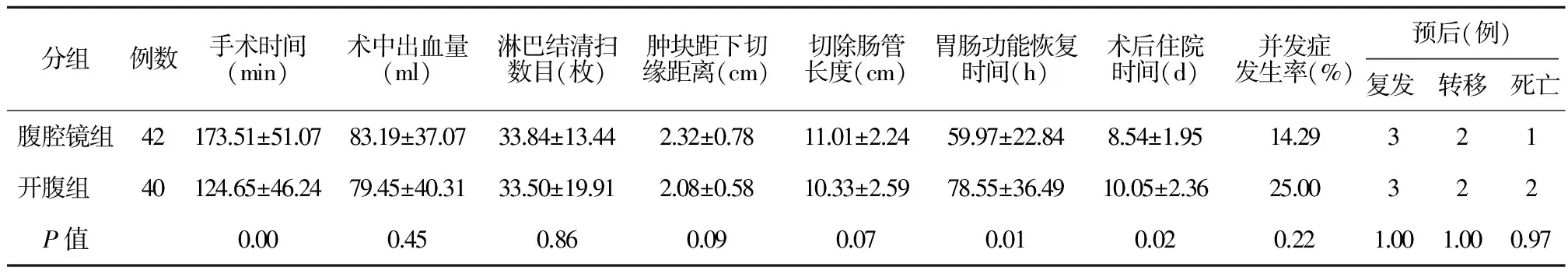
表2 腹腔镜组与开腹组术手术指标比较
3 讨 论
近年来,随着腹腔镜技术的提高,超声刀、Ligasure及各类切割闭合器等新的医疗器械的出现,腹腔镜手术获得了快速的发展。与开腹手术相比,腹腔镜手术具有创伤小、并发症少、术后恢复快等优点,得到了患者和外科医生的认可[3]。
本研究中,腹腔镜组中低位直肠癌手术时间平均(173.51±51.07)min,较传统开腹手术时间(124.65±46.24)min延长,差异具有统计学意义(P<0.05)。但随着“学习曲线”(learning curve)的结束,术者技术经验的积累、手术人员配合的逐渐熟练,以及新医疗器械的出现,腹腔镜手术时间将逐渐缩短。有文献报道[4,5]腹腔镜和开腹手术时间无差别甚至可以更短。本研究中腹腔镜组胃肠功能恢复时间和术后住院时间均较开腹组缩短(P<0.05),与腹腔镜手术创伤小、术中对胃肠道刺激小有关。
我科手术切除的结直肠癌标本,均由专人采用脂肪清除技术[6]收集标本中的淋巴结。本研究中,两组患者淋巴结清扫数目相当,组间比较差异无统计学意义(P>0.05),且两组所获得的淋巴结数量均明显高于美国癌症联合会(American Joint Committee on Cancer, AJCC)和国立癌症研究所(national cancer institute, NCI)所推荐的结直肠癌患者至少应该检测12枚淋巴结以确认淋巴结累及的状态[7~9]。以上数据说明,对于中低位直肠癌患者,腹腔镜手术可达到开腹手术的切除范围和根治目的。
本研究中,腹腔镜组并发症发生率为14.29%(6/42),低于开腹组的25%(10/40),但两者比较差异并无统计学意义(P>0.05)。其中,腹腔镜组吻合口瘘发生率为4.76%, 低于开腹组的7.50%。腹腔镜组有5例行Miles术, 比例为11.90%, 而在开腹组, 这个比例为20%(8/40);腹腔镜组有8例行预防性或永久性造口,比例为19.05%,而在开腹组比例为30.0%(12/40)。本研究显示腹腔镜组与开腹组预后相当。过去由于受到术式和医疗器械的限制,腹膜反折以下的直肠癌均推荐行腹会阴联合直肠癌根治术(Miles术)[10]。随着医学的发展,不断有低位保肛和超低位保肛的病例报告[11,12]。这主要得益于TME技术的普及和标准化以及腹腔镜技术设备的发展。国内资料显示,标准TME可显著提高低位直肠癌保肛率, 且不增加吻合口瘘的发生率[13,14]。国外资料研究了102例中低位直肠癌患者,结果显示99例成功完成腹腔镜手术,另外3例中转开腹,并发症发生率为27%,吻合口漏发生率为17%,死亡率为2%,局部复发率为6%,5年生存率为75%[15]。近年来,国内外比较腹腔镜与开腹行TME治疗中低位直肠癌的研究[16~19]显示,腹腔镜组在术中出血量、并发症发生率、下床活动时间、胃肠功能恢复时间及住院时间等方面有一定优势,而在肿块距下切缘距离、肠段切除长度和淋巴结清扫范围以及远期疗效等方面差异无统计学意义。腹腔镜手术拥有理想的视野,能发现并处理细小转移灶或其他系统器官的病变;能放大局部视野,使视野更加清晰,而且可以从不同的角度进行观察,可直视下行锐性分离,切除更精准且出血损伤较少,避免了开腹时因为肿瘤位置较深而无法操作或“盲目操作”引起的损伤,为中低位直肠癌在根治的前提下实现保肛提供了基础。吻合器的出现和改进,特别是双吻合器的出现很好地解决了在盆腔深部进行低位和超低位吻合的困难,让很多患者避免了临时性或永久性造口的痛苦。然而腹腔镜也有其不足之处,由于术中无法直接触摸肿瘤及淋巴结的累及情况,对早期患者不能很好定位,且易遗漏结肠多源性肿瘤,戳孔部位或开窗部位肿瘤细胞种植机会可能增加等问题,故有学者对腔镜下行TME仍有一定质疑。
总之,只要严格掌握手术适应证,熟悉腹腔镜手术操作技巧,腹腔镜手术疗效确切、安全、可靠,在中低位直肠癌手术中显示出独特的优越性,拥有广阔的应用前景。
[参考文献]
[1] Rullier E, Denost Q, Vendrely V, et al. Low rectal cancer: classification and standardization of surgery[J]. Dis Colon Rectum, 2013, 56(5):560-567. doi: 10.1097/DCR.0b013e31827c4a8c.
[2] Jemal A, Murray T, Samuels A, et al. Cancer statistics, 2003[J]. CA Cancer J Clin, 2003, 53(1):5-26.
[3] Aziz O, Constantinides V, Tekkis PP, et al. Laparoscopic versus open surgery for rectal cancer: a meta-analysis[J]. Ann Surg Oncol, 2006, 13(3):413-424.
[4] Davies MM, Larson DW. Laparoscopic surgery for colorectal cancer: the state of the art[J]. Surg Oncol, 2004, 13(2-3):111-118.
[5] Maeda T, Tan KY, Konishi F, et al. Accelerated learning curve for colorectal resection, open versus laparoscopic approach, can be attained with expert supervision[J]. Surg Endosc, 2010, 24(11):2850-2854. doi: 10.1007/s00464-010-1063-5.
[6] 李英儒, 赖东明, 陈双. 脂肪清除技术在结直肠癌病理分期中的应用[J]. 中华胃肠外科杂志,2011,14(7):529-531.
[7] Agrelo R, Cheng WH, Setien F, et al. Epigenetic inactivation of the premature aging Werner syndrome gene in human cancer[J]. Proc Natl Acad Sci U S A, 2006, 103(23):8822-8827.
[8] 董新舒, 李志高, 崔滨滨, 等. 低位直肠癌侧方淋巴结清扫的临床意义[J]. 中国普外基础与临床杂志,2003,10(2):103-105.
[9] 刘宝善, 燕锦, 左明, 等. 直肠癌侧方淋巴结清扫的效果分析[J]. 中华外科杂志,2004,42 ( 15 ):908-910.
[10] 汪建平. 结、直肠与肛管疾病[A]. 见吴在德,吴肇汉主编. 外科学[M]. 第7版. 北京:人民卫生出版社,2008. 476-511.
[11] Adamina M, Delaney CP. Laparoscopic total mesorectal excision for low rectal cancer[J]. Surg Endosc, 2011, 25(8):2738-2741. doi: 10.1007/s00464-011-1626-0.
[12] 郑民华. 腹腔镜低位超低位直肠癌保肛手术方式的选择[J]. 中华胃肠外科杂志,2007,10(4):311-313.
[13] Rahman MS, Khair MA, Khanam F, et al. Sphincter saving surgery is the standard procedure for treatment of low rectal cancer[J]. Mymensingh Med J, 2013, 22(2):281-288.
[14] 郑民华, 胡艳艳, 陆爱国, 等. 腹腔镜与开腹直肠全系膜切除术治疗低位直肠癌的临床对比研究[J]. 中华胃肠外科杂志,2004,7(3):177-180.
[15] Leroy J, Jamali F, Forbes L, et al. Laparoscopic total mesorectal excision (TME) for rectal cancer surgery: long-term outcomes[J]. Surg Endosc, 2004, 18(2):281-289.
[16] 施德兵, 李心翔, 蔡三军, 等. 腹腔镜与开腹全直肠系膜切除术治疗中低位直肠癌的近期疗效比较[J]. 中国临床医学,2012,19(1):40-42.
[17] 顾晋, 姚云峰. 低位直肠癌的TME与重建方式对远期疗效的影响[J]. 中国实用外科杂志,2004,24(9):522-525.
[18] Kuo LJ, Hung CS, Wang W, et al. Intersphincteric resection for very low rectal cancer: clinical outcomes of open versus laparoscopic approach and multidimensional analysis of the learning curve for laparoscopic surgery[J]. J Surg Res, 2013, 183(2):524-30. doi: 10.1016/j.jss.2013.01.049.
[19] Siani LM, Ferranti F, Benedetti M, et al. Laparoscopic versus open total mesorectal excision for stage I-III mid and low rectal cancer: a retrospective 5 years analysis. G Chir, 2012, 33(11-12):404-408.
