肺动脉血栓内膜剥脱术治疗慢性栓塞性肺动脉高压的临床研究▲
2013-05-16雷宾峰郑宝石
曾 超 黎 伟 罗 程 雷宾峰 冯 旭 郑宝石
(广西医科大学第一附属医院心胸外科,南宁市 530021)
慢性栓塞性肺动脉高压(chronic thromboembolic pulmonary hypertension,CTEPH)是由于肺动脉内反复栓塞和血栓形成而造成的肺动脉高压,可由急性肺动脉栓塞转变而来,也可因下肢深静脉血栓等反复栓塞肺动脉所致。慢性栓塞性肺动脉高压呈渐进性,最终会导致右心衰竭。近年来肺动脉内膜剥脱术(PTE)的手术适应证的把握、手术方式选择及围手术期处理逐渐成熟,大大降低了手术死亡率。我院应用PTE手术方式治疗4例CTEPH患者,效果满意,现报告如下。
1 资料与方法
1.1 一般资料 观察研究对象为我院2008年7月至2013年7月收治的5例病人。男4例,女1例,年龄39~64岁,平均44.8岁,病程50d至1年不等,术前心功能(NYHA):Ⅳ级2例,Ⅲ级2例,Ⅱ级1例;5例患者主要共同症状有:胸闷,劳力性呼吸困难,2例患者有下肢静脉血栓形成,服用华法林抗凝治疗;1例患者出现咳嗽、咳痰、咯血;1例患者入院时出现右心功能不全的表现,包括端坐呼吸、咳粉红色泡沫痰等,入院即在重症监护室监护。4例病人都行心脏彩超、胸片、CTPA等检查,其中1例CTPA检查显示右肺动脉主干及其上下叶各分支动脉内栓塞,心脏彩超显示肺动脉主干及左右分支分别增宽23mm、44mm,右侧分支可见不规则稍强实质性回声填充49mm×26mm,肺动脉右支近端血流信号充盈缺损。5例病人的病变均以中央型为主,栓塞部位自左或右肺动脉主干开始,累及肺叶、肺段肺动脉,其中心脏彩超示主肺动脉内径46~61mm(平均53 mm),右室内径35~48mm(平均41mm),心脏彩超估测肺动脉压52~156mmHg(平均73mmHg)。
1.2 手术方法 本组患者都采用全身麻醉,常规建立体外循环,手术均在浅低温心脏不停跳下进行。患者经胸骨正中切口开胸,悬吊心包,进行体外循环插管,充分游离上腔静脉、不阻断主动脉,暴露肺动脉,切开右房,探查有无卵圆孔未闭或心内肿瘤。切开主肺动脉至近上下肺叶分界处,清除陈旧血栓及剥离增厚的肺动脉内膜,血栓多为混合血栓,有1例机化严重,完成后恢复循环,缝合右肺动脉切口并开始复温,逐步撤离体外循环。其中1例男性病人为术前误诊左房黏液瘤,术中探查未见肿瘤,经术中食管超声探查诊断为双侧肺动脉栓塞,经升主动脉-上腔静脉窗切开右肺动脉,完整取出一大小约1.5cm×1.3cm的新鲜活动栓子,再经主肺动脉切开左肺动脉取出一大小约2.0cm×1.8cm的陈旧性血栓。术前术中均用前列地尔降肺动脉压。术中转机时间(92±22.3)min。
1.3 术后监护及术后继续治疗 手术后病人转入重症监护室监护,术后6h继续用低分子肝素抗凝,术后24h用口服华法林(INR维持于2~3),重症监护室中位监护时间为2d(1~4d),中位拔管时间为1d(0.5~2d)。在监护室内治疗予以呼吸机辅助正压通气,心电监护,适当过度通气,使用利尿剂、脱水剂、血浆、胶体等使机体出入量处于负平衡状态,减轻肺水肿。按千克体重微泵泵入多巴胺或多巴酚丁胺等正性肌力药维持心功能。
2 结 果
2.1 治疗效果 5例病人均顺利转回普通病房,继续强心、利尿、补钾、抗凝、降肺动脉压等治疗,无1例死亡,无术后残余肺动脉高压、灌注肺等并发症。术后各病人肺动脉压力和肺血管阻力明显降低,术后复查心脏彩超估测肺动脉压为35~44mmHg(平均37mmHg),提示肺动脉血流通畅,血管管壁光滑,术后均顺利出院。患者的ST检查表现及手术取出的血栓见图1和图2。
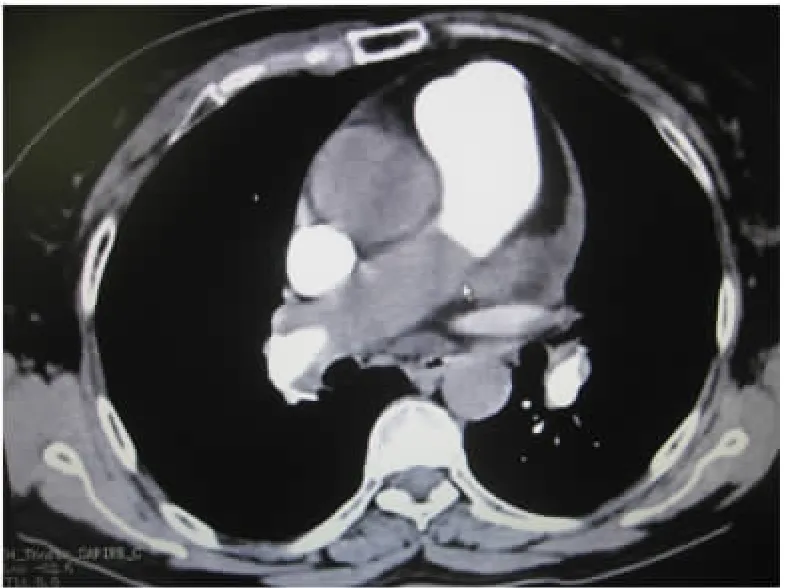
图1 CTPA示右肺动脉主干栓塞的CT表现
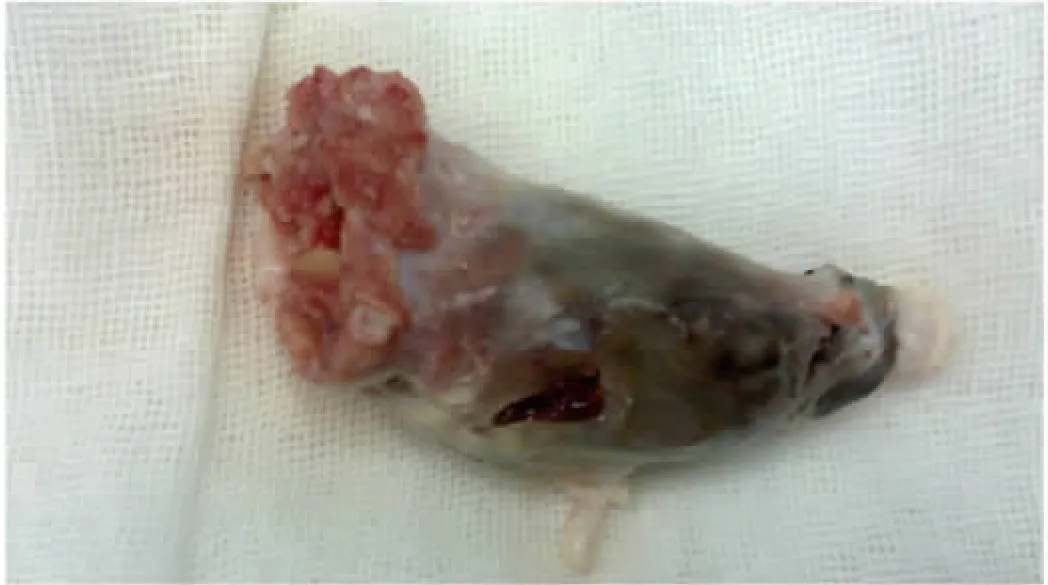
图2 手术取出的混合血栓(大体标本)
2.2 随访情况 病人出院后均有专人电话不定期随访及门诊随访,电话随访时间为6~12个月,随访期间无死亡,肺动脉栓塞消失,心功能恢复至Ⅰ级。术后3个月和6个月以门诊随访方式复查心脏彩超及CTPA,肺动脉压均较前降低,CTPA未见明显充盈缺损。
3 讨 论
美国加州大学圣迭戈分校的贾米森博士和他的团队在1970年开始就致力于PTE的研究,迄今为止,已经有超过2 500个病例的积累[1],总体的死亡率为6.4%。随着科学技术、设备以及术者手术技巧的进步,近年来的死亡率日益下降。在最新的一组统计上,他们已经做到围手术期零死亡率[2]。由此可见,把握手术适应证及时机,完善围手术期的用药及术前准备,手术技巧的提高,术后完善的监护以及适当的抗凝,使得PTE手术成为治疗CETPH的首选治疗手段。
3.1 手术适应证 临床上确诊的慢性肺动脉栓塞,理论上来说只要能够耐受麻醉及体外循环者均可以接受手术治疗,即无绝对禁忌证。但下列因素可作为手术的相对禁忌证:①肺血管阻力(PVR)大于1 000达因单位:Thistlethwaite和他的团队在一个超过1100例手术的研究中发现,手术中有34例病人死亡,其中绝大多数发生在那些在PVR大于500达因单位的病人身上,而有研究表明,另一组PVR较低的对照组病人,术后血流动力学的稳定性较高,死亡率更低[3]。②远端肺动脉栓塞:根据圣迭戈大学的统计,病变位于远端的病人的平均住院天数和围手术期死亡率均高于病变位于近端的病人[4]。除此之外,高龄、肥胖等也是手术的高危因素。
3.2 手术方式的选择 在早期的病例中,正中开胸,建立体外循环,在深低温停循环(DHCA)下行PTE[5]。这种方法的好处在于能够避免从支气管动脉反流,从而提供一个清晰的术野以及对肺的保护。但是随之而来的则是深低温带来的神经系统并发症,如中风、谵妄、舞蹈样运动等。以下数据是Mayer和他的团队在几个较大心脏中心对神经系统并发症与DHCA时间所作的统计:当DHCA在20min以内时,发生神经系统并发症的可能性为1.9%,当这个数字上升到21min至40min、41min至60min以及60min以上时,这个可能性逐渐上升至10.8%、14.6%和18.4%[6]。由此说明DHCA在没有脑保护的情况下,对神经系统的影响是显而易见的。对此,选择性脑灌注技术的发展弥补了这个弊端,加上糖皮质激素和甘露醇等药物对神经系统的保护,使神经系统并发症发生率大幅度降低。对于栓子为中央型的病例,体外循环不停跳并行循环下行PTE术,较之DHCA有其独特的优势,并行循环下PTE。不阻断主动脉,不灌注心脏停跳液,维持冠状动脉持续有效灌注,使心脏有节律空跳,心肌持续得到氧合血供应,在不影响术野清晰度的前提下,可减轻了心肌缺血缺氧及再灌注损伤,并且使脑、肾等重要器官得到充分灌注。本组5例病人均采取这种方法,术后无一出现神经系统并发症,无灌注性肺损伤。但术后残余肺动脉高压的发生率较DHCA高[12],但在栓子为外周型。术者认为,栓塞不易剥离以及术野布满从支气管动脉或其他体肺侧支循环反流的血而影响操作时,DHCA能够提供一个“无血”的视野,增加了手术的安全系数;并且随着选择性脑灌注及间断停循环等新技术的应用,进一步降低了神经系统并发症的发生率。
3.3 围手术期的处理 肺血管阻力(PVR)是CETPH治疗中很重要的一个指标,术前数值作为手术指证的重要参考指标,术后的数值则作为并发症发生率的一个参考。围手术期药物治疗(前列腺素、内皮素受体抑制剂、磷酸二酯酶抑制剂)主要以扩张肺动脉、降肺动脉压为主。Reesink和他的同事对手术之前服用双重内皮素-1拮抗剂波生坦治疗慢性血栓栓塞性肺动脉高压患者的观察表明,在血流动力学和临床表现上均有显著改善,但没有明确的证据证明对手术的预后有无影响[7]。
早期术后监护的原则为降低全身氧的消耗,提高右心室前负荷及心肌收缩力,但在术后早期不推荐尝试降低右心室后负荷,因为术后早期肺血管阻力往往是没有较大的变化,降低右心室后负荷,有可能导致全身性低血压以及冠脉灌注压下降。有限的数据表明,术后用药吸入伊洛前列素或一氧化氮对肺血流动力学和气体交换可能有正面的影响[8,9]。
术后最常见的并发症为再灌注肺水肿所造成的持续性的肺动脉高压,通常发生在体外循环停止后72h内,由于血栓清除,使血液在内膜剥脱段形成再分布血流,表现为肺泡间质性水肿,轻者出现呼吸困难,严重者可出现术后大出血。所以,术后的呼吸辅助支持非常重要。术后应用呼气末正压低流量进行缓慢通气。有研究结果表明,低流量通气可有效降低术后急性肺损伤的发生率[10]。单侧肺动脉栓塞患者,尽可能应用双腔通气,尽可能使机体负平衡,减少入量,增加出量,以减轻肺水肿。同时,术后积极抗凝、预防再栓塞与预后息息相关,术后6h后若引流量不大,可用肝素抗凝;术后24h开始服用华法林抗凝,可以根据PT及INR的值调整用药剂量[11]。
总而言之,在术前评估得当,严格把握手术指征,术中仔细操作,术后严密监护的前提下,肺动脉血栓内膜剥脱是治疗慢性栓塞性肺动脉高压的有效手段。
[1]Madani MM,Jamieson SW.Technical advances of pulmonary endarterectomy for chronic thromboembolic pulmonary hypertension[J].Semin Thorac Cardiovasc Surg,2006,18(3):243-249.
[2]Madani MM,Wittine LM,Auger WR,et al.Chronic thromboembolic pulmonary hypertension in pediatric patients[J].JThorac Cardiovasc Surg,2011,141(3):624-630.
[3]Thistlethwaite PA,Kaneko K,Madani MM,et al.Techniques and outcomes of pulmonary endarterectomy surgery[J].Ann Thorac Cardiovasc Surg,2008,14(5):274-282.
[4]Jaff MR,McMurtry MS,Archer Sl,et al.Management of massive and submassive pulmonary embolism,ili of emoral deep vein thrombosis,and chronic thromboembolic pulmonary hypertension:A scientific statement from the American Heart Association[J].Circulation,2011,123(2):1788-1830.
[5]Daily PO,Auger WR.Historical perspective:surgery for chronic thromboembolic disease[J].Semin Thorac Cardiovasc Surg,1999,11(2):143-151.
[6]Mayer E,Jenkins D,Lindner J,et al.Surgical management and outcome of patients with chronic thromboembolic pulmonary hypertension:results from an international prospective registry[J].J Thorac Cardiovasc Surg,2011,141(3):702-710.
[7]Reesink HJ,Surie S,Kloek JJ,et al.Bosentan as a bridge to pulmonary endarterectomy for chronic thromboembolic pulmonary hypertension,2010,139(1):85-91.
[8]Imanaka H,Miyano H,Takeuchi M,et al.Effects of nitric oxide inhalation after pulmonary thromboendarterectomy for chronic pulmonary thromboembolism[J].Chest,2000,118(1):39-46.
[9]Kramm T,Eberle B,Guth S,et al.Inhaled iloprost to control residual pulmonary hypertension following pulmonary endarterectomy[J].Eur JCardiothorac Surg,2005,28(6):882-888.
[10]Mares P,Gilbert TB,Tschernko EM,et al.Pulmonary artery thromboendarterectomy:a comparison of two different postoperative treatment strategies[J].Anesth Analg,2000,90(3):267-273.
[11]任 华,苏丕雄,张超纪,等.慢性肺动脉血栓栓塞的外科治疗[J].中华外科杂志,2005,43(6):345-347.
[12]李浩杰,宋云虎.慢性血栓栓塞性肺动脉高压的外科治疗[J].中国循环杂志,2009,24(5):396-398.
