AIIIBV型异构化合物热容优化
2013-04-24瓦列里瓦西里耶夫龚伟平TaldrikKulinich
瓦列里·瓦西里耶夫, 龚伟平,张 瑞,Taldrik A F,Kulinich S A
(1.莫斯科大学化学系,莫斯科119992;2.惠州学院电子功能材料实验室,广东 惠州 516007;3.中南大学粉末冶金研究院,湖南 长沙 410083 ;4.俄罗斯库尔恰托夫研究院超导与固体物理研究所,莫斯科;5.東海大学創造科学技術研究機構,平塚市 神奈川県259-1292)
以AIIIBV相为基的半导体具有优异的光谱性,可以应用于太阳能电池、发光二极管、镭射二极管等线性光学和非线性光学设备[1],近年来受到人们的广泛关注。了解不同AIIIBV相的热力学性质有助于优化这些化合物在从气相状态生长单晶或者外延结构过程中的热平衡,提高此类材料的生产技术和产品质量。


表1 通过多项式描述的AIIIBV相热容值(单位:J/(mol·K)[4] for AIIIBV compounds[4]
分析文献报道的热容数据发现,具有相同原子总数的AIIIBV异构相化合物的低温热容值在实验误差范围内几乎相同,并且这种规律可以推广到熔点温度,即具有相同原子总数的AIIIBV异构相化合物,它们在熔点以下的热容值基本相等。为此,本工作假设这些化合物不发生结构转变,分析其低温热容数据,并采用最小二乘法对所研究相的热容函数关系进行计算,推导得到该化合物的热容表达式Cp=a+b·10-3·T-c·105·T-2+d·103·T-1,以及热容与组元A和B原子数的函数关系(Cp-ZA,ZB)。另外,本工作所提出的数据遴选方法,有助于利用等式来计算和表述AIIIBV相的热容值。
1 文献数据评估
评估热化学实验结果的难点在于,目前对有些化合物的研究和分析还不够透彻,文献数据较为缺乏。因此,收集、补充热化学数据是现代热力学研究的一个主要方面。而计算热力学及其相关研究方法的进步则推动着现代热力学的发展。
总体说,热化学实验包含两个相对独立且同样重要的方面,一是实验设备或者量热计,它们用来测量实验过程中样品的能量或者电位变化;其二则可以理解为与“化学”有关的方面,通过精确设计目标体系的初始状态和终止状态,同时尽可能避免样品的挥发、氧化、分解以及样品与容器之间的化学反应,以保证热化学实验的测量精度。
通过研究两组具有相同分子质量的AIIIBV相(第一组:AlSb,GaAs,InP,第二组GaSb和InAs),Lichter和Sommelet[7]首次指出,当温度高于298 K时,AIIIBV相的热容与分子质量具有一定的函数关系。本次工作在全面分析文献报道和本工作实验测量的热容数据的基础上,对如图1-8所示的16种AIIIBV化合物进行分析评估,以期验证Lichter和Sommelet[7]的结论。

图1 优化所得hBN的热容与文献数据[6,9-10]的比较Fig.1 Heat capacity of hBN vs temperature, compared with the literature data[6,9-10]
Ge在元素周期表中介于Ga、As之间,其热容与化合物AlSb、GaAs、InP (Zi=64)的热容相等。图6为计算所得所示AlSb、GaAs、InP的热容。
图2-7分别为原子数为20、38、56、46、64、82的六组AIIIBV化合物的热容。从图可以看出,这几组具有相同原子总数的AIIIBV化合物,它们的低温热容在实验误差范围内具有很高的一致性,并且我们有理由推断:这些具有相同原子数的AIIIBV化合物的室温热容也应该相似;当这些化合物在研究温度范围内不发生结构转变时,它们的热容值也应具有相似的变化规律,并且这种变化规律只与AIIIBV化合物的分子质量和原子总数(Zi)有关;在相同温度下,所有具有闪锌矿结构和纤锌矿结构的AIIIBV化合物的热容与化合物原子总数的对数成严格的线性关系。以上研究证实并拓展了Lichter和Sommelet[7]的结论。
图3所示为分子质量为38(Zi=38)的两个化合物GaN、BAs热容随温度变化情况,可以看出,这两个化合物的低温热容具有很好的一致性,但是当温度高于300 K时,它们的热容值却存在较大差异。全面分析样品制备、测量过程,我们认为热容数据在高温出现差异的原因是由于试样BAs中引入了其它晶体混合物,比如BN的四种不同晶体结构Gavrichev[9-10]。

Fig.2 优化所得化合物BP、AlN (Zi=20)的热容与文献数据[11-14]的比较Fig.2 Heat capacity of BP and AlN (Zi=20) vs temperature, compared with literature data [11-14] respectively

图3 计算所得化合物BAs和GaN (Zi=38)的热容与文献数据[6, 15-20]的比较Fig.3 Heat capacity of BAs and GaN (Zi=38)vstemperature, compared with literature data[6,15-20]
图4为文献[20]报道的InN热容值,在此工作中清楚地证实了InN化合物的分解反应[20],但至今为止还没有其它文献证实此分解反应,而且他们还发现InN的热容值在整个温度范围内保持不变(如图4中的固态三角形所示),这一事实也不支持InN的分解反应。但我们认为不同研究者报道的热容数据存在差异的原因应该就是源于氮化物的分解。图3所示的数据差异也应该包含这类原因。

图4 计算所得化合物InN (Zi=56)的热容与文献数据[20, 22-24]的比较 Fig.4 Heat capacity of InN (Zi=56)vstemperature, compared with literature data [20,22-24]
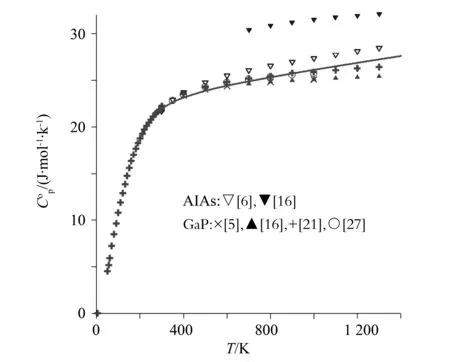
图5 优化计算所得AlAs、GaP (Zi=46)的热容与文献数据[5, 6, 16, 21, 27] 的比较。Fig.5 Heat capacity of AlAs and GaP (Zi=46)vs temperature, compared with literature data [5-6, 16, 21, 27]
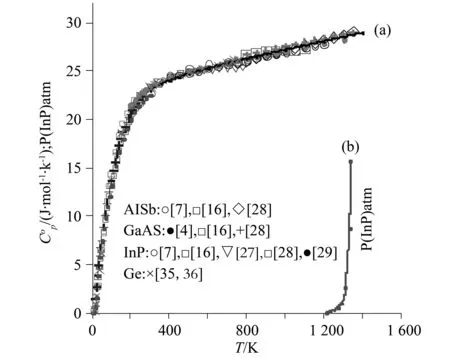
图6 优化计算所得AlSb、GaAs、InP (Zi=64)的热容与文献数据[4, 7, 16, 27-29]的比较,纯Ge的热容与之相等Fig.6 Heat capacity of AlSb, GaAs and InP (Zi=64)vs temperature, compared with literature data [4, 7, 16, 27-29]

图7 优化计算所得GaSb、InAs (Zi=82)的热容与文献数据[6-7, 28, 30]的比较Fig.7 Heat capacity of GaSb and InAs (Zi=82)vs temperature, compared with literature data [6-7,28,30]

图8 优化计算所得InSb、GaSb、AlSb的热容与文献数据[7, 16, 28]的比较Fig.8 Comparison of heat capacity of InSb、GaSb、AlSb vs temperature,compared with literature data [7,16,28]
图6中的曲线b所示为InP的蒸汽压对温度的函数关系,由图可以看出在升温过程中磷大量分解与蒸发,这主要由于磷与第三主族元素形成的化合物具有很高的蒸汽压。这种现象在第三主族砷化物中也广泛存在,这必将影响这类化合物热力学性质的测量。除此之外,AlP、AlAs等化合物在空气中
很容易水解也将给实验测量带来较大误差。为此,一方面在实验中应当尽量避免,另一方面在数据分析时应当对这些因素加以考虑。
如图9所示为Unlande等[18]建立的Ga-N体系相图,可以看出液相线从熔点处偏离至非挥发性组元处,这主要是由于第三主族元素氮化物在接近熔点温度时很容易分解失氮,因此,为了保证此类含氮体系的平衡,应当将氮压控制在6到10 GPa之间时测量熔点。
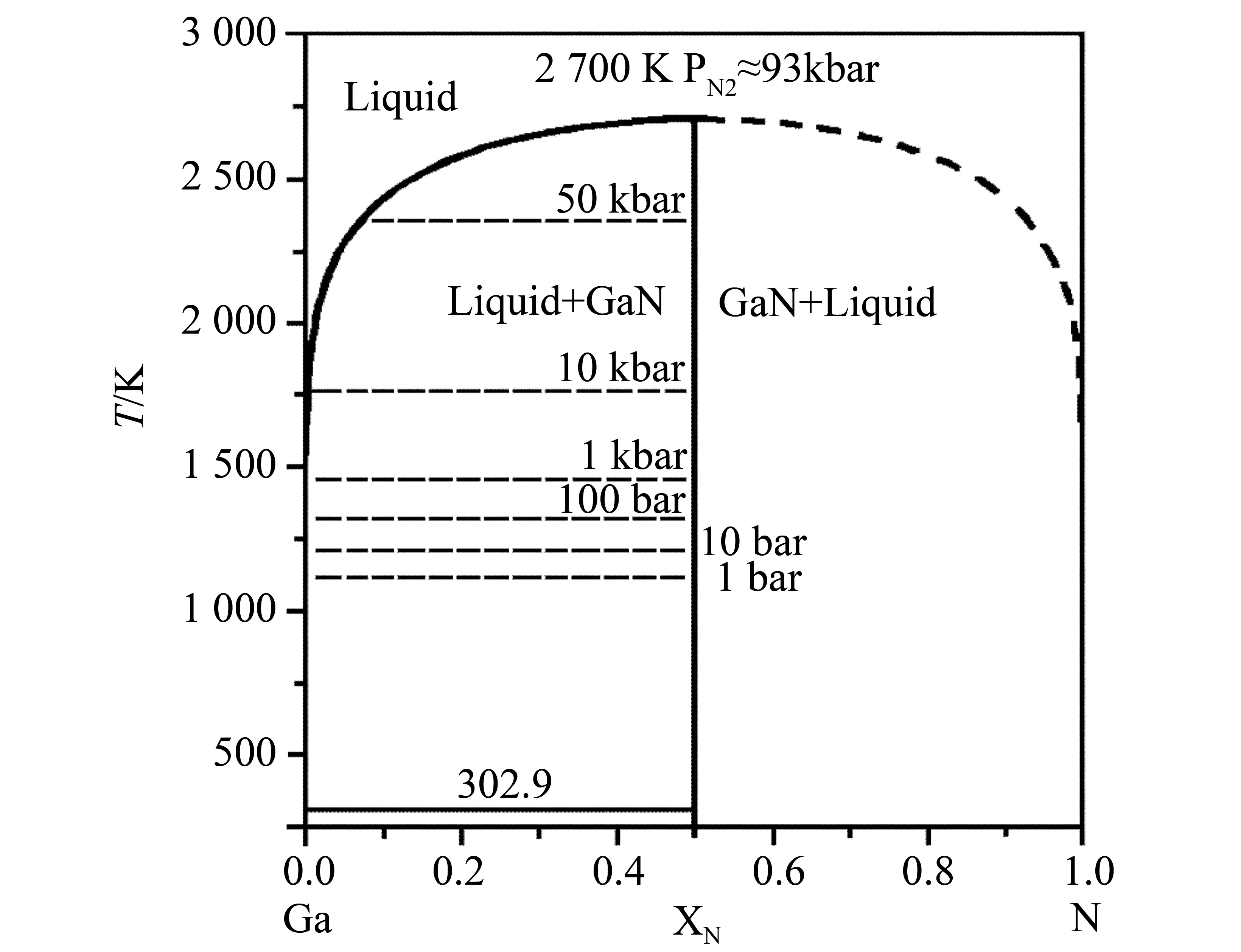
Fig.9 文献报道Ga-N体系计算相图[18]Fig.9 Calculated phase diagram of the Ga-N system[18]
图10为文献报道的AlP热容,可以看出,不同研究者报道的数据存在较大差异[6, 16, 26, 31]。正如上文所说,AlP相在空气中容易水解,很难获得纯AlP相的实验数据。由于文献[31]报道的数据有可能仅是猜测的结果,在此不予讨论。 文献[6]是目前广为接受的数据手册,将其报道的AlP热容数据与文献[16, 26]相比较,发现差异高达4 J/(mol·K),甚至超过了图3所示化合物BAs和GaN在1 400 K以上的误差,这么大的差异除了测量的误差,应该还包含样品纯度的原因。

图10 优化所得AlP的热容于文献数据的比较+ -[6],○-[16], △-[26],- - - [31]Fig.10 Heat capacity of AlP vs temperature, compared with literature data - [6], ○ - [16], △- [26], - - - [31]
文献[32]理论计算了GaN和InN的热容与温度的函数关系。图11比较了本次工作的计算结果与Marmallyuk[32]等的结果,可以看出化合物 GaN的热容值最大差异不超过0.6 J/(mol·K),InN的最大差异不超过0.8 J/(mol·K),可以认为在误差范围内一致。

图11 本工作计算所得GaN、InN热容与文献[32]计算的比较Fig.11 Present calculated heat capacity of GaN and InN, compared with [32]
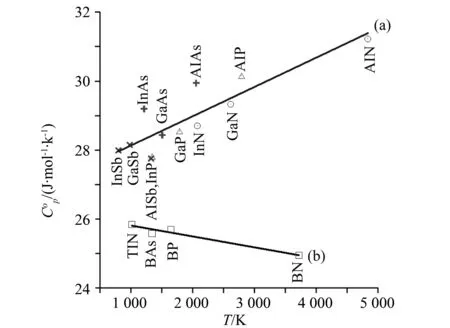
图12 化合物AIIIBV热容关系比较Fig.12 Correlation between heat capacities of AIIIBV in solid state near their temperature of fusion
以图1-8所示的热容值为基础,采用最小二乘法可以得到具有不同原子数的各组化合物的热容函数表达式,结果如表2所示。利用此函数可以计算得到除硼化物和氮化铊(图12曲线b)以外的所有化合物熔点以下温度的热容,如图12曲线a所示,在高达1 200 K的温度下,这些AIIIBV相化合物热容值的误差仅有(±1 J/(mol·K),可以认为是合理的。

表2 AIIIBV相的热容值Table 2 Heat capacities of AIIIBV phases
图12中的曲线a和b可以分别用以下等式来表达:
r=0.77, 2So=(±1 J/ (mol·K)
(1)
r=0.95, 2So=(±0.25 J/ (mol·K)
(2)
由表2还可以得出AIIIBV化合物的热容值与原子总数的函数关系,如图13、14所示分别为本工作推导得到的闪锌矿结构、纤锌矿结构两类AIIIBV化合物在298-1 500 K温度范围的热容与原子总数对数的线性关系式。运用这种函数关系,预测了化合物AlP、TlN的热容,结果见图13、14和表2。
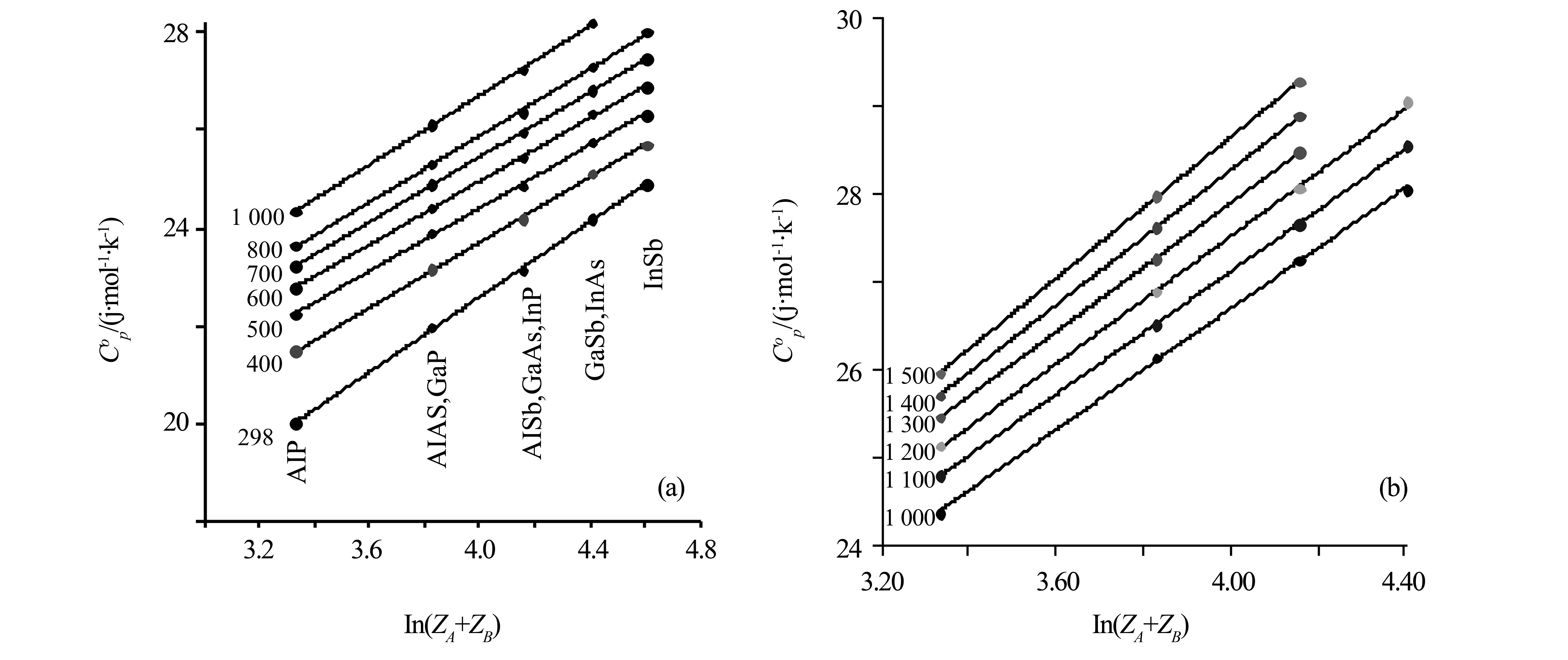
图13 闪锌矿型AIIIBV化合物Cp (T)值与原子总数Zi自然对数的关系图a.298-1 000 K; b.1 000-1 500 KFig.13 Cp(T)vs logarithm of the sum of atomic numbers of elements for sphalerite type AIIIBV phases(a) at 298-1 000 K range;(b) at 1 000-1 500 K range.

图14 纤锌矿型AIIIBV化合物Cp(T)与原子总数Zi自然对数的关系图(a)298 -1000 K; (b)1000-1500 K.Fig.14 Cp(T)vs logarithm of the sum of atomic numbers of elements for wurtzite type AIIIBV phases at (a) 298 -1000 K; (b)1000-1500 K.
假设所有晶体相在其固态存在温度范围内都有序并且不发生结构转变,这样就可以利用如图13和14所示的Cp(T)值与原子总数的函数关系,计算化合物的热容,所得热容的误差值不大于±0.3 J/(mol·K)。由图1-8可以看出,根据本工作优化建立的热容函数(表2)计算Cp(T)的误差接近于±0.3 J/(mol·K),在1 200 -1 600 K温度区间则达±0.3 - 0.5 J/(mol·K),这一误差是可以接受的。然而在1 700 K以上时,误差达到±0.6 - 1.0 J/(mol·K)。如图曲线(a)所示,GaAs、GaP、AlAs、AlP等化合物的热容与原子数的函数较为偏离线性关系,这是因为正如上文所提到的,砷化物和磷化物的测量实验在高于1 200 K时会出现很多问题,当这些化合物的蒸汽压达到与气氛的气压一样高时,有必要把砷和磷的高化学势考虑到实验测量当中(和反应元素活性相当),所以本工作建议使用最大误差来处理。
(3)
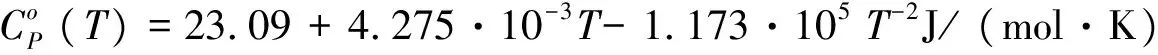
2 结 论
本次工作通过使用相关性优化的方法分析了16个AIIIBV相化合物,获得了闪锌矿和纤维锌矿结构相在298 K到1 500 K温度范围的热容函数关系,并且分别预测了氮化铊(TlN)、磷化铝(AlP)在298~1 018 K、298~1 500 K温度范围的热容,所获得的数据可以用来计算以AIIIBV化合物为基的伪二元或者伪三元体系的热力学性质,同时可以用来优化这些相从气相到单晶生长和外延结构生长的热平衡,这些都有利于从基础理论方面来了解光电材料。本文中采用相关性方法所得到的热力学函数也可以应用至其他的异构材料和无机化合物当中。
参考文献:
[1] YADAV D S, SINGH D V.Statistic and dynamic properties of II-VI and III-V group binary solids[J].J Phys Scr,2012, 85: 015701.
[2] VASSILIEV V P, LEGENDRE B, ZLOMANOV V P.The critical analysis and mutual coherence of thermodynamic data of the AIIIBV phases[J]. Intermetallics Intermetallics, 2011, 19: 1891-1901.
[3] GORBOV S I.Thermodynamics of III-V Semiconductors[J]. Itogi Nauki Tekh, Ser: Khim Termodinicheskie Ravnovesiya, 1975, 3: 151. (in Russian)
[4] PASHINKIN A S, FEDOROV V A, MALKOVA A S, et al. Heat capacity of GaBVand InBV(BV= P, As, Sb) above 298 K[J]. Inorg Mater, 2010, 46: 1007-1012.
[5] PASHINKIN A S, MALKOVA A S. Specific heat of solid gallium phosphide[J].Russ J Phys Chem, 2003, 77: 1889-1891.
[6] LANDOLT-Börnstein. Handbook[M].New York:Springer-Verlag Berlin, Heidelberg,1982, III/17a:14.
[7] LICHTER B D, SOMMELET P. Thermal properties of AIIIBV- high temperature heat contents and heat of fusion of InSb, GaSb and AlSb[J].Trans Met,1969, 245: 99 -105.
[8] KNACKE O, KUBASCHEWSKI O, HESSELMANN K. Thermodynamical properties of inorganic substances[M].2 ed. V 1 Berlin. Heidelberg; N Y: Springer Verlag, Stahleisen. 1992:1113.
[9] GAVRICHEV K S, SOLOZHENKO V L, GORBUNOV V E. et al. Low-temperature heat capacity and thermodynamic properties of four boron nitride modifications[J].Thermochim Acta,1993, 217 : 77-89.
[10] GAVRICHEV K S, SOLOZHENKO V L, LAZAREV V B. Thermodynamic properties of boron nitride from calorimetric studies[J].Inorg Mater 1994, 30: 1025-1033.
[11] KOSHCHENKO V I, GRINBERG YaH, DEMIDENKO A F. Thermodynamic properties of AlN (5-2 700 K),GaP (5-1 500 K) and BP (5-800 K)[J]Inorg Mater,1984, 20: 1550-1554.
[12] KUMASHIRO Y.Refractory semiconductor of boron phosphide[J]. J Mater Res,1990, 5:2933-2947.
[13] OHSAWA J, NISHNAGA T, UCHIYAMA S.Measurements of specific heat of boron monophosphide by AC calorimetry[J].Jpn J Appl Phys, 1978, 17: 1059-1065.
[14] MAH A D, KING E G, WELLER W W, et al. Bur Mines Rep[M].Invest, 1961:5716.
[15] KOSHCHENKO V, DEMIDENKO A F, SABANOVA L D, et al. Thermodynamic properties of gallium nitride from 5 to 300 K[J]. Izv Akad Nauk SSSR Neorg. Mater. 1979, 15: 1686-1687.
[16] YAMAGUCHI K, ITAGAKI K, YASAWA A. Heat capacity of AIIIBV[J]. J Jpn Inst Met,1989, 53:764-770.
[17] CHEN X L, LAN Y C, LIANG J K, et al. Structure and heat capacity of wurtzite GaN from 113 to 1073 K[J].Chin Phys Lett,1999, 16:107-108.
[18] UNLANDE J, ONDERKA B, DAVIDOV A, et al. Thermodynamics and phase stability in the Ga-N system[J]. J Cryst Growth,2003,256:33-51.
[19] TOMASZKIEWICZ I Z, ULTZIG E, GIERYCZ P.Heat capacity of crystalline GaN[J].J Therm Anal Calorim, 2008, 91:329-332.
[20] TOMASZKIEWICZ I Z, ULTZIG E, GIERYCZ P. Heat capacity of indium nitride[J].J Therm Anal Calorim, 2008, 91: 649-653.
[21] DEMIDENKO A F, KOSHCHENKO V I, SABANOVA L D, et al. Low-temperature heat capacity. Entropy and enthalpy of aluminum and gallium nitrides[J].Zh Fiz Khim, 1975, 49:1585-1586(in Rusian)
[22] LEITNER J, STEJSKAL J.Thermodynamic aspects of the Ga1-xInxN growth by MOCVD[J]. J Mater Lett,1998, 35: 85-89.
[23] ONDERKA B, UNLANDE J, SCHMID-FETZER R.Thermodynamics and phase stability in the In-N System[J]. J Mater Res, 2002, 17:3065-3083.
[24] KRUKOWSKI S, WITEK A, ADAMCZYK J, et al.Thermal properties of indium nitride[J].J Phys Chem Solids, 1998, 59: 289-295.
[25] DEMIDENKO A F, KOSHCHNKO V I, MEDVEDEVA Z S, et al. Thermal capacities and thermodynamic functions of BAs and B6As[J].Russ Inorg Mater, 1975, 11: 2117-2019.
[26] NEVIAK S O, SANDULOVA A B, Izv Akad Nauk SSSR.Thermodynamic properties of AlP[J]. Rus Neorg Mater,1974, 10: 146-147.
[27] PANKRATZ L B. High-temperature heat contents and entropies of gallium phosphide. indium phosphide and indium sulphide[C]∥US Bureau of Mines Rep Invest, 6592; US Department of the interior: Washington. DC. 1965.
[28] PIESBERGEN U. Die durchschnittlichen Atomwärmen der A3B5Halbleiter AlSb,GaAs,GaSb,InP,InAs,InSb und die Atomwarme des Elements Germanium zwischen 12 - 273 К[C].Naturwissenschaften 1963, l8a:141 -147.
[29] SIROTA N N, ANTJUKHOV A M, NOVIKOV V V. Temperature dependence of the capacity and characteristic thermodynamics functions of solid solutions of GaAs and InP in the range 5-300 К[J].Doklady AN SSSR, 1982, 266: 105-108.
[30] GLAZOV V M, PASHINKIN A S. Thermal expansion and heat capacity of GaAs and InAs[J].Rus Inorg Mater,2000, 36: 225-231.
[31] COX R H, POOL M J. Heat contents and heats of fusion of III-V[J].J Chem Eng Data, 1967, 12: 247-248.
[32] MARMALLYUK A A, AKCHURIN R Kh, GORBYLEV V A. Theoretical calculation of the Debye temperature and temperature dependence of heat capacity of aluminum, gallium, and indium nitrides[J]. High Therm, 1998, 36: 839-841.
