斑块成份对经皮冠状动脉介入治疗术后再狭窄的影响*
2013-04-19罗江宾王天松方明
罗江宾,王天松,方明
斑块成份对经皮冠状动脉介入治疗术后再狭窄的影响*
罗江宾,王天松,方明
目的:应用血管内超声虚拟组织成像技术(IVUS-VH)量化评价斑块成份对经皮冠状动脉介入治疗(PCI)术后再狭窄的影响。
动脉粥样硬化斑块;再狭窄;血管内超声-虚拟组织学
(Chinese Circulation Journal, 2013,28:176.)
支架术后再狭窄一直是困扰介入治疗的最大难题。裸 支 架 时 代, 支 架 术 后 再狭 窄率 高达 30%[1]。药物洗脱支架使简单病变再狭窄率降至 8%,但复杂病变仍可高达 20%,且存在晚期血栓形成问题[2]。以往研究表明,不同类型斑块介入术后再狭窄发生率存在明显差别[3,4]。血管内超声虚拟组织成像技术(IVUS-VH)是利用超声射频信号的反向散射原理,通过计算机的功率频谱进行处理并比较分析,可精确分析冠状动脉(冠脉)斑块成份。本研究利用 IVUS-VH,探索斑块成份与支架术后再狭窄关系,为揭示再狭窄机制提供临床证据。
1 资料与方法
一般资料:自 2009-06 至 2011-06,共连续入组 300 例患者。入选标准:所有患者均符合世界卫生组织冠心病诊断标准,具有择期PCI指征,同意入选本研究并签署知情同意书。排除标准(符合任一项):合并糖尿病者;急性心肌梗死者;血管内超声导管不能通过病变者;左心室射血分数 <35% 者;严重的肝、肾或凝血功能障碍者。本研究方案获得医学伦理委员会批准且符合赫尔辛基宣言精神。
方法:依据择期冠脉造影结果,纳入具有 PCI指征的非糖尿病患者,采集患者临床资料。在支架置入术前,对所有罪犯病变行血管内超声检查,并应用虚拟组织学软件分析斑块成份;所有患者均采用雷帕霉素洗脱支架,支架置入要求全病变覆盖;手术成功标准为残余狭窄≤ 30%,前向血流心肌梗死溶栓治疗临床试验(TIMI) Ⅲ级,无急性并发症。术后所有患者严格戒烟,均接受阿司匹林 100 mg/d(终身 ),氯吡格雷 75 mg/d(至少 1 年 ),并根据病情给予他汀类、血管紧张素转换酶抑制剂及β受体阻断剂等药物规范治疗。1年后复查冠脉造影,以支架内及支架近、远端 5 mm 血管狭窄≥ 50% 为标准,将所有患者分为无再狭窄组 245 例和再狭窄组 47 例(另 8 例为失访患者),比较两组间临床特征和斑块成份。
血管内超声虚拟组织成像技术采集及分析:将3.5 F 的导管送至罪犯病变远端,造影确定顶端位置,以自动回撤装置将血管内超声导管以 1.00 mm/s 速度回撤,同时采集影像数据,录盘分析。由一名分析员在不清楚诊断情况下,手工描记管腔与中、外膜界面轮廓,利用VH软件构建组织图像,利用客户端软件将每个切面获得的数据汇总得出每种成份在斑块中所占比例,并计算出斑块体积。
统计学处理:计量资料用均数±标准差表示;计量资料比较采用t 检验,样本不符合正态分布时,采用t '检验;计数资料用率(或百分位数)表示。计数资料比较采用卡方(χ2)检验, P< 0.05(双侧)有统计学意义。采用 Logistic 多元回归分析,计算比数比(OR )及 95% 可信区间(95% CI)。全部统计分析采用 SAS 软件包处理。
2 结果
随访结果: 300 例入选患者中,随访期间失访 8例(失访率 2.7%)。随访 1 年后,292 例患者复查冠脉造影结果显示,无再狭窄组 245 例,再狭窄组 47例(20 例为局限性支架内再狭窄,10 例为弥漫性支架内再狭窄,14例为增生性再狭窄,3例为完全闭塞),其中有 12 例患者术后再狭窄伴有血栓成份。再狭窄组中 100%闭塞为 3 例,狭窄 90%~95%的患者有 5 例,狭窄 80%~89%的患者有 15 例,狭窄70%~79%的患者有 24 例。
两组患者临床特征比较:术前两组间性别、年龄、高血压、吸烟、血脂比较差异均无统计学意义(P> 0.05),无再狭窄组高敏 C 反应蛋白明显高于再狭窄组差异有统计学意义(P<0.05 )。表1

表1 两组患者临床特征比较 [例(%)]
两组患者罪犯病变粥样硬化斑块成份特征比较:PCI术前,共对 292 例患者的 330 处罪犯病变行IVUS-VH 检查。两组间斑块成份比较发现,再狭窄组坏死组织比例较高,无再狭窄组钙化组织比例较高,差异均有统计学意义(P<0.05)。表2

表2 两组罪犯病变粥样硬化斑块成份特征比较(±s)
两组患者病变类型及支架应用情况:冠脉病变分型标准:参考 1988 年美国心脏病学会和美国心脏协会 (ACC/AHA)制定的标准(病变类型分:A、B、C型病变,B型又分两个亚型,仅有1个B型病变特征为 B1型,有 2个或 2个以上的 B 型病变特征为B2 型)。比较两组患者 PCI的病变类型及支架应用情况,结果显示两组间在病变类型上及支架的应用情况差异均无统计学意义(P> 0.05)。表3
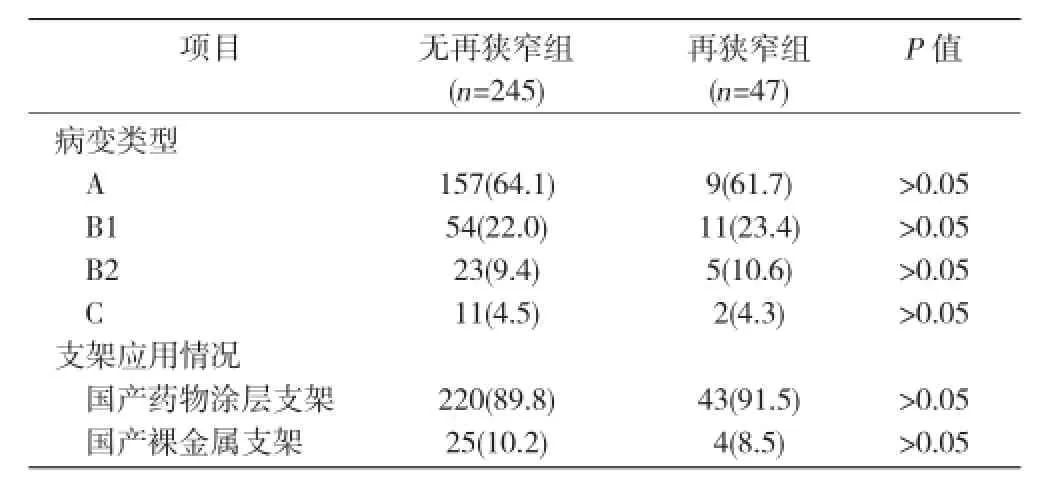
表3 两组患者病变类型及支架应用情况 [例(%)]
支架术后再狭窄因素分析:单因素比较显示,两组间坏死组织比例、钙化组织比例、高敏C反应蛋白比较,差异有统计学意义(P<0.05);对上述因素进一步作 Logistic 多元分析显示,高敏 C 反应蛋白 (比值比 =1.24,95%可信区间:1.05~1.81,P=0.027)和坏死核心成份比例 (比值比 =1.18,95%可信区间:1.05~1.66,P=0.041)是支架术后再狭窄的独立危险因素。
3 讨论
药物洗脱支架术后再狭窄主要与内中膜过度增生有关,平滑肌细胞过度增殖和细胞外基质分泌增多是内中膜增生的基础[5]。既往研究已经发现,糖尿病和吸烟可刺激平滑肌细胞增殖和分泌,是支架术后再狭窄的独立危险因素[6,7]。因此,本研究排除糖尿病患者,且支架术后均实行严格戒烟,避免二者对研究的直接影响。
既往曾有学者利用血管内超声对再狭窄进行过定性研究。Hong 等[8]的研究表明,含脂质比例较高的软斑块术后再狭窄率明显高于其它类型的斑块。本研究利用虚拟组织学(VH)量化分析斑块成份,证实罪犯病变中,坏死核心成份越大,再狭窄的发生率越高,这与 Hong等学者的结论相一致。
PCI术后高敏 C 反应蛋白水平显著升高患者,具有较高的致残率和再狭窄率,炎症与术后再狭窄的发生密切相关;炎症相关血清学标志物可用于识别再狭窄高危个体[9]。IVUS-VH 相关研究显示,冠脉粥样斑块中坏死组织体积与血浆高敏C反应蛋白的水平呈正相关,大量坏死组织的存在提示血管有炎症活动[10]。本研究中,再狭窄组斑块坏死成份比例显著高于无再狭窄组,高敏C反应蛋白水平明显增高,炎症趋于活跃,故再狭窄组支架术后,可能有更多的炎症细胞、炎性介质及趋化因子刺激平滑肌细胞增殖、分泌,诱使内中膜增生,导致再狭窄发生。这也提示,临床上可通过他汀等药物,有效控制血管炎 症,进而 预 防 再 狭窄 的 发 生。Niccoli等[11]学 者的研究已经证实,炎症与术后再狭窄的发生密切相关,炎症相关血清学标志物可用于识别再狭窄高危个体。本研究中,再狭窄组无再狭窄组高敏C反应蛋白水平明显增高,我们推测斑块内的炎性反应产生大量的新生滋养血管和炎性坏死物,引起斑块的体积迅速增大;另外,大量炎性细胞可释放溶解酶是纤维帽变薄,从而引起纤维帽的破裂,导致斑块表明血栓的形成,进一步加重管腔的狭窄度[12]。
本研究排除合并有糖尿病的患者,因此,研究结果可能无法代表整个患病群体。此外,由于患者在PCI术前吸烟时间上存在差异,虽然术后实行严格戒烟,但吸烟因素仍可能对研究结果有一定影响,尚需远期进一步随访观察。
[1]Nikolsky E,Kosinski E,Mishkel GJ,et al. Impact of obesity on revascularization and restenosis rates after bare-metal and drugeluting stent implantation (from the TAXUS-IV trial). Am J Cardiol,2005,95:709-715.
[2]Steigen TK,Maeng M,Wiseth R,et al. Randomized study on simple versus complex stenting of coronary artery bifurcation lesions:the Nordic bifurcation study. Circulation,2006,114:1955-1961.
[3]Hong YJ,Jeong MH,Lim SY,et al. Relation of soft plaque and elevated preprocedural high-sensitivity C-reactive protein levels to incidence of in-stent restenosis after successful coronary artery stenting. Am J Cardiol,2006,98:341-345.
[4]Shimada Y, Kataoka T, Courtney BK, et al. Influence of plaque calcium on neointimal hyperplasia following bare metal and drug-eluting stent implantation. Catheter Cardiovasc Interv, 2006, 67:866-869.
[5]Caixeta AM, Brito FS Jr, Costa MA, et a1. Enhanced inflammatory response to coronary stenting marks the development of clinically relevant restenosis.Catheter Cardiovasc Interv, 2007,69:500-507.
[6]Abizard A, Kornowski R, Mintzgs, et al. The influence of diabete mellitus on acute and late clinical outcomes following coronary stent implantation. J Am Coll Cardiol,1998,32:584-589.
[7]Nishio K, Fukui T, Tsunoda F, et al. Insulin resistance as a predictor for restenosis after coronary stenting. Int J Cardiol, 2005,103:128-134.
[8]Hong YJ, Jeong MH, Lim SY, et al. Relation of soft plaque and elevated preprocedural high-sensitivity C-reactive protein levels to incidence of in-stent restenosis after successful coronary artery stenting. Am J Cardiol,2006,98:341-345.
[9]Niccoli G, Montone RA, Ferrante G, et al. The evolving role of inflammatory biomarkers in risk assessment after stent implantation. J Am Coll Cardiol, 2010,56:1783-1793
[10]Sawada T, Shite J, Shinke T, et al.Relationship between high sensitive C-reactive protein and coronary plaque component in patients with acute coronary syndrome: Virtual Histology study. J Cardiol,2006,48: 141-150.
[11]Niccoli G, Montone RA, Ferrante G, et al. The evolving role of inflammatory biomarkers in risk assessment after stent implantation. J Am Coll Cardiol, 2010,56:1783-93
[12]李建军 .再狭窄发生的相关研究是冠心病介入治疗的长期课题 .中国循环杂志 ,2008, 23:401-403.
Effect of Coronary Plaque Composition on In-Stent Restenosis in Patients After Percutaneous Coronary Intervention Treatment
LUO Jiang-bin, WANG Tian-song, FANG Ming.
Department of Cardiology, People’s Hospital of Sanya, Sanya (572000), Hainan, China
Corresponding Author: WANG Tian-song, Email: wts0425@163.com
Objective: To assess the effect of coronary plaque composition on in-stent restenosis in patients after percutaneous coronary intervention (PCI) treatment by intravascular ultrasound-virtual histology (IVUS-VH).Methods: A total of 300 consecutive non-diabetic patients with the indication of elective PCI were studied. Before PCI, all culprit lesions were detected by IVUS and the plaque compositions obtained by VH software analysis. After PCI, all patients were followed-up for 1 year and examined by coronary angiography. The restenosis was defined as the reduction of lumen diameter≥50% at instent and at 5mm of near or remote sites of stent respectively. There were 8 patients lost contact and the rest 292 patients were divided into two groups as Non-restenosis group, n=245 and Restenosis group, n=47, the clinical characteristics and plaque compositions were compared between two groups.Results: The necrotic core in Restenosis group was higher than that in Non-restenosis group as (22.9±10.2)% vs. (14.7±6.9)%, P<0.05, and the calcification in Non-restenosis group was higher as (17.6±8.5)% vs. (10.2±6.8)%, P<0.05. There were significant differences in hs-CRP between two groups, P<0.05. Logistic multi-regression analysis presented that hs-CRP (OR= 1.24, 95% CI: 1.05~1.81, P=0.027)and the ratio of necrotic core (OR=1.18,95%CI:1.05~1.66,P=0.041)were the independent risk factors for restenosis in patients after PCI treatment.Conclusion: For culprit lesions, more necrotic core may cause higher incidence of in-stent restenosis, and inflammation is also an important risk factor for restenosis in patients after PCI.
Coronary plaque; Restenosis; Intravascular ultrasound-virtual histology
2012-06-28)
(编辑:梅平)
海南省自然科学基金资助项目(310184)
572000 海南省,三亚市人民医院 心内科(罗江宾、王天松 );同济大学附属东方医院 心内科(方明 )
罗江宾 副主任医师 学士 主要研究方向冠心病及介入治疗 Email:hn_ning@tom.com
王天松 Email:wts0425@163.com
R541.4
A
1000-3614(2013)03-0176-03
10.3969/j.issn.1000-3614.2013.03.006
方法:连续纳入 300 例具有择期 PCI指征的非糖尿病患者。在支架置入术前,对所有罪犯病变行血管内超声检查,并应用虚拟组织学软件分析斑块成份;随访 1 年,复查冠状动脉造影以支架内及支架近、远端 5 mm 血管狭窄≥ 50%为标准,将所有患者分为无再狭窄组和再狭窄组,比较两组间临床特征和斑块成份。
结果:两组间斑块成份比较,再狭窄组坏死组织比例较高 [(14.7±6.9)% vs (22.9±10.2)%, P<0.05];无再狭窄组钙化组织比例较高 [(17.6±8.5)% vs (10.2±6.8)%, P<0.05],差异均有统计学意义。两组间高敏 C 反应蛋白存在统计学差异(P<0.05);Logistic 多元分析显示, 高敏 C 反应蛋白 (比值比 =1.24,95%可信区间:1.05~1.81,P=0.027)和坏死核心成份比例 (比值比 =1.18,95%可信区间:1.05~1.66,P=0.041)是支架术后再狭窄的独立危险因素。
结论:罪犯病变中,坏死核心成份越大,支架术后再狭窄发生率越高。炎症是引起再狭窄的高危因素。
