镁掺杂对锰酸锂结构和性能的影响
2013-04-08付春明叶学海张晓波于晓微夏继平
付春明,叶学海,张晓波,于晓微,夏继平
(中海油天津化工研究设计院,天津 300131)
电池材料
镁掺杂对锰酸锂结构和性能的影响
付春明,叶学海,张晓波,于晓微,夏继平
(中海油天津化工研究设计院,天津 300131)
采用高温固相法合成不同镁元素掺杂量的尖晶石型锰酸锂。X射线衍射(XRD)表征结果表明,样品都具有尖晶石结构,无杂质相。扫描电镜(SEM)表征结果显示,掺杂前后所有样品的颗粒大小和形貌差别不大。对样品进行电化学性能测试,结果表明:当LiMgxMn2-xO4中镁的掺杂量x=0.09时,样品具有较佳的电化学性能,首次放电比容量为110.5 mA·h/g,在55℃1 C充放电循环50次后容量保持率为91.22%。
锰酸锂;镁;掺杂;电化学性能
锂离子二次电池正极材料锰酸锂具有原料资源丰富、价格低廉、无毒无污染等优点,因此成为被广泛看好的锂离子电池正极材料之一[1]。但是,由于锰溶解和姜-泰勒效应(Jahn-Teller effect)的存在,使其存在充放电循环中比容量下降快,尤其是高温性能差的问题[2-5],限制了其进一步的推广使用。目前,改善尖晶石型锰酸锂电化学性能的途径主要有离子掺杂改性[6-7]和表面包覆改性[8-9]两种。笔者采用氧化镁为镁源,对尖晶石型锰酸锂进行掺杂改性,以改善其高温循环性能。通过对合成材料的各项性能指标进行分析表征,研究了掺杂比例对改性尖晶石型锰酸锂结构和性能的影响。
1 实验部分
1.1 样品制备
采用高温固相法制备锂离子电池正极材料尖晶石型锰酸锂。按照化学计量比称取一定量电解二氧化锰、氢氧化锂和氧化镁进行配料,球磨6 h混匀后放入匣钵,在箱式电阻炉内升温至800℃焙烧18 h,然后自然冷却,产物经粉碎制得镁掺杂改性的尖晶石型锰酸锂正极材料。镁的掺杂量按照化学式LiMgxMn(2-x)O4(x=0.00、0.03、0.06、0.09、0.12)计算,按上述工艺制备不同镁掺杂量的样品。
1.2 模拟电池组装
将制得的锰酸锂正极材料与乙炔黑、聚偏氟乙烯(PVDF)按质量比为90∶5∶5配料,加入适量的有机溶剂N-甲基吡咯烷酮(NMP)调浆,混合均匀后涂布于铝箔上,烘干后冲片制得正极极片。采用金属锂片作对电极,聚丙烯微孔膜celgard2400为隔膜,LiPF6/碳酸乙烯酯(EC)+碳酸二甲酯(DMC)(EC与DMC的体积比为1∶1)为电解液,在手套箱内组装成CR2032扣式电池。
1.3 样品表征
采用D/Max-2500/PC型X射线衍射仪测试样品的结构组成。采用S-4800型冷场发射电子显微镜对样品进行颗粒形貌观察。采用蓝电(LAND)电池测试仪对电池进行充放电测试,充放电电压范围为3.0~4.3 V。采用PARSTAT 2273电化学工作站对扣式电池作循环伏安测试,循环电压为3.0~4.5 V,扫描速率为0.1mV/s。
2 结果与讨论
2.1 不同镁掺杂量对锰酸锂样品结构的影响
图1为5个不同镁掺杂量锰酸锂样品XRD谱图,图2是锰酸锂标准卡片(PDF#35-0782)。对照图2可以看出,所有样品的主要衍射峰都为纯相尖晶石结构的衍射峰,表明合成的产物均为尖晶石结构的锰酸锂。样品XRD谱图中没有发现镁化合物的衍射峰,不存在杂质相,说明镁离子完全掺杂进入锰酸锂晶体结构中,镁的掺杂并没有明显影响样品的尖晶石结构,起到了稳定材料结构的支撑作用。
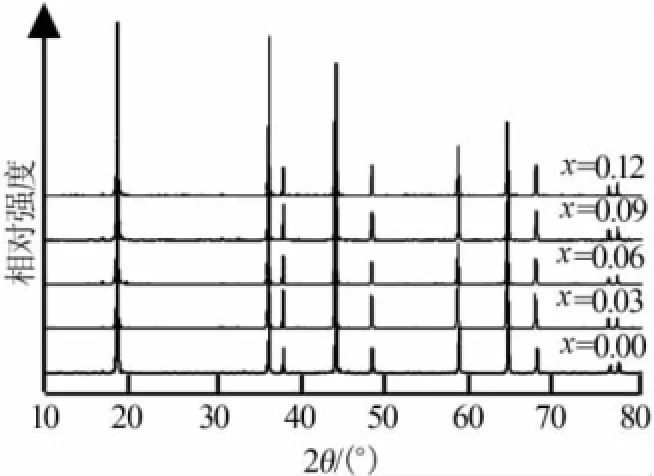
图1 不同镁掺杂量锰酸锂样品XRD谱图
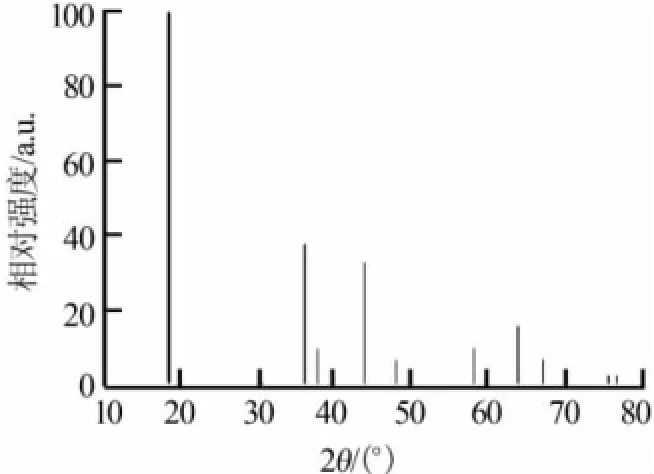
图2 锰酸锂标准XRD谱图(PDF-35-0782)
2.2 不同镁掺杂量对锰酸锂样品形貌的影响
图3为不同镁掺杂量锰酸锂样品SEM照片。从图3可以看出,掺入不同比例的镁元素,对尖晶石型锰酸锂颗粒的大小和形貌影响不大,均形状规整,表面平滑,颗粒大小较均匀。这是由于,样品中镁掺杂量不大,合成工艺一致,因此样品的颗粒大小和形貌基本没有差别,这与图1的XRD结果一致。
2.3 不同镁掺杂量对锰酸锂样品电化学性能的影响
2.3.1 不同镁掺杂量对样品初始放电比容量的影响

图3 不同镁掺杂量锰酸锂样品SEM照片
图4为不同镁掺杂量锰酸锂样品在55℃的首次放电曲线。由图4可知,当x=0.00、0.03、0.06、0.09、0.12时,样品的初始放电比容量分别为120.5、 117.2、114.8、110.5、104.0 mA·h/g,没有掺杂镁的样品放电比容量最高,随着镁掺杂量的增加,样品的初始放电比容量也随之降低。这是因为,Mg2+的价态低于纯相锰酸锂(LiMn2O4)中锰的平均价态(+3.5),进行镁掺杂以后,为维持LiMgxMn2-xO4的化合价平衡,锰的平均化合价必然升高,使部分Mn3+的价态升高变为Mn4+,这就减少了充电过程中Li+脱嵌时所必需的Mn3+→Mn4+反应,降低了脱锂量,充电比容量降低,放电比容量也随之降低。随着镁掺杂量的增加,锰酸锂中Mn3+的数量减少,因而样品的初始放电比容量也降低。
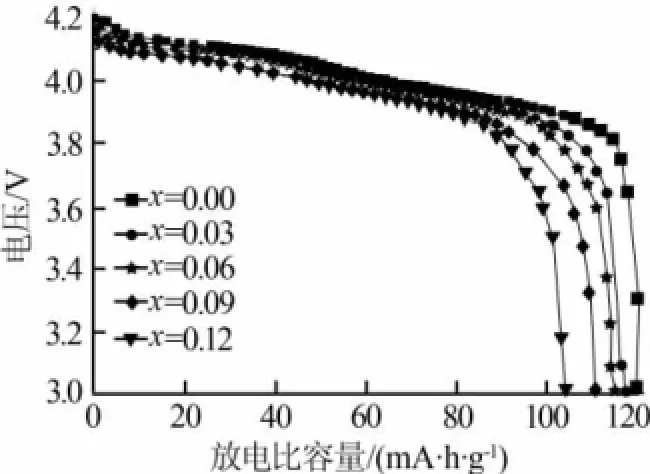
图4 不同镁掺杂量锰酸锂样品首次放电曲线
2.3.2 不同镁掺杂量对锰酸锂样品循环性能的影响
图5为不同镁掺杂量锰酸锂样品55℃循环性能曲线。由图5看出:未掺杂镁的样品(x=0.00)在55℃1C充放电循环50次后,比容量由120.5mA·h/g降至85.9 mA·h/g,容量保持率只有71.29%;当镁掺杂量x=0.03、0.06、0.09、0.12时,在55℃1 C充放电循环50次后,比容量分别由117.2、114.8、110.5、104.0 mA·h/g降至92.2、98.2、100.8、94.9 mA·h/g,容量保持率分别为78.67%、85.54%、91.22%、91.25%。可以看出,掺杂镁以后锰酸锂样品的循环性能较未掺镁的样品有显著提高。这可能是因为,掺杂镁以后,Mg2+取代了Mn3+,减少了活性离子Mn3+的数量,同时提高了锰离子的平均氧化态,而Mn4+的离子半径小于Mn3+,这样Mn—O键长变短,键能提高,使晶体的结构稳定性增强,抑制了Jahn-Teller效应,更有利于锂离子在晶格中的脱嵌,在充放电循环中不易发生晶格塌陷。因此在进行镁掺杂以后,样品的高温循环性能得到了明显提高。

图5 不同镁掺杂量锰酸锂样品循环性能曲线
虽然随着镁掺杂量的增加锰酸锂样品的循环性能越来越好,但同时也使得样品初始充放电比容量逐渐降低。对比各样品综合分析可知,当x=0.09,即按照化学式LiMg0.09Mn1.91O4配比时,制备的锰酸锂样品的电化学性能较优。
为进一步说明LiMg0.09Mn1.91O4优良的电化学性能,对样品做了循环伏安测试。图6为LiMg0.09Mn1.91O4在0.1 mV/s扫描速率下测得的第1次和第10次循环的循环伏安曲线。由图6看出,两次循环分别有两对氧化还原峰,对应于样品脱锂过程的两个充电平台和嵌锂过程的两个放电平台。两次扫描所得的循环伏安曲线的氧化峰和还原峰都是对称的,并且基本重叠,峰面积相当,说明样品LiMg0.09Mn1.91O4的电化学可逆性好,具有很好的循环性能。

图6 样品循环伏安曲线
3 结论
1)采用高温固相法合成了镁元素掺杂改性的尖晶石型锰酸锂。2)XRD表征结果表明,掺杂后的锰酸锂样品均为尖晶石结构,不存在杂质相。3)SEM照片显示,掺杂前后所有样品的颗粒大小和形貌基本没有差别,均形状规整。4)电化学测试结果表明,当镁掺杂量x=0.09时,样品具有较佳的电化学性能,首次放电比容量达到110.5 mA·h/g,在55℃1 C充放电循环50次后容量保持率为91.22%。
[1]Luo J Y,Li X L,Xia Y Y.Synthesis of highly crystalline spinel LiMn2O4by a soft chemical route and its electrochemical performance[J].Electrochem.Acta,2007,52:4525-4531.
[2]Xia Y,Zhou H,Yoshio M.Capacity fading on cycling of 4 V Li/LiMn2O4cells[J].J.Electrochem.Soc.,1997,144(8):2593-2600.
[3]Jang D H,Oh S M.Electrolyte effects on spinel dissolution and cathodic capacity losses in 4 V Li/LixMn2O4rechargeable cells[J].J. Electrochem.Soc.,1997,144(10):3342-3348.
[4]Pasquier A D,Blyr A,Courjal P,et al.Mechanism for limited 55℃storage performance of Li1.05Mn1.95O4electrodes[J].J.Electrochem. Soc.,1999,146(2):428-436.
[5]唐致远,李建刚,薛建军.锂电池正极材料LiMn2O4的改性与循环寿命[J].化学通报,2000,63(8):10-14.
[6]Wu X M,Chen S,He Z Q,et al.Solution-derived lithium manganese oxide thin films with silver additive and their characterization[J].Mater.Chem.Phys.,2007,101(1):217-220.
[7]Song D,Ikuta H,Uchida T,et al.The spinel phases LiA1yMn2-yO4(y=0,1/12,1/9,1/6,1/3)and Li(A1,M)l/6Mn11/6O4(M=Cr,Co)as the cathode for rechargeable lithium batteries[J].Solid Stale Ionics,1999,117:151-156.
[8]Gnanaraj J S,Pol V G,Gedanken A,et al.Improving the hightemperature performance of LiMn2O4spinel electrodes by coating the active mass with MgO via a sonochemical method[J].Electrochem.Commun.,2003,5(11):940-945.
[9]Lee S W,Kim K S,Moon H S,et al.Electrochemica1 characteristics of Al2O3-coated lithium manganese spinel as a cathode material for a lithium secondary battery[J].J.Power Sources,2004,126(1/2):150-155.
联系方式:chunmingsfu@163.com
Effects of Mg doping on structure and performance of lithium manganate
Fu Chunming,Ye Xuehai,Zhang Xiaobo,Yu Xiaowei,Xia Jiping
(CNOOC Tianjin Chemical Research&Design Institute,Tianjin 300131,China)
Spinel lithium manganate samples modified with different proportions of magnesium element were prepared by high temperature solid state reaction.The X-ray diffraction(XRD)analysis indicated that the samples were all spinel structure without impurity phase.The Scanning electron microscopy(SEM)results showed that the size and morphology of all the samples before and after doping made little difference.The results of charge-discharge test showed that the sample had better electrochemical properties when x=0.09 in LiMgxMn2-xO4.The initial discharge specific capacity was 110.5 mA·h/g,and the specific capacity retention was 91.22%after 50 cycles at 1C rate and 55℃.
lithium manganate;magnesium;doping;electrochemical properties
TQ131.11
A
1006-4990(2013)12-0057-03
2013-07-02
付春明(1981—),男,工程师,研究方向为锂离子电池材料,已发表论文1篇。
