间歇式泡沫分离法回收海水中硼的研究
2013-04-08关凤禹张永强
关凤禹,张永强
(1.燕山大学环境与化学工程学院,河北秦皇岛 066004;2.中国-阿拉伯化肥有限公司)
间歇式泡沫分离法回收海水中硼的研究
关凤禹1,2,张永强1
(1.燕山大学环境与化学工程学院,河北秦皇岛 066004;2.中国-阿拉伯化肥有限公司)
采用间歇式泡沫分离法研究了海水中硼的回收工艺。主要考察了表面活性剂种类及用量、溶液pH、气体流量等因素对海水中硼的分离性能的影响。实验结果表明:十二烷基三甲基氯化铵(DTAC)、十四烷基三甲基氯化铵(TTAC)、十六烷基三甲基氯化铵(CTAC)以及十八烷基三甲基氯化铵(OTAC)4种表面活性剂中CTAC对海水中硼的分离效果最好;随溶液pH的增加,硼的回收率和富集比均先增大后减小;随CTAC用量的增加,硼的回收率逐渐增大并趋于稳定,而富集比先增大后减小;随气体流量的增加,硼的回收率先增大后减小,而富集比则逐渐减小。在实验条件范围内,当CTAC质量浓度为0.2 g/L、溶液pH为9、气体流量为200 mL/min时,硼的回收率达到90%,富集比达到8。
泡沫分离法;回收;海水;硼;十六烷基三甲基氯化铵
硼及其化合物在冶金、建材、核工业、纺织印染、环境保护等领域应用广泛,而且是动植物及人体必需的微量元素。近年来,随着硼矿物资源的减少,对于从海水、盐湖水等含硼水资源中分离硼的研究逐渐引起人们的广泛关注。王路明[1]、袁建军[2]、周磊[3]等采用氢氧化镁吸附法研究了海水镁砂生产过程中除硼的工艺;闫春燕等[4]采用活性炭吸附海水中的硼;N.Geffen等[5]采用甘露醇作为络合剂与海水中的硼形成络合物并结合反渗透法分离海水中的硼;张金才等[6]综述了盐湖卤水提取硼的方法,主要有酸化法、萃取法、沉淀法以及结晶法等;P.Remy等[7]采用氢氧化钙为沉淀剂从废水中沉淀回收硼。对于从海水中提取分离微量硼,泡沫分离法是一种较为可行的方案。泡沫分离(foam separation)又称泡沫吸附分离(foam adsorbent separation),是根据表面吸附的原理,即表面活性物质优先吸附和浓集在气液界面处,通过向溶液鼓泡并形成泡沫层,使泡沫层与液相主体分离[8]。泡沫分离法的研究较为活跃,其中关于无机阴离子分离提取领域的应用报道不多[9-15]。笔者采用间歇式泡沫分离法,以阳离子表面活性剂十六烷基三甲基氯化铵为起泡剂,研究了回收海水中微量硼的分离性能。
1 实验材料与方法
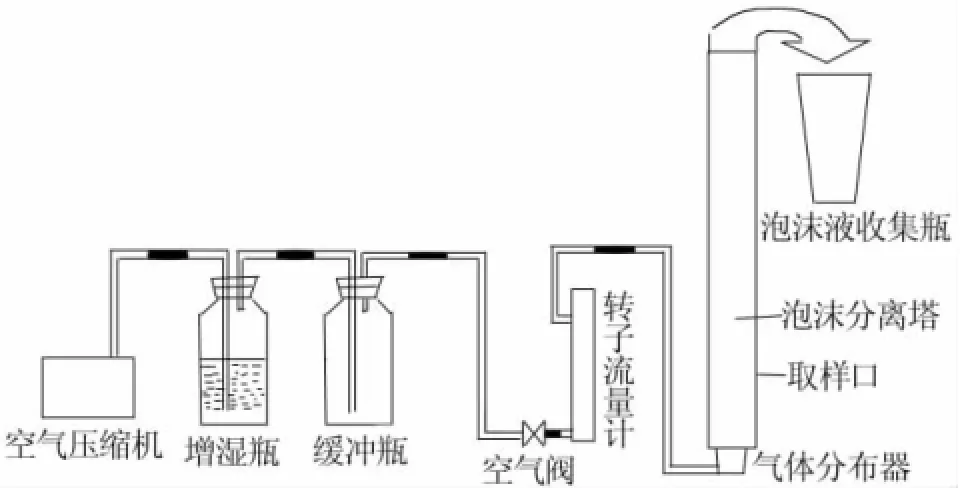
图1 间歇泡沫分离实验装置
实验装置采用间歇式泡沫分离装置,如图1所示。气体由空气压缩机提供,通过增湿瓶、缓冲瓶、转子流量计经由泡沫塔底部的气体分布器分散到塔中,泡沫相经塔顶部的弯头溢出并进入收集器,泡沫经破碎后形成泡沫液。泡沫塔内径为30 mm,塔高为1 000 mm。用于分离的溶液为过滤后的渤海海水,加料量为500 mL,用NaOH调整海水pH。实验进行到塔中无泡沫排出时结束,关闭空气压缩机,将转子流量计调为零,打开排气阀门放空。记录最终液面高度。将塔中剩余海水和泡沫液分别取样至具塞瓶中,采用紫外可见分光光度法测定硼的浓度[16]。
2 实验结果与讨论
2.1 表面活性剂种类对硼回收率和富集比的影响
海水为弱碱性介质,在此条件下硼主要以B(OH)4-络阴离子形式存在于海水中,因此选用季铵盐型阳离子表面活性剂作为起泡剂。备选表面活性剂主要有十二烷基三甲基氯化铵(DTAC)、十四烷基三甲基氯化铵(TTAC)、十六烷基三甲基氯化铵(CTAC)以及十八烷基三甲基氯化铵(OTAC)。表面活性剂种类对硼回收率和富集比的影响见图2。由图2可以看出,CTAC和OTAC的分离效果相当,均优于其他两种表面活性剂,表明随着碳链长度的增加,硼在气泡上的吸附随之增加,从而提高分离效果。但是,富集比随着碳链长度的增加而减小,表明随着碳链长度的增加,泡沫稳定性增强,泡沫相排液量逐渐减少,从而使富集比减小。综合考虑上述两种因素,选用CTAC作为起泡剂。

图2 表面活性剂种类对硼回收率和富集比的影响
2.2 海水pH对硼回收率和富集比的影响
图3为海水pH对硼回收率和富集比的影响。由图3可以看出,当初始海水pH由7上升至11时,硼的回收率和富集比的变化规律相同,均是先增大后减小,并且均在pH为9时达到最大值,表明溶液pH对泡沫分离硼的影响较大。硼在海水中存在以下动态平衡:
H3BO3+2H2O⇌B(OH)4-+H3O+
在pH较低时,硼主要以硼酸分子形态存在,其与阳离子表面活性剂结合能力较弱,故回收率不高。随着溶液pH增大,平衡向右移动,四羟基硼络阴离子逐渐增多,与CTAC阳离子的络合能力增强,硼回收率逐渐升高。然而,当pH过高时,溶液中的OH-含量高,OH-与B(OH)4-竞争在气-液吸附界面上的位置,不利于硼的吸附,导致硼回收率下降。由于所加入的表面活性剂的量相同,泡沫相体积也基本相同,所以富集比与回收率的变化趋势一致。

图3 pH对硼回收率和富集比的影响
2.3 表面活性剂质量浓度对硼回收率和富集比的影响
图4为CTAC质量浓度对硼回收率和富集比的影响。由图4可以看出,随着表面活性剂质量浓度由0.1 g/L增加到0.5 g/L,富集比先增大后逐渐减小,而回收率则逐渐增大并趋于稳定。这主要是因为,当表面活性剂质量浓度较小时,产生的泡沫量少,所吸附的硼就少,并且泡沫的稳定性较差,导致富集比较小;随着表面活性剂质量浓度的增大,所生成的泡沫量也随之增加,吸附的硼量也逐渐增加,富集比增大;但是,随着表面活性剂质量浓度的进一步增大,破沫后的液体体积量也增加,从而导致富集比又逐渐降低。同时,随着表面活性剂质量浓度的增加,增加了表面活性剂对硼的结合与吸附的机率,而且所生成的泡沫的稳定性也随之增强,因此回收率逐渐增加;然而,当表面活性剂的用量增加到一定程度时,其在气液界面处的吸附量也将达到饱和,故再增加表面活性剂的量并不会增大吸附量,故回收率基本保持恒定。

图4 CTAC质量浓度对硼回收率和富集比的影响
2.4 空气流量对硼回收率和富集比的影响
图5为空气流量对硼回收率和富集比的影响。由图5可以看出,随着空气流量由100 mL/min增加到500 mL/min,硼的回收率先增加后减少,而富集比则逐渐减小。这是因为,当气体流量较低时,所形成的气泡体积小,比表面较大,并且在溶液中的停留时间较长,使CTAC所电离的阳离子与硼的结合更充分,并在气液界面的吸附传质更充分,因此富集比较高;随着气体流量的增大,虽然较易形成气泡,但气泡在溶液中的停留时间缩短,气、液两相传质不充分,因此富集比逐渐降低。当气体流量较低时,由于小的气速降低了泡沫的间隙水量,泡沫相体积很小,所以硼回收率很少;随着气体流量的增加,泡沫所夹带的间隙水量增加,所以硼回收率逐渐增加,当气速增加到200 mL/min时,硼回收率达到最大值;再继续增加气速,回收率逐渐降低。这是因为,随着气速的增加,在逆流接触的气-液传质分离设备中,液体受到的阻力过大,返混程度增大,因此出现回收率下降的情况。气体流量较小时,气泡在溶液中的停留时间长,气液界面传质充分,泡沫夹液量较少,因此富集比较大。在气体流量较大时,较易形成气泡,但气泡在溶液中的停留时间较短,气、液两相传质不充分,泡沫层上升速度加快,这些因素都会使泡沫的夹液量变大,富集比逐渐下降。

图5 空气流量对硼回收率和富集比的影响
3 结论
泡沫分离法是一种新型绿色分离技术,具有工艺流程短、操作难度低、设备投资少等优点,其主要能耗来自于气液输送过程的动力消耗,目前还处于试验研究阶段,对于低浓度溶质的分离回收具有潜在的应用价值。笔者对海水脱硼工艺进行了初步研究,取得了较好的实验结果。在适宜条件下,硼的回收率最高达到90%,富集比最高达到8。
[1]王路明.Mg(OH)2对海水中硼的吸附效果[J].海湖盐与化工,2003,32(5):5-7.
[2]袁建军,崔蕊,张勇.海水氢氧化镁对硼的吸附及卤水降硼的研究[J].盐业与化工,2007,36(1):1-3.
[3]周磊,衣守志,潘娟,等.海水预处理氢氧化镁浆料制备及对硼吸附研究[J].盐业与化工,2011,40(6):18-21.
[4]闫春燕,伊文涛,邓小川,等.活性炭对海水中硼的吸附研究[J].无机盐工业,2007,39(3):34-36.
[5]Geffen N,Semiat R,Eisen M S,et al.Boron removal from water by complexationtopolyolcompounds[J].J.Membr.Sci.,2006,286(1/2):45-51.
[6]张金才,王敏.盐湖卤水提硼方法的研究概述[J].化工矿物与加工,2005,34(5):5-7.
[7]Remy P,Muhr H,Plasari E,et al.Removal of boron from wastewater by precipitation of a sparingly soluble salt[J].Environ.Prog.,2005,24(1):105-110.
[8]常志东,刘会洲,陈家镛.泡沫分离法的应用与发展[J].化工进展,1999,18(5):18-21.
[9]宋伟光,吴兆亮,卢珂,等.泡沫分离除去水溶液中微量硫酸根离子[J].过程工程学报,2008,8(3):489-493.
[10]A·A·克列米亚托夫.用泡沫浮选萃取法从废液中回收钼[J].国外金属矿选矿,2007,44(7):28-30.
[11]Kinoshita T,Ishigaki Y,Yamaguchi K,et al.Novel operational method of continuous foam separation of gold-Injection of metal and/or surfactant solutions into rising foam bed[J].Sep.Purif. Technol.,2006,52(2):357-362.
[12]Qu Yunhuan,Zeng Guangming,Huang Jinhui,et al.Recovery of surfactant SDS and Cd2+from permeate in MEUF using a continuous foam fractionator[J].J.Hazard.Mater.,2008,155(1/2):32-38.
[13]Zhang Jian,Jing Yingjun,Wu Zhaoliang,et al.Removal of trace Cu2+from aqueous solution by foam fractionation[J].Desalination,2009,249(2):503-506.
[14]Rujirawanich V,Chavadej S,O′Haver J H,et al.Removal of trace Cd2+using continuous multistage ion foam fractionation:PartⅠ-The effect of feed SDS/Cd molar ratio[J].J.Hazard.Mater.,2010,182(1/2/3):812-819.
[15]矫彩山,丁岩.泡沫分离法处理含Cr6+废水[J].化工环保,2008,28(1):20-23.
[16]黄运显,孙维贞.常见元素化学分析方法[M].北京:化学工业出版社,2008:42-43.
联系方式:zhangyongqiang4@163.com
Study on recovering boron from seawater by batch foam fractionation method
Guan Fengyu1,2,Zhang Yongqiang1
(1.School of Environmental and Chemical Engineering,Yanshan University,Qinhuangdao 066004,China;2.Sino-Arab Chemical Fertilizers Co.,Ltd.)
The process for recovering boron from seawater was studied by batch foam fractionation method.The influences of type and concentration of surfactants,initial pH,and air flow etc.on separation performance of the boron in seawater were investigated.The experimental results showed that CTAC was of the best separation characteristics among DTAC,TTAC,CTAC,and OTAC four surfactants.The recovery and enrichment ratio of boron both increased firstly and then decreased with the increase of the solution pH;The recovery of boron increased gradually at first and then tended to be stable,whereas the enrichment ratio increased firstly and then decreased,with the increase of concentration of CTAC;the recovery ratio increased firstly and then decreased,and enrichment ratio decreased gradually with the increase of air flow.When CTAC was as surfactant,pH=9,mass concentration of CTAC was 0.2 g/L,and air flow rate was 200 mL/min,recovery and enrichment ratio of boron were 90%and 8,respectively.
foam fractionation method;recovery;seawater;boron;CTAC
TQ128.1
A
1006-4990(2013)12-0024-03
2013-06-18
关凤禹(1977—),男,燕山大学环境与化学工程学院工程硕士,中国-阿拉伯化肥有限公司技术开发部研发工程师。
张永强
