例析注射器在中学化学实验改进中的妙用
2013-03-15张正飞
张正飞
(淮安中学 江苏 淮安 223200)
一、探究稀硝酸与铜的反应实验改进方案
稀硝酸与铜反应往往因为空气的影响而无法观察到产生NO 的现象,利用注射器进行实验改进后就可以进行实验现象的观察,实验改进方案如下:
1.实验用品
一次性小注射器、镊子、烧杯、试管、稀硝酸、铜片(细条状)、热水。
2.实验步骤及现象
(1)如(图1)所示取一支小注射器,取下活塞,装入铜片(细条状),然后再装好活塞;
(2)在小试管中加入稀硝酸,用注射器吸入一定量的稀硝酸,翻转注射器将空气排尽;
(3)将注射器放入热水浴中加热,开始时反应缓慢,后逐渐加快,并看到有无色气体产生,溶液变蓝,生成的气体将硝酸从注射器中逐渐排出,当完全排出后反应立即停止。
(4)拉动活塞吸入少量空气,发现注射器中的无色气体逐渐变为红棕色,说明反应生成的一氧化氮转化为二氧化氮。

图1
3.实验优点
本实验属于微型实验,操作简便,药品用量少,生成无色一氧化氮气体现象明显,成功地将一氧化氮气体转化成二氧化氮气体;控制了较多量的一氧化氮生成,有效地防止了一氧化氮气体对空气的污染,有助于同学们增强环保意识。
二、验证卤素单质间的置换反应
1.实验用品
注射器、氯气、KI 溶液、NaBr 溶液。
2.实验步骤及现象:
(1)如(图2)所示,先用注射器抽取10mL 左右的氯气 (上课前预先准备好);
(2)再抽取几滴NaBr 溶液,摇晃几下注射器(现象:在注射器壁上出现橙红色的溴单质,几秒钟后溴就挥发,橙红色的溴蒸气充满了整个针筒空间);
(3)再抽取几滴KI 溶液,充分接触(现象:橙红色的溴蒸气消失,针筒壁上出现紫黑色的固体),再用强光照射注射器壁,碘单质就升华成紫色的气体。
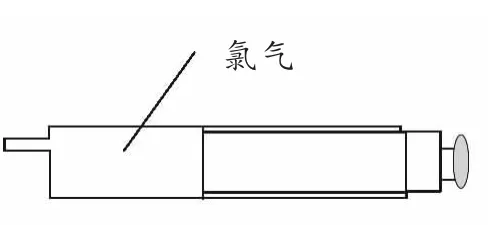
图2
3.实验优点
药品用量少,现象非常直观,对比鲜明;反应器相对封闭,这样基本做到无污染,环保效果好。本实验利用氯水和溴水易挥发的性质,使学生更好地理解了Cl2、Br2、I2单质之间的相互置换反应及Br2、I2的特性。
三、验证温度和压强对化学平衡的影响实验改进方案
1.实验用品
带针头的注射器 橡胶塞 冰水 热水 浓硝酸 铜片
2.实验步骤及现象
(1)将一小片金属铜放入注射器内,塞上注射器活塞,吸入适量浓硝酸,将针头插入橡胶塞中密封;
(2)待注射器内产生约5 毫升NO2后,取下橡胶塞,挤尽浓硝酸,再将针头插入橡胶塞中密封;
(3)向内推进活塞或向外抽出活塞,验证压强对化学平衡移动的影响;
(4)将装置分别放入冰水或热水中,验证温度对化学平衡移动的影响。
3.实验优点
这是一个集NO2的制备和温度、压强对化学平衡的影响为一体的综合实验方案,操作简单,现象明显,药品用量少,污染小。
四、Fe(OH)2 的制备实验
Fe(OH)2的制备过程中往往难避开空气的影响,不容易观察到Fe(OH)2的颜色,利用注射器进行Fe(OH)2的制备实验的改进后就可以避开空气的影响,使Fe(OH)2的颜色能保持较长时间,改进方案如下:
1.实验用品
带针头的注射器,橡胶塞,稀硫酸,铁片,蒸馏水,氢氧化钠溶液。
2.实验步骤及现象
(1)将一小片金属铁放入注射器内,塞上注射器活塞,吸入少量煮沸过后的蒸馏水,以排出注射器内的空气。
(2)吸入适量稀硫酸(注意:注射器内不能有气泡),将针头插入橡胶塞内,如(图3),以保证注射器的密封,观察现象。(现象:注射器内产生无色气泡,活塞向右移动)
(3)取下橡胶塞,吸入适量的NaOH 溶液,观察现象。
3.方案优点
该方案利用铁与稀硫酸现制Fe2+,并利用蒸馏水和产生的H2排出空气,并使实验在H2中进行,可以实现整个操作在在隔绝空气的条件下进行。
总之,由于注射器具有体积小、密封性强、可伸缩性、安全可靠、操作简便、污染少、实验现象明显等优点,在与常规仪器及微型实验仪器配套应用的基础上,在制气、收集、尾气处理、家庭实验、微型实验等各实验环节中都能发挥积极作用,真正做到了一器多用,它的灵活运用使中学化学实验变得更完美,也培养了学生自主探究能力。

图3
[1] 王祖浩.普通高中课程标准实验教科书《化学1》[M].南京.江苏教育出版社,2012:100
[2] 张正飞,柏书梅.利用胶头滴管演示铜与硝酸的反应[J].化学教学,2010,(2):8
[3] 柏书梅.电解食盐水实验的创新设计[J].化学教与学,2011,(10):86
