2,5-二亚苄基环戊酮衍生物的合成及抑制K562 细胞生长活性
2013-03-08董金华
梁 琳,刘 红 ,马 娟,董金华
(1. 沈阳药科大学 基于靶点的药物设计与研究教育部重点实验室,辽宁 沈阳110016;2. 佳木斯大学 研究生学院,黑龙江 佳木斯154007;3. 广东食品药品职业学院 制药系,广东 广州510520)
姜黄素(curcumin)是从姜黄(Curcuma longaLinn,Turmeric)中提取的酚性化合物,具有抗氧化、抗肿瘤、降血脂、降血糖、抗溃疡、抗心肌缺血、抗抑郁、抗菌、消炎、抗病毒和肝肾保护等作用,可用于治疗癌症、糖尿病、冠心病、关节炎、阿尔茨海默氏病以及其他慢性疾病[1-4]。然而,姜黄素水溶性差、体内吸收少、生物利用度低、代谢过快,导致其临床应用受到了极大的限制[5-6]。研究表明,姜黄素结构中的β-二酮片段为肝组织中醛酮还原酶的底物,因而致使姜黄素在体内代谢过快[7];鉴于此,从增加代谢稳定性的角度出发,近十多年,国内外科研工作者设计、合成了许多单羰基姜黄素类似物,发现了EF24 等具有显著抗癌活性的化合物[8-12]。

Figure 1 Structures of curcumin and EF24
单羰基姜黄素类似物与2-(E)-亚芳基环酮Mannich 碱类化合物结构相似[13-14],生物活性也相近。两类化合物均含有芳基α,β-不饱和羰基结构片段(Michael 受体),且都有抗癌、抗炎等作用。本文的研究中,作者沿用环酮Mannich 碱类化合物的修饰方法,在单羰基姜黄素类似物结构中引入亲水性的胺类基团,合成了15 个未见文献报道的化合物,并初步考察了目标化合物体外对K562 细胞增殖的抑制作用。目标化合物的合成路线如图2 所示。

Figure 2 The synthetic route to the target compounds
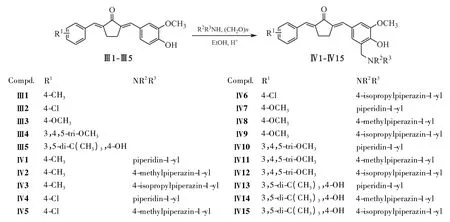
Continued Figure 2
1 合成实验
熔点采用Yanaco 显微熔点测定仪测定(温度未经校正);核磁共振氢谱采用Brucker ARX -500 型核磁共振仪测定(DMSO-d6或CDCl3为溶剂,TMS 为内标);质谱采用Agilent 6890N -5975iGC 质谱仪测定。薄层色谱用硅胶GF254、柱色谱用硅胶均为青岛海洋化工厂生产。所用原料和试剂均为市售分析纯。
中间体2-(E)-(3-甲氧基-4-羟基)亚苄基环戊酮(Ⅱ)按文献[13]方法合成。
1.1 2-(E),5-(E)-二取代亚苄基环戊酮(Ⅲ1 ~Ⅲ5)的合成通法
将20 mmol 2-(E)-(3-甲氧基-4-羟基)亚苄基环戊酮(Ⅱ)、25 mmol 取代苯甲醛置于反应瓶中,加入无水乙醚50 mL、氯仿20 mL,室温下搅拌至反应物全部溶解,向反应液中滴加饱和氯化氢乙醚溶液20 mL,继续搅拌12 h。抽滤,水洗滤饼,干燥得固体。
1.2 2-(E),5-(E)-二取代亚苄基环戊酮曼尼希碱衍生物(Ⅳ1 ~Ⅳ15)的合成通法
将2-(E),5-(E)-二取代亚苄基环戊酮1.0 mmol(Ⅲ)、仲胺3.0 mmol 溶于30 mL 无水乙醇中,加多聚甲醛0.22 g,用浓盐酸调pH =4,加热回流2 h 后,补加多聚甲醛0.1 g,继续回流4 ~8 h。冷却,抽滤,水洗滤饼,干燥。经硅胶柱色谱分离纯化(洗脱剂为二氯甲烷-甲醇),得到目标化合物。
合成的中间体及目标化合物经波谱测试确证结构,理化数据见表1。

Table 1 The spectral and experimental data of the target compounds
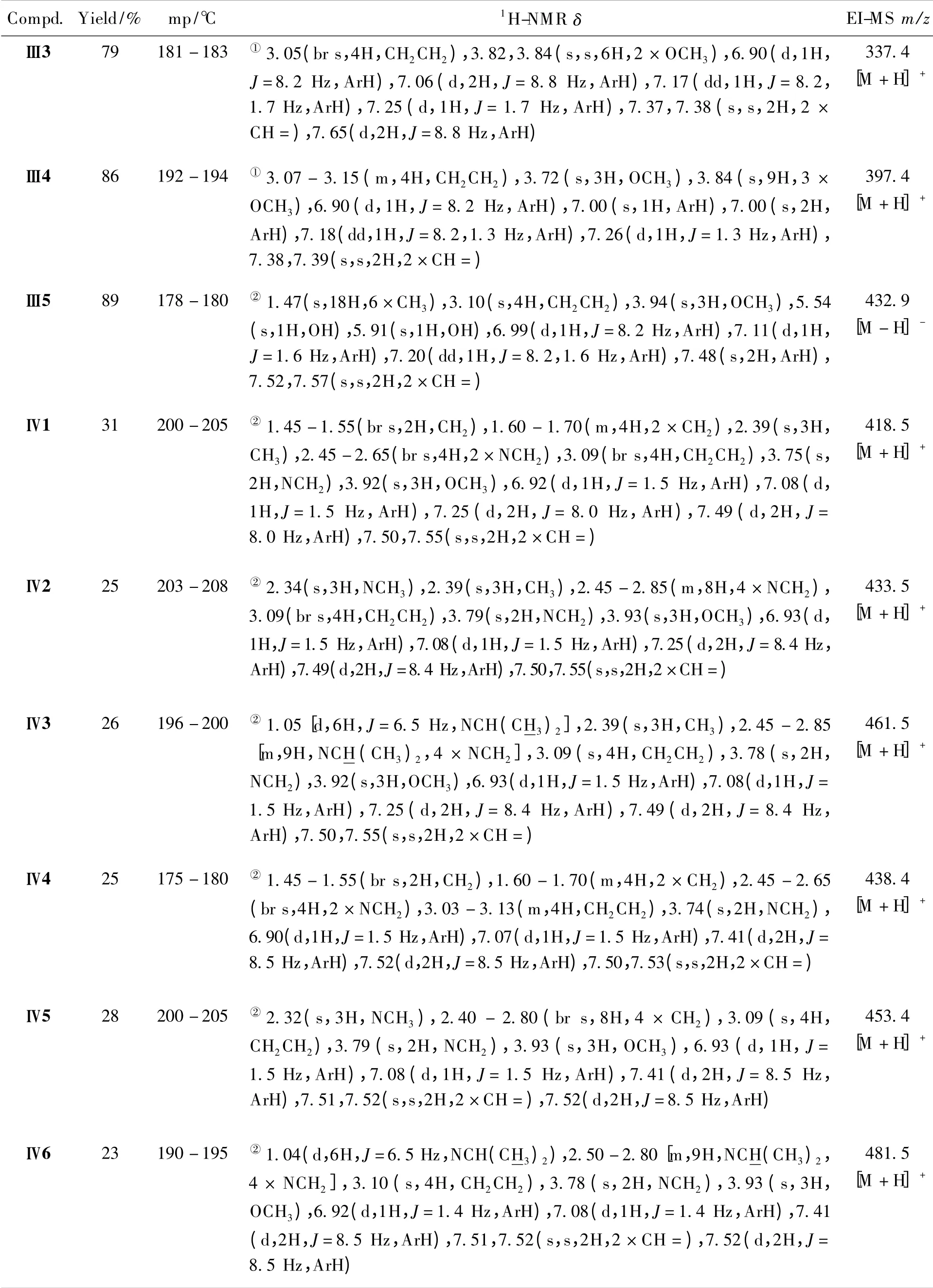
Continued Table 1
2 体外抑制K562 细胞增殖活性筛选
将人类慢性粒细胞白血病急变细胞株K562细胞培养于添加10% (体积分数)小牛血清的RPMI 1640 培养液中,于37 ℃、体积分数为5%的CO2饱和湿度培养箱中培养。取对数生长期细胞用于抑制率测定实验,接种细胞浓度为每毫升1 ×105个。
将处于对数生长期的细胞,按一定密度接种于96 孔板中。实验组分别加入不同浓度的受试药物,对照组加含等量浓度的DMSO 无血清培养液,空白对照组为190 μL RPMI 1640 加10 μL 无药溶剂。每组设3 个平行孔,37 ℃培养48 h。加入5 g·L-1的MTT 溶液,每孔20 μL,继续培养4 h。离心弃上清液,加入150 μL DMSO,振荡10 min,充分裂解后,用全自动酶标仪(美国BIORAD 公司生产)于570 nm 处检测吸光度(OD)值。按下式计算细胞生长抑制率。
抑制率% =(1 -药物处理孔平均OD 值/细胞对照孔平均OD 值) ×100%。
以同一药物的不同浓度对肿瘤细胞生长抑制率作图,根据线性回归方程求出该药物对细胞生长抑制率为50%的浓度,即半数抑制浓度IC50。
姜黄素及目标化合物对K562 细胞的IC50值见表2。

Table 2 Antiproliferative effect of the compounds against K562 cells
3 结果与讨论
合成中间体2,5-二取代亚苄基环戊酮时,鉴于取代苯甲醛碱性条件下易发生自身歧化,实验中改用酸催化,得到的产物单一且收率较高。
药理研究结果显示:中间体Ⅲ1 ~Ⅲ5 与姜黄素的活性差别不大,含有3,4,5-三甲氧基苯基、3,5-二叔丁基-4-羟基苯基结构片段的Ⅲ4、Ⅲ5 活性略高于姜黄素。目标化合物Mannich 碱的活性存在显著的差异:由吗啉衍生的化合物Ⅳ1、Ⅳ4、Ⅳ7、Ⅳ10 活性显著低于对应的中间体;而由甲基哌嗪、异丙基哌嗪衍生的化合物除Ⅳ2 外,活性均比中间体强。
[1] AGGARWAL B B,KUMAR A,BHARTI A C.Anticancer potential of curcumin:preclinical and clinical studies[J]. Anticancer Res,2003,23(1A):363 -398.
[2] AGGARWAL B B. Targeting inflammation-induced obesity and metabolic diseases by curcumin and other nutraceuticals[J]. Annu Rev Nutr,2010,30(1):173 -199.
[3] MARATHE S A,DATEY A A,CHAKRAVORTTY D.Herbal cocktail as anti-infective:promising therapeutic for the treatment of viral diseases[J]. Recent Pat Antiinfect Drug Discov,2012,7(2):123 -132.
[4] VENKATESAN N,PUNITHAVATHI D,ARUMUGAM V. Curcumin prevents adriamycin nephrotoxicity in rats[J]. Br J Pharmacol,2000,129(2):231 -234.
[5] WAHLSTROM B,BLENNOW G. A study on the fate of curcumin in the rat[J].Acta Pharmacol Toxicol,1978,43(2):86 -92.
[6] RAVINDRANATH V,CHANDRASEKHARA N.Absorption and tissue distribution of curcumin in rats[J].Toxicology,1980,16(3):259 -265.
[7] ROSEMOND M J,St JOHN-WILLIAMS L,YAMA GUCHI T,et al.Enzymology of a carbonyl reduction clearance pathway for HIV integrase inhibitor,S-1360:role of human liver cytosolic aldo-keto reductases[J]. Chem Biol Interact,2004,147(2):129 -139.
[8] DIMMOCK J R,JHA AZELLO G A,QUAIL J W,et al.CytotoxicN-[4-(3-aryl-3-oxo-l-propenyl)phenylcarbonyl]-3,5-bis (phenylmethylene)-4-piperidones and related compounds[J].Eur J Med Chem,2002,37(12):961 -972.
[9] ADAMS B K,FERSTL E M,DAVIS M C,et al.Synthesis and biological evaluation of novel curcumin analogs as anti-cancer and anti-angiogenesis agents[J].Bioorg Med Chem,2004,12(14):3871 -3883.
[10] JIANG Y F,DU Z Y,XUE G H,et al.Synthesis and biological evaluation of unsymmetrical curcumin analogues as tyrosinase inhibitors[J]. Molecules,2013,18(2):3948 -3961.
[11] XU Y Y,CAO Y,MA H K,et al. Design,synthesis and molecular docking of α,β-unsaturated cyclohexanone analogous of curcumin as potent EGFR inhibitors with antiproliferative activity[J]. Bioorg Med Chem,2013,21(1):388 -394.
[12] MANOHAR S,KHAN S I,KANDI S K,et al.Syn
thesis,antimalarial activity and cytotoxic potential of new monocarbonyl analogues of curcumin[J].Bioorg Med Chem Lett,2013,23(1):112 -116.
[13] DONG J H,XU L Y,QIN H,et al.Synthesis and antiinflammatory activity of 2-(E)-(4-hydroxy-3-methoxy benzylidene)-5-(N-substituted aminomethyl)cyclopentanones[J].J Chin Pharm Sci,1998,7(4):186 -190.
[14] 徐莉英,唐虹,董金华,等.2-甲基-5-(E)-(邻甲氧基苯亚甲基)环戊酮Mannich 碱的合成及其抗癌抗炎活性研究[J].中国药物化学杂志,2002,12(1):1-4.