花期对益母草药材中盐酸水苏碱和盐酸益母草碱含量的影响
2013-03-06黄健浙江省新昌县人民医院浙江新昌312500
黄健(浙江省新昌县人民医院,浙江 新昌 312500)
花期对益母草药材中盐酸水苏碱和盐酸益母草碱含量的影响
黄健(浙江省新昌县人民医院,浙江 新昌 312500)
目的 研究开花对益母草药材中盐酸水苏碱和盐酸益母草碱含量的影响。方法 在同一地区不同时期采收益母草药材样品,按照药典方法对其中的盐酸水苏碱和盐酸益母草碱含量进行测定,纵向比较。结果 开花过程中益母草药材中盐酸水苏碱及盐酸益母草碱的含量不断降低。结论 开花对益母草药材中盐酸水苏碱及益母草碱含量影响较大,花后期因益母草碱不达标不建议使用。
益母草;盐酸水苏碱;盐酸益母草碱;药材质量
益母草为唇形科植物益母草Leonurus japonicus Houtt.的新鲜或干燥地上部分。鲜品春季幼苗期至初夏花前期采割;干品夏季茎叶茂盛、花未开或初开时采割,晒干,或切段晒干[1]。益母草的药用有效成分是生物碱,现已知有水苏碱、益母草碱等多种生物碱[2]。水苏碱是中药益母草中的主要有效成分之一,具有多方面的生理活性:能提高冠状动脉和心肌营养性血流量、减少心肌细胞坏死、降低血管阻力、改善微循环,减慢心率、减少心输出量等作用[3];能抑制乳腺癌和子宫肌腺病的发生[4];具有祛痰、镇咳、松弛支气管平滑肌的作用[5]。益母草碱能够抑制血小板的聚集,防止血栓形成。笔者对不同生长期益母草中水苏碱和益母草碱进行含量测定,纵向比较其含量变化,论证药典中益母草的采收期是否合理。
1 材料
1.1 仪器
岛津LC-15C高效液相色谱仪(日本岛津);Alltech 3300 ELAD蒸发光检测器(美国奥泰科技有限公司);BT125D电子天平(塞多利斯科学仪器北京有限公司);AL104电子天平(梅特勒-托利多仪器上海有限公司)。
1.2 对照品
盐酸水苏碱 (中国药品生物制品检定所,批号:110712-201111,含量:99.60%,使用前五氧化二磷减压干燥12 h);盐酸益母草碱(中国药品生物制品检定所,批号:110736-201111,含量:99.60%,使用前五氧化二磷减压干燥12 h)。
1.3 样品
本试验所用益母草样品均为笔者在不同时期采自浙江省新昌县同一群落。经陈宗良副主任中药师鉴定为唇形科植物益母草Leonurus japonicas Houtt.的地上部分。样品1:2012年4月1日采收干燥,此时益母草生长较旺盛期,习称童子益母草;样品2:2012年5月6日采收干燥,此时益母草处于花前期,花苞小部分形成;样品3:2012年6月1日采收干燥,此时益母草处于花中期,花部分开发;样品4:2012年7月10日采收干燥,此时益母草处于花后期,花全部凋谢。
2 方法与结果
2.1 盐酸水苏碱的含量测定[6-7]
2.1.1 色谱条件 色谱柱:Venvsil 100A C18柱(4.6 mm×250 mm,5 μm);蒸发光散射检测器(空气流速:1.6 L·min-1,漂移管温度:48.0 ℃);流动相:乙腈-0.2%冰醋酸溶液(80∶20);流速:1.0 mL·min-1;理论板数按盐酸水苏碱峰计算应≥6 000。
2.1.2 对照品溶液的制备 取盐酸水苏碱对照品10.39 mg,置25 mL量瓶中,加70%乙醇溶液至刻度,摇匀,制成每1 mL含0.413 9 mg的溶液,即得。
2.1.3 供试品溶液的制备 取本品1 g,精密称定,置具塞锥形瓶中,精密加入70%乙醇溶液25 mL,称定重量,加热回流2 h,放冷,再称定重量,用70%乙醇溶液补足减失的重量,摇匀,滤过,取滤液,即得。
2.1.4 线性范围 精密吸取对照品溶液5,10,15,20,25 μL分别注入高效液相色谱仪,按“2.1.1”项下色谱条件测定,以进样量的对数为横坐标,峰面积对数为纵坐标,进行线性回归,得回归线方程Y=1.658 4X-5.401 5,r=0.996 5。表明进样量在2.07~10.35 μg内线性关系良好。
2.1.5 仪器精密度试验 精密吸取对照品溶液10 μL,按“2.1.1”项下色谱条件测定,重复进样5次,结果盐酸水苏碱峰面积RSD为0.8%,表明仪器精密度良好。
2.1.6 稳定性试验 取上述供试品溶液,在0,3,6,12,15 h分别进样10 μL进行测定,结果盐酸水苏碱峰面积RSD为1.3%,表明该方法15 h内稳定性良好。
2.1.7 重复性试验 取同一采收时期样品5份,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件测定,结果RSD为1.0%,表明该方法重复性良好。
2.1.8 回收率试验 精密称取益母草样品(含量2.34%)6份,各约0.2 g,分别精密加入盐酸水苏碱对照品适量,按“2.1.3”项下方法制备供试品溶液并进行测定,结果平均回收率为97.9%,RSD=1.0%,见表1。
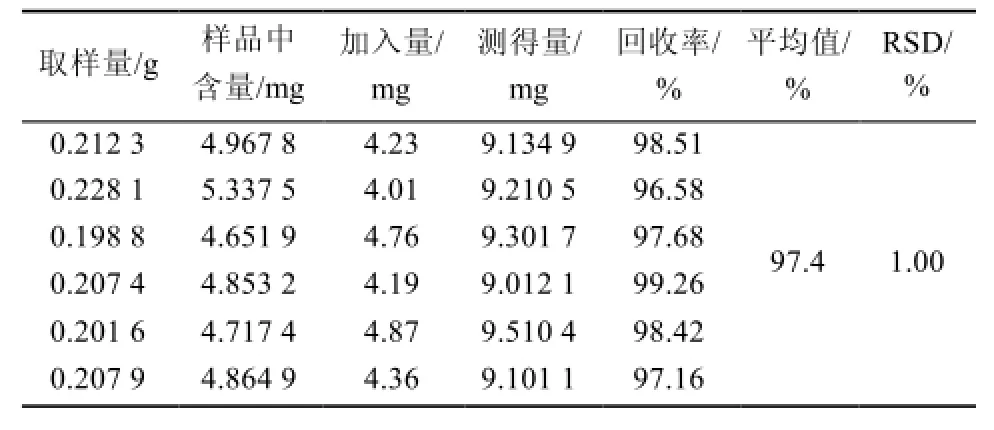
表1 盐酸水苏碱回收率试验表Tab 1 Recovery test of stachydrine hydrochloride
2.1.9 样品测定 取不同花期的益母草样品,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件测定盐酸水苏碱的含量(n=3),计算各样品中盐酸水苏碱的含量,测得结果见表2;不同时期的样品色谱图见图1。
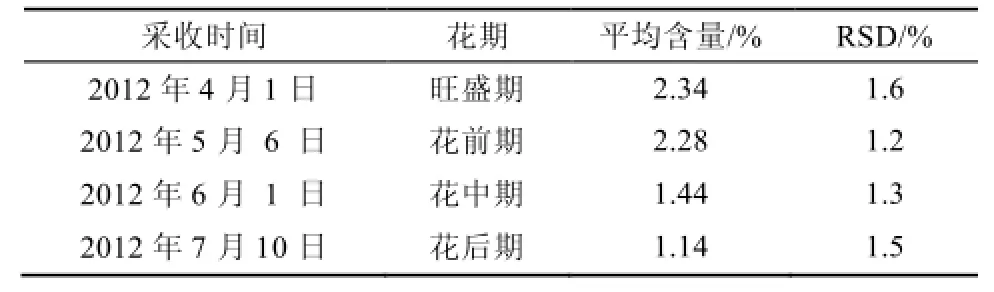
表2 样品中盐酸水苏碱的含量(n=3)Tab 2 Determination results of stachydrine hydrochloride in samples(n=3)
2.2 盐酸益母草碱的含量测定
2.2.1 色谱条件 色谱柱Venvsil 100A C18柱(4.6mm×250 mm,5 μm);流动相:乙腈-0.4%辛烷磺酸钠的0.1%磷酸溶液(24∶76);检测波长:277 nm。理论板数按盐酸益母草碱峰计算应不低于6 000。
2.2.2 对照品溶液的制备 取盐酸益母草碱对照品8.48 mg,置100 mL量瓶中,加入70%乙醇溶液至刻度,摇匀,制成每1 mL含0.084 8 mg的溶液,即得。
2.2.3 供试品溶液的制备 取“2.1.3”项下制备的供试品溶液。
2.2.4 线性范围 分别精密吸取对照品溶液1,2,5,10,15,25 μL注入高效液相色谱仪,按“2.2.1”项下色谱条件测定,以进样量为横坐标,峰面积为纵坐标,进行线性回归,得回归线方程Y=57 983 689.03X+102 810.59,r=0.998。表明进样量在0.088 5~2.212 5 μg内线性关系良好。
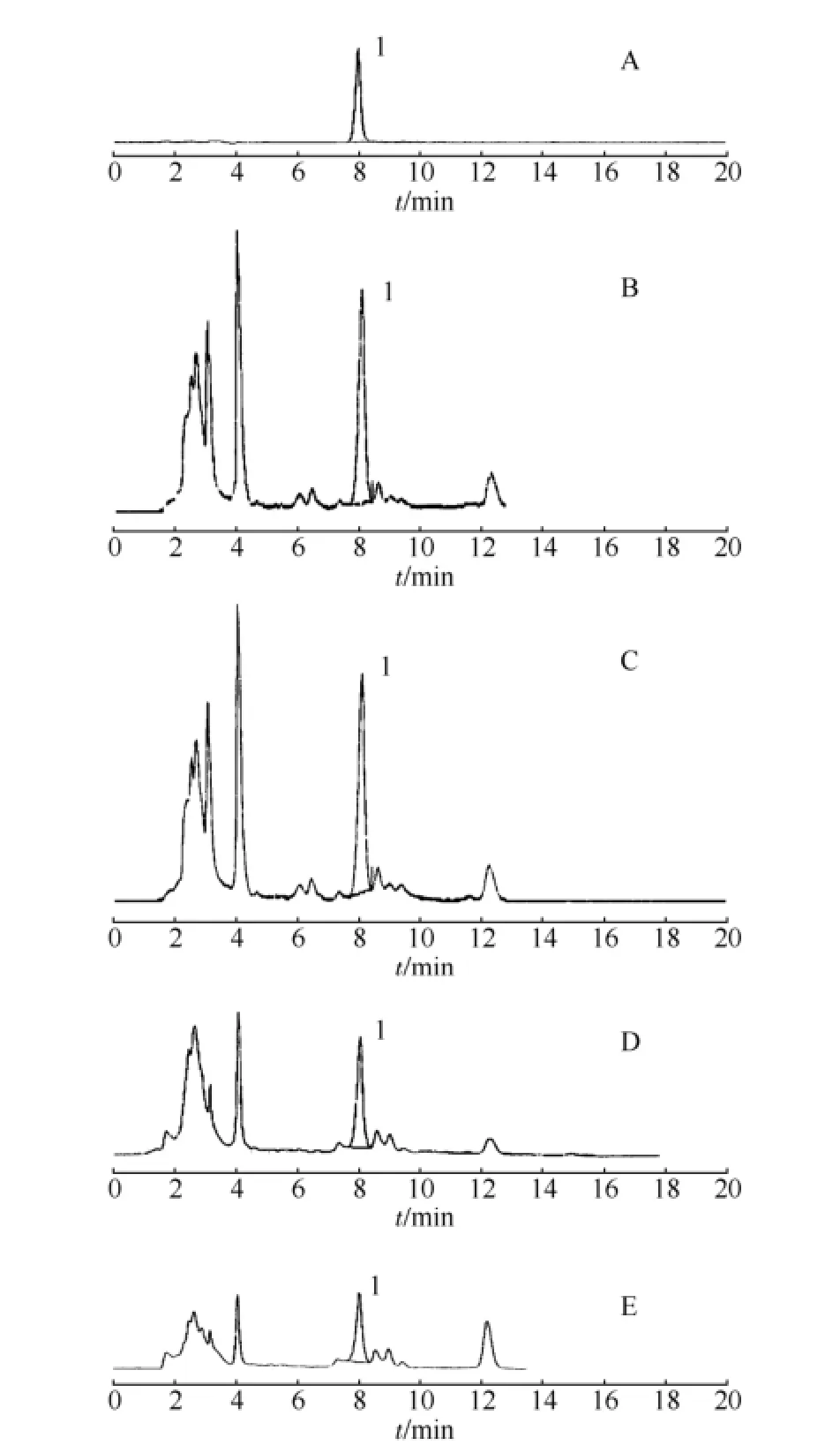
图1 盐酸水苏碱HPLC色谱图A-对照品;B-旺盛期样品;C-花前期样品;D-花中期样品;E-花后期样品;1-盐酸水苏碱Fig 1 HPLC chromatograms of stachydrine hydrochloride A-reference substances; B-vigorous growth period; C-flower prophase; D-flower midterm; E-flower later; 1-stachydrine hydrochloride
2.2.5 仪器精密度试验 取盐酸益母草碱对照品溶液10 μL,重复进样5次,结果峰面积RSD为1.2%,表明仪器精密度良好。
2.2.6 稳定性试验 取“2.2.3”项下供试品溶液10 μL,在0,6,12,18,24 h分别进样10 μL进行测定,结果峰面积的RSD为1.0%,表明其在24 h内稳定性良好。
2.2.7 重复性试验 取同一采收时期样品5份,按“2.2.3”项下方法制备,按“2.2.1”项下色谱条件测定盐酸益母草碱含量,结果RSD为1.9%,表明重复性良好。
2.2.8 回收率试验 精密称取益母草(含量为0.20%)样品6份,各约0.2 g,分别精密加入盐酸益母草碱对照品溶液5 mL,再精密加入70%乙醇溶液20 mL,按“2.1.3”项下方法制备溶液,按“2.2.1”项下色谱条件测定。结果平均回收率为97.8%,RSD=0.9%,见表3。

表3 盐酸益母草碱回收率试验表Tab 3 Recovery test of leonurine hydrochloride
2.2.9 样品测定 取不同花期的益母草样品粉末,按“2.1.3”项下方法制备溶液,按“2.2.1”项下色谱条件测定,计算各样品中盐酸益母草碱的含量,结果见表4;不同时期的样品色谱图见图2。
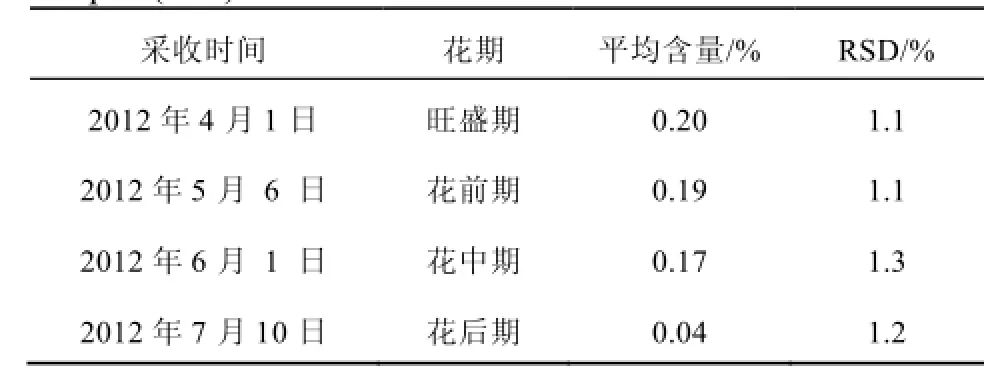
表4 益母草样品中盐酸益母草碱含量(n=3)Tab 4 Determination results of leonurine hydrochloride in samples(n=3)
3 讨论
开花对益母草药材中水苏碱的含量有较大的影响。开花过程中益母草药材中的含量不断降低,以开花前期到中期较为明显。虽然各个时期益母草药材中含量都能符合药典要求(盐酸水苏碱应≥0.50%),但开花过程中耗损严重。各个时期盐酸益母草碱的差异较大,尤其是开花后期盐酸益母草碱的损失较大,不能达到药典的含量要求(含盐酸益母草碱应≥0.050%)。故益母草含量以童子益母草为优,花前期较童子益母草略差,花中期又次于花前期,花后期最差不能达到药典要求。
不同产地的益母草品质不同,虽然炮制过程、储存可能对总碱含量差异有一定影响,但由于益母草的炮制只是简单的烘干切割,而且其有效成分生物碱又较为稳定,经过笔者的实验发现益母草药材的质量主要取决于产地采收时间,在花未开或花初开时,茎叶旺盛期采收的药材水苏碱及益母草碱含量最高,与药典收载的干品夏季茎叶茂盛、花未开或初开时采割相吻合。建议在选用药材时应考虑到这一因素,从而提高生药质量,使之得到更好的用药效果[2]。
开花对益母草药材中其他物质含量的影响有待进一步研究。
REFERENCES
[1] Ch.P(2010)Vol Ⅰ(中国药典 2010年版.一部) [S]. 2010: 550-501.
[2] KE Y, CHE S Q. Comparison of different origin Motherwort total alkaloid content [J]. Chin Tradit Herb Drugs(中草药), 1999, 30(4): 270-271.
[3] Cooperative Research Group of Shanghai Medical College of Coronary Heart Disease. Leonurus Japonicus Houtt therapeutic effect and mechanism of rat isoproterenol myocardial ischemia [J]. J Tradit Chin Med(中医杂志), 1980, 22(10): 68.
[4] YASUDA M. Leonurus japonicus Houtt the composition stachydrine of mice breast cancer and adenomyosis inhibition [J]. Magazines and Chinese Medicine(和汉医药学杂志), 1996, 13(1): 87-93.
[5] SUN W J. Concise Handbook of the Active Ingredients of Natural Medicine (天然药物活性成分简明手册) [M] Beijing: Chinese Medical Science and Technology Press, 1998: 531.
[6] XU D Q. Determination of stachydrine hydrochloride in Leonuri granule by HPLC-ELSD [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2013, 30(2): 189-191.
[7] LI C J, GUO F Y. Studies on the determination of stachydrine hydrochloride in Compound Motherwort capsules by HPLC-ELSD [J]. Chin J Mod Appl Pharm(中国现代应用药学), 2013, 30(1): 72-74.
Impact of the Flowering on the Content of Stachydrine Hydrochloride and Leonurine Hydrochloride in Leonuri Herba
HUANG Jian
(Xinchang People’s Hospital, Xinchang 312500, China)
OBJECTIVE To study the impact of the flowering on the content of stachydrine hydrochloride and leonurine hydrochloride in Leonuri Herba. METHODS The samples of Leonuri Herba were harvested in different harvest period in Xinchang province. The content of stachydrine hydrochloride and leonurine hydrochloride in Leonuri Herba was determined according to pharmacopoeia methods. RESULTS In the flowering period, the content of stachydrine hydrochloride and leonurine hydrochloride kept decreasing. CONCLUSION Flowering had a great impact on the content of stachydrine hydrochloride and leonurine hydrochloride in Leonuri Herba, thus in the end of flowering period, Leonuri Herba cann’t be used as medicine.
Leonuri Herba; stachydrine hydrochloride; leonurine hydrochloride; quality of medicine
R284.1;R917.101
B
1007-7693(2013)10-1077-05
2013-03-05
黄健,女,主管中药师 Tel: (0575)86022082 E-mail: 2213726815@qq.com
