七叶皂苷钠微乳注射剂的安全性及药效学研究
2013-03-06覃瑶阳勇龚晓丽李紫薇赵嘉将罗维早
覃瑶,阳勇,龚晓丽,李紫薇,赵嘉将,罗维早*
(1.太极集团有限公司,重庆 401147;2.重庆市中药研究院,重庆 400065;3.四川省中医药科学院中医研究所,成都 610041;4.重庆医科大学,重庆 400016)
·论 著·
七叶皂苷钠微乳注射剂的安全性及药效学研究
覃瑶1,2,阳勇2,龚晓丽3,李紫薇4,赵嘉将1,罗维早1,2*
(1.太极集团有限公司,重庆 401147;2.重庆市中药研究院,重庆 400065;3.四川省中医药科学院中医研究所,成都 610041;4.重庆医科大学,重庆 400016)
目的 对市售七叶皂苷钠粉针及自制七叶皂苷钠微乳注射剂的安全性和疗效进行对比研究。方法 以新西兰家兔为试验用动物,进行溶血试验和血管刺激性试验,对用药安全性进行考察;对二甲苯致小鼠耳肿胀及耳廓毛细血管通透性增加的抑制作用进行考察,作出初步药效学评价。结果 市售粉针和自制微乳剂均有轻微的溶血和一定的刺激性,组间无明显差别;高、低剂量的七叶皂苷钠粉针及微乳注射剂对二甲苯所致小鼠耳肿胀及耳廓毛细血管通透性增加均有明显的拮抗作用,其中七叶皂苷钠微乳注射剂的拮抗作用更为明显。结论 市售粉针剂和自制微乳注射剂均存在一定的静脉注射安全性风险,两者抗炎消肿作用明显,七叶皂苷微乳注射剂疗效更为显著。
注射用七叶皂苷钠;微乳剂;安全性;有效性
七叶皂苷钠为七叶树科植物天师栗的干燥成熟果实(娑罗子)提取得到的皂苷钠盐,主要成分是七叶皂苷,属于三萜皂苷类药物[1]。七叶皂苷不溶于水,其钠盐具有很好的水溶性。七叶皂苷钠具有显著的抗炎消肿功能,临床用于多种疾病的治疗。市售剂型主要有片剂、粉针剂、凝胶剂,其中七叶皂苷钠粉针应用最为广泛,但其静脉给药对血管刺激性大,可致静脉疼痛和静脉炎[2]。微乳是一种新型理想的药物释放载体,具有透明、稳定、吸收完善和靶向释药等特点,能够提高药物储藏稳定性和生物利用度,并能提高疗效。同时,微乳对炎症病灶具有一定的趋向性,微乳的相关辅料已有注射用标准,使其新药开发前景乐观,临床应用价值日益提高[3]。因此,本研究将七叶皂苷钠在酸性条件下制备成注射用水包油型微乳剂型。在此条件下,七叶皂苷钠游离为七叶皂苷,脂溶性显著增加溶于油相,降低了水相中的含量,从而降低了与血管壁接触的机会,减少对血管壁的刺激,增强患者用药的安全性。同时借助微乳对炎症病灶的趋向性,以期提高药物在炎症病灶的浓集,增加疗效。
1 仪器与试药
1.1 仪器设备
JB-2型恒温磁力搅拌器(上海智光仪器仪表有限公司);万分之一电子分析天平(德国赛多利斯);DT5-2型低速台式离心机(北京时代北利离心机有限公司);电子恒温水浴锅(北京中兴伟业仪器有限公司);BS224电子天平(北京赛多利斯仪器系统公司);756PC紫外-可见分光光度计(上海舜宇恒平科学仪器有限公司);Allegra X-12离心机(美国贝尔曼库尔特有限公司);LDZM-50立式压力蒸汽灭菌器(上海申安医疗器械厂)。
1.2 供试品溶液
七叶皂苷钠微乳注射剂(自制,2 mg·mL-1);注射用七叶皂苷粉针(武汉爱民制药有限公司,批号:1111078,规格:10 mg·瓶-1);实验时均用0.9%生理盐水配制成适当浓度对动物尾静脉注射给药。
1.3 试剂
二甲苯(重庆川东化工集团有限公司,批号:20091020);伊文思兰(B.D.H进口分装产品,实验时用无菌生理盐水配制成0.5%的溶液);丙酮[重庆川东化工(集团)有限公司化学试剂厂,批号:20091118];生理盐水(重庆天圣制药股份有限公司,批号:090804)。
1.4 动物
新西兰家兔,普通级,体质量2.0~2.5 kg,♀♂各半,由四川省医学实验动物中心提供,实验动物合格证号:0044303;KM小鼠,♀♂各半,体质量18~22 g,由重庆市中药研究院实验动物中心提供,实验动物合格证号:SCXK(渝)20070006。
2 方法和结果
2.1 溶血试验
取新西兰家兔,耳缘静脉取血约15 mL,用玻棒轻轻搅动血液以除纤维蛋白原,使成脱纤血液[4]。加入生理盐水约10倍量,摇匀,2 000 r·min-1离心10 min,除去上清液,沉淀的红细胞再用生理盐水按上述方法洗涤3~4次,直至上清液不显红色为止,按所得红细胞容积用生理盐水配成2%兔血红细胞混悬液,备用。取洁净试管7支,1~5号管为供试品,按表1依次加入2%兔血红细胞混悬液、生理盐水、注射用七叶皂苷钠微乳注射剂(5 mL溶于生理盐水125 mL)、七叶皂苷钠粉针液(5 mg溶于生理盐水250 mL);6号管为阴性对照;7号管为阳性对照。混匀l~7号管,置(37±0.5)℃恒温水浴箱中温育。3 h后观察溶血与凝集现象,按表2判断是否溶血,结果见表3。

表1 注射用七叶皂苷钠微乳溶血试验加样表Tab 1 The sample loading amount of hemolysis test about sodium aescinat micro-emulsion injection

表2 溶血试验判断标准Tab 2 Judging criteria of hemolysis test

表3 注射用七叶皂苷钠微乳溶血试验结果Tab 3 Hemolysis results of sodium aescinat micro-emulsion injection
结果表明,7号阳性对照管液体澄明鲜红色,管底几乎无红细胞残留,为全溶血;6号阴性对照管上层液无色澄明,红细胞逐渐沉于管底,颜色呈鲜红色,轻轻振摇后管底沉积的红细胞均能完全分散,为无溶血;兔血红细胞的1~4号各浓度七叶皂苷钠微乳供试管、5号七叶皂苷钠粉针供试管上层溶液呈澄明红色,管底有少量红细胞残留,轻摇后红细胞不能完全分散,表明部分溶血[5]。但注射用七叶皂苷钠微乳与七叶皂苷钠粉针供试管比较,无明显差别。
2.2 血管刺激性试验
取新西兰家兔6只,随机分成2组。第1组按0.6 mg·kg-1家兔右耳注射七叶皂苷钠粉针注射剂(5 mg溶于生理盐水10 mL);第2组注射等给药体积的生理盐水作自身阴性对照,2组分别左耳缘静脉注射七叶皂苷钠微乳注射剂(5 mL溶于生理盐水20 mL)。每天1次,连续给药5 d,肉眼观察注射部位及周围组织是否有红肿、充血等刺激现象。末次给药后24 h,于注射部位及周围组织处拔毛,75%乙醇消毒,恢复3 h以上。按30 mg·kg-1注射戊巴比妥钠局部麻醉,沿注射部位1 cm开始取0.5 cm组织,取多段,各间隔1 cm,生理盐水冲洗,用10%中性福尔马林液固定24 h。常规脱水,石蜡包埋,切片,HE染色,光镜下组织学检查并比较[6]。结果见图1。
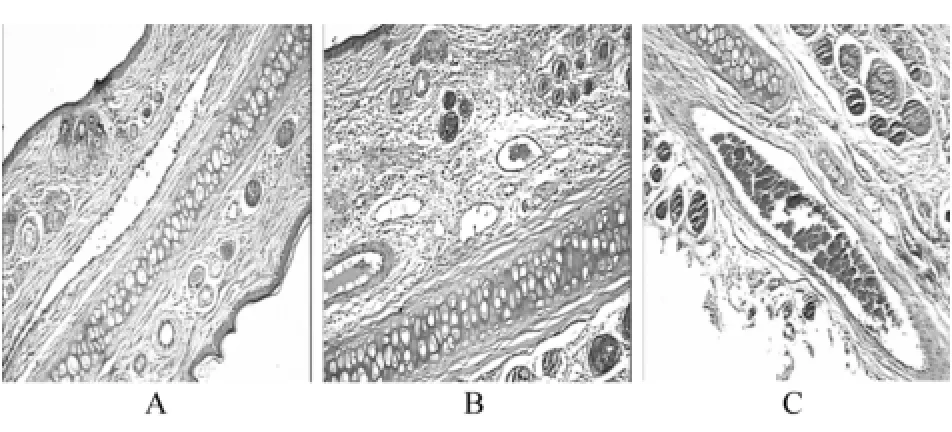
图1 血管刺激性试验病理图片A-生理盐水;B-七叶皂苷钠粉针;C-注射用七叶皂苷钠微乳Fig 1 Pathology photos of vascular stimulation test A-saline; B-sodium aescinat powder injection; C-sodium aescinat micro-emulsion injection
图1 结果表明,注射生理盐水组,3只家兔耳缘静脉无明显充血,血管内皮细胞结构完整,无肿胀、变性、坏死及增生,管壁及周围组织无炎症改变。耳廓皮肤表面复层鳞状上皮结构完整,上皮细胞无水肿、变性、坏死、增生及萎缩性改变,无炎症及溃疡形成。深层毛囊、皮脂腺及汗腺组织无特殊病变。中心部位弹性软骨形态正常,软骨细胞、软骨基质及软骨膜结构和染色反应正常。耳廓间质纤维组织无增生及变性,无急性及慢性炎症改变[7]。
七叶皂苷钠粉针组的3只家兔耳缘静脉充血明显,血管内皮细胞轻度肿胀,管壁周围组织有出血以及炎性细胞浸润。耳廓皮肤表面复层鳞状上皮结构完整,上皮细胞无水肿、变性、坏死、增生及萎缩性改变,无炎症及溃疡形成。深层毛囊、皮脂腺及汗腺组织无特殊病变。中心部位弹性软骨形态正常,软骨细胞、软骨基质及软骨膜结构和染色反应正常。耳廓间质纤维组织无增生及变性,无急性及慢性炎症改变。
注射用七叶皂苷钠微乳注射的3只家兔的耳缘静脉充血,血管内皮细胞轻度肿胀,管壁周围组织有出血以及炎性细胞浸润。耳廓皮肤表面复层鳞状上皮结构完整,上皮细胞无水肿、变性、坏死、增生及萎缩性改变,无炎症及溃疡形成。深层毛囊、皮脂腺及汗腺组织无特殊病变。中心部位弹性软骨形态正常,软骨细胞、软骨基质及软骨膜结构和染色反应正常。耳廓间质纤维组织无增生及变性。与生理盐水对照组比较,有显著的病理组织学差异。
2.3 对二甲苯致耳肿胀的抑制作用
对小鼠耳肿胀模型静脉注射给药,有效剂量拟定为0.9 mg·kg-1(低剂量组)、4.5 mg·kg-1(高剂量组)。将50只小鼠按体质量随机分为阴性对照组、七叶皂苷钠粉针组和七叶皂苷钠微乳注射剂组,每组10只。小鼠适应性饲养后,七叶皂苷钠微乳注射剂组及七叶皂苷钠粉针组均分别按剂量静脉注射给药,阴性对照组静脉注射0.2 mL生理盐水。给药后30 min,在每鼠右耳涂上二甲苯(0.03 mL·只-1)。15 min后处死动物,用直径为0.6 cm的打孔器在相同位置取两耳片称重,以两耳片之差为肿胀度[8]。结果见表4。

表4 对二甲苯致耳肿胀的抑制作用(n=10)Tab 4 Inhibitory effect on xylene-induced mouse ear edema (n=10)
结果表明,与阴性对照组比较,高、低剂量的七叶皂苷钠粉针及注射用七叶皂苷钠微乳对二甲苯致小鼠耳肿胀均有明显的抑制作用;其中七叶皂苷钠微乳的效果更为明显。
2.4 对二甲苯致毛细血管通透性增加的拮抗作用选50只健康小鼠进行实验,按“2.3”项下进行动物分组、剂量设计,小鼠适应性饲养后,注射用七叶皂苷钠微乳组及阳七叶皂苷钠粉针组均分别按剂量静脉注射给药,阴性对照组静脉注射0.2 mL生理盐水。给药后30 min,每只动物尾静脉注射0.2 mL 0.5%伊文思蓝生理盐水溶液,立即在每鼠右耳涂二甲苯(0.03 mL·只-1)。15 min后处死动物,用直径为0.6 cm的打孔器在相同位置取右耳片,剪碎,置盛有4 mL丙酮:生理盐水(7∶3)的有塞试管内,浸泡96 h。离心,倾出上清液于590 nm比色,以吸光度值进行统计,结果见表5。
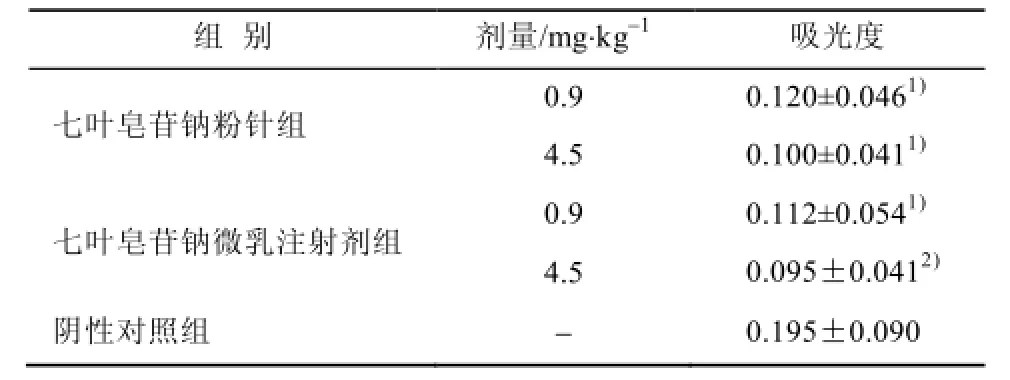
表5 对二甲苯致毛细血管通透性增加的拮抗作用(n=10)Tab 5 The antagonism on xylene-induced capillary permeability-increasing(n=10)
结果表明,当二甲苯涂小鼠右耳,因刺激作用导致毛细血管通透性增加,吸光度和毛细血管通透性成正比。与阴性对照组相比,高、低剂量的七叶皂苷钠粉针及七叶皂苷钠微乳注射剂对二甲苯引起的小鼠耳廓毛细血管通透性增加均有明显的拮抗作用。七叶皂苷钠微乳注射剂的拮抗作用更为明显。
3 讨论
3.1 安全性
实验结果表明七叶皂苷钠微乳注射剂和七叶皂苷钠粉针注射剂家兔静脉给药有部分溶血和血红细胞凝聚反应,且有血管刺激性反应,七叶皂苷微乳注射剂的充血现象略弱于七叶皂苷粉针剂,但无显著差异,提示该药物本身静脉注射给药存在一定风险性,还需要进一步的实验研究七叶皂苷钠引起溶血和血管刺激性反应的原因。
3.2 有效性
实验结果表明高、低剂量的七叶皂苷钠粉针及七叶皂苷钠微乳注射剂对二甲苯致小鼠耳肿胀及耳廓毛细血管通透性增加均有明显的抑制作用,其中七叶皂苷钠微乳的效果更为明显,为后续研究提供了一定的基础。粉针组与微乳注射剂间无显著性差异,其原因可能在于七叶皂苷钠自身的抗炎效果较为明显,故其组间差异难以分析。
本次对七叶皂苷钠粉针剂和微乳注射剂的安全性及药效学的对比研究中,市售粉针和自制微乳剂均有轻微的溶血和一定的刺激性。溶血和刺激性可能还源于主药七叶皂苷钠本身,也可能源于微乳剂中的乳化剂和助乳化剂等辅料[9],其注射用安全性还有待进一步的考察。自制微乳剂较市售粉针剂有明显的抗炎消肿作用,可能是选用有双亲性的微乳作为药物载体,避免了药物与血管壁的直接接触,增加了药物在炎症部位的富集,从而使其抗炎消肿作用增强[10]。总而言之,微乳作为一种新型药物载体,稳定、吸收迅速完全、能增强疗效,如能降低其不良反应,其制剂有很大潜力。随着研究的深入,微乳中药制剂将有更广阔的发展前景。
REFERENCES
[1] XU F. Clinical use and the adverse reactions of sodium aescinate [J]. Dis Monitor Control(疾病监测与控制杂志), 2011, 5(2): 123-124.
[2] XUE Y L, HOU J L, W Y, et al. Study on anti-inflammatory effects and acute toxicity of sodium aescinate with different proportion [J]. Qilu Pharm Aff(齐鲁药事), 2009, 28(5): 305-307.
[3] WANG D Z, WANG P, LIU X Y, et al. Micro-emulsification technology and its application progress [J]. Chem Intermed(化工中间体), 2011, (9): 6-8.
[4] ZHANG Y F, ZHAO X X, XIN Z W. Experiment studies of Maodongqing injection on vascular stimulation, haemocytolysis and anaphylaxis [J]. China Pract Med(中国实用医药), 2012, 7(23): 64-65.
[5] RAO Y, WANG Y L, ZHANG W S, et al. Hemolysis test of emulsified isoflurane in vitro and in vivo [J]. Chin J Clinicians(中华临床医师杂志), 2011, 5(20): 6039-6044.
[6] ZHOU Q H, DING M, WANG B J, et al. The improved ammonium acetate method in the application of DNA extraction from formalin-fixed and paraffin-embedded(FFPE) tissues [J]. Chin J Forensic Med(中国法医学杂志), 2012, 27(3): 225-227.
[7] QU J. The evaluation on safety of Chinese medicine injection [J]. Chin Hosp Pharm J(中国医院药学杂志), 2009, 29(2): 93-98.
[8] GUO L F, FAN W X, TANG A M. Dinitrofluorobenzene and fluorescein isohiocyanate induced mouse model of allergic contact dermatitis [J]. Chin J Dermalol(中华皮肤科杂志), 2005, 38(4): 12-15.
[9] YANG H, YI H. Advances on pharmaceutical microemulsion in China [J]. Chin J New Drugs(中国新药杂志), 2006, 15(10): 764-768.
[10] ZHANG L, ZHOU Q H, LÜ X, et al. The preparationn of microemulsion and its application in pharmacy of Chinese herbal medicine [J]. Acta Chin Med Pharmacol(中医药学报), 2007, 35(6): 37-39.
Study on the Safety and Pharmacodynamics of Sodium Aescinat Micro-emulsion Injection
QIN Yao1,2, YANG Yong2, GONG Xiaoli3, LI Ziwei4, ZHAO Jiajiang1, LUO Weizao1,2*
(1.Taiji Group, Chongqing 401147, China; 2.Chongqing Institute of Traditional Chinese Medicine, Chongqing 400065, China; 3.Sichuan Academy of Chinese Medicine Sciences, Chengdu 610041, China; 4.Chongqing Medical University, Chongqing 400016, China)
OBJECTIVE To undertake a contrastive study on safety and pharmacodynamics of sodium aescinat powder injection and micro-emulsion injection. METHODS New Zealand rabbits were chosen as experimental animals for hemolysis and vascular stimulation tests, and its safety for therapy was probed. Investigate the inhibitory effect on xylene-induced mouse ear edema and capillary permeability-increasing, and a preliminary pharmacodynamics evaluation was made. RESULTS Both of sodium aescinat powder injection and micro-emulsion injection had slight hemolysis and stimulation, there was no evident difference between the two groups; both groups of high dose and low dose sodium aescinat powder injection and micro-emulsion injection had remarkable restrictive effect on mouse ear edema and capillary permeability-increasing, the antagonistic action of micro-emulsion injection was more apparent. CONCLUSION Both of sodium aescinat powder injection and micro-emulsion injection have a certain intravenous security risk, and they also have significant anti-inflammatory effects, the anti-inflammatory effects of sodium aescinat micro-emulsion injection is more apparent.
sodium aescinat for injection; micro-emulsion for injection; safety; validity
R965.3
A
1007-7693(2013)10-1043-04
2013-03-07
国家自然科学基金(81073062);重庆市中药产业“重构提升”行动科技攻关项目
覃瑶,女,博士 Tel: 13527482150 E-mail: trowa1982@126.com*
罗维早,男,研究员 Tel: 18623088135 E-mail: loweizao@163.com
