红花色素的荧光性能
2013-01-28李学琴程建文魏玲徐家宁范勇
李学琴,程建文,魏玲,徐家宁,范勇
(1.昌吉学院化学与应用化学系,新疆昌吉831100;2.吉林大学化学学院,吉林长春130012)
红花属菊科,现今主要栽种于新疆、甘肃、河南、浙江、四川等地,其中新疆是我国种植历史最悠久,种植面积最大的红花产地之一,品种资源占到全国的50%以上。红花中主要含有红色素和黄色素,其中红色素含量约占0.1%~0.2%,黄色素含量为30%左右[1]。
红花色素在医药、化妆品、食品等领域都有广泛的应用。目前对红花色素分析的主要方法有,分光光度法[2-3]、高效液相色谱法[4-5]、荧光分析法[6]。其中荧光分析法具有操作简单、灵敏度高等特点。本文采用荧光分析法分别对红花红色素和红花黄色素分别进行研究,研究pH、温度、溶剂、金属离子对红花红色素和红花黄色素荧光性能的影响,为以后的探索研究提供参考。
1 材料与方法
1.1 仪器与试剂
RF-5301 荧光分光光度计:日本岛津;SHB-Ⅲ循环水式多用真空泵:上海嘉鹏科技有限公司;KQ-100型超声波清洗器:昆山超声仪器有限公司;XYJ-802离心成淀机:江苏医疗仪器厂;HR-200 电子天平:A&D Company,Limited;微量取液器:北京青云航天仪表有限公司。
红花:新疆产,粉碎(过120 目筛);丙酮:分析纯,天津市北方天医化学试剂厂;氢氧化钠:分析纯,西安化学试剂厂;硫酸:分析纯,乌鲁木齐市天岳化学试剂有限公司;硫酸亚铁:分析纯,上海第二钢铁厂;氯化铝:分析纯,北京市朝阳区化肥厂;硝酸铅:分析纯,北京红星化工厂;硫酸铵:分析纯,成都化学试剂厂。
1.2 方法与步骤
1.2.1 红花红、黄色素的处理
取2 g 红花粉末,经蒸馏水多次浸泡,超声振荡过滤,收集滤渣,合并滤液,该滤液作为黄色素待测液。滤渣晾干后用50%丙酮溶液浸泡,重复提取3 次,滤渣呈土黄色,合并滤液,该滤液作为红花红色素待测液。
1.2.2 红色素荧光分析条件的选择
取10 mL 比色管,加入红色素样品滤液3 mL,用50%丙酮溶液定容、摇匀。在220 nm~780 nm 间扫描得知样品溶液的最佳激发波长和发射波长(λex=365 nm,λem=735 nm)。
1.2.2.1 红花红色素在50%丙酮溶剂中的荧光性能
50%丙酮溶剂,在激发波长λex=365 nm,在700 nm~750 nm 的扫描范围条件下,测定50%丙酮溶剂荧光性能。用同样的方法,取3 mL 的50%丙酮提取液,测提取液的荧光性能。
1.2.2.2 荧光分析中红色素用量的选取
取9 种不同浓度的溶液,在激发波长λex=365 nm,在700 nm~750 nm 的扫描范围条件下,测定不同浓度红花红色素的荧光性能。
1.2.2.3 温度对红花红色素荧光性能的影响
取4 只10 mL 比色管,各加入5.2.1 的红色素滤液3 mL,然后各加入50%丙酮溶液7 mL,搅匀。将试管放入水浴锅中,温度控制在25、35、50、65 ℃条件下水浴2 min,然后冷却至室温。分别取上述4 种不同温度的溶液各3L,置荧光分析皿中,在λex=365nm,在700nm~750 nm 的扫描范围条件下测定不同温度环境下红花红色素的荧光性能。
1.2.2.4 pH 对红花红色素荧光性能的影响
取10 只比色管,各加入50%丙酮溶液7 mL,用0.2 moL/L 氢氧化钠和0.1 moL/L 硫酸溶液分别调节酸碱度使10 只比色管中的pH 从1~10 排列,再分别加入5.2.1 的红色素滤液3 mL,摇匀。取上述10 种不同pH 的溶液各3 mL,置荧光分析皿中,在λex=365 nm,在700 nm~750 nm 的扫描范围条件下测定不同pH 环境下红花红色素的荧光性能。
1.2.2.5 金属离子对红花红色素荧光性能的影响
取4 只10 mL 比色管,分别加入1.2.1 的红色素滤液3 mL,然后将等量的0.01 moL/L 金属化合物(FeSO4,AlCl3,Pb(NO3)2)及硫酸铵溶液加入相应的比色管中,用50%丙酮溶液定容,摇匀。分别取上述4 种含不同盐的溶液3 mL,在λex=365 nm,在700 nm~750 nm 的扫描范围条件下测定红花红色素的荧光性能。
1.2.3 黄色素荧光分析条件的选择
黄色素水溶液,在220 nm~780n m 之间扫描,得知样品溶液的最佳激发波长和发射波长λex= 242 nm,λem=485 nm。
1.2.3.1 红花黄色素在水作溶剂中的荧光性能
取3 mL 的蒸馏水,在激发波长λex= 242 nm,在460 nm~550 nm 的扫描范围条件下,测定蒸馏水荧光性能。用同样的方法,取3 mL 的水提取液,测提取液的荧光性能。
1.2.3.2 荧光分析中黄色素用量的选取
在室温条件下,分别系列浓度的黄色素提取液,用荧光分光光度计扫描,激发波长λex=242 nm,扫描范围在460 nm~550 nm 得到黄色素用量—荧光强度曲线。
1.2.3.3 温度对红花黄色素荧光性能的影响
黄色素水提取液,控制在25、35、50、65、80、90 ℃等温度下水浴2 min,冷却至室温。在激发波长λex=242 nm,扫描范围:460 nm~550 nm 条件下测定不同温度环境下红花黄色素的荧光性能。
1.2.3.4 pH 对红花黄色素荧光性能的影响
黄色素样品滤液40 μL,用0.2 moL/L 氢氧化钠和0.1 moL/L 硫酸溶液分别调节蒸馏水酸碱度pH 从1~10,室温下在激发波长λex= 242 nm,扫描范围:460 nm~550 nm 条件下测定不同pH 环境下红花黄色素的荧光性能。
1.2.3.5 金属离子对红花黄色素荧光性能影响
取3 只10 mL 比色管,分别加入黄色素样品滤液120 μL,将等量0.01 moL/L 金属化合物[FeSO4,AlCl3,Pb(NO3)2]加到相应的比色管中,用蒸馏水定容,摇匀。分别取上述3 种含不同金属离子的溶液3mL,室温下在激发波长λex=242 nm,扫描范围:460 nm~550 nm 条件下测定黄色素的荧光性能。
2 结果与讨论
2.1 红花红色素50%丙酮溶液荧光性能
取3 mL 的50%丙酮溶剂,在激发波长λex=365 nm,在700 nm~750 nm 的扫描范围条件下,测定50%丙酮溶剂的荧光性能。用同样的方法,取3 mL 的50%丙酮提取液,置于荧光分析皿中,测定提取液的荧光性能见,图1。
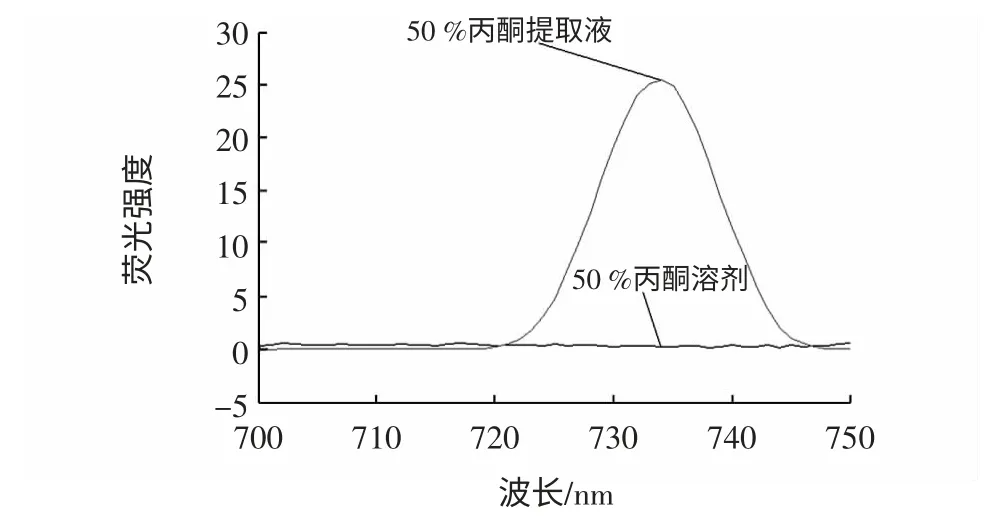
图1 50%丙酮溶剂中红花红色素荧光性能Fig.1 Fluorescentspectral properties of the carthamine in 50%acetone
由图1 可知,50%丙酮溶剂在700 nm~750 nm 波长范围内没有出现波峰,表明在735 nm 处的波峰是由红色素产生的,50%丙酮溶剂对红花红色素的荧光性能没有影响。
2.2 荧光分析中红色素用量的选取
取9 只试管,各加入1、2、3、4、5、6、7、8、9 mL 50%的丙酮溶液,再各加入1.2.1 的红色素提取液3 mL,摇匀。取9 种不同浓度的溶液3 mL,在激发波长λex=365 nm,在700 nm~750 nm 的扫描范围条件下,测定不同浓度红花红色素的荧光性能,见图2。

图2 红色素用量对红色素荧光性能的影响Fig.2 Effect of carthamine content to fluorescent spectral properties
从图2 可知,分别用1 mL 到7 mL 的50%丙酮溶液稀释3 mL 红色素提取液,红色素发出的荧光强度逐渐增强,用7 mL 的50%丙酮溶液稀释时,红色素的荧光强度最达到最强。而用8、9 mL 的50%丙酮溶液稀释时,红色素的荧光强度逐渐减弱。推测其原因:红色素浓度较大时,激发态分子和基态分子发生碰撞,产生荧光猝灭现象。
2.3 温度对红花红色素荧光性能的影响
取4 只10 mL 比色管,各加入1.2.1 的滤液3 mL,用50%丙酮溶液定容搅匀。将比色管放入水浴锅中,温度控制在25、35、50、65 ℃条件下水浴2 min,然后冷却至室温。分别取上述4 种不同温度的溶液各3 mL,在λex=365 nm,在700 nm~750 nm 的扫描范围条件下测定不同温度环境下红花红色素的荧光性能,见图3。
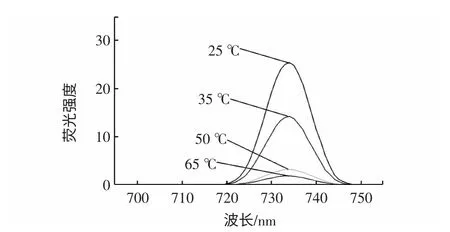
图3 温度对红色素荧光性能的影响Fig.3 Effect of temperature to fluorescent spectral propertiesof the carthamine
从图3 可以看出,随着温度的升高红色素的荧光强度逐渐减弱,其中65 ℃时红色素发出的荧光强度最弱,25 ℃时红色素发出的荧光强度最强。推测其可能的原因是,温度升高时,介质黏度减小,分子运动加快,分子间碰撞几率增加,从而使分子无辐射跃迁增加,荧光效率降低。
2.4 pH 对红花红色素荧光性能的影响
取10 只比色管,各加入50%丙酮溶液7 mL,用0.2 moL/L 氢氧化钠和0.1 moL/L 硫酸溶液分别调节酸碱度使10 只比色管中的pH 从1~10 排列,再分别加入1.2.1 的红色素滤液3 mL,摇匀。取上述10 种不同pH 的溶液各3 mL,在λex=365 nm,在700 nm~750 nm的扫描范围条件下测定不同pH 环境下红花红色素的荧光性能,见图4。
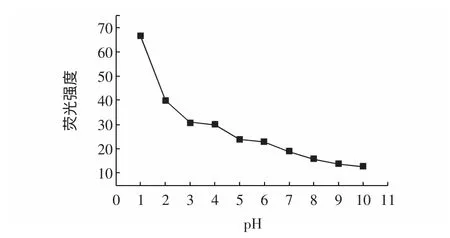
图4 pH 对红色素荧光性能的影响Fig.4 Effect of pH to fluorescent spectral propertiesof the carthamine
由图4 得知,红花红色素溶液pH 从1 到10 的荧光强度逐渐减弱,且pH=1 时,红花红色素的荧光强度最强。推测其原因:由于分子内存在氢键作用,使分子结构呈多环状。pH=1 时,质子化作用比较强,使得氢键的键能增强,致使整个分子结构的刚性增强,所以在pH=1 时红色素的荧光强度最强。
2.5 金属离子对红花红色素荧光性能影响
取4 只10 mL 比色管,分别加入1.2.1 的红色素滤液3 mL,然后将等量的0.01 moL/L 金属化合物[FeSO4,AlCl3,Pb(NO3)2]及硫酸铵溶液加入相应的试管中,用50%丙酮溶液定容,摇匀。分别取上述4 种含不同盐的溶液3 mL,在λex=365 nm,700 nm~750 nm 的扫描范围条件下测定红花红色素的荧光性能,见图5。
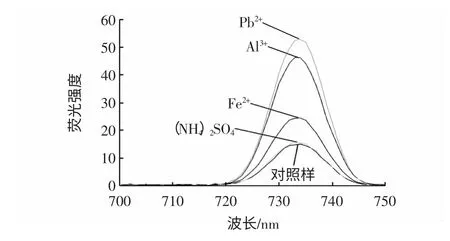
图5 金属离子对红花红色素荧光性能的影响Fig.5 Effect of metal ion to fluorescent spectral propertiesof the carthamine
由图5 可知,Pb2+、Al3+、Fe2+离子的存在,使得红花红色素的荧光性能增强。一般而言,铝离子可能与红色素形成配合物,使红色素分子结构发生变化,峰位发生变化,重金属离子会使物质的荧光性能产生猝灭现象,但实验得出的结果却正好相反,峰位没有发生变化,而重金属离子使红色素的荧光性能增强。而(NH4)2SO4的影响不大,为以后用硫酸铵/丙酮双水相提取红花红色素提供参考。
2.6 水溶剂对红花黄色素荧光性能的影响
取3 mL 的蒸馏水,在激发波长λex=242 nm,在460 nm~550 nm 的扫描范围条件下,测定蒸馏水的荧光性能。用同样的方法,取3 mL 的水溶剂提取液,置于荧光分析皿中,测定提取液的荧光性能,见图6。
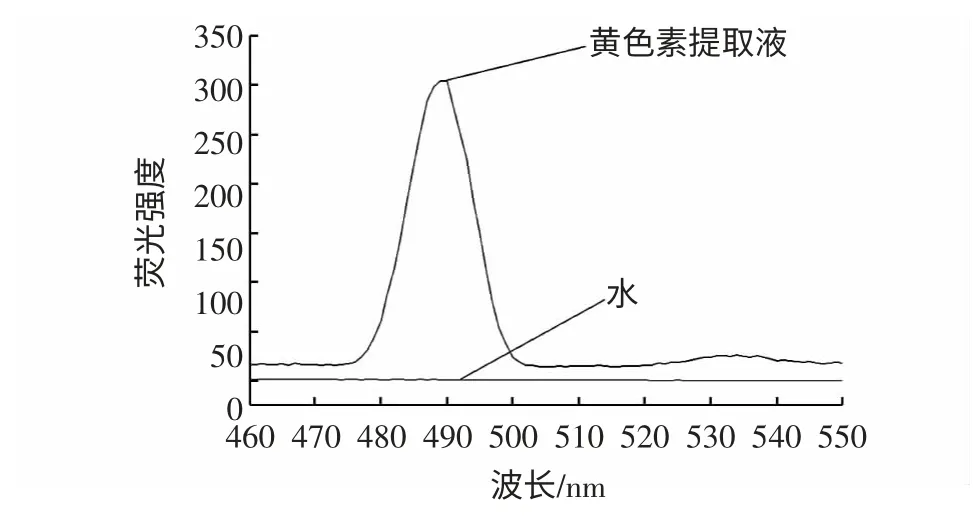
图6 水作溶剂中红花黄色素荧光性Fig.6 Fluorescentspectral properties of safflower yellow in water
由图6 得知,水作溶剂在460 nm~550 nm 波长扫描范围内没有出现波峰,表明在485 nm 处的波峰是由黄色素产生的。
2.7 荧光分析中黄色素用量的选取
取5 只10 mL 比色管,用微量取液器分别加黄色素提取液60、90、120、150、180 μL 于比色管中,再用蒸馏水定容。在室温条件下,分别取上述五种浓度的溶液各3 mL,激发波长λex=242 nm,扫描范围在460 nm~550 nm 得到一系列荧光发射曲线,见图7。
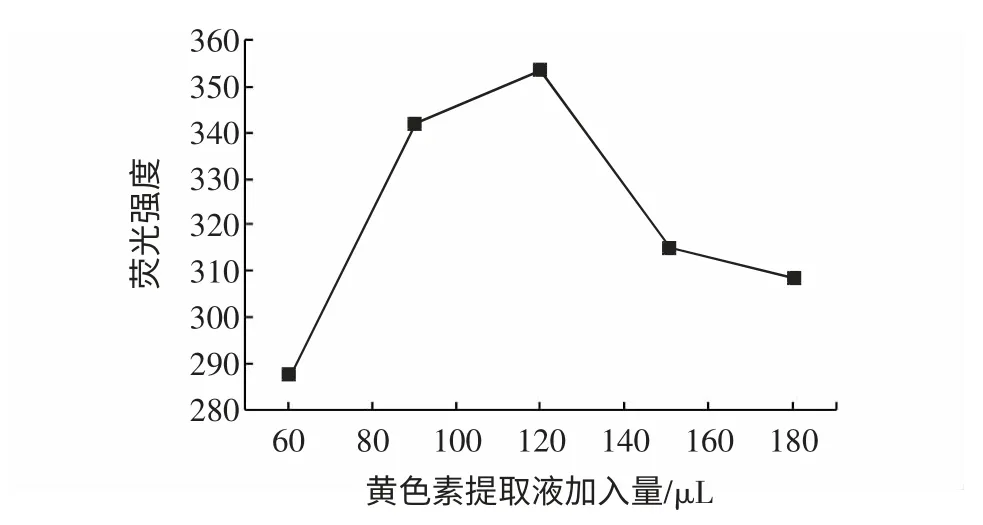
图7 黄色素用量对荧光性能的影响Fig.7 Effect of safflower yellowcontent to fluorescent spectral properties
由图7 可知,提取液用量为120 μL 时红花黄色素发出的荧光强度最强。当用量大于120 μL 时荧光强度呈减弱的趋势,推测其原因黄色素浓度较大时,激发态分子和基态分子发生碰撞,产生荧光自熄灭现象。
2.8 温度对红花黄色素荧光性能的影响
取6 只10 mL 比色管,分别加入黄色素样品滤液120 μL,用蒸馏水定容,摇匀。将比色管放入水浴锅中,温度控制在25、35、50、65、80、90 ℃等温度下水浴2 min,冷却至室温。分别取上述六种温度的溶液各3mL,在激发波长λex=242 nm,扫描范围:460 nm~550 nm 条件下测定不同温度环境下红花黄色素的荧光性能,见图8。
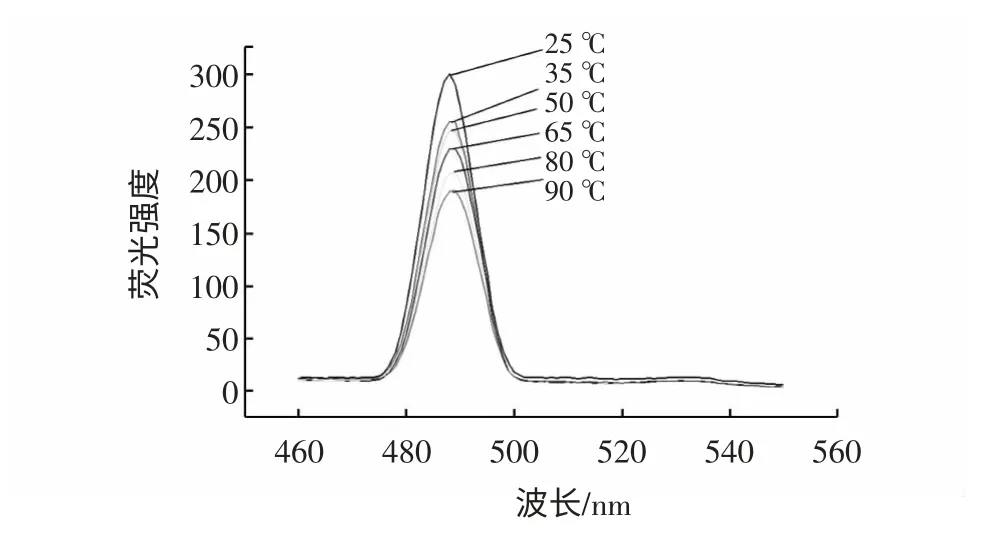
图8 温度对红花黄色素荧光性能的影响Fig.8 Effect of temperature to fluorescent spectral propertiesof safflower yellow
由图8 可知,随着温度的提高红花黄色素的荧光强度逐渐减弱,其中90 ℃时黄色素发出的荧光强度最弱,25 ℃时黄色素发出的荧光强度最强。推测其可能的原因是,温度升高时,介质粘度减小,分子运动加快,分子间碰撞几率增加,从而使分子无辐射跃迁增加,荧光效率降低。
2.9 pH 对红花黄色素荧光性能的影响
取10 只100 mL 玻璃烧杯,各加入蒸馏水50 mL,用0.2 moL/L 氢氧化钠和0.1 moL/L 硫酸溶液分别调节酸碱度使10 只烧杯中的pH 从1~10 排列,分别取上述10 种不同pH 的溶液各3 mL,各加入黄色素样品滤液40 μL,室温下在激发波长λex=242 nm,扫描范围:460 nm~550 nm 条件下测定不同pH 环境下红花黄色素的荧光性能,见图9。
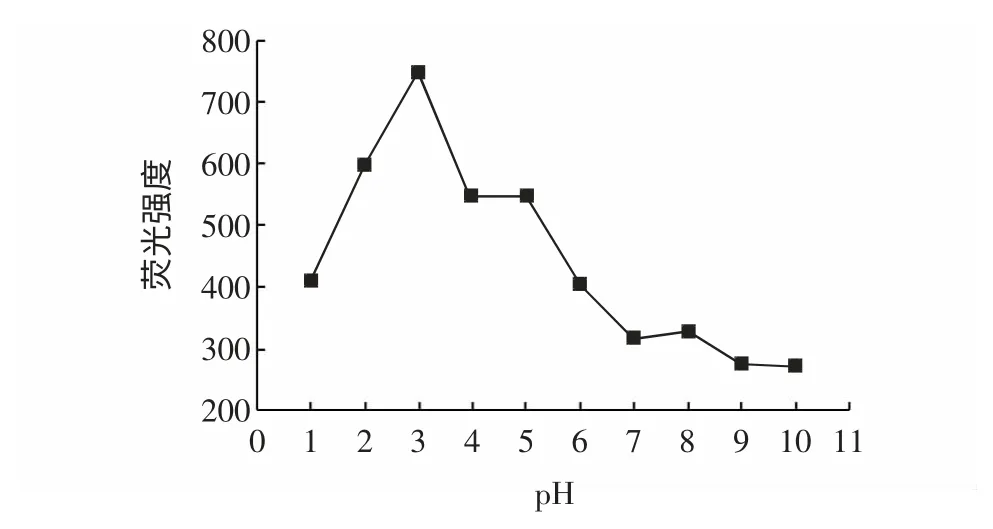
图9 pH 对黄色素荧光性能的影响Fig.9 Effect of pH to fluorescent spectral propertiesofsafflower yellow
由图9 可知,黄色素溶液的pH 在1~3 时,溶液的荧光性能逐渐增强,pH=3 时荧光强度达到最大。黄色素溶液的pH 在3~10 时,溶液的荧光强度逐渐减弱。推测其原因:黄色素溶液的pH 减小,因质子化作用-O(C5H11O5)变成-OH+(C5H11O5),使得左端的氧吸电子作用增强,与羰基间位连接的C=C 双键发生断裂,羰基间位的C 与-OH+(C5H11O5)左端的氧形成新键,从而形成一个环状结构,此时羰基临位的C 显正电性,容易发生烯醇互变异构现象,使得环状结构刚性增强,荧光性能也较强,当pH<3 时使得环上的-OH 容易形成-OH2+发生脱落,给电子基团减少,所以荧光性能较弱。
2.10 金属离子对红花黄色素荧光特性的影响
取3 只10 mL 比色管,分别加入黄色素样品滤液120 μL,将等量0.01 moL/L 金属化合物[FeSO4,AlCl3,Pb(NO3)2]加到相应的比色管中,用蒸馏水定容,摇匀。分别取上述3 种含不同金属离子的溶液3 mL,室温下在激发波长λex=242 nm,扫描范围:460 nm~550 nm 条件下测定红花黄色素的荧光特性,见图10。
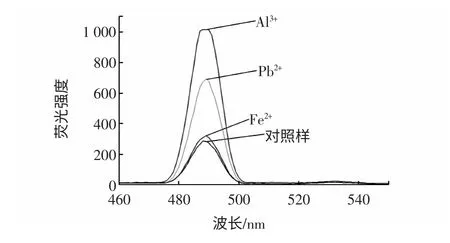
图10 金属离子对红花黄色素荧光特性的影响Fig.10 Effect of metal ion to fluorescent spectral propertiesof the carthamine
由图10 可知,Pb2+、Al3+、Fe2+离子的存在,使得红花黄色素的荧光性能增强,推测其原因:一般而言,铝离子可能与黄色素形成配合物,使黄色素分子结构发生变化,导致峰位发生变化;而重金属离子会使物质的荧光性能产生猝灭现象,但实验得出的结果却正好相反,峰位没有发生变化,且重金属离子使黄色素的荧光性能增强。
3 结论
本实验分别提取红花红、黄色素,分别进行荧光分析性能检测,分析溶剂、温度、pH、金属离子对红花红、黄色素荧光性能的影响。实验结果如下。
1)红花红色素50%丙酮溶液荧光性能实验研究结果表明:λex=365 nm,λem=735 nm,在pH=1,温度25 ℃时,红花红色素荧光强度最大,金属离子(Fe2+、Pb2+、Al3+)使红色素荧光性能增强,而(NH4)2SO4对红花红色素荧光性能的影响不大。
2)红花黄色素水溶剂荧光性能实验研究结果表明:λex=242 nm,λem=485 nm,在pH=3、温度25 ℃时,红花黄色素荧光强最大,金属离子(Fe2+、Pb2+、Al3+)使黄色素荧光性能增强。而文献报道[10]中红花甲醇提取液荧光性能研究结果为:λex=340 nm,λem=440 nm,红花色素在pH=12 的碱性环境中所发出的荧光强度达到最大。
[1] 吴德意.红花红色素的提取工艺及产品质量控制[J].化工进展,2003,22(1):26-28
[2] 朱文明.红花黄色素的提取精制及稳定性研究[D].合肥工业大学,2007:1-47
[3] 许钢.天然红花黄色素稳定性研究[J].食品工业科技,2000,21(1):16-18
[4] 王慧琴,谢明勇,付博强,等.RP-HPLC 法测定红花中红色素的含量[J].分析测试学报,2004,11(2):98-100
[5] 刘月庆,王睿,毕开顺.HPLC 法测定红花中黄色素A 的含量[J].药物分析杂志,2004,24(4):356-357
[6] 葛尔宁,张毅璇.红花及番红花色素的荧光特性分析[J].浙江中医学院学报,2005,29(6):85-86
