从HbA1c分层管理看基础胰岛素的应用策略
2012-12-23四川大学华西医院内分泌代谢科李益童南伟
四川大学华西医院内分泌代谢科 李益 童南伟
HbA1c分层管理的概念
糖化血红蛋白(HbA1c)分层管理,即不笼统推荐糖尿病的固定“一刀切”式控制HbA1c目标,而是根据患者疾病状态和社会因素的差异进行分层,然后根据各层次的具体情况制定适合该层次的HbA1c控制目标。该概念由中华医学会内分泌学分会在《中国成人2型糖尿病HbA1c控制目标的专家共识》提出[1-2]。
控制血糖可延缓糖尿病的发展及并发症的发生,但其公认的控制目标值一直存在争议。近年来包括糖尿病患者心血管风险干预研究(ACCORD)、退伍军人糖尿病研究(VADT)和糖尿病与心血管疾病行动研究(ADVANCE)等众多有关血糖控制与并发症关系的临床研究表明,5年左右强化降糖治疗对某些特殊(相当部分已有大血管疾病,病程近10年,平均年龄60岁左右)的2型糖尿病患者的大血管病变无明显益处,ACCORD研究甚至显示,控制HbA1c水平接近正常值(<6.4%)反而增加这类患者的死亡风险。另外,我国2型糖尿病患者血管并发症以脑血管病和肾损害相对高发,与白种人有些不同。基于以上背景,参考国际权威指南的建议并结合我国糖尿病特点特别是经济、卫生、文化等方面的地域和个体差异,2010年中华医学会内分泌学分会制定了该《共识》。
《共识》推崇个体化血糖控制,提出了HbA1c分层管理的理念,制定了根据病情并结合社会因素分层的具体HbA1c控制目标,并对HbA1c目标值的适用人群以HbA1c水平进行了分层(见表1)。《共识》具有实用性和针对性,对于临床中为患者制定个体化的降糖策略具有重要指导作用。
胰岛素的起始治疗
1. 胰岛素起始治疗的时机
胰岛素是控制血糖的重要手段,具有高效、经济、较安全的特点,其在糖尿病管理中的作用不容忽视。多项研究表明,亚裔人胰岛B细胞胰岛素储备能力较白种人低,因此我国2型糖尿病患者更应在适当的时候启动胰岛素治疗[3]。
1.1 1型糖尿病速发型患者 在发病时就需要启动胰岛素替代治疗,且需持续终生使用[4]。
1.2 非妊娠的2型糖尿病和成人隐匿性免疫性糖尿病患者 胰岛素起始治疗的时机:对于新诊断的患者,除了感染和各种应激状态外,依据血糖和HbA1c水平启动胰岛素治疗的指征各学术组织的推荐大致相同。2011年美国内分泌医师协会(American Association of Clinical Endocrinologists,AACE)《糖尿病临床实践指南》建议HbA1c>9%且有明显糖毒性临床表现甚至有酮症酸中毒倾向者需起始胰岛素治疗[5]。2012年4月美国糖尿病学会(American Diabetes Association,ADA)和欧洲糖尿病研究协会(European Association for the Study of Diabetes,EASD)《关于2型糖尿病高血糖治疗的联合声明》中将初始使用胰岛素的血糖水平提高了,即血浆葡萄糖高于16.7~19.4mmol/L或HbA1c>10%~12%且有明显的高血糖症状者,或发生了酮血症则强烈推荐于确诊后即起始胰岛素治疗,但安全稳定后应过渡至口服降糖药治疗[6]。
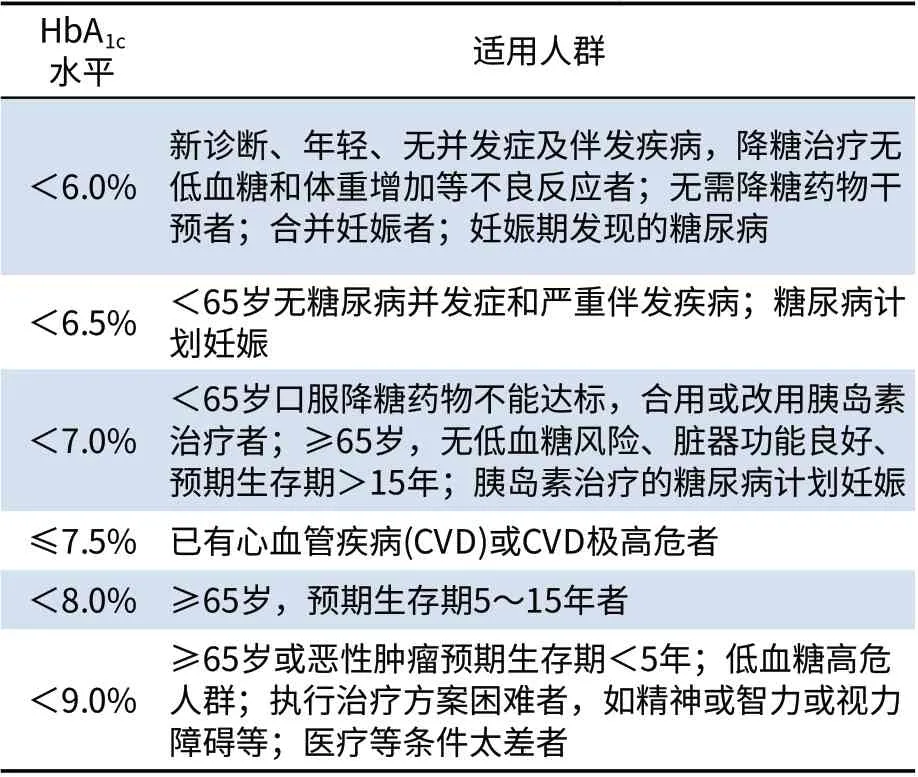
表1 中国成人2型糖尿病HbA1c目标值建议
需要强调的是,目前没有任何指南推荐新诊断的或初治的非妊娠2型糖尿病患者无指征地随意首选胰岛素治疗。
对于已确诊并开始接受治疗的患者,中华医学会内分泌学分会《成人2型糖尿病胰岛素临床应用中国专家共识》中建议,在采用有效地生活方式干预及两种或两种以上口服降糖药较大剂量治疗3个月后血糖仍不达标时或病程中出现无确切诱因的体重下降时,需考虑启动胰岛素治疗[3]。2012年4月ADA和EASD《关于2型糖尿病高血糖治疗的联合声明》中指出,在生活方式干预和二甲双胍联合治疗3个月HbA1c仍未达标者,可根据患者自身特点及意愿、控制靶目标、药物特性,选择以下五种药物中任何一种联用:磺脲类药物、噻唑烷二酮类药物、二肽基肽酶-4抑制剂、胰高糖素样多肽-1受体激动剂、胰岛素(通常选用基础胰岛素),以求在最小的不良反应下达到血糖靶目标[6]。所以,我们推荐在生活方式干预及两种或三种降糖药物治疗3个月后血糖未达标时或病程中出现无确切诱因的体重下降时均可启动胰岛素治疗。
2. 胰岛素起始治疗时胰岛素种类选择
目前各学术组织推荐的胰岛素起始治疗方案不完全一致[3]。多数国家和地区推荐起始治疗使用基础胰岛素,如血糖控制不达标,可加用餐时胰岛素。《美国内分泌医师协会专家共识》指出根据不同的HbA1c水平和血糖谱,基础胰岛素、预混胰岛素、基础-餐时胰岛素或餐时胰岛素一日多次注射、餐时胰岛素加二甲双胍这四种胰岛素方案中任一种均可作为起始治疗,应该说此方案更科学、更合理,但相对难掌握,特别是非内分泌专科医生。目前尚无循证医学证据证实何种胰岛素起始治疗方案更优。基于IMPROVE研究的结果[7]和我国糖尿病患者的血糖谱特点,《中国成人2型糖尿病胰岛素临床应用专家共识》将基础胰岛素、预混胰岛素均列为胰岛素起始治疗方案的备选方案,这一推荐与2010年版《中国2型糖尿病防治指南》一致[4],此方案尤其适合非内分泌专科医生。
迄今,尚缺乏量化指标来判断起始选择基础或预混胰岛素。但依据基础胰岛素和预混胰岛素的降糖特点,即基础胰岛素降空腹血糖为主而餐后血糖有一定降低,预混胰岛素则是在基础胰岛素降糖的基础之上可较多降低餐后血糖。由此推论,空腹血糖升高为主或空腹餐后血糖需相似水平的降低宜选择基础胰岛素;以餐后血糖升高为主同时伴空腹血糖升高则宜选择预混胰岛素。
基础胰岛素的应用
1. 基础胰岛素种类的选择
中效人胰岛素和长效胰岛素类似物甘精胰岛素和地特胰岛素均可作为基础胰岛素[3,4,6]。Cochrane一项系统评价显示,对于2型糖尿病患者,长效胰岛素类似物和中效人胰岛素对血糖的控制作用无显著差异,长效胰岛素类似物在患者导向的结果(即死亡率、致残率、生活质量)或者费用方面亦相似[8]。但是,长效胰岛素类似物作用时间比中效人胰岛素长,在长期治疗情况下,血清游离胰岛素浓度可保持稳定。这些特性使得与中效人胰岛素相比,长效胰岛素类似物较少发生严重和夜间低血糖[3]。AACE认为,长效胰岛素类似物是较理想的基础胰岛素[5,7]。因此,胰岛素的选择应综合考虑患者疾病状态、经济状况和健康需求,选择安全、有效、成本-效益高的基础胰岛素。
2. 基础胰岛素治疗患者的血糖监测
血糖监测是糖尿病管理的重要组成部分,其监测结果可用于评估糖尿病患者糖代谢紊乱程度、制定合理的降糖方案、反映降糖效果并指导治疗方案调整。下面我们将结合2011年中华医学会糖尿病学分会发布的《中国血糖监测临床应用指南》,简要阐述接受基础胰岛素治疗患者的血糖监测[9]。
目前应用于临床的血糖监测方法包括下列四种:自我血糖监测(SMBG)、动态血糖监测(CGM)、糖化血清白蛋白(GA)测定及HbA1c测定。
2.1 SMBG方案 SMBG即患者利用血糖仪在家中开展的血糖监测,能实时反映血糖水平,便于降糖方案调整,同时有助于及时发现和处理低血糖,避免严重低血糖的发生。相关研究显示,在接受胰岛素治疗的患者中应用自我血糖监测能改善代谢控制、并可能减少糖尿病相关终点事件。接受基础胰岛素治疗的患者在血糖达靶目标之前,需每周监测3天的空腹血糖,每两周复诊1次,复诊前1天加测5个时间点血糖谱。在血糖达标后每周监测3次血糖,即:空腹、早餐后、晚餐后,每月复诊1次,复诊前1天加测5个时间点血糖谱(见表2)。

表2 基础胰岛素治疗SMBG方案
2.2 CGM CGM是通过葡萄糖感应器监测皮下组织间液的葡萄糖浓度来间接反映血糖水平的监测技术,可以提供连续、全面、可靠的全天血糖信息,了解血糖波动的趋势,发现传统监测方法不易探测到的高血糖或低血糖。CGM适用于以下患者或情况:①1型糖尿病。②需要胰岛素强化治疗的2型糖尿病患者。③在SMBG指导下使用降糖治疗的2型糖尿病患者,仍出现无法解释的严重低血糖或反复低血糖,无症状性低血糖、夜间低血糖,无法解释的高血糖,特别是空腹高血糖、血糖波动大,处于对低血糖的恐惧,刻意保持高血糖状态的患者,SMBG结果良好但HbA1c始终不达标者。④妊娠期糖尿病或糖尿病合并妊娠。⑤患者教育。进行CGM可以促使患者选择健康的生活方式,提高患者依从性,促进医患双方更有效的沟通。⑥其他糖尿病患者如病情需要也可进行CGM,以了解其血糖谱的特点及变化规律。⑦其他伴有血糖变化的内分泌代谢疾病,如胰岛素瘤等,也可应用CGM了解血糖变化的特征。
2.3 GA GA反映患者近2~3周内平均血糖水平,为评价患者短期糖代谢控制情况的良好指标,尤其是对于糖尿病患者治疗方案调整后疗效评估有重要意义。
2.4 HbA1cHbA1c是反映既往2~3月平均血糖水平的指标,是临床上作为评估长期血糖控制状况的金标准,也是临床决定是否需要调整治疗的重要依据。根据《中国2型糖尿病防治指南》的建议,HbA1c在治疗之初至少每3个月检测1次,一旦达到治疗目标可每6个月检查一次。
基础胰岛素的剂量调整策略
2010年《中国2型糖尿病防治指南》推荐,基础胰岛素需与口服降糖药物联用,于睡前注射[4]。
1. 基础胰岛素起始剂量的确定
基础胰岛素治疗一般应从小剂量开始[6],ADA曾推荐起始剂量可为固定值10IU/d[10]。但这不适合中国患者的特点,因其肥胖及体重情况不同。我们认为,中国以千克体重和血糖为参照较合理,即可按0.1~0.2IU/·kg-1·d-1[6]计算。当出现严重高血糖时(血浆葡萄糖高于16.7~19.4mmol/L、HbA1c大于10%~12%),起始剂量可增大为0.3~0.4IU/·kg-1·d-1[6]。若就诊前连续数天监测过空腹血糖值,可将最高血糖值作为起始剂量(如最高血糖值为15.8mmol/L,则以16IU/d作为起始剂量)[12]。通常起始剂量无法使血糖达标,需要对剂量进行适时适量的调整后才能有效控制血糖。
2. 基础胰岛素剂量调整策略
胰岛素是降糖最有效的措施。但2011年我国糖尿病现况调查结果显示,口服降糖药物联合胰岛素治疗的患者HbA1c控制达标率并不高,仅为15%[3]。血糖成功达标的关键在于安全和行之有效的剂量调整策略[11],因此避免低血糖的发生是首要的。
SMBG是剂量调整的基础。一旦接受基础胰岛素治疗,患者就需详实地记录自我血糖监测结果、胰岛素用量、饮食及运动情况,以作为剂量调整的依据。治疗之初,每3个月监测一次HbA1c,用以评估血糖控制情况[6]。
自我剂量调整(self-titration),即患者自己根据血糖监测结果对胰岛素剂量进行调整,近年来相关研究已经证实,与医生为主导的剂量调整模式相比,自我剂量调整有着潜在优势[11]。ATLANTUS研究[12]为前瞻性多中心随机对照试验,5033名血糖控制不佳的患者均使用甘精胰岛素治疗,被随机分成两组,即自我剂量调整组和医生主导剂量调整组。自我剂量调整组由患者自己根据前3天平均空腹血浆葡萄糖值每3天调整一次基础胰岛素用量,医生主导剂量调整组则由医生每周对患者进行电话或门诊随访,并根据患者前3天平均空腹血浆葡萄糖值对剂量进行调整。该研究将空腹血浆葡萄糖目标值设定为≤5.5mmol/L。两组具体剂量调整方案(见表3)。结果显示,自我剂量调整组与医生主导剂量调整组相比,其HbA1c和空腹血糖值下降幅度更大,而且并未增加严重低血糖的发生率。该研究纳入对象中,有一部分患者进入研究前从未接受过胰岛素治疗。调查员观察发现,这部分患者在被分入自我剂量调整组后,同样可以安全、有效地对基础胰岛素剂量进行自我调整。这说明自我剂量调整策略在基础胰岛素起始治疗中的可行性。
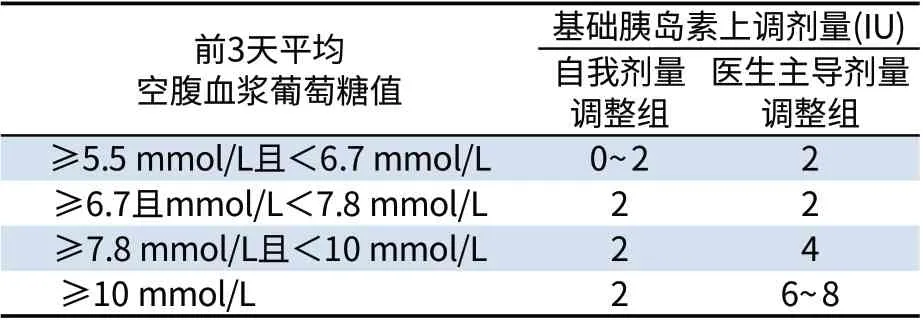
表3 ATLANTUS研究剂量调整方案
另一方面,如何根据HbA1c控制靶目标确定剂量调整的空腹血糖目标值,对于血糖达标也有着举足轻重的作用[11]。TITRATE研究[13]显示,在基础胰岛素自我剂量调整的策略下,空腹血糖目标值(FPG titration targets)不同会引起最终血糖控制情况的差异。 3.9~5.0mmol/L 组与4.4~6.1mmol/L组相比,前者HbA1c下降幅度显著大于后者,且前者HbA1c的达标率(HbA1c<7.0%)可达64.3%,后者仅为54.5%,两者具有显著差异。而两者的低血糖发生率和体重增加幅度大致相当。可见较低的空腹血糖剂量调整目标值有助于提高HbA1c的达标率,但决不能完全靠空腹血糖来控制HbA1c,特别是以低血糖为代价尤其是夜间低血糖,这样会增加死亡率尤其是血管事件的死亡率。至于如何根据不同的控制靶目标确定合适的空腹血糖值,尚无研究给出明确的答案。我们可根据HbA1c对应的平均血糖水平(见表4)[14],以及现有相关《指南》推荐的血糖控制目标(见表5)[5,15],并结合自己的临床经验确定一个空腹血糖目标值,以用于指导基础胰岛素剂量的调整。
综上,一个行之有效的剂量调整策略应包含以上两个要素。首先根据不同人群的HbA1c控制目标制定一个合适的空腹血糖目标值,然后由患者根据血糖监测结果进行自我基础胰岛素剂量调整。调节的频度可为每3天一次,当前3天的平均空腹血糖值高于空腹血糖目标值时每次可上调1~2IU;当靠近目标值时,上调的频度应降低,上调的剂量应减少;若出现任何形式的低血糖时,均应适量下调胰岛素用量[4,6,10]。同时在血糖未达标前,每3个月复查一次HbA1c,评估血糖控制情况。当空腹血糖显示已达标而HbA1c却未达标时,或基础胰岛素用量大于0.5IU/(kg·d)时,均应考虑依据餐后血糖情况适当加用餐时胰岛素或改用预混胰岛素[4,6]。
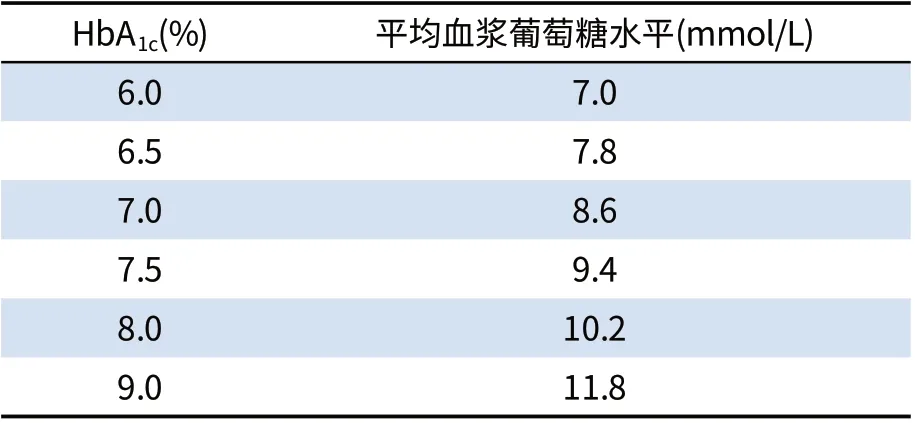
表4 糖化血红蛋白(HbA1c)与平均血糖水平的关系

表5 各指南推荐的血糖控制目标
通过上述讨论,我们认为根据患者的不同情况制定“量身定做”式的HbA1c靶目标,而不是笼统的HbA1c<7%的靶目标;一般情况下胰岛素不应作为初治2型糖尿病患者的首选;依据血糖谱选择基础或预混胰岛素作为起始治疗;若以基础胰岛素为起始治疗,应与口服药合用,且从小剂量开始,逐渐达标,作好血糖监测,尽量避免低血糖发生即安全达标。
[1] 中华医学会内分泌学分会.中国成人2型糖尿病HbA1c控制目标的专家共识[J]. 中华内分泌代谢杂志, 2011, 27(5): 371-374.
[2] 曹明明,童南伟.中国成人2型糖尿病HbA1c控制目标的专家共识解读[J].中国实用内科杂志, 2011, 31(2): 113-115.
[3] 中华医学会内分泌学分会.成人2型糖尿病胰岛素临床应用中国专家共识[J]. 药品评价, 2012, 9(1): 42-44.
[4] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2010年版)[M]. 北京: 北京大学出版社, 2011.
[5] American Association of Clinical Endocrinologists. American Association of Clinical Endocrinologists Medical Guidelines for Clinical Practice for Developing A Diabetes Mellitus Comprehensive Care Plan[J]. Endocr Pract, 2011, 17(Suppl2): 1-53.
[6] Inzucchi SE, Nauck M, Bergenstal RM, et al. Management of Hyperglycemia in Type 2 Diabetes: A Patient-Centered Approach:Position statement of the American Diabetes Association and the European Association for the Study of Diabetes[J]. Diabetes Care, 2012, 35(6): 1364-1379.
[7] Valensi P,Benroubi M, Borzi V, et al. Initiating insulin therapy with,or switching existing insulin therapy to,biphasic insulin aspart 30/70 (NovoMix® 30) in routine care: safety and effectiveness in patients with type 2 diabetes in the IMPROVE™ observational study[J]. Int J of Clin Pract, 2009, 63(3): 522–531.
[8] Horvath K, Jeitler K, Berghold A, et al. Long-acting insulin analogues versus NPH insulin (human isophane insulin) for type 2 diabetes mellitus[DB/OL]. Cochrane Database of Systematic Reviews, 2007, 2: CD005613.
[9] 中华医学会糖尿病学分会.中国血糖监测临床应用指南(2011年版)[J]. 中华糖尿病杂志, 2011, 3(1): 13-21.
[10] Nathan DM, Buse JB, Davidson MB, et al. Medical management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy: A consensus statement of the American Diabetes Association and the European Association for the study of diabetes[J]. Diabetes Care, 2009, 32(1): 193–203.
[11] Garber AJ. The importance of titrating starting insulin regimens in patients with type 2 diabetes[J]. Diabetes Obesity Metab, 2009, 11(Suppl.5): 10-13.
[12] Davies M, Bianchi-Biscay M, Storm F, et al. Improvement of Glycemic Control in Subjects With Poorly Controlled Type 2 Diabetes: Comparison of two treatment algorithms using insulin glargine[J]. Diabetes Care, 2005, 28(6): 1282-1288.
[13] Blonde L, Merilainen M, Karwe V, et al. Patient-directed titration for achieving glycaemic goals using a once-daily basal insulin analogue: an assessment of two different fasting plasma glucose targets - the TITRATETM study[J]. Diabetes Obesity Metab, 2009, 11, 623-631.
[14] American Diabetes Association. Correlation of A1C with average glucose[DB/OL]. http://professional. diabetes. org/eAG.
[15] American Diabetes Association. Standards of Medical Care in Diabetes-2012[J]. Diabetes Care, 2012, 35(Suppl1): 11-63.
